计算化学在本科生金属腐蚀与防护实验教学中的应用
任雪峰,安茂忠,杨培霞,张锦秋,刘安敏
(1.大连理工大学海洋科学与技术学院,辽宁 盘锦 124221;2.哈尔滨工业大学化工与化学学院,城市水资源与水环境国家重点实验室,黑龙江 哈尔滨 150001;3.大连理工大学化工学院盘锦分院,精细化工国家重点实验室,辽宁 盘锦 124221)
腐蚀是金属材料在环境介质中发生的表面破坏,直至材料失效的化学或电化学反应[1-3]。金属腐蚀普遍存在于工业生产与日常生活的各个方面,造成国民经济的重大损失,并危害人们的生命和财产安全[4]。数据显示,2014年,我国腐蚀成本为21 278.2亿元人民币,约占当年国内生产总值的3.34%[5]。“金属腐蚀与防护”是金属材料专业方向的重要专业课,在学习腐蚀与防护原理的同时与生产实际紧密相连,具有极强的实践性[6]。
金属腐蚀与防护实验是“金属腐蚀与防护”“过程装备腐蚀与防护”等课程的重要组成部分和实践环节[7]。通过理论学习及实验教学,可以使学生更深刻地理解金属腐蚀与防护的理论知识及应用价值,并有助于明确金属腐蚀与防护研究的手段及其在国民经济和新材料科学技术发展中的重要作用[8]。在金属腐蚀与防护实验中可以开展金属材料镀层保护[9-10]、牺牲阳极保护[11]以及缓蚀剂保护[12-14]的防腐蚀研究。其中,缓蚀剂保护具有操作方便、投入量少、成本低、见效快等优点[15]。使用含有未配对电子的元素(如N、O、S等)、不饱和键或可形成共轭体系的有机化合物作为缓蚀剂,使其在金属表面发生物理或化学吸附,从而隔离腐蚀性介质与金属的接触,就可以达到抑制腐蚀的目的[16]。选取有效的缓蚀剂是提升防护效果的关键。
对于有机缓蚀剂的研究而言,由于有机物种类较多,且存在同分异构体,因此实验筛选缓蚀剂的难度较大。随着计算化学的不断发展,量子化学计算与分子动力学模拟[17-19]在缓蚀剂研究中的应用逐渐增多。
在金属腐蚀与防护实验的教学过程中,希望通过引入量子化学计算与分子动力学模拟,以理论计算来辅助缓蚀剂的设计或筛选。要求学生掌握Materials Studio(MS)软件的具体操作与数据分析,在课程演示与MS软件自带教程的指导下,可以熟练建立理论模型,并开展量子化学计算与界面吸附行为的研究,掌握以理论计算筛选缓蚀剂的技能。将计算化学手段引入课题教学,有助于培养学生的创新思维,提升其创新能力,以及通过信息化手段解决复杂问题的能力。
1 理论设计环节
在计算化学的具体实践环节,使用可以在可视化界面操作的 MS软件开展缓蚀剂的量子化学性质与界面吸附行为研究。量子化学性质主要是指缓蚀剂的前线分子轨道,使用 DMol3模块,采用 BLYP泛函(DNP basfile_v4.4基组)来研究缓蚀剂的前线分子轨道分布与轨道能级,预测其作为缓蚀剂的可能性。
在界面吸附行为研究方面,利用 Forcite模块对缓蚀剂在金属铁表面的分子动力学(MD)行为进行模拟,其间加入水分子来模拟潮湿环境中的有机物吸附行为。使用恒体积(NVT)系统、COMPASS力场模拟室温(298 K)下500 ps(步长1 fs)时间内的界面吸附行为。到达平衡状态时缓蚀剂在铁表面的吸附能(EAdsorption)可用式(1)计算。

其中ETotal是铁与缓蚀剂分子的总能量,EFe和EInhibitor分别指铁和缓蚀剂分子单独存在时的能量。
2 教学示范内容
2.1 同分异构体性质对比
在教学示范环节,以由2个碳原子和3个氮原子组成的五元杂环有机化合物──三氮唑(C2H3N3)的量子化学性质与界面吸附行为研究为例,图1示出了1,2,3-三氮唑和1,2,4-三氮唑这2种三氮唑同分异构体的分子结构与前线分子轨道。
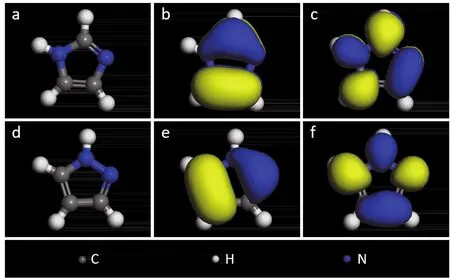
图1 1,2,3-三氮唑的分子结构(a)、最高占据分子轨道(HOMO)(b)和最低未占据分子轨道(LUMO)(c);1,2,4-三氮唑的分子结构(d)、HOMO(e)和LUMO(e)Figure 1 Molecular structures of 1H-1,2,3-triazole (a) and 1H-1,2,4-triazole (d); HOMO of 1H-1,2,3-triazole (b) and 1H-1,2,4-triazole (e); and LUMO of 1H-1,2,3-triazole (c) and 1H-1,2,4-triazole (f)
量子化学计算结果表明,两个三氮唑同分异构体表现出不同的前线分子轨道电子云分布,其中含氮结构是电子云相对集中的位置,说明其反应活性较高,在发生界面吸附行为时优先产生良好吸附。前线分子轨道的电子云分布可以初步预测其吸附活性位点,而轨道能级可以定量描述有机物分子的得失电子能力,也就是与外界发生化学反应的能力。HOMO值的高低决定有机物分子向外供给电子能力的大小,LUMO值则是其接受电子能力的量度。HOMO值决定了有机物向金属空轨道供给电子而引发配位或吸附作用的能力,LUMO值则反映出有机物分子从外界得到电子的能力,也就是从外界得到电子而形成反馈键的能力。采用量子化学计算进行缓蚀剂的前线分子轨道研究,可以初步预测其界面吸附行为。1,2,3-三氮唑、1,2,4-三氮唑的前线分子轨道能级如图2所示。

图2 1,2,3-三氮唑与1,2,4-三氮唑的前线分子轨道能级Figure 2 Values of frontier molecular orbitals of 1H-1,2,3-triazole and 1H-1,2,4-triazole
在两个三氮唑同分异构体中,1,2,3-三氮唑具有相对较高的HOMO值,说明在发生吸附时,1,2,3-三氮唑具有较强的供电子能力,可以向金属原子提供电子并发生稳定的吸附作用。在LUMO值方面,1,2,3-三氮唑较低,因此易于得到电子而形成反馈键,提升吸附稳定性。同时,由于1,2,3-三氮唑的前线分子轨道能级差(ΔE=ELUMO-EHOMO)较小,而电子在分子轨道间的迁移越快,有机物在金属表面发生的化学吸附就越稳定,因此量子化学计算预测1,2,3-三氮唑在金属铁表面具有更好的吸附行为。1,2,3-三氮唑和1,2,4-三氮唑分子在金属铁表面发生的吸附作用可以通过MD模拟进一步研究,如图3、图4所示。
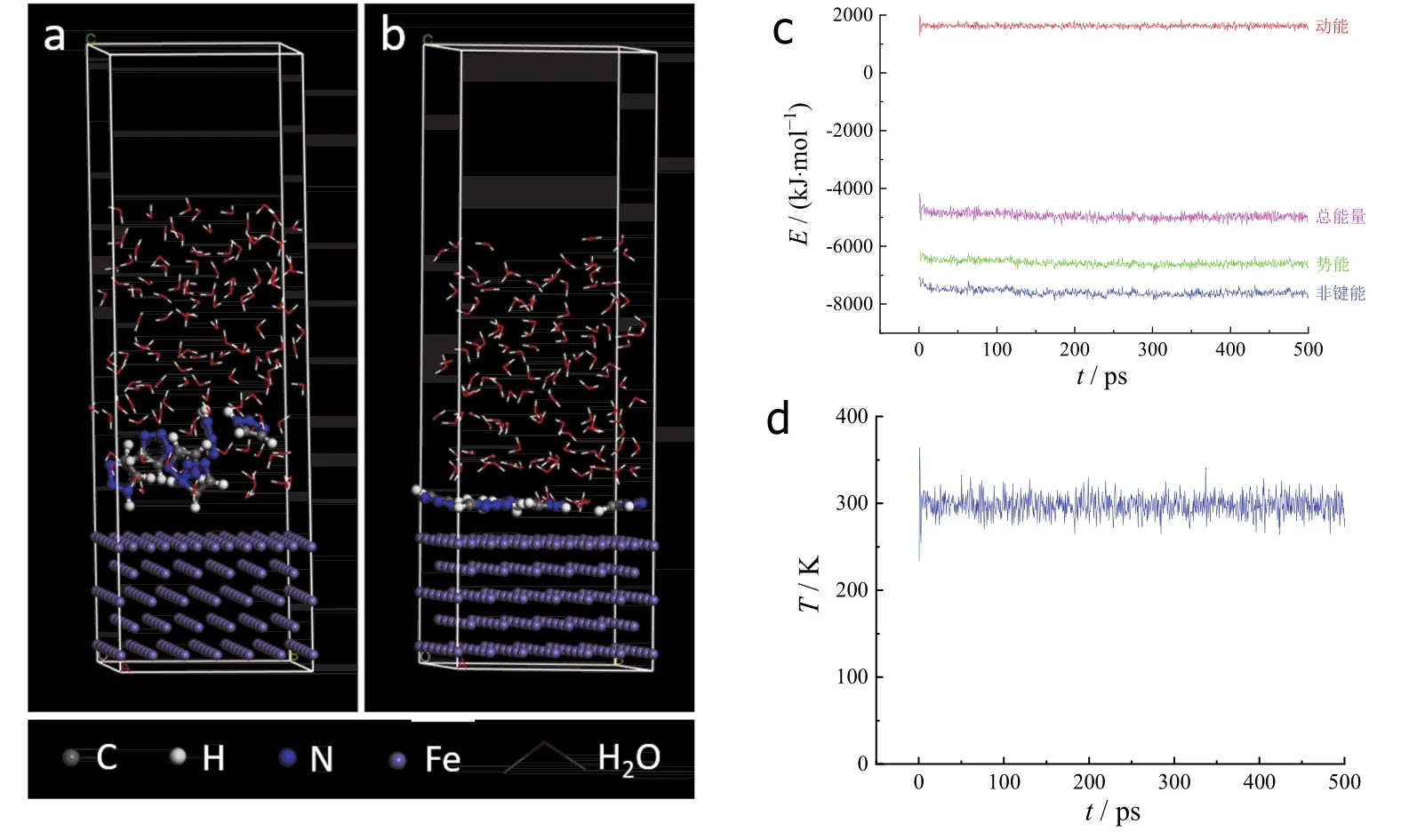
图3 1,2,3-三氮唑分子在铁表面的吸附行为: (a)初始构型;(b)最终构型;(c)能量波动曲线;(d)温度波动曲线Figure 3 Adsorption behavior of 1H-1,2,3-triazole on Fe surface: (a) initial configuration; (b) final equilibrium configuration;(c) energy fluctuation curves; and (d) temperature fluctuation curve by molecular dynamics simulation

图4 1,2,4-三氮唑分子在铁表面的吸附行为: (a)初始构型;(b)最终构型;(c)能量波动曲线;(d)温度波动曲线Figure 4 Adsorption behavior of 1H-1,2,4-triazole on Fe surface: (a) initial configuration; (b) final equilibrium configuration;(c) energy fluctuation curves; and (d) temperature fluctuation curve by molecular dynamics simulation
在 500 ps的 MD模拟过程中,能量和温度波动曲线证明体系迅速进入稳定状态,并保持一定的平衡。1,2,3-三氮唑与1,2,4-三氮唑分子在吸附平衡后向金属铁表面迁移,证明两种分子在金属铁表面能够发生优异的吸附行为。金属铁表面1,2,3-三氮唑和1,2,4-三氮唑分子的吸附能较高,分别达到了-272.21 kJ/mol和-233.53 kJ/mol。另外,1,2,3-三氮唑分子在具备更高吸附能的同时,以其氮杂环平铺吸附于金属表面,说明其具备更加优异的吸附能力。以上结果证明了分子结构会显著影响缓蚀剂的界面吸附行为。
综合量子化学计算与分子动力学模拟的结果后可以认为,1,2,3-三氮唑与1,2,4-三氮唑分子具有相似的分子结构、较高的HOMO和较小的ΔE,在金属铁表面具有优异的吸附行为,有望成为潜在的金属铁的缓蚀剂。
在上述示例中展示了1,2,3-三氮唑与1,2,4-三氮唑分子的量子化学性质与界面吸附行为的对应关系。作为课程练习,安排学生根据实验课的软件操作演示与 MS软件自带的官方教程,对其他具有同分异构体的有机缓蚀剂(如咪唑)的性质进行研究。
2.2 杂原子对界面吸附行为影响的示范讲解
承接2.1节的内容,通过研究苯并三氮唑(BTA)、2-巯基苯并噻唑(MBT)、2-巯基苯并咪唑(MBI)等1,2,3-三氮唑类衍生物的界面吸附行为差异,可以进一步明确分子结构与杂原子对界面吸附行为的影响。BTA、MBT和MBI的分子结构及前线分子轨道如图5所示。BTA中氮杂环表现出与1,2,3-三氮唑明显不同的电子云分布,进一步说明分子结构对有机缓蚀剂性能有一定的影响。MBT、MBI与BTA的前线分子轨道分布存在明显差别(见图6),证明杂原子种类对其吸附性能与活性中心具有潜在影响。
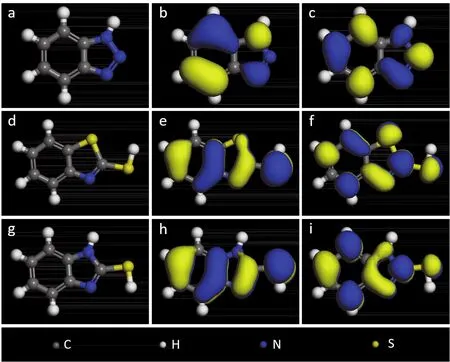
图5 BTA的分子结构(a)、HOMO(b)和LUMO(c);MBT的分子结构(d)、HOMO(e)和LUMO(f);MBI的分子结构(g)、HOMO(h)和LUMO(i)Figure 5 Molecular structures of BTA (a), MBT (d), and MBI (g); HOMO of BTA (b), MBT (e), and MBI (h);LUMO of BTA (c), MBT (f), and MBI (i)
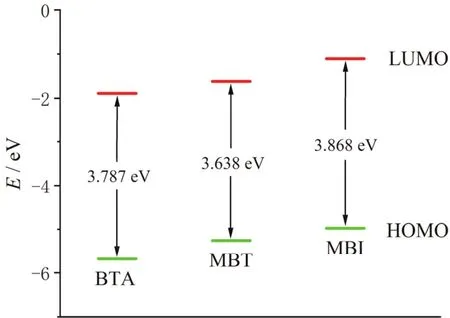
图6 BTA、MBT和MBI的前线分子轨道能级Figure 6 Values of frontier molecular orbitals of BTA, MBT, and MBI
与1,2,3-三氮唑相比,BTA、MBT和MBI具有较高的HOMO能级,因而具备更强的给电子能力,有望成为更加优异的金属缓蚀剂。而在轨道能级差值ΔE相差较小的情况下,BTA、MBT和MBI的HOMO轨道能级逐渐上升,说明三者的给电子能力依次上升,这将显著影响其界面吸附行为。
因此量子化学计算预测,BTA、MBT和MBI在金属铁表面均具有良好的吸附行为,同时三者的吸附能力依次增强。BTA、MBT和MBI在金属铁表面发生的吸附作用可以通过MD模拟进一步研究,如图7所示。
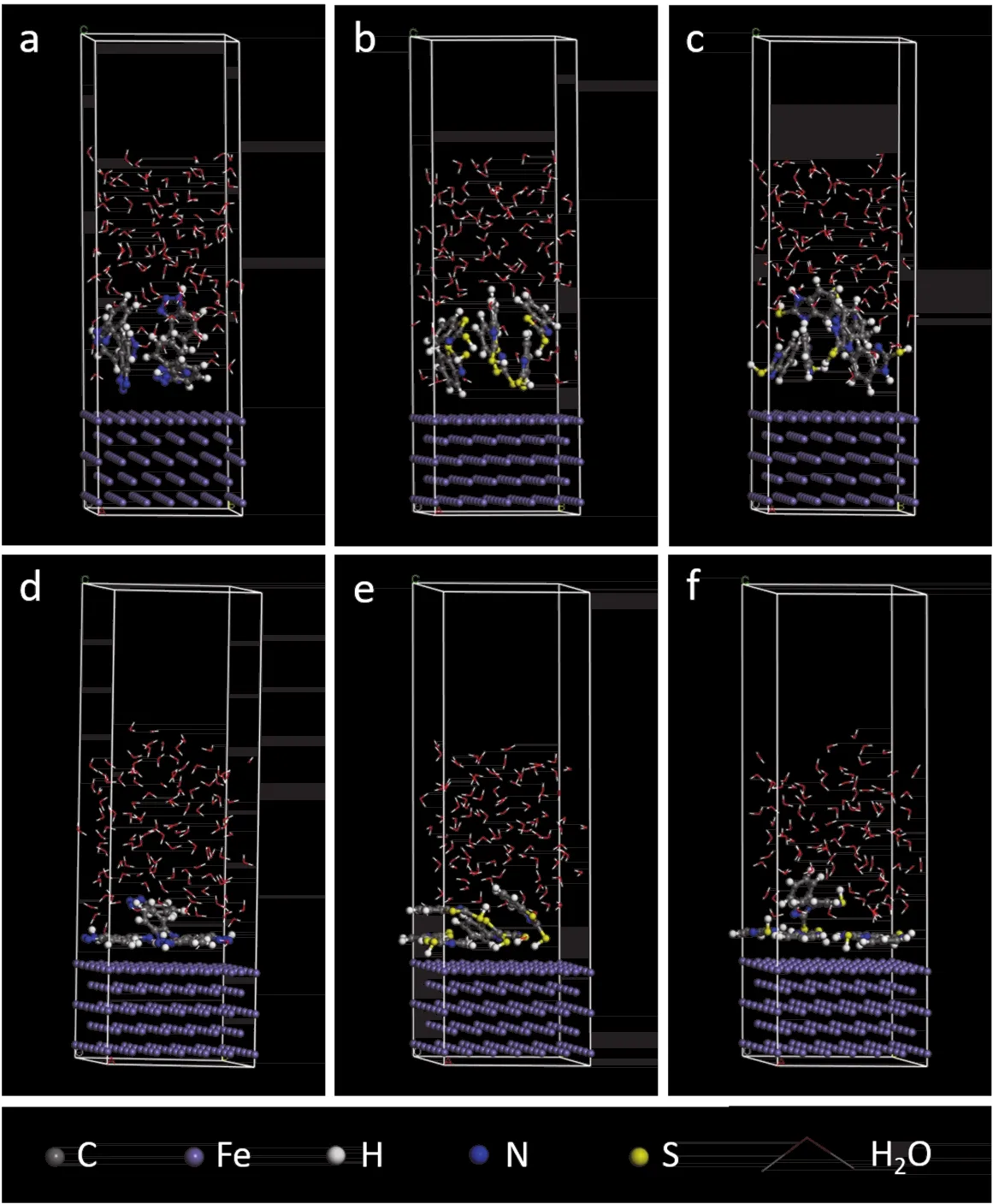
图7 3种分子在铁表面吸附的初始构型(a: BTA; b: MBT; c: MBI)和最终构型(d: BTA; e: MBT; f: MBI)Figure 7 Initial configurations of BTA (a), MBT (b), and MBI (c) as well as final equilibrium configurations of BTA (d), MBT (e), and MBI (f) for their adsorption on Fe surface
在500 ps的MD模拟过程中,BTA、MBT和MBI在铁表面均具有稳定的吸附,吸附平衡后向金属铁表面迁移,证明BTA、MBT和MBI在金属铁表面能够发生优异的吸附行为,并保持一定的平衡。BTA、MBT和MBI在金属铁表面的吸附能较高,分别为-371.56、-401.88和-421.71 kJ/mol,表明它们在金属铁表面均具有良好的吸附行为。
量子化学计算与分子动力学模拟的结果均表明BTA、MBT和MBI具有良好的界面吸附行为,是潜在的金属铁的缓蚀剂。另外,通过1,2,3-三氮唑、1,2,4-三氮唑与BTA、MBT、MBI的对比,证明缓蚀剂的HOMO轨道能级与其界面吸附行为相关。
在练习环节,要求学生在之前布置的咪唑类缓蚀剂作业的基础上,构建出有杂原子或外接基团修饰的缓蚀剂,对其结构稳定性、量子化学性质及界面吸附行为进行分析,进一步掌握相关计算化学软件的操作。在练习与设计过程中,注意查阅文献,给出设计的依据,并结合理论计算的结果,判断开展有关研究的可行性。
3 总结与提高
以通过量子化学计算与分子动力学模拟筛选金属缓蚀剂为教学范例,直观地展示了计算化学在本科生金属腐蚀与防护实验教学中的应用。当学生掌握了相关软件的操作以及理论计算技能后,可以开展分组讨论,以 Fe、Cu、Zn等金属为研究对象,限定于常见的缓蚀剂,在理论计算的基础上对缓蚀剂的作用能力进行排序,开展电化学实验加以验证和对照分析,进一步明确计算化学在金属腐蚀与防护实验教学中的指导意义。