高铁酸钾氧化降解萘的性能研究
韩佳琪,李 爽,马会强
(辽宁石油化工大学环境与安全工程学院,辽宁抚顺 113001)
萘由两个苯环构成,是多环芳烃(PAHs)中结构最简单的物质[1],外观呈白色,有光亮,常温即可挥发和升华[2]。萘主要源自提炼及加工煤焦油的过程和以萘为原材料的化工行业及石油的加工生产[3],以上过程中产生的萘质量浓度大,毒性高,严重污染水体、土壤和大气环境,甚至造成接触者的死亡[4]。目前,常用的萘处理方法为物理法、化学法和生物法[5]。生物法具有降解效率高和低成本的特点,但环境因素对降解效果的影响较大[6]。物理法中的吸附法和萃取法并不能将污染物降解彻底,污染物的溶解性和吸附剂的性质均会影响降解效果。化学法因具有见效迅速、修复时间短、处理效果明显等特点被广泛用于污染物的降解[5]。
高铁酸钾常被用于化学氧化法,因具有比传统氧化剂更高的氧化还原电位(在酸性条件下电势高达2.2 V[7]),反应速度快[8],不会有其他副产物生成[9],具有一定的絮凝、杀菌作用,不产生二次污染[10],也被称为“环境友好型氧化剂”[11]。畅彤等[12]的研究表明,高铁酸钾能高效氧化降解苯酚及其有毒中间体。臧淑艳等[13]的研究表明,高铁酸钾能高效去除复合污染废水中的有机砷。李腾飞等[14]的研究表明,高铁酸钾作为实验预氧化剂,在高铁酸钾-磁性离子交换树脂(K2FeO4-MIEX)联用处理污水的过程中可表现出明显的协同效应。
鉴于高铁酸钾极强的氧化效果,本实验采用高铁酸钾氧化降解萘,通过单因素实验探究高铁酸钾质量浓度、p H、温度和萘初始质量浓度对萘降解率的影响,确定影响萘降解率的主要因素,并用响应面分析法优化高铁酸钾对萘的降解条件,以期为多环芳烃污染地下水的修复提供数据基础。
1 实验部分
1.1 仪器与试剂
试剂:萘(C10H8)、高铁酸钾(K2FeO4)、过硫酸钠(Na2S2O8)、冰乙酸(CH3COOH),天津大茂化学试剂厂;氢氧化钠(Na OH)、亚硫酸钠(Na2SO3)、磷酸氢二钠(Na2HPO4)、磷酸二氢钠(Na H2PO4)、磷酸氢二 钾(K2HPO4)、磷 酸 二 氢 钾(KH2PO4)、硼 砂(Na2B4O7),天津恒兴化学试剂厂;正己烷(C6H14),天津富宇精细化工厂。以上所有试剂均为分析纯。
仪器:UV-5100紫外分光光度计,上海元析仪器有限公司;Jan-79恒温水浴磁力搅拌器,江苏省金坛市大地自动化仪器厂;JA2003N电子天平,上海佑科仪器仪表有限公司;PHS-25p H计,上海仪电科学仪器股份有限公司。
1.2 实验方法
1.2.1 萘溶液的配制及测定方法 配制质量浓度为25 mg/L的萘母液,量取20 mL,用不同缓冲液稀释至100 mL,配制质量浓度为5 mg/L的不同p H萘溶液。p H为3.0、5.0、6.0的萘溶液用Na2HPO4和NaH2PO4配制;p H为7.0的萘溶液用K2HPO4和KH2PO4配制;p H为9.0的萘溶液用Na2B4O7配制,并用CH3COOH溶液和稀Na OH溶液进行调节。测定萘质量浓度时,按一定时间间隔提取5 mL降解后的萘于小瓶中,加入20μL1 mol/L的Na2SO3猝灭剂终止反应;加入C6H14,萃取后倒入比色皿中,用紫外分光光度计测定反应前后的萘质量浓度,并计算降解率。每组实验重复3次,取平均值。
1.2.2 单因素实验
(1)K2FeO4质量浓度对萘降解率的影响。在温度为25℃、溶液的pH为7.0、萘质量浓度为10 mg/L的条件下,向萘溶液中分别添加0.15、0.30、0.45、0.60、0.75、0.90 g/L的K2FeO4,30 min后测定萘的质量浓度并计算萘降解率,确定K2FeO4的最佳质量浓度。
(2)p H对萘降解率的影响。在温度为25℃的条件下,向溶液的p H分别为3.0、5.0、6.0、7.0、9.0的萘溶液中添加最佳质量浓度的K2FeO4,30 min后测定萘的质量浓度并计算萘降解率,确定最佳p H。
(3)温度对萘降解率的影响。将温度分别调为25、35、45℃,并将萘溶液的p H调至最佳,然后向萘溶液中添加最佳质量浓度的K2Fe O4,30 min后测定萘质量浓度并计算萘降解率,确定最适宜温度。
(4)萘初始质量浓度对萘降解率的影响。在温度为25℃的条件下,将萘溶液的pH调为最佳,向初始质量浓度分别为2.5、5.0、7.5 mg/L的萘溶液中添加最佳质量浓度的K2FeO4,30 min后测定萘质量浓度并计算萘降解率。
1.2.3 多因素实验 萘降解率的主要影响因素为K2Fe O4质量浓度、pH和萘初始质量浓度。利用Design Expert 10.0软件中的Box-Behnken设计三因素三水平实验,以萘降解率为响应值,K2FeO4质量浓度、p H和萘初始质量浓度为自变量,分析实验数据,优化降解条件。表1为响应面的实验因素水平。
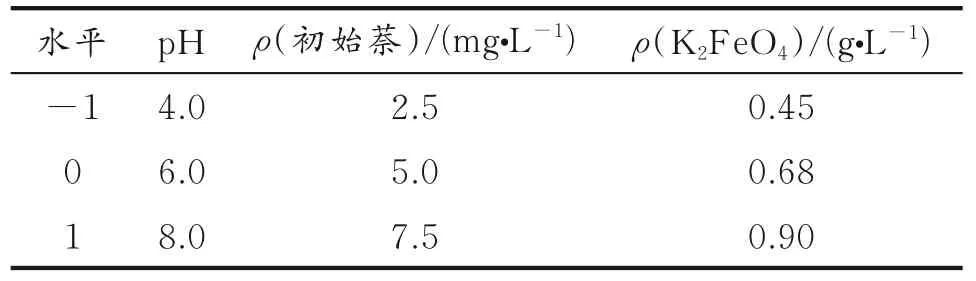
表1 响应面的实验因素水平Table 1 The experimental factor level table of the response surface
2 结果与讨论
2.1 单因素实验
2.1.1 K2FeO4质量浓度对萘降解率的影响 温度为25℃,p H为7.0,K2Fe O4质量浓度分别为0.15、0.30、0.45、0.60、0.75、0.90 g/L时,K2Fe O4质量浓度对萘降解率的影响如图1所示。由图1可知,萘的氧化降解主要发生在前20 min,萘降解率呈先上升后平稳的趋势。加大K2Fe O4质量浓度对萘的降解有促进作用,这是因为K2Fe O4质量浓度越高,Fe O2−4与萘分子的碰撞次数越多,随着K2Fe O4质量浓度从0.15 g/L增加到0.90 g/L,萘的降解率从25.30%提高到78.80%。然而,当K2FeO4质量浓度由0.60 g/L增加至0.75 g/L时,萘降解率仅提高了1.30%;K2FeO4质量浓度由0.75 g/L增加至0.90 g/L时,萘降解率也仅提高1.90%。这可能是因为K2FeO4质量浓度为0.60 g/L时,FeO2−4与萘分子的碰撞次数已达到最多;K2FeO4呈碱性,K2FeO4质量浓度越大,溶液pH越高,且Fe O2−4过于稳定,导致萘降解速率减慢[15]。从经济成本和降解效果考虑,最佳K2FeO4质量浓度为0.60 g/L。

图1 K2 FeO4质量浓度对萘降解率的影响Fig.1 Effect of K2FeO4 mass concentration on the degradation rate of naphthalene
2.1.2 p H对萘降解率的影响 温度为25℃、K2FeO4质量浓度为0.60 g/L,pH分别为3.0、5.0、6.0、7.0、9.0时,p H对萘降解率的影响如图2所示。
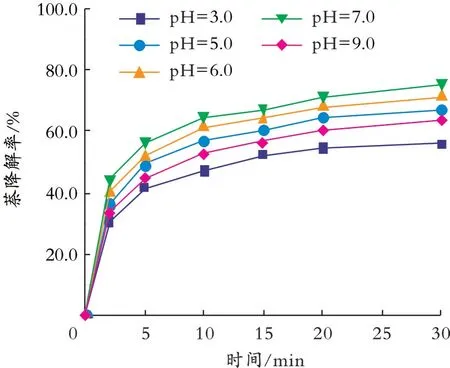
图2 pH对萘降解率的影响Fig.2 The effect of p H on the degradation rate of naphthalene
由图2可知,当萘溶液的p H从3.0增加到7.0时,萘降解率从56.20%增加到75.60%;当p H进一步上升到9.0时,萘降解率却降低到63.50%。这是因为在酸性条件下,K2Fe O4氧化还原电位较高,具有很强的氧化性,但是在强酸性条件下,K2Fe O4具有不稳定性,从而导致部分发生无效分解,Fe以Fe3+的形式存在,影响了萘的降解效果[16]。由图2还可以看出,随着溶液的p H继续增大到9.0时,虽然K2Fe O4稳定性增强,但氧化还原电位较低,氧化能力较差,导致萘降解率下降,故p H为7.0时萘的降解效果最好。
2.1.3 温度对萘降解率的影响 温度分别为25、35、45℃,K2Fe O4质量浓度为0.60 g/L,p H为7.0时,温度对萘降解率的影响如图3所示。由图3可知,随着温度的升高,萘降解率呈先升高后下降的趋势,25℃升高至35℃时,降解率由75.60%升高至76.80%,仅提升了1.20%。这是因为温度升高,K2Fe O4的氧化能力增强[17],升温促进了溶液中的分子间运动,增加了分子间的有效碰撞机率,有助于提高降解率。由图3还可以看出,温度继续升至45℃时,萘降解率逐渐降低至72.70%,说明温度上升破坏了K2Fe O4的稳定性[18],使K2Fe O4自分解成氧化性较低的物质[19],导致萘降解率下降。由此可见,在25~45℃,温度的改变对萘的降解效果影响并不大,故实验选在25℃进行即可。

图3 温度对萘降解率的影响Fig.3 Effect of temperature on the degradation rate of naphthalene
2.1.4 萘初始质量浓度对萘降解率的影响 温度为25℃、p H为7.0,K2FeO4质量浓度为0.60 g/L时,萘初始质量浓度对萘降解率的影响如图4所示。由图4可知,萘初始质量浓度为5.0 mg/L时,萘降解率为75.60%;萘初始质量浓度升高至7.5 mg/L时,萘降解率为60.40%;萘初始质量浓度降低至2.5 mg/L时,萘降解率为88.10%。这是因为溶液中Fe O2−4的质量浓度一定时,提高萘初始质量浓度,增加了FeO2−4周围的萘分子的数量,这虽然增加了与萘接触的机会,但随着反应时间的延长,K2Fe O4被逐渐消耗,溶液中的萘越来越少,与萘的氧化降解反应逐渐减弱;相反,萘初始质量浓度降低,则会增强萘降解率。
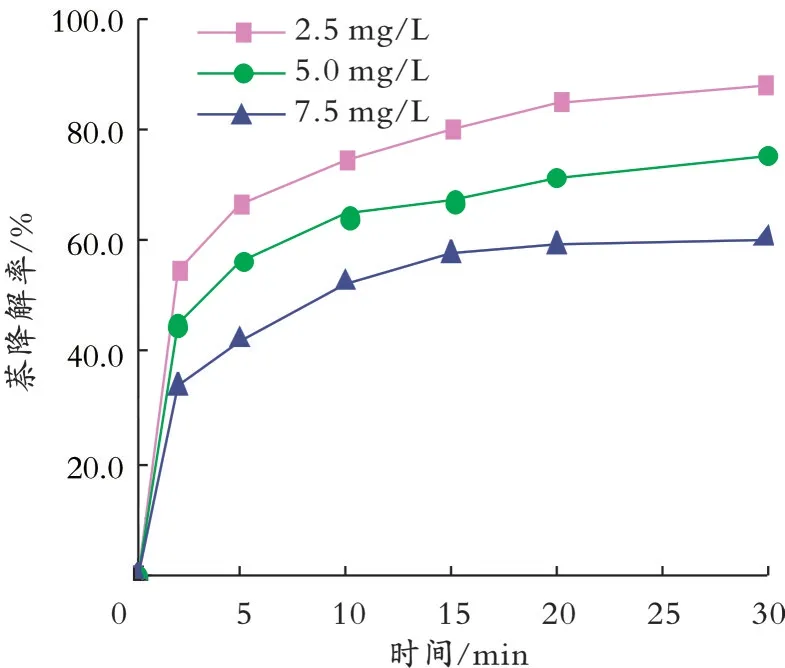
图4 萘初始质量浓度对萘降解率的影响Fig.4 Effect of initial mass concentration of naphthalene on the degradation rate of naphthalene
2.2 多因素实验
2.2.1 模型建立及显著性检验 采用响应面分析法,在反应时间为30 min的条件下,对p H(A)、萘初始质量浓度(B)和K2FeO4质量浓度(C)进行分析,实验结果如表2所示。
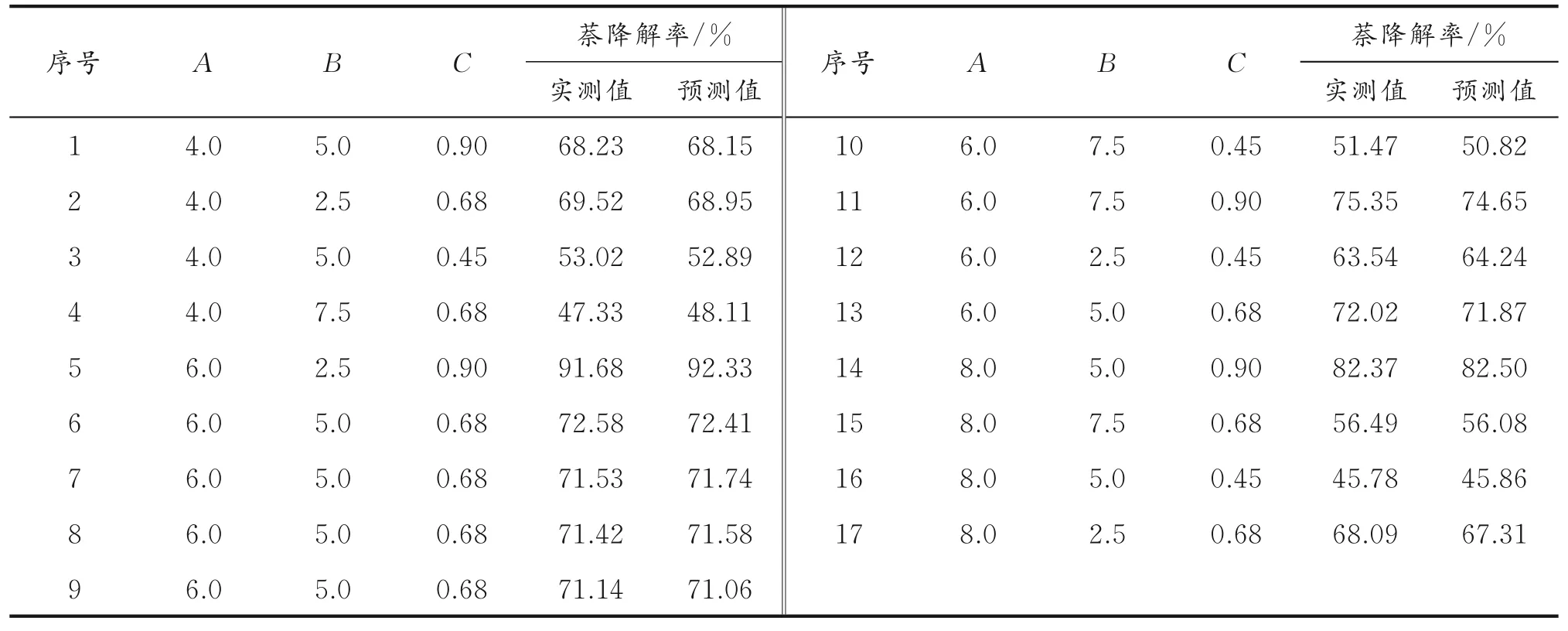
表2 响应面实验结果Table 2 Response surface experimental results
拟合方程为:
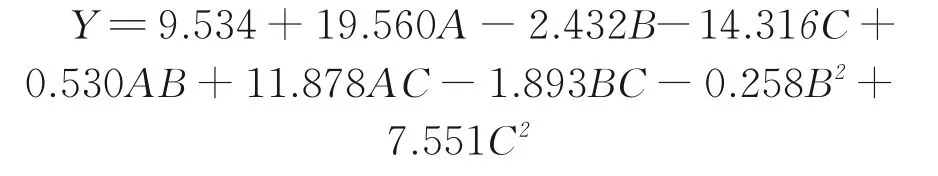
表3为响应面模型方差分析。由表3可知,当模型的P<0.000 1时,此模型高度显著;当失拟项的P>0.050 0时,失拟项不显著。因此,该模型在研究区间拟合良好。R2为0.997 9,接近于1,说明模型有很好的相关性;稳定程度为1.26%,小于10%,说明此模型比较稳定;信噪比为71.589,远大于4,说明此模型可信程度较高。因此,本模型预测pH、K2Fe O4质量浓度和萘初始质量浓度对萘降解率的影响有良好的适应性。由F可知,三个因素对萘降解率的影响程度从大到小的顺序为C>B>A,相互因素对萘降解率的影响程度从大到小的顺序为A C>A B>B C。
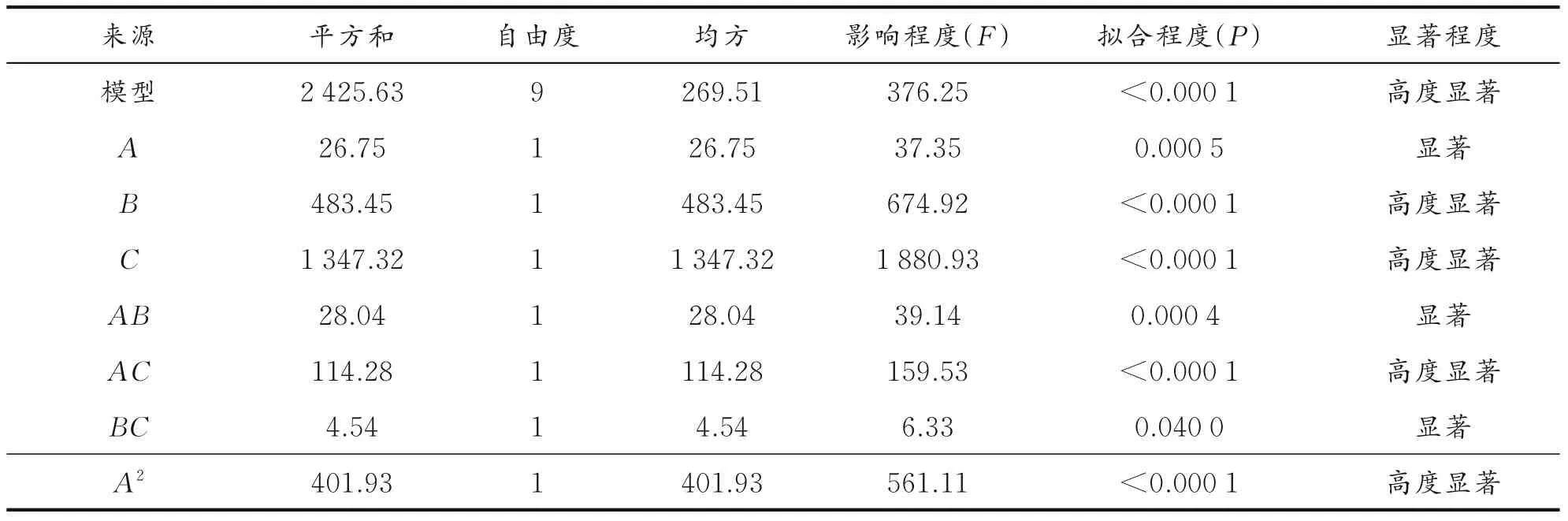
表3 响应面模型方差分析Table 3 Response surface model analysis of variance
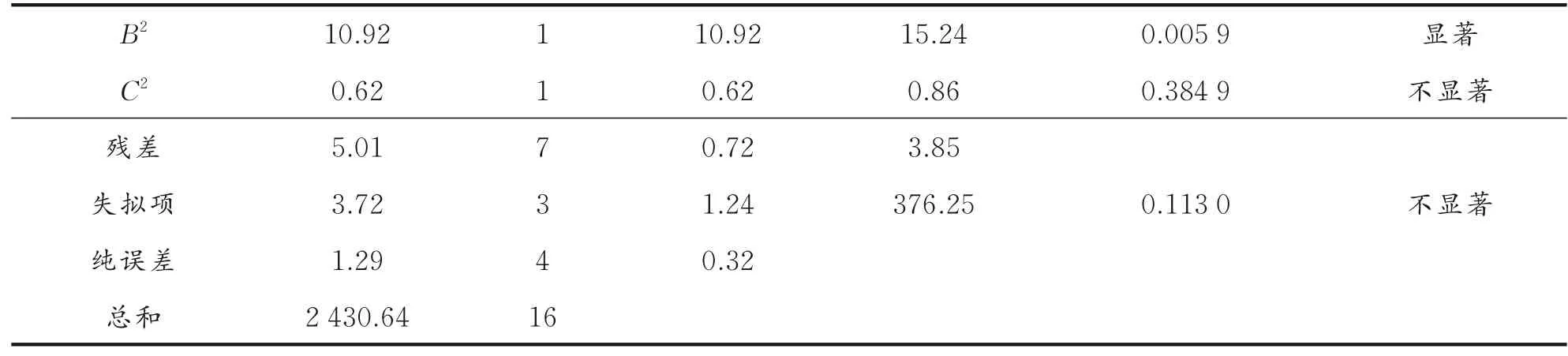
续表3
2.2.2 响应面模型分析 图5为萘初始质量浓度和p H相互作用对萘降解率的影响。由图5可知,响应面平缓;当p H一定时,萘降解率随萘初始质量浓度的增大而减小;当萘初始质量浓度一定时,萘降解率随p H增加先升高后下降。这说明p H在一定范围增加可以提高萘降解率,过高则会抑制萘降解率。由图5还可知,等高线左侧比右侧紧密,当溶液为酸性时萘初始质量浓度对萘降解率影响较大。这是因为K2Fe O4在酸性时易分解,与萘分子接触较少,所以萘初始质量浓度对萘降解率的影响较大。
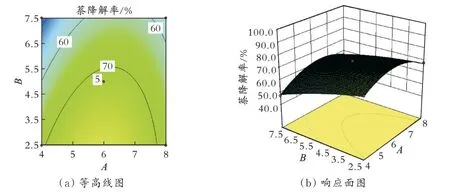
图5 萘初始质量浓度和pH相互作用对萘降解率的影响Fig.5 Effect of initial naphthalene mass concentration and p H interaction on naphthalene degradation rate
图6为K2FeO4质量浓度和pH相互作用对萘降解率的影响。图7为K2Fe O4质量浓度和萘初始质量浓度相互作用对萘降解率的影响。
对比图5和图6可知,图6的响应面较图5陡峭,等高线右侧比左侧紧密。这是因为K2FeO4在偏碱性时稳定,与萘反应更充分,K2FeO4质量浓度影响较大。对比图6和图7可知,图7的响应面较图6陡峭,二者相互作用不明显,等高线在纵坐标方向较为集中,K2FeO4质量浓度一侧坡度较陡,K2Fe O4质量浓度对萘降解率影响较大。由以上分析可知,模型预测K2Fe O4对萘的最佳降解条件:温度为25℃,萘初始质量浓度为2.79 mg/L,p H为6.8,K2Fe O4质量浓度为0.90 g/L,反应时间为30 min;在最佳降解条件下,萘的最高降解率为91.82%。
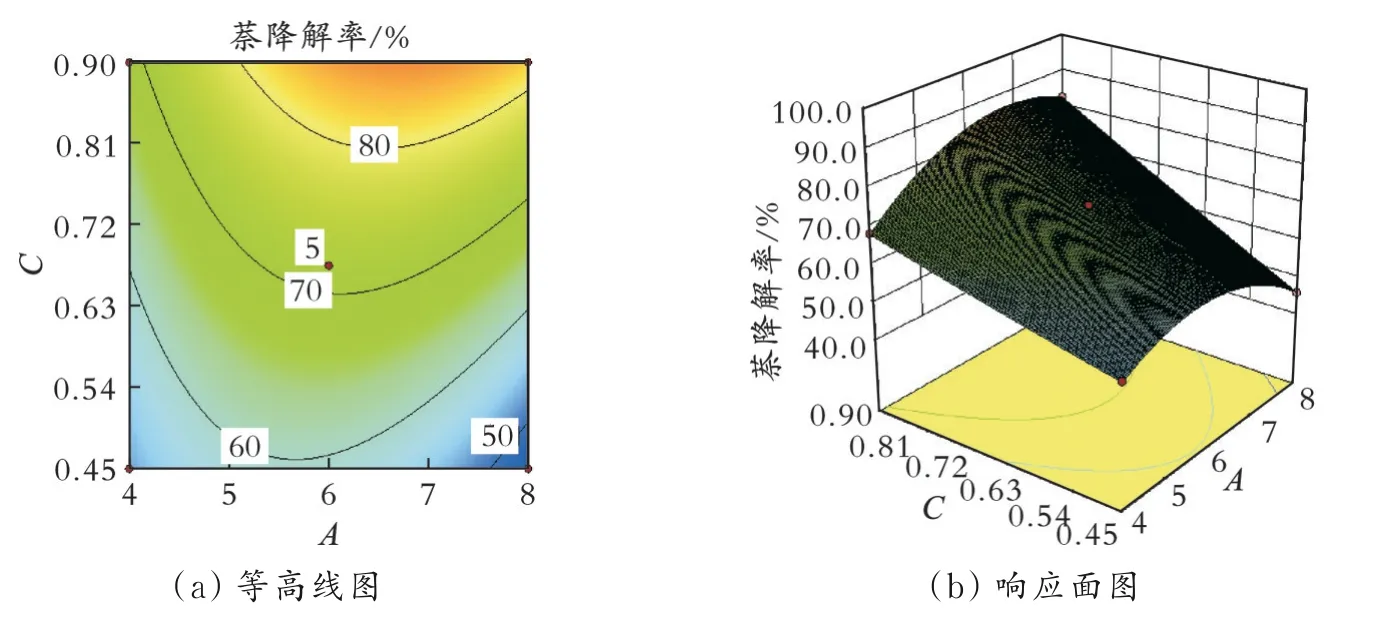
图6 K2Fe O质量浓度和pH相互作用对萘降解率的影响Fig.6 Effect of potassium ferrate dosage and p H interaction on naphthalene degradation rate
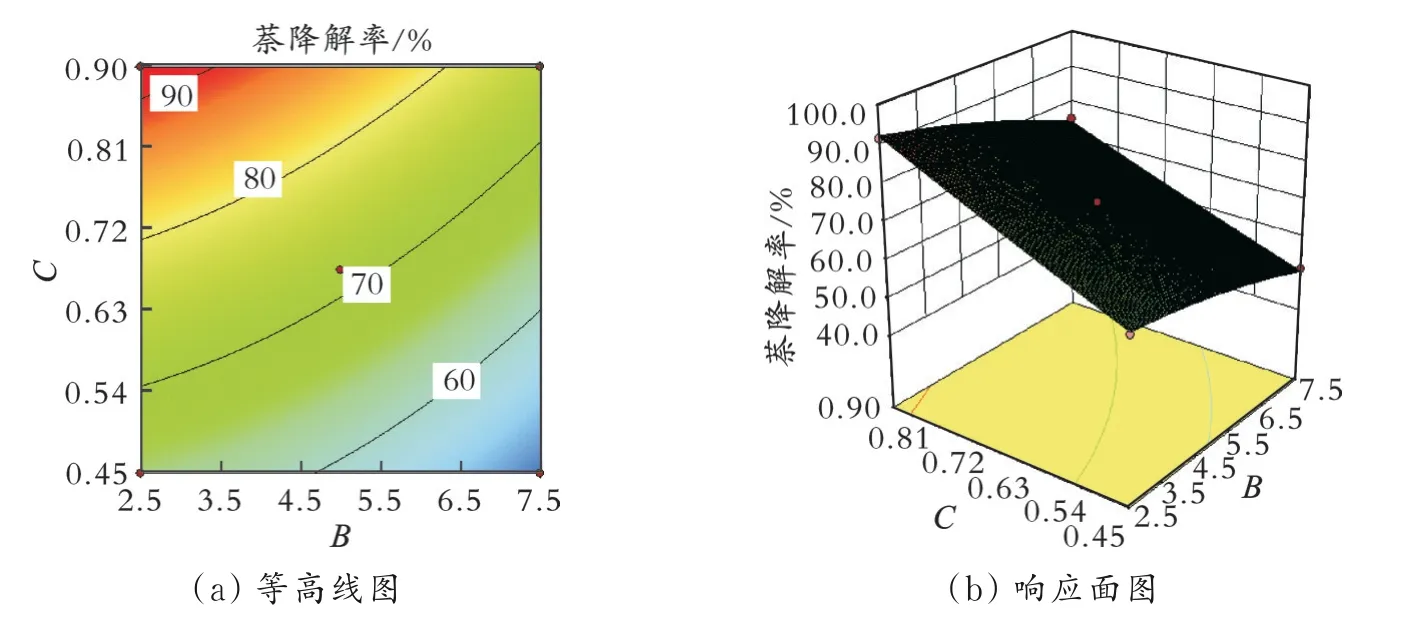
图7 K2Fe O质量浓度和萘初始浓度相互作用对萘降解率的影响Fig.7 Effect of potassium ferrate dosage and initial concentration of naphthalene on the degradation rate of naphthalene
3 结 论
(1)5.0 mg/L萘的最佳降解条件:温度为25℃,p H为7.0,K2FeO4的质量浓度为0.60 g/L,反应时间30 min。在最佳降解条件下,萘的降解率为75.60%。
(2)在单因素实验中,p H(A)、萘初始质量浓度(B)和K2Fe O4质量浓度(C)是影响萘降解率的主要因素,影响程度从大到小的顺序为C>B>A。在多因素实验中,相互因素的影响程度从大到小的顺序为A C>A B>B C。模型预测萘的最佳降解条件:温度为25℃,萘初始质量浓度为2.79 mg/L,pH为6.8,K2FeO4质量浓度为0.90 g/L,反应时间为30 min;在最佳降解条件下,萘的降解率最高为91.82%。研究结果可为治理萘污染的地下水提供基础数据。

