替格瑞洛对轻型急性脑卒中和TIA患者血小板功能的影响
宫垒,孙海英,蒋显锋,宫平,杨学军
急性缺血性脑卒中和短暂性脑缺血发作(TIA)患者再发卒中和心血管事件的风险明显增高[1-2]。快速的评估和有效的抗栓治疗对降低继发性缺血事件和致残性卒中的发生至关重要。目前,阿司匹林联合氯吡格雷已成为标准的抗血小板聚集治疗方案。然而,机体对氯吡格雷的反应性存在个体差异,血小板的低反应性加速动脉粥样硬化的进程,增加缺血性脑血管疾病的复发率和病死率[3]。替格瑞洛为新型P2Y12 受体拮抗剂,目前尚鲜有研究报道机体存在替格瑞洛抵抗。研究表明,急性冠脉综合征患者应用替格瑞洛较氯吡格雷能更有效地抑制血小板功能,降低缺血事件发生率且不增加出血风险[4],但其对轻型急性缺血性脑卒中和TIA患者血小板功能影响的研究仍较少。因此,快速评估替格瑞洛对血小板的影响对降低继发性缺血事件和致残性卒中发生率至关重要。目前快速检测血小板功能的方法较多,包括光学比浊法、维梵纳血小板功能分析仪(VerifyNow 法)检测、血栓弹性描记仪(TEG)检测、Sonoclot凝血与血小板分析法、血小板血管舒张剂刺激磷蛋白(VASP)磷酸化法等。其中,Sonoclot 凝血与血小板分析法是一种简便、快捷的检测全血凝血状态的方法,可用于指导临床抗血小板聚集和抗凝治疗。本研究应用该法检测轻型急性缺血性脑卒中和TIA患者应用替格瑞洛后的血小板功能。
1 对象与方法
1.1 研究对象 选取2018年5月—2020年10月在武警特色医学中心就诊的非心源性轻型急性缺血性脑卒中(美国国立卫生研究院卒中量表NIHSS评分≤5)或TIA(TIA早期卒中风险预测工具ABCD2评分≥6)患者81例,年龄40~75岁。排除标准:(1)拟接受其他特定抗血小板聚集、抗凝治疗。(2)拟行颈动脉、脑血管、冠状动脉重建治疗。(3)对阿司匹林、氯吡格雷、替格瑞洛过敏。(4)有房颤、室壁瘤或怀疑心脏血栓导致的卒中或TIA病史。(5)24 h内接受过静脉溶栓或取栓。(6)有出、凝血功能障碍。(7)肝、肾功能异常。本研究经我院伦理委员会批准,所有患者均签署知情同意书。
1.2 仪器与药物 氯吡格雷片(25 mg/片,深圳信立泰药业,中国);替格瑞洛片(90 mg/片,AstraZeneca AB,瑞典)。Sonoclot 凝血与血小板功能分析仪及含有干粉的检测杯(ADP,Sienco公司,美国)。
1.3 方法
1.3.1 给药方法和标本采集 轻型急性脑卒中或TIA 患者出现症状后的24 h内,采用随机数字表法分为试验组(39例)和对照组(42 例)。试验组入院后予以负荷剂量阿司匹林300 mg 和替格瑞洛片180 mg,第2 天改为阿司匹林100 mg,每日1次,联合替格瑞洛片90 mg,每日2次,21 d后改为替格瑞洛片90 mg,每日2 次,继续观察90 d。对照组入院后予以负荷剂量阿司匹林300 mg和氯吡格雷片300 mg,第2天改为阿司匹林100 mg,每日1次,联合氯吡格雷片75 mg,每日1次,服用21 d后改为氯吡格雷片75 mg,每日1次,继续观察90 d。
所有患者分别于入院时、治疗7 d、治疗90 d 抽取静脉血,测定血细胞各项参数、凝血功能参数、生化指标等。观察发病90 d内主要不良事件,包括脑卒中、心肌梗死、出血等。
1.3.2 Sonoclot 凝血和血小板功能分析 根据Sonoclot 凝血分析仪使用说明进行操作。首先,将蒸馏水加入含有促凝剂腺苷二磷酸(ADP)的检测杯内,37 ℃预热30 s;每0.5 mL 全血加入20µL CaCl2溶液(0.25 mol/L),使抗凝血液再钙化;然后取360µL 再钙化的全血加入检测杯内。分析仪自动记录塑料探针遇到的阻力,标记为凝血信号值与时间曲线图即为Sonoclot 凝血标记曲线,不同颜色图像为不同患者血标本同时检测,见图1。Sonoclot 参数及意义:(1)激活凝血时间(activated clotting time,ACT),血液标本保持液态的时间,即指从探针插入检测杯至纤维蛋白开始形成的时间。(2)凝血速率(clot rate,CR),曲线上升的第1个斜率,反映纤维蛋白的形成速率和纤维蛋白原水平。(3)血小板功能(platelet function,PF),依据血液标本结束液态阶段(纤维蛋白多聚体形成)后凝血收缩的强度及速度计算出的相对值。(4)达峰时间(time to peak,TP),凝血信号曲线达到最高点所需的时间。(5)最大凝血标记值(maximal clot signal,MCS),代表探针遇到的最大阻力值,其高度代表凝血收缩的强度。
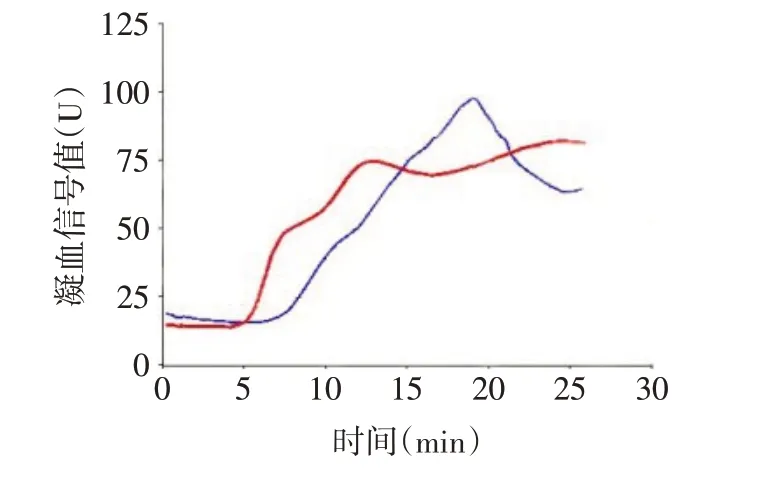
Fig.1 The curve of Sonoclot coagulation analysis图1 Sonoclot凝血标记曲线
1.4 统计学方法 应用Graphpad 6.0软件进行数据分析,计量资料首先进行正态性检验,符合正态分布的计量资料以±s表示,2组间比较采用独立样本t检验,组内比较采用配对t检验或重复测量资料的方差分析;计数资料用例(%)表示,2组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 2组患者临床和实验室指标比较 2 组患者一般临床资料比较差异均无统计学意义(P>0.05),见表1。2 组患者入院和治疗90 d 时血小板计数(PLT)、活化部分凝血酶时间(APTT)、凝血酶原时间(PT)、凝血酶时间(TT)比较差异均无统计学意义(P>0.05),治疗90 d时对照组PLT较入院时降低,试验组PLT、APTT、PT和TT均降低(P<0.05),见表2。
2.2 Sonoclot 凝血和血小板功能指标变化 入院时2 组ACT、CR、PF、TP、MCS 比较差异均无统计学意义(P>0.05);治疗7 d,试验组较对照组ACT、TP 升高,PF 降低(P<0.05);治疗90 d,试验组较对照组ACT升高(P<0.05)。2组在治疗过程中CR、MCS比较差异均无统计学意义(P>0.05)。2 组ACT 和TP均在治疗7 d 和90 d 时较入院时升高,PF 和MCS 降低(P<0.05),见表3。
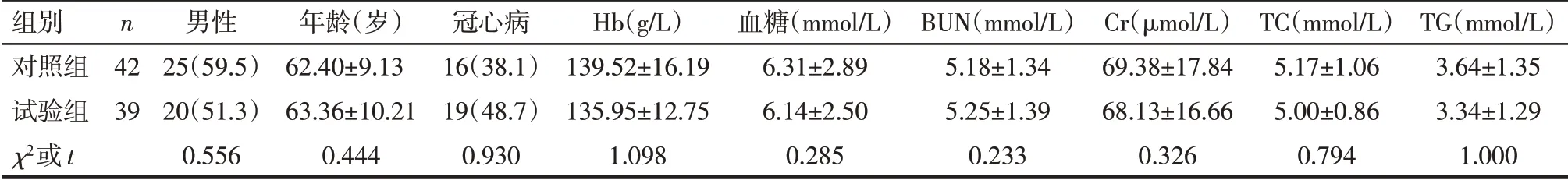
Tab.1 Comparison of baseline data between the two groups of patients表1 2组患者基线临床资料的比较
Tab.2 Comparison of platelet and coagulation indexes at different time points between the two groups表2 2组患者不同时间点血小板和凝血指标比较 (±s)

Tab.2 Comparison of platelet and coagulation indexes at different time points between the two groups表2 2组患者不同时间点血小板和凝血指标比较 (±s)
*P<0.05,**P<0.01。
组别对照组试验组t n 42 39 PLT(×109)入院时202.7±65.05 212.6±53.39 0.739 90 d 183.5±35.20 171.5±29.80 1.637 t 2.610*5.082**APTT(s)入院时34.12±2.53 34.78±2.93 1.092 90 d 33.21±2.54 32.32±3.33 1.348 t 1.776 4.631**PT(s)入院时12.90±1.08 12.96±1.00 0.233 90 d 12.84±0.95 12.59±0.67 1.343 t 1.106 2.402*TT(s)入院时18.08±1.34 18.26±1.54 0.580 90 d 17.67±1.25 17.59±1.18 0.294 t 1.359 3.327**
Tab.3 Comparison of Sonoclot test parameters at different time points between the two groups表3 2组患者Sonoclot检测法各参数不同时间点比较(±s)
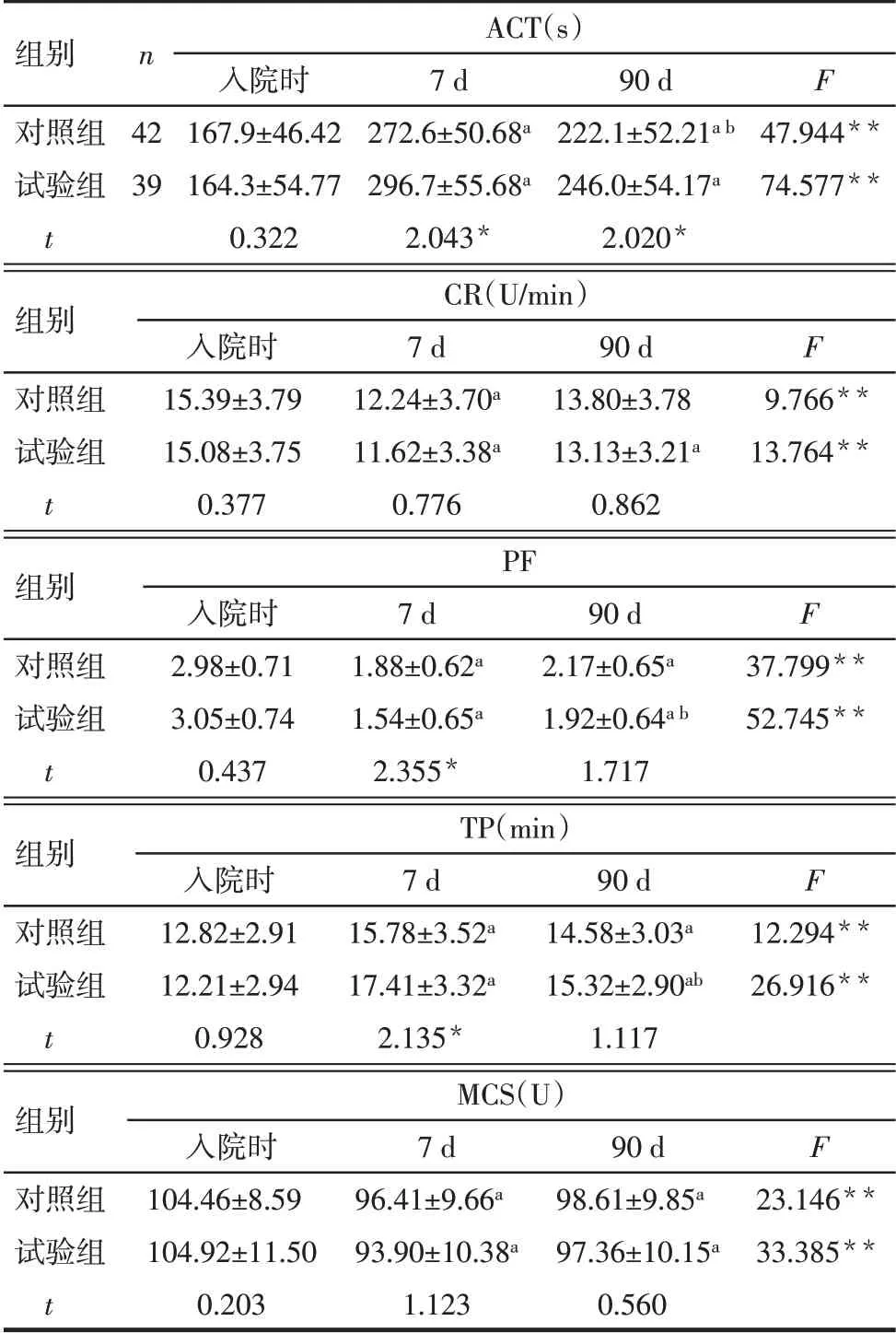
Tab.3 Comparison of Sonoclot test parameters at different time points between the two groups表3 2组患者Sonoclot检测法各参数不同时间点比较(±s)
*P<0.05,**P<0.01;a与入院时比较,b与7 d比较,P<0.05;ACT:F组间=3.826,F时间=74.577**,F交互=1.413;CR:F组间=0.907,F时间=23.502**,F交互=0.178;PF:F组间=3.246,F时间=80.158**,F交互=1.785;TP:F组间=1.211,F时间=39.573**,F交互=2.950;MCS:F组间=0.309,F时间=56.723**,F交互=1.319。
组别对照组试验组t TP(min)入院时12.82±2.91 12.21±2.94 0.928 7 d 15.78±3.52a 17.41±3.32a 2.135*90 d 14.58±3.03a 15.32±2.90ab 1.117 F 12.294**26.916**组别对照组试验组t MCS(U)入院时104.46±8.59 104.92±11.50 0.203 7 d 96.41±9.66a 93.90±10.38a 1.123 90 d 98.61±9.85a 97.36±10.15a 0.560 F 23.146**33.385**组别对照组试验组t PF入院时2.98±0.71 3.05±0.74 0.437 7 d 1.88±0.62a 1.54±0.65a 2.355*90 d 2.17±0.65a 1.92±0.64a b 1.717 F 37.799**52.745**组别对照组试验组t CR(U/min)入院时15.39±3.79 15.08±3.75 0.377 7 d 12.24±3.70a 11.62±3.38a 0.776 90 d 13.80±3.78 13.13±3.21a 0.862 F 9.766**13.764**组别对照组试验组t n 42 39 ACT(s)入院时167.9±46.42 164.3±54.77 0.322 7 d 272.6±50.68a 296.7±55.68a 2.043*90 d 222.1±52.21a b 246.0±54.17a 2.020*F 47.944**74.577**
2.3 2组治疗期间的主要不良事件 治疗期间,2组缺血和出血事件发生率差异均无统计学意义(P>0.05),且2 组出血事件均主要为微出血事件,见表4。
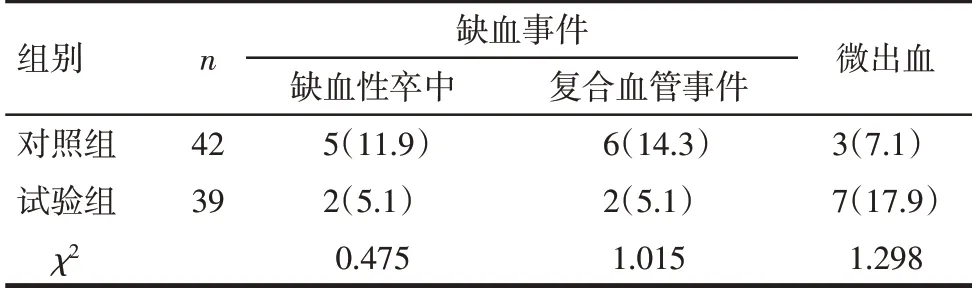
Tab.4 Comparison of major adverse events between the two groups表4 2组主要不良事件比较 [例(%)]
3 讨论
3.1 替格瑞洛的抗血栓作用 急性脑缺血常见的表现为轻型急性缺血性脑卒中或TIA,患者发病后90 d 内再发脑缺血事件的发生率高达10%~15%[5]。阿司匹林联合氯吡格雷双联抗血小板聚集治疗是卒中二级预防的有效策略,但机体对氯吡格雷反应存在个体差异,血小板对氯吡格雷的低反应性增加了心脑血管疾病的复发率及病死率[6-7]。替格瑞洛为不需要代谢活化而快速抑制P2Y12受体的新型抗血小板聚集药物,可更快、更强效地抑制血小板功能,降低缺血事件的发生率,且对血小板的抑制作用具有可逆性。研究显示,在冠心病患者中,替格瑞洛对血小板的抑制效应优于氯吡格雷[4,8],但轻型急性缺血性脑卒中或TIA患者应用替格瑞洛后的临床获益仍需进一步研究。本研究采用凝血和血小板功能分析仪Sonoclot床旁检测全血凝血过程,结果显示试验组在治疗7 d的ACT、TP均显著高于对照组,PF低于对照组,治疗90 d ACT仍显著高于对照组,ACT、PF、TP均能较准确反映血小板功能,以上说明替格瑞洛对血小板的抑制作用起效更快、作用更强。
3.2 替格瑞洛的出血风险 PLATO研究发现,急性冠脉综合征患者应用替格瑞洛相较于氯吡格雷不仅具有较高的血小板抑制率,也能够降低心肌梗死、脑卒中或血管源性死亡的发生率,并且不增加主要出血事件发生率[9]。Johnston 等[1]研究显示替格瑞洛较阿司匹林可更有效地降低脑卒中或TIA患者的主要不良事件的发生率,且不增加主要出血事件,具有良好的临床净获益。双联抗血小板聚集治疗用于轻型卒中或TIA 患者中被证明是安全的,但可增加非颅内出血风险,如皮下出血、牙龈出血、消化道出血等,可能影响医生的决策和降低患者的依从性,需要进一步研究以提高依从性。本研究中试验组出血事件发生率较对照组未见增高,且均为微出血事件,如鼻黏膜、牙龈出血等,说明替格瑞洛治疗轻型急性缺血性脑卒中和TIA 患者并不增加严重出血风险,但对于出血风险较高患者仍需进一步研究。
3.3 Sonoclot 检测的有效性 Sonoclot 凝血和血小板功能分析仪可提供全血在体外的整个凝血过程,其检测参数可反映纤维蛋白原转化为纤维蛋白以及纤维蛋白与血小板的相互作用,因此该检测方法被广泛应用于肝胆外科、心脏外科、神经外科、心内科等[10-11]。Sonoclot检测方法具有所需标本少、时间短等优点,且与临床最常用的血小板检测方法光学比浊法具有良好的相关性[12]。Sonoclot 检测方法同时也能为临床诊断和治疗提供更加精准的技术支持。有研究显示,弥散性血管内凝血患者Sonoclot参数的变化与病死率增高有关,ACT和PF均为30 d生存率的独立预测因素[10]。不稳定型心绞痛患者的ACT、CR 高于稳定型心绞痛患者[13]。本研究2 组对比ACT、PF 和TP 均有显著差异,反映不同药物对患者血小板抑制作用不同。因此,Sonoclot检测法可用于评估替格瑞洛对轻型急性缺血性脑卒中或TIA患者血小板的抑制作用,为临床精准治疗提供支持。但因本研究样本量偏小,其结果尚需更大样本量的研究进一步证实。

