子宫腺肌病对冻融胚胎移植周期妊娠结局的影响
徐士儒,莫美兰,张宏展,耿蔷,周林燕
(深圳中山泌尿外科医院生殖中心,深圳 518000)
子宫腺肌病(AM)是生育年龄妇女的常见病,其引起的月经过多、严重痛经和不孕对患者的身心健康造成严重的影响。2020年《子宫腺肌病诊治中国专家共识》[1]对AM的发病机制、临床表现、分型、诊断及治疗进行了系统阐述和归纳,同时对AM合并不孕的治疗给予了专家建议和指导。共识推荐行辅助生殖技术(ART)助孕的AM患者采用全胚冷冻策略,经药物或保留生育功能手术治疗后,待子宫基本恢复正常或到达可妊娠时限后,行冻融胚胎移植(FET)。该共识推出后AM患者行FET周期逐渐增多,生殖领域学者对AM患者FET周期妊娠结局的影响因素也越来越关注。因此本研究回顾性分析AM患者与不明原因不孕患者FET周期的妊娠结局,以及AM患者不同内膜准备方案的助孕结局,探讨AM对FET周期妊娠结局的主要影响和不同内膜准备方案对AM患者的治疗效果。
资料与方法
一、研究对象
收集2015年1月至2020年12月在我院生殖中心行FET助孕、符合AM诊断的373例患者为AM组,共580个FET周期;收集同期就诊的不明原因不孕患者3 382例为不明原因组,共5 716个FET周期。
纳入标准:(1)经阴道超声诊断为AM患者。AM共8项超声特征,分别为:子宫肌层不对称增厚;子宫肌层囊性灶;岛状高回声信号;扇形阴影;子宫内膜下线状或点状回声;病灶内有条状血流信号穿过;结合带形态不规则;结合带不连续。如超声检查存在2项或2项以上上述征象则诊断AM[2]。(2)不明原因组为未发现明确不孕相关因素的患者;(3)均为FET周期。
排除标准:(1)夫妇双方任意一方染色体异常;(2)合并子宫内膜异位症(EMs)、子宫畸形、子宫肌瘤、宫腔粘连、输卵管积水等器质性病变者;(3)复发性流产患者。
为了减少样本选择偏倚的影响,以使用女方取卵年龄、女方移植年龄、体质量指数(BMI)、不孕年限、内膜厚度、内膜准备方案、胚胎属性、移植胚胎数、移植优胚数作为匹配因素,使用近邻法进行匹配。按照AM组和不明原因组的样本比例1∶3进行倾向性得分匹配,最终确定AM组纳入患者372例(576个周期),不明原因组纳入患者1 343例(1 629个周期)。
进一步根据AM患者的内膜准备方案不同进行分组:使用降调节方案+激素替代周期方案的为降调+替代组(197个周期),单纯使用激素替代周期方案的为替代周期组(244个周期),以及自然周期组(124个周期)。另外有11个周期采用促排卵周期准备内膜,考虑到例数太少会使统计结果产生偏倚,故这11个周期的样本剔除。最终纳入不同内膜准备方案分析的样本为565个周期,比较各组的一般情况及临床结局。
二、研究方法
1.子宫内膜准备方案:对于月经周期正常且排卵规律的患者采用自然周期方案,即根据阴道超声监测情况,当月经天数≥10 d、优势卵泡直径≥18 mm、子宫内膜厚度达到7~8 mm以上时注射HCG(珠海丽珠)10 000 U,HCG注射后第1天口服地屈孕酮片(达芙通,雅培,荷兰)40 mg/d进行黄体转化。排卵后第3天行卵裂期胚胎移植、第5天行囊胚移植。自移植次日改用黄体酮凝胶(雪诺同,默克雪兰诺,瑞士)90 mg/d阴道给药和地屈孕酮片40 mg/d口服。囊胚移植后11 d、卵裂期胚胎移植后13 d测血β-HCG。
对于月经周期不正常或排卵不规律的患者采用替代周期方案,根据FET前是否采用长效促性腺激素释放激素激动剂(GnRH-a)垂体降调节将患者分为降调+替代周期组和替代周期组。(1)降调+替代组:月经第2~3天或黄体中期注射1次GnRH-a(达菲林,辉凌,德国)3.75 mg/d,GnRH-a降调后28 d采用戊酸雌二醇(补佳乐,拜尔,德国)递增方案:口服补佳乐4 mg×5 d,6 mg×5 d,8 mg×5 d,根据内膜情况调整剂量及天数。15 d后B超监测内膜厚度7~8 mm以上时,肌肉注射黄体酮针剂(浙江仙琚制药)60 mg/d至移植日,注射第5天移植卵裂期胚胎,注射第7天行囊胚移植,戊酸雌二醇维持原剂量至验孕日,黄体支持方案同自然周期。(2)替代周期组:单纯采用戊酸雌二醇递增方案,雌、孕激素用药方法及监测时间同降调+替代组。
2.胚胎评分与冷冻标准:使用Peter卵裂期胚胎评分系统结合本中心实际情况制定出取卵后第3天的D3卵裂期胚胎的评分标准:1级:卵裂球数目≥7个,碎片数量≤10%;2级:卵裂球数目≥7个,10%<碎片数量≤20%;3级:卵裂球数目≥7个,碎片数量>20%或5个≤卵裂球数目<7个,碎片数量≤10%;4级:5个≤卵裂球数目<7个,碎片数量>10%或卵裂球数目<5个。根据此评分标准,将1、2级卵裂期胚胎定义为优质胚胎。对于囊胚而言,根据Gardner评分标准,3期及3期以上且内细胞团和滋养层评分不含C级的囊胚为优质胚胎。按本中心常规玻璃化冷冻复苏流程复苏胚胎后行FET。
3.妊娠判断及观察指标:卵裂期胚胎移植后13 d(囊胚移植后11 d)检测血β-HCG,血β-HCG>5 U/L为HCG阳性;胚胎移植后28 d行阴道超声检查见妊娠囊及原始心管搏动或流产、异位妊娠经病理学检查证实妊娠者,确定为临床妊娠;胎龄<12周的妊娠丢失为早期流产;胎龄≥12周且<28周的妊娠丢失为晚期流产;活产儿胎龄≥28周且<37周为早产。
主要观察指标:HCG阳性率(HCG阳性周期数/移植周期数×100%)、临床妊娠率(临床妊娠周期数/移植周期数×100%)、早期流产率(妊娠12周前流产的周期数/临床妊娠周期数×100%)、晚期流产率(妊娠12~28周流产的周期数/临床妊娠周期数×100%)、早产率(胎龄28~37周的活产周期数/活产周期数×100%)、活产率(活产周期数/移植周期数×100%)。
三、统计学处理


结 果
一、两组患者的一般资料比较
本研究最终纳入AM组患者372例(576个周期),不明原因组患者1 343例(1 629个周期)。两组患者的女方取卵年龄、女方移植年龄、BMI、不孕年限、内膜厚度、不同内膜准备方案比例、不同胚胎类型比例、移植胚胎数、移植优胚数均无显著性差异(P>0.05)(表1)。
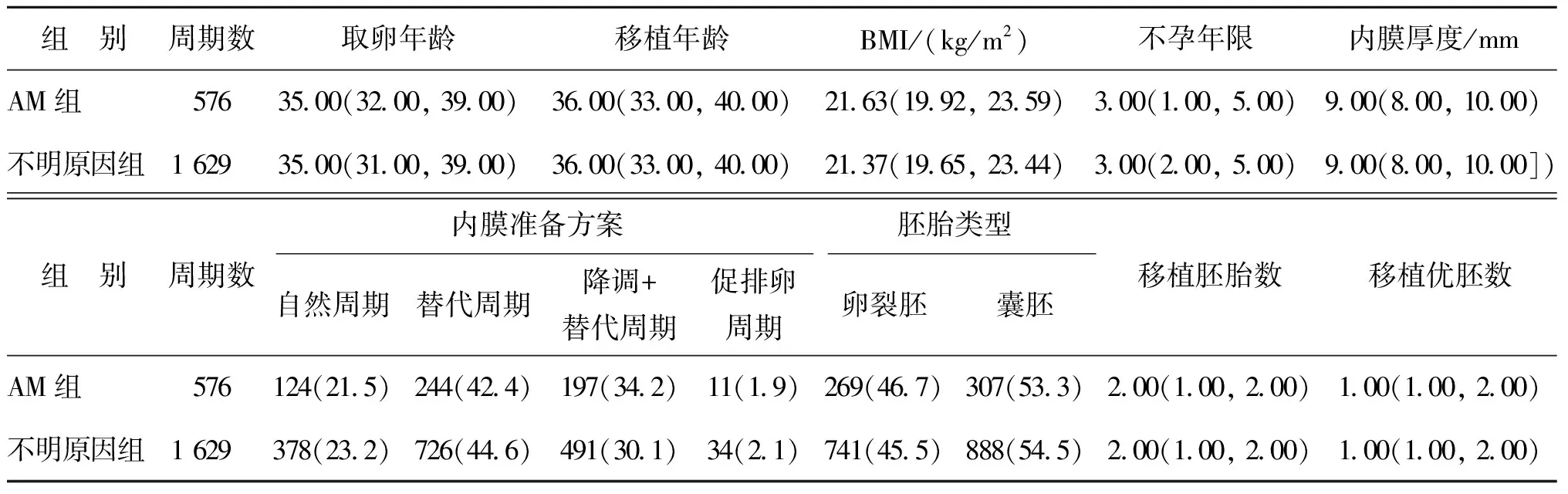
表1 两组患者一般资料比较[M(P25,P75),n(%)]
二、两组患者妊娠结局比较
两组患者的HCG阳性率、临床妊娠率、异位妊娠率、晚期流产率无显著性差异(P>0.05),但AM组的早期流产率、早产率和剖宫产率显著高于不明原因组(P<0.05),活产率显著低于不明原因组(P<0.05)(表2)。

表2 两组患者的妊娠结局比较(%)
三、早期流产率及活产率多因素Logistic回归分析结果
进一步行多因素Logistic回归分析显示,不孕因素、取卵年龄、内膜厚度、内膜准备方案、移植胚胎类型和移植优胚数是早期流产率的独立影响因素(P<0.05),替代周期的早期流产率较自然周期高(OR=1.569,P=0.037),移植卵裂期胚胎的早期流产率较移植囊胚高(OR=1.658,P=0.039)。取卵年龄、内膜厚度、内膜准备方案、移植胚胎类型和移植优胚数为活产率的独立影响因素(P<0.05),替代周期和降调+替代周期准备内膜的活产率较自然周期低(OR分别为0.741和0.742,P<0.05),移植卵裂期胚胎的活产率较移植囊胚低(OR=0.271,P=0.000);AM可能会降低FET周期的活产率,但差异尚未见统计学意义(P=0.05)(表3)。

表3 早期流产率和活产率影响因素的多因素Logistic回归分析
四、AM患者不同内膜准备方案亚组一般资料及妊娠结局比较
对AM组565个周期中不同内膜准备方案3个亚组患者进行比较,取卵年龄、移植年龄、不孕年限、BMI、移植胚胎数等基础资料比较均无显著性差异(P>0.05)(表4)。3个亚组患者的HCG阳性率、临床妊娠率、异位妊娠率、早产率、剖宫产率和活产率均无显著性差异(P>0.05);降调+替代组的早期流产率较替代周期组有降低的趋势(26.2% vs. 40.4%),但尚无显著性差异(P>0.017)(表5)。
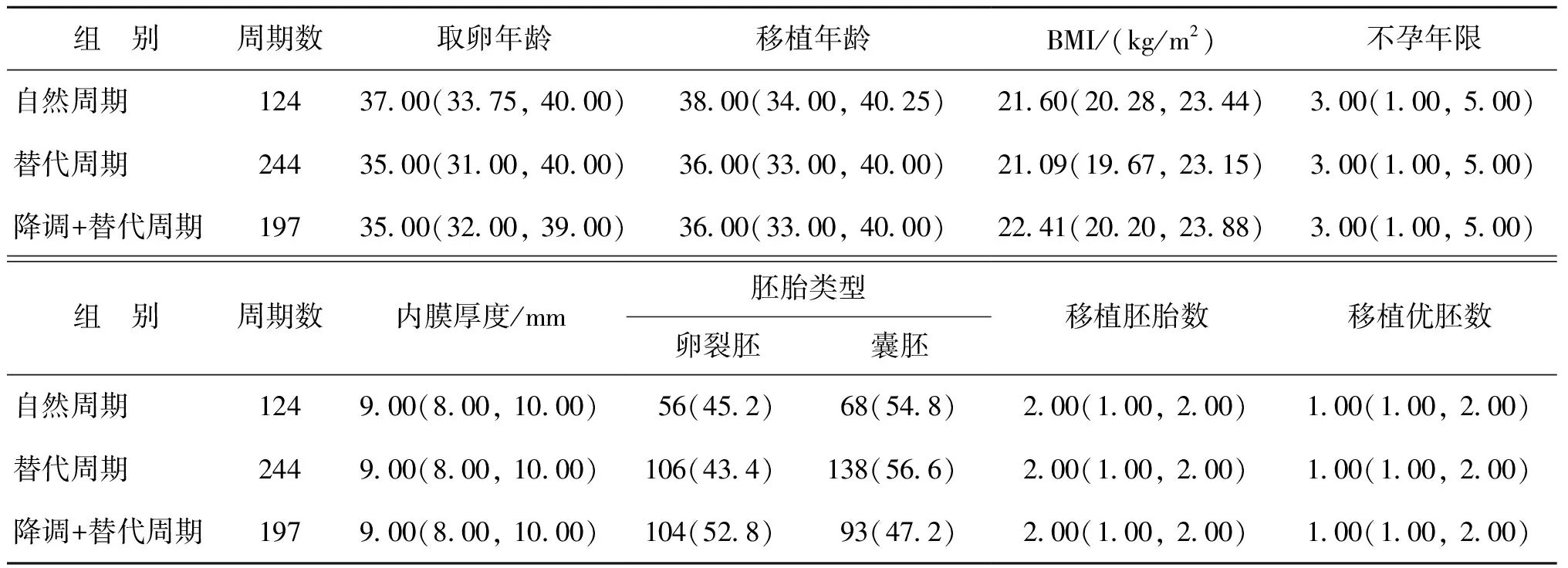
表4 AM患者不同内膜准备方案亚组一般资料比较[M(P25,P75),n(%)]
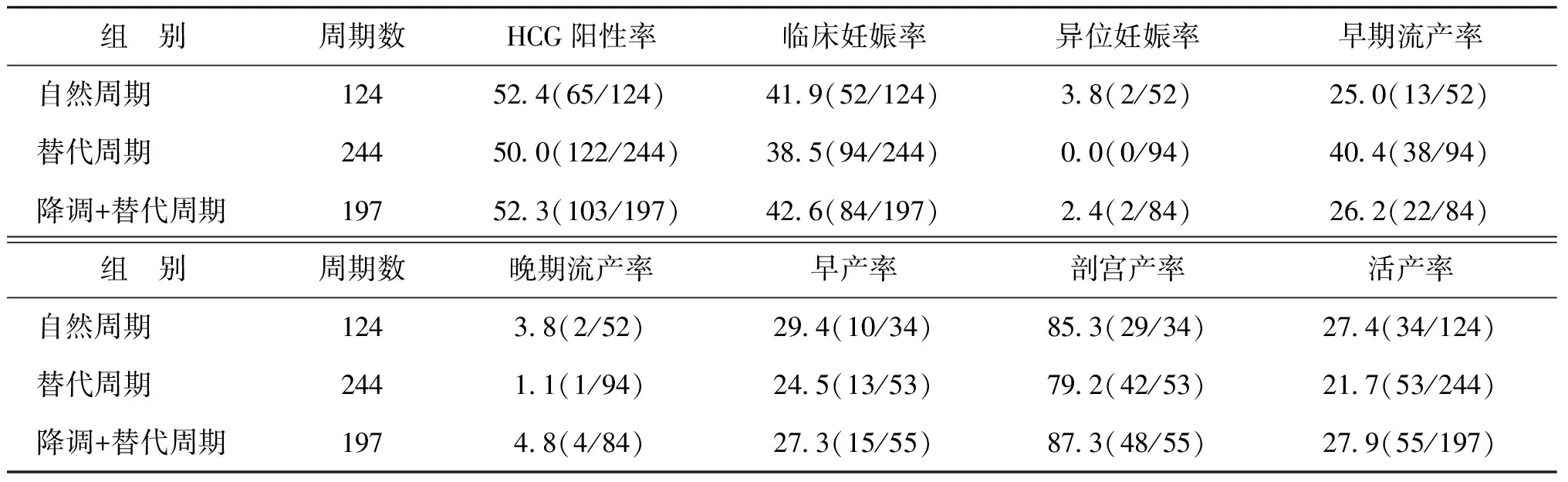
表5 AM患者不同内膜准备方案亚组妊娠结局比较(%)
五、不同内膜准备方案对AM患者早期流产率的多因素Logistic回归分析
考虑到前述分析中早期流产率的组间差别相对较大,故对AM组的早期流产率进一步行多因素Logistic分析显示,内膜厚度是早期流产率的独立影响因素(OR=0.773,P=0.004);不同内膜准备方案对早期流产率的影响未见显著差异(P>0.05),但替代周期组的早期流产率较降调+替代组有升高趋势(表6)。

表6 影响AM患者早期流产率的多因素Logistic回归分析
讨 论
近年来,由于诊断水平的不断提高,越来越多的不孕症患者在诊治过程中被检查出AM,因而AM与不孕症的相关性日益受到重视[3]。AM对生育力会产生不良影响,主要机制包括子宫肌层与内膜基底层结合带功能障碍、子宫内膜容受性改变、雌孕激素受体调节失衡、宫腔氧自由基水平异常、免疫调节紊乱等[4]。AM对IVF-ET的结局也有不良影响,表现为种植率、临床妊娠率、持续妊娠率、活产率下降,流产率升高,早产、胎膜早破等不良产科结局的发生概率明显增加[5]。Sharma等[6]为研究AM对ART结局的影响,回顾性分析EMs组、EMs合并AM组、单纯AM组及输卵管因素不孕组患者的助孕结局,结果显示输卵管因素不孕组与EMs组的临床妊娠率、流产率及活产率无显著性差异(P>0.05),而AM组、EMs合并AM组的活产率显著低于输卵管因素不孕组(P<0.05),因此认为AM会对ART结局产生负面影响。Younes等[7]对11项研究进行Meta分析,最终纳入AM患者519名和对照组1 535名,结果显示AM女性IVF治疗的胚胎植入率、每周期临床妊娠率、持续妊娠率和活产率显著低于对照组(P<0.05),流产率显著高于对照组(P<0.05)。本研究结果发现AM组与不明原因组的HCG阳性率、临床妊娠率、异位妊娠率、晚期流产率均无显著性差异(P>0.05),但AM组的早期流产率、早产率和剖宫产率显著高于不明原因组,活产率显著低于不明原因组(P<0.05),本研究结果与既往多项临床研究[7-9]结论相似。
考虑到FET周期的妊娠率受多方面因素影响,但主要涉及胚胎质量和子宫内膜容受性[10],因此本研究采用倾向性匹配研究方法,尽量减少样本选择偏倚的影响,使数据分析的结论更加可靠。并且本研究进一步对早期流产率和活产率的影响因素进行多因素回归分析,结果显示AM是影响早期流产率的独立影响因素。既往研究显示AM主要通过影响子宫内膜厚度和容受性,导致FET周期早期流产率的增高,AM患者的内膜由于受到肌层腺肌病病灶的压迫变薄,同时宫腔的解剖学变形会扰乱子宫蠕动,而子宫内部肌层,尤其是内膜-肌层交接区,常伴有功能失调的过度蠕动和子宫内压增高,以及子宫肌层超微结构异常引起正常肌细胞收缩性紊乱,随后丧失正常的节律性收缩,进而影响早期胚胎的着床和继续发育,导致早期流产率和异位妊娠率明显增加[11]。本研究多因素回归分析的结果也显示内膜厚度是影响早期流产率和活产率的独立影响因素(P<0.05)。
2021年《子宫腺肌病伴不孕症诊疗中国专家共识》[2]指出AM患者FET前建议进行预处理;多数学者建议应用≥1支长效GnRH-a进行预处理,GnRH-a降调节比非降调节激素替代周期FET有较高的种植率、临床妊娠率和持续妊娠率。GnRH-a治疗通过缩小子宫体积、减轻炎症、改善免疫功能、提高子宫内膜容受性,达到改善生育的目的[12-13]。2013年有学者比较了AM患者行降调+人工周期与单纯人工周期内膜准备方案的FET临床结局,结果显示降调+人工周期组的胚胎种植率、临床妊娠率分别为28.37%(61/215)、48.11%(51/106),显著高于单纯人工周期组[分别为19.14%(31/162)、31.65%(25/79)](P<0.05),而流产率两组比较无显著性差异(P>0.05)[14-15]。Younes[7]等对AM患者IVF治疗结局进行系统评价和荟萃分析表明,IVF治疗前使用GnRH-a降调节能明显提高妊娠率(P<0.05)。既往也有Meta分析结果表明,IVF前采用GnRH-a垂体降调3~6个月,可使EMs和AM患者临床妊娠率增加4倍[16]。本研究根据AM患者内膜准备方案的不同分为降调+替代周期、替代周期和自然周期3个亚组进行比较,3组患者的一般情况、HCG阳性率、临床妊娠率和活产率均无显著性差异(P>0.05)。降调+替代周期组的早期流产率较替代周期组有降低趋势,但尚无显著性差异(P>0.017)。进一步对AM患者早期流产率的影响因素进行多因素回归分析显示,不同内膜准备方案对早期流产率的影响未见显著性差异(P>0.05),这与既往多项研究结果[17-20]不相符,可能与治疗的具体操作有关,2020年《子宫腺肌病诊治中国专家共识》[1]发表之前,本中心对AM患者降调+替代周期的内膜准备方案为仅注射1次GnRH-a后即开始进行替代周期,并没有根据子宫缩小程度来决定GnRH-a降调的次数以及激素替代开始的时间,因此可能尚未达到较好的治疗效果,导致该方案降低早期流产率的效果不明显。AM合并不孕患者在实施FET前,有无最佳的内膜准备方案来改善妊娠结局,是临床医生们所关注的焦点。在2021年的《子宫腺肌病伴不孕症诊疗中国专家共识》[2]中也明确指出:对于年龄>35岁或伴有卵巢储备下降或合并其他不孕因素者,建议先行积累冻存胚胎,后续GnRH-a治疗3~6个月,待子宫体积接近正常再行FET;如经GnRH-a治疗3~6个月后子宫体积或腺肌瘤体积缩小不理想,可改行保守性手术加GnRH-a治疗3~6个月或更长时间,待子宫体积恢复接近正常及子宫瘢痕修复后行FET。既往研究均只比较AM患者降调+替代周期和单纯替代周期FET的结局,目前仍无相关研究分析注射GnRH-a不同次数对FET结局的影响,后续应进一步完善研究设计对相关问题加以探讨。
FET周期的妊娠率受多方面因素影响,本研究结果显示,除了不孕因素及内膜准备方案外,子宫内膜厚度、移植胚胎类型、移植优胚数均是早期流产率和活产率的独立影响因素,这也进一步证实胚胎质量和子宫内膜容受性对FET妊娠结局的影响。既往也有研究证实女性年龄对FET妊娠结局起关键作用[21],本研究结果也显示女方取卵年龄是FET周期早期流产率和活产率的独立影响因素。
综上所述,本倾向性匹配研究结果显示AM患者FET周期早期流产率、早产率、剖宫产率明显升高,活产率明显降低;进一步对AM患者不同内膜准备方案进行分析显示,仅注射1次GnRH-a后直接进行激素替代内膜准备对改善AM患者FET妊娠结局效果不佳,临床医生应根据子宫体积缩小的情况来决定GnRH-a的注射次数和方案选择。但因为本研究是回顾性分析,研究性质限制了研究结论的总体概括性,且该研究未对AM患者亚型以及子宫大小进行分层分析,可能造成结论偏倚;未来还需要开展多中心大样本量的前瞻性随机对照研究探讨不同分型AM患者的最佳治疗方案。

