不同内膜准备方案在OHSS高风险患者首次FET中的应用比较
苏宁 夏薇 王维 何燕
广州市第一人民医院生殖健康与不孕症专科,广州 510180
冻融胚胎移植(FET)因能增加体外受精-胚胎移植(IVF-ET)及其衍生技术的累积妊娠率而被广泛应用[1-2],通过该项技术出生的子代数量逐年增加[3]。尤其是对有卵巢过度刺激综合征(OHSS)高风险的患者,越来越多的专家共识以及治疗指南建议进行全胚冷冻,其后采用FET 助孕,以改善妊娠结局,降低治疗风险[4-6]。
影响FET 临床妊娠率因素包括胚胎质量、子宫内膜容受性和内膜与胚胎的同步性。其中,内膜准备方案是影响内膜容受性和内膜与胚胎同步性的重要因素。临床常用的内膜准备方案包括自然周期(NC)方案、激素替代周期(HRT)方案、促排卵周期方案和降调节(GnRHa)+HRT周期方案。对于OHSS 高风险患者首次FET 应该采用哪种内膜准备方案尚无统一定论,给临床诊疗带来一定困惑。本研究回顾性分析广州市第一人民医院生殖健康与不孕症专科2019 年1 月至2020 年10 月收治的35 岁以下不孕女性患者行IVF-ET 助孕治疗,因OHSS高风险全胚冷冻首次行FET,3种内膜准备方案对FET周期治疗结局的影响,总结如下。
资料与方法
1、一般资料
选择2019 年1 月至2020 年10 月在广州市第一人民医院生殖健康与不孕症专科行IVF-ET 助孕、因OHSS 高风险行全胚冷冻者共226 名。OHSS 高风险患者纳入标准:所有患者均采用黄体中期短效长方案促排,扳机日雌二醇(E2)≥6 500 pg/ml,或获卵数≥20 个,或在移植日出现腹胀、少尿,血象显示高凝状态,B 超显示患者有腹水、双侧卵巢体积明显增大的患者。排除标准:因其他因素如子宫内膜因素、输卵管积水、扳机日孕酮(P)≥1.5 μg/L、微刺激方案促排、黄体期方案促排或个人因素等原因行全胚冷冻者。根据FET 周期内膜准备方案分为:自然周期(NC)组74 名,激素替代周期(HRT)组108名,GnRHa+HRT 组44名。因促排卵周期方案在本中心应用较少,未纳入统计分析。
本研究获广州市第一人民医院伦理委员会批准实施(K-2021-152-01)。
2、研究方法
2.1、促排卵方案 月经黄体中期给予短效GnRHa(德国辉凌制药有限公司提供,批准文号H20100365,0.1 mg/支),0.10 mg皮下注射共10 d,其后0.05 mg皮下注射共4 d,达到降调标准后给予人促卵泡激素(FSH)(意大利Merck Serono S.P.A.提供,批准文号S20160040,450 IU/支;丽珠集团丽珠制药厂提供,国药准字H20052130,75 IU/支)注射。阴道B超监测卵泡发育情况,当有1个卵泡直径达20 mm 或2个达18 mm 或3个达17 mm 时肌肉注射绒促性腺素(HCG)(丽珠集团丽珠制药厂提供,国药准字H44020673,2 000单位/支)4 000~6 000 IU 或皮下注射重组人绒促性素(意大利Merck Serono S.P.A.提供,批准文号S20110045,250 μg/支)250 μg,36~38 h 后经阴道取卵,采用IVF/ICSI 技术进行受精,D3胚胎评分标准参照Peter[7]方法,D5/D6囊胚的评分采用Gardner[8]评分,胚胎均采用快速玻璃化冷冻方法进行冷冻保存。
2.2、FET子宫内膜准备
2.2.1、NC 方案适用于月经周期规律且排卵正常的患者。通常在月经周期的第8~10 天开始阴道超声监测卵泡发育和排卵情况。依据卵泡发育情况、子宫内膜形态和促黄体生成素(LH)峰出现的时间决定胚胎移植时间。当主导卵泡直径14~15 mm 时开始测尿LH,尿LH 峰出现当天抽血检查LH、E2、P,B 超显示排卵为D0;卵泡发育到18 mm未测出LH 峰,可肌注HCG 5 000~10 000 IU,以注射HCG日次日为D0;若该周期有LH峰出现但未排卵,而P有升高,提示卵泡未破裂黄素化,以LH 出峰次日为D0。D3 行卵裂期胚胎移植,D5 行囊胚移植。黄体支持治疗给予黄体酮胶囊口服(浙江仙琚制药股份有限公司提供,国药准字H20041902,50 mg/粒),每天2 次,每次150 mg;联合HCG 肌肉注射2 000 IU,隔天1次,共6次。
2.2.2、HRT 方案适用于月经不规则、排卵障碍、子宫内膜薄、自然周期FET 失败或无法监测排卵的患者。采用雌二醇片/雌二醇地屈孕酮片恒量方案:从月经来潮第3 天起每天口服E2(由荷兰Abbott Biologicals B.V.提供,注册证号H20150345,2 mg/片)1片,每天3次,连用12 d后开始B超监测内膜。当用药时间≥12 d,内膜≥8 mm,E2≥200 pg/ml,则给予孕激素转化内膜,E2+地屈孕酮(由荷兰Abbott Biologicals B.V.提供,注册证号H20150345,E22 mg 和地屈孕酮10 mg)1片,每天3次,联合黄体酮注射液(广州白云山明兴制药有限公司提供,国药准字H44020229,20 mg/支)60 mg/d 或者黄体酮阴道缓释凝胶(由英国Fleet laboratories limited 提供,国药准字H20140552,90 mg/支)90 mg/d,连续使用14 d。在内膜转化的第4天移植D3卵裂期胚胎,第5天移植囊胚。
2.2.3、GnRH-a+HRT方案适用于子宫内膜异位症、子宫腺肌症、反复种植失败、子宫内膜薄或其他方案均未能成功妊娠的患者。月经来潮第2~3 天给予GnRH-a(由阿斯利康制药有限公司提供,国药准字J20160091,3.6 mg/支;由法国Ipsen Pharma Biotech 提供,批准文号:H20090274,3.75 mg/支),必要时可重复注射2~3次,末次注射后14 d抽血测FSH、LH 和E2,达到降调标准后给予HRT 方案进行内膜准备,方法同HRT周期冻融胚胎移植。
3、观察指标
比较分析3 组患者妊娠结局的指标:临床妊娠率、胚胎种植率、早期流产率、异位妊娠率以及多胎妊娠率等情况。临床妊娠的判断标准:胚胎移植后28 d B 超显示妊娠囊者确定为临床妊娠(包括异位妊娠)。
4、统计学分析
采用SPSS 23.0 统计学软件进行统计学分析,符合正态分布的计量资料用()表示,采用单因素方差分析,计数资料用例(%)表示,采用χ2检验,P<0.05 时为差异有统计学意义。
结果
1、3 组患者一般情况比较
3 组患者平均年龄、不孕年限、体质量指数(BMI)、平均移植胚胎数、胚胎种植率差异均无统计学意义(均P>0.05)。基础性激素以及AMH 比较差异均无统计学意义(均P>0.05)。HRT 组基础FSH 水平高于NC 组,移植日子宫内膜厚度明显低于NC 组和GnRHa+HRT 组(均P<0.05),NC 组和GnRHa+HRT 组差异无统计学意义(P>0.05)。HRT 组囊胚所占比例HRT 组明显高于NC 组(P<0.05),NC 组和GnRHa+HRT组差异无统计学意义(P>0.05)。见表1。
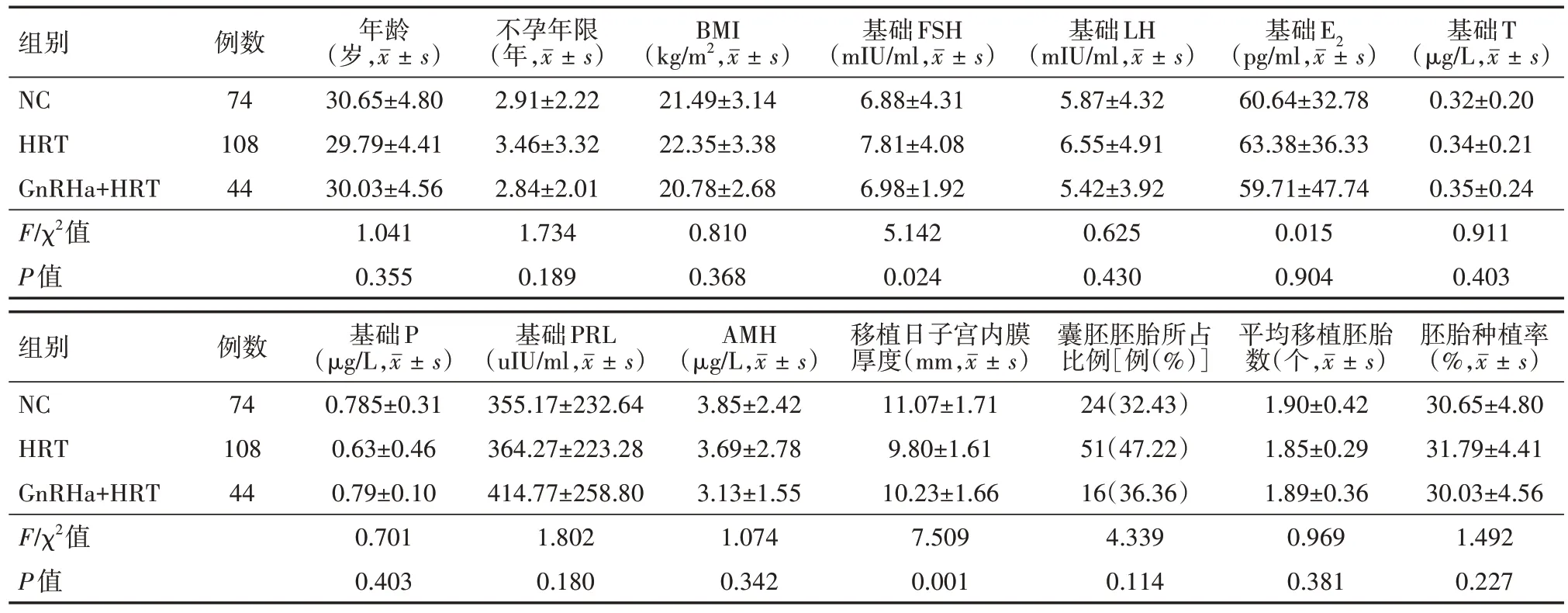
表1 3组行体外受精-胚胎移植、因卵巢过度刺激综合征高风险行全胚冷冻患者的一般情况比较
2、3 组患者妊娠结局比较
3组患者的临床妊娠率、异位妊娠率、早期流产率、多胎妊娠率比较差异均无统计学意义(均P>0.05),见表2。
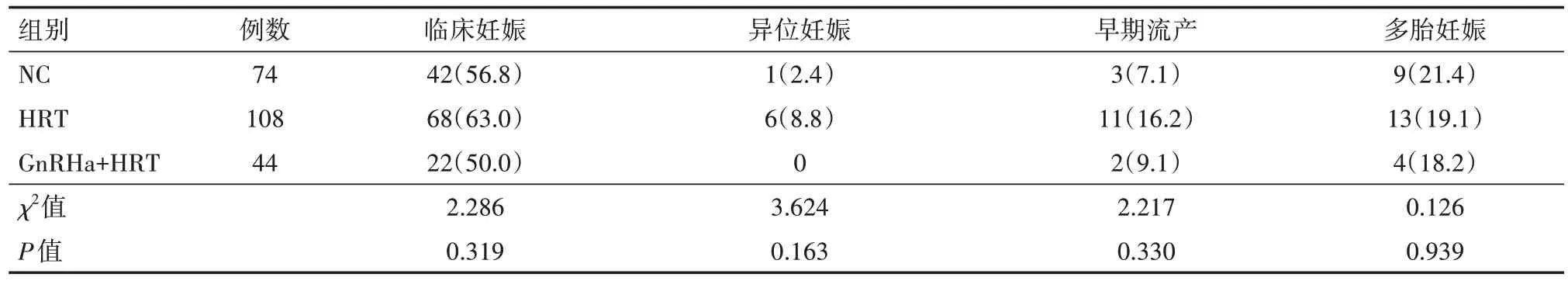
表2 3组行体外受精-胚胎移植、因卵巢过度刺激综合征高风险行全胚冷冻患者的妊娠结局比较[例(%)]
讨论
随着辅助生殖技术(ART)的发展和胚胎冻存技术的不断提高,FET 已成为IVF 治疗的重要组成部分[9]。控制性卵巢刺激(COS)周期中高水平E2有可能导致子宫内膜种植窗提前关闭,从而影响子宫内膜容受性[10],尤其是伴有OHSS高风险的患者,卵巢刺激周期中E2水平更高,越来越多的临床共识建议OHSS 高风险患者进行全胚冷冻以改善治疗结局,降低治疗风险[11-12]。
胚胎质量和子宫内膜容受性是胚胎种植的关键因素[13]。胚胎质量主要取决于新鲜周期COS过程及实验室胚胎培养,因此要改善FET 治疗结局,选择合适的子宫内膜准备方法和黄体支持方案就显得尤为重要[14]。临床上常用的FET 周期内膜准备方案各有优缺点,需针对不同人群的特点进行选择。NC 方案子宫内膜变化最符合生理状态,用药少,花费低,多用于月经周期规律且能监测卵泡发育的患者,如采用HCG 诱导排卵,则HCG 注射后3~5 d 移植卵裂期胚胎和5~7 d 移植囊胚期胚胎均可取得相似的临床结局[15]。但由于需多次进行超声检查,增加患者来院次数,不能灵活安排就诊和胚胎移植时间,容易因无优势卵泡生长、卵泡黄素化等原因取消周期[16-17]。HRT 方案内膜发育均由外源性雌孕激素调控,可以灵活安排就诊计划,复诊次数少,多用于排卵障碍、内膜薄、既往自然周期失败、无法回院监测排卵的患者,但是外源性的雌激素可能影响子宫内膜容受性,改变患者种植窗从而导致着床失败[18],同时也要警惕雌孕激素带来的不良反应和相关风险。降调节激素替代周期是先给予GnRHa 降调节预处理,后期再采用HRT 方案准备内膜,由于降调节可能提高子宫内膜容受性,避免内源性LH 的影响,在临床上多用于子宫内膜异位症、子宫腺肌病、多囊卵巢综合征、反复种植失败、薄型内膜、高龄患者或其他方案均未能成功妊娠的患者[19-26]。有meta 分析认为,目前尚无证据表明哪一种内膜准备方案更有优势[27]。
本研究显示,OHSS 高风险患者全胚冷冻后首次FET 采用3 种内膜准备方案,HRT 组患者移植日子宫内膜最薄,明显低于NC 组,与GnRHa+HRT 组相比差异无统计学意义(P>0.05),但HRT 组临床妊娠率最高,为63.0%,NC 组为56.8%,GnRHa+HRT 组为50.0%,3 组之间比较差异无统计学意义(P>0.05)。HRT 组移植日子宫内膜最薄但临床妊娠率最高,可能原因为:其一,虽然HRT 组移植日子宫内膜最薄,但平均为9.80 mm,已经满足胚胎着床的要求。研究发现,新鲜周期移植前内膜厚度≥8 mm、FET 周期内膜≥7 mm,常预示着较好的妊娠结局[28-29]。其二,HRT 组移植囊胚比例为47.22%,明显高于NC 组,差异有统计学意义。胚胎种植率HRT 组为31.79%,高于NC 组的30.65%和GnRHa+HRT 组的30.03%,平均移植胚胎数HRT 组为1.85 个,低于NC 组的1.90 个和GnRHa+HRT 组的1.89 个。由于HRT 组囊胚移植比例高,胚胎种植率高,虽然移植胚胎数量少,但仍然取得63.0%的临床妊娠率。3组之间临床妊娠率、异位妊娠率、早期流产率、多胎妊娠率均差异均无统计学意义(均P>0.05),与其他研究结论一致[30]。
由于本研究是一项回顾性研究,FET 内膜准备方案均根据患者自身特点选择,在治疗经过上缺乏均一性,因此还不能得出对于OHSS 高风险患者全胚冷冻后首次FET 采用HRT 方案更优的结论。GnRHa+HRT 临床妊娠率为50.0%,低于HRT 组的63.0%和NC 组的56.8%,但差异无统计学意义(P>0.05),可能与样本量少、患者疾病特点不同有关,在后期研究中可以扩大样本量、选择单一疾病进行治疗方案优劣性的比较。
综上所述,OHSS 高风险患者全胚冷冻后首次FET 3 种子宫内膜准备方案均可获得较好的临床结局,可根据病情、患者及医生的时间安排等选择合适的内膜准备方案。
利益冲突所有作者均声明不存在利益冲突

