经脐单孔腹腔镜全子宫切除手术的临床研究
杨聪 苑中甫 贾丛
郑州大学第一附属医院妇科 郑州 450052
经自然腔道内镜手术(natural orifice transluminal endoscopic surgery,NOTES)是不在腹壁做切口,通过胃、直肠或阴道等自然腔道的合适位置,应用内镜切开进入腹腔实施手术。多用于胆囊、阑尾、结肠、子宫等病变的手术[1]。其中经脐单孔腹腔镜手术(transumbilical 1aparoendoscopic single-site surgery,TU-LESS)作为由传统腹腔镜手术到经阴道自然腔道内镜手术(V-NOTES)之间的过渡方式,通过单一脐部小戳孔进行手术,即可基本达到“无瘢痕”效果,满足更多患者的需求;又可减少经阴道手术引起的上行感染。本研究通过对150例行腹腔镜全子宫切除术患者的临床资料进行分析,以探讨TU-LESS全子宫切除术的临床价值。
1 资料与方法
1.1一般资料回顾性分析2019-05—2021-07我院妇科行腹腔镜全子宫切除术的150例患者的临床资料。纳入标准:(1) 无生育要求,因妇科良性疾病、子宫内膜癌前病变,以及宫颈高级别病变行择期全子宫切除术的患者。(2)均由同一组腔镜手术医师成功实施手术。(3)术后病理检查结果均为非恶性病变。排除标准:(1)患有其他恶性肿瘤、自身免疫性疾病,以及无法耐受麻醉的患者。(2)长期服用抗凝药物、有精神性疾病的患者。(3)临床资料不完整。根据不同手术方法分为3组。A组41例,TU-LESS全子宫切除术后于腹腔镜下缝合阴道残端。B组34例,TU-LESS全子宫切除术后经阴道缝合阴道残端。C组75例,行传统多孔腹腔镜全子宫切除后在腹腔镜下缝合阴道残端。3 组患者间的一般资料差异均无统计学意义(P>0.05),见表1。患者均签署知情同意书。

表1 3组患者的一般资料比较
1.2手术方法常规腹腔镜术前准备,气管插管全麻,消毒、铺巾。患者取头低臀高截石位,放置举宫杯。TU-LESS全子宫切除术:于脐部做一长约2.5 cm的纵切口,逐层切开进入腹腔,置入单孔三通道腹腔镜穿刺套管(3个孔道的直径分别为10 mm、5 mm、5 mm)。建立CO2气腹,腹腔镜探查盆(腹)腔。双极钳依次电凝切断子宫两侧的圆韧带、输卵管的间质部,以及卵巢固有韧带。沿圆韧带断端剪开阔韧带前叶至膀胱折返处,打开反折腹膜,分离下推膀胱至宫颈外口。超声刀将两侧的子宫主血管、子宫主韧带,以及骶韧带依次电凝切断。在举宫杯的指引下,电钩环切阴道穹窿一周,将整个子宫与阴道的连接分离,切除子宫从阴道取出。A组:纱布填塞阴道,腹腔镜下电凝残端止血,倒刺线缝合残端,冲洗盆腔,查无明显出血,常规关腹结束手术。B组:经阴道连续锁边缝合前后腹膜及阴道残端。腹腔镜下再次探查盆腹腔,创面电凝止血,查无明显出血,常规关腹结束手术。C组实施传统多孔腹腔镜全子宫切除术:于脐部上缘行1 cm 横行切口,置入10 mm Trocar,充入CO2,形成人工气腹后置入腹腔镜探查。分别于两侧髂前上棘与脐连线中外1/3处作切口,置入5 mm Trocar,再于左下腹无血管区置入另一Trocar。全子宫切除及阴道残端缝合步骤同 A组。
1.3观察指标观察3组的手术时间(从切开皮肤到缝合切口)、术中出血量、术后排气时间、术后住院时间、手术前后血红蛋白(Hb)差值、术后24 h伤口疼痛程度、术后并发症及腹部切口愈合满意度等。伤口疼痛程度用VAS量表评分:0分为患者无明显疼痛感;1~3分自觉有轻度疼痛,不影响睡眠;4~6分疼痛明显,影响睡眠;7~10分剧烈疼痛并难以忍受,需止痛对症处理。切口满意度采取问卷评价。

2 结果
3组均顺利完成手术,无中转多孔或开腹手术。A组与C组、B组间的手术时间差异均有统计学意义(P<0.05)。3组间的术中出血量、手术前后Hb差值,以及术后肛门排气时间、住院时间差异均无统计学意义(P>0.05)。见表2。C组后24 h的VAS评分与A组差异有统计学意义(P<0.05),B组与A组差异无统计学意义(P>0.05)。3组并发症发生率差异无统计学意义 (P>0.05)。C组术后切口满意度与A组差异有统计学意义(P<0.05),B组术后切口满意度与A组差异无统计学意义(P>0.05)。见表3。3组术后病理检查结果均为良性。术后随访1个月,腹部切口和阴道残端均愈合良好。A组1例患者术后阴道少量出血4 d,考虑为术后缝线脱落吸收引起,应用止血药物、阴道纱布填塞后24 h出血停止。

表2 3组手术时间等围术期指标比较
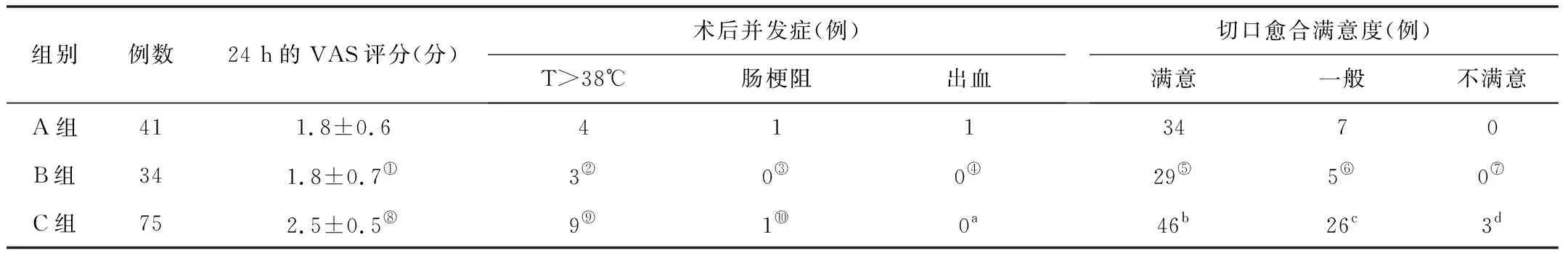
表3 3组术后并发症等围术期指标比较
3 讨论
V-NOTES通过人体自然腔道阴道进入盆腹腔行手术操作,整合了TU-LESS及传统阴式技术手段,被称为继开放手术及传统腹腔镜手术之后的“第三代外科手术”。 TU-LESS作为其过渡形式之一,利用脐部天然瘢痕处肌肉薄弱、血管少的特点做切口,具有瘢痕隐蔽、套管穿刺相关并发症风险低,以及术后疼痛轻等优势[1-2]。
本研究中无1例发生中转手术方式。与C组比较,A组的术中出血量、手术前后Hb差值,以及术后排气时间、出院时间差异无统计学意义。A、B 2组均为TU-LESS,减少了疼痛来源,故术后VAS评分与C组差异有统计学意义。这与一项荟萃分析[3]所报道的结果不相符合,可能与不同的脐部入路(如脐正中、脐轮等)、切口长度、所使用的入路平台等不同有关。A、B 2组手术时间较C组相对延长,考虑与手术机械及光源均由同一切口进入,操作孔位于脐部,位置较传统腹腔镜组稍高,丧失手术的三角区域,由平面视野变为线性视野;器械与器械、器械与光源之间相互干扰,易影响手术操作的精确度;Trocar与器械间的间距小,活动范围受限,影响了对周围组织的牵引及手术区域的暴露。增加了操作难度所致。但龚瑶[4]等认为,单孔腹腔镜下只是将“大三角”转变为了“小三角”,且“小三角”所要求的精细操作更利于手术完成。随着单孔手术熟练度和规范度的提高,在认清“小三角”优势后,其手术时间可有显著下降。此外,B组较A组手术时间相对较短,考虑与单孔腹腔镜下缝合较困难,而经阴道缝合使用传统腹腔镜缝线,操作简单易行有关。手术医师可根据自身手术经验及熟练程度,选择合适的缝合方式。
由于TU-LESS手术难度相对增加,手术时需注意:(1)适应证选择。脐部发育、体型、盆腔粘连程度、子宫大小、子宫活动度等,都是影响手术效果的因素。国内外相关研究[5-6]均证实单孔腹腔镜手术在子宫小于孕16周患者中的安全性和可行性,但亦有报道证实子宫大小超过10孕周或严重粘连患者中转开腹或多孔腹腔镜手术的概率明显增大[7]。故对于初学者,建议选择标准体型、子宫小于孕10周、盆腔无明显粘连、子宫活动度较好的患者。(2)脐部操作。术前应彻底清除脐部污垢。脐正中、脐上缘纵切口,以及沿脐轮切开,均是目前常用的经脐单孔切开方式。脐部血运差且褶皱多,术后缝合时应注意严格止血和对合紧密,恢复其解剖结构,不留死腔避免愈合不良。(3)腹(盆)腔操作。单孔腹腔镜由于线性视野及操作时的“筷子效应”,造成手术操作困难。应重视弯器械和直器械配合上下、前后操作;扶镜者应与术者默契配合,同时举宫杯暴露视野,无性生活者亦可通过悬吊法暴露手术部位[8],这在打开膀胱腹膜反折下推膀胱的过程中尤为重要;术中善用能量器械及血管闭合器辅助操作,切割电凝时注意避免损伤肠管、膀胱及其周围组织。确切止血,尽量保证组织离断后无明显活动性出血。(4)子宫取出。术中切除的子宫可经阴道取出,子宫过大取出困难者也可置于取物袋分解后经脐部切口取出。(5)残端缝合。根据个人手术经验及熟练程度,选择经阴道缝合或经腹腔镜倒刺线缝合残端,确定无明显出血后,方可结束手术。(6)器械选择。本研究中使用一次性入路平台与传统腹腔镜器械可顺利完成手术,无明显术后并发症。TU-LESS手术可使用一次性多通道入路平台和自制入路平台[9],使用传统腹腔镜器械完成手术,可降低手术成本,有利于在基层医院开展。
目前,我国妇科机器人单孔腹腔镜、V-NOTES,以及微切口TU-LESS等均有相关报道。但机器人单孔腹腔镜因设备价格昂贵,国内普及率不高;V-NOTES因其倒置的盆腔解剖,特殊的学习曲线,且阴道壁较腹壁血供丰富,易发生出血,而出血多可遮盖光源影响手术操作等,故要求术者必须具备丰富的阴式手术及单孔腹腔镜手术经验;微切口TU-LESS因其更为严重的“筷子效应”和手术器械和光学设备的局限性,对术者也有更高的要求。故以上术式均要求术者有丰富的TU-LESS手术经验。现国内的单孔腹腔镜手术正处于快速稳定发展时期,2020年有相关资料报道[10]了单孔腹腔镜手术在妊娠合并妇科良性疾病的应用效果,证实了其在孕期使用的可行性和安全性,进一步扩大了TU-LESS在妇科良性肿瘤手术中的应用范围。2011年,刘木彪等[11]完成了单孔腹腔镜下的早期子宫内膜癌分期手术; 近几年文献先后报道了LESS在宫颈癌及早期卵巢癌中的应用[9]。从早期的附件区手术、子宫肌瘤剥除术,到子宫切除手术,再到近几年报道的部分妇科恶性肿瘤手术等,相信随着术者经验的积累、手术技术的提升、单孔手术器械及光学设备的不断完善,以及患者对美容的需求和国内众多专家的推广,LESS手术治疗妇科良性疾病有望得到进一步普及。对于部分恶性肿瘤,亦有潜在的发展空间。

