中药调控阿尔茨海默病tau蛋白过度磷酸化的研究进展
周 君,李明成,米彩云,王虎平
甘肃中医药大学 甘肃省中医方药挖掘与创新转化重点实验室,兰州 730000
目前全球人口格局呈现老龄化发展态势,阿尔茨海默病(Alzheimer’s disease,AD)的患病率逐年攀升,30年后全球老年痴呆患者总量将高达1.38亿,其中绝大多数为AD患者[1]。受当前新型冠状病毒疫情的影响,AD患者的护工数量锐减[2],加剧了庞大的AD患者群体对个人,家庭,乃至整个社会的压力。AD的起病及病程演变尚不可控,进行性情感和认知障碍及记忆力衰退是其显著的临床表现。tau蛋白过度磷酸化是导致神经元纤维缠结(neurofibrillary tangles,NTFs)的主要因素,而NFTs正是AD的主要病理特征[3]。tau蛋白是一种微管相关蛋白,tau蛋白与微管结合后可保障微管结构的稳定[4],从而维持微管的生理功能。位于tau蛋白上的苏氨酸(Thr)、丝氨酸(Ser)、酪氨酸(Tyr)称为可磷酸化位点,在激酶的作用下发生磷酸化[5],形成磷酸化tau蛋白;磷酸化tau蛋白与已结合的微管发生解离,导致微管稳定性降低进而引发细胞骨架坍塌,解离下来的磷酸化tau蛋白形成双螺旋结构后形成NFTs;磷酸酶可去除磷酸化tau蛋白上的磷酸基团,恢复tau蛋白的生理功能(见图1)。总而言之,tau蛋白磷酸化水平有赖于激酶与磷酸酶的共同调控[6]。
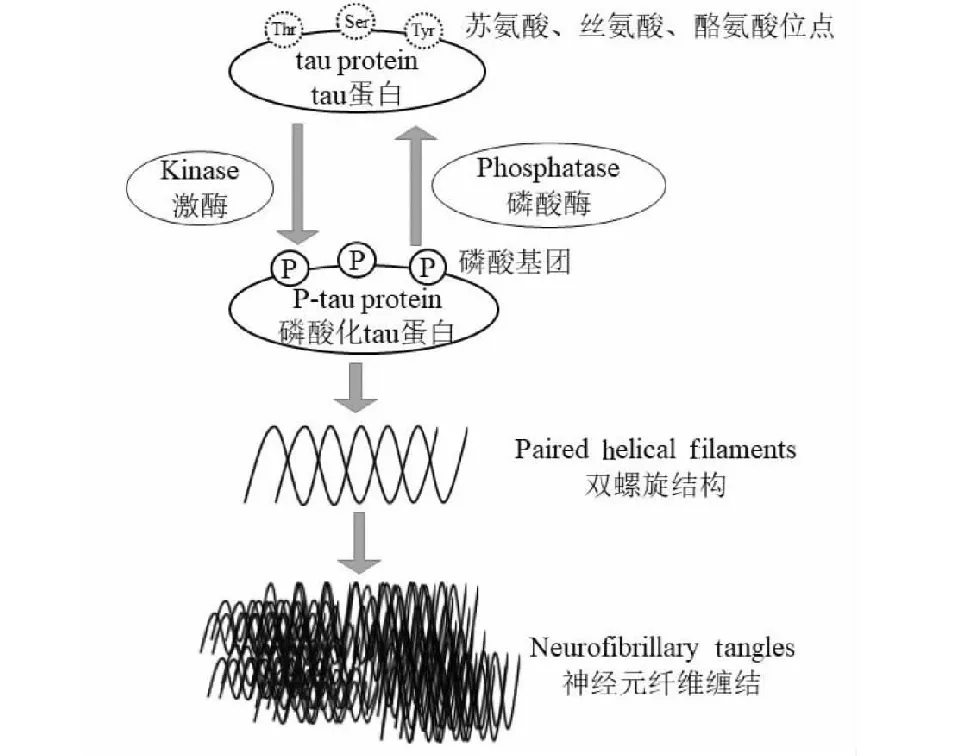
图1 tau蛋白受激酶和磷酸酶的调控示意图
AD在中医中类属“痴呆”的范畴,中医有辨证论治、整体观念、病证结合等特点,运用中药在防治AD方面具有独到优势。据现有临床和动物研究表明,中药防治AD有多途径抑制tau蛋白过度磷酸化的优势(如表1、2所示),如中药通过调控激酶、磷酸酶的活性,达到降低tau蛋白磷酸化水平,继而减缓NFTs形成的目的。由此,本文从中药调控激酶和磷酸酶的角度,探究中药干预tau蛋白过度磷酸化,防治AD的相关机制。
1 中药对tau蛋白激酶的调控
1.1 单味中药对tau蛋白激酶的调控
吴茱萸提取物——吴茱萸次碱干预高糖诱导的AD大鼠后缓解了大鼠的认知障碍,降低GSK-3β的活性,进而降低tau蛋白磷酸化水平[10]。淫羊藿提取物——淫羊藿苷灌胃干预用β-淀粉样蛋白(amyloidβ-protein,Aβ)诱导的AD小鼠后,其认知障碍得到有效改善,海马区tau蛋白磷酸化现象得到缓解,同时激素膜受体和c-Jun水平也受到调控[11];用淫羊藿苷预处理后诱导细胞损伤的实验认为其可通过调控磷脂酰肌醇-3激酶(phosphatidylinositol 3-kinase,PI3K)/蛋白激酶B(protein kinase B,Akt)/GSK-3β信号通路,降低tau蛋白磷酸化水平[12],淫羊藿苷有一定抗AD的功效。五味子提取物——北五味子酸性多糖(acidic polysaccharose of schisandrae chinensis,SCP-A)灌胃干预Aβ25-35诱导的AD小鼠后,测得GSK-3β活性减弱,削弱其对tau蛋白的磷酸化力度,此外小鼠的认知功能也得到改善[13]。采取腹腔注射D-半乳糖联合双侧海马注射Aβ25-35的方式建立AD模型大鼠后,用不同剂量的黄连素(黄连提取物)对其灌胃,发现黄连素剂量在150 mg/kg时对AD大鼠的GSK-3β和磷酸化tau蛋白表达的下调作用最强[14],另一项对APP/PS1双转基因小鼠进行黄连素灌胃的研究表明,黄连素可抑制核转录因子(nuclear factor kappa-B,NF-κB)信号通路,缓解tau蛋白过度磷酸化,减轻小鼠的认知障碍,抑制神经炎症[15]。Yang等[16]用人参皂苷Rb1溶液培养Aβ1-42诱导的AD模型小鼠脑片,结果显示人参皂苷Rb1能够下调因造模引起的tau蛋白过度磷酸化水平,并通过抑制激酶ERK1/2的活性来减少NFTs的形成。Xiong等[17]认为荔枝核的有效成分可通过调控胰岛素受体基因-1(insulin receptor substrate-1,IRS-1)/PI3K/Akt/GSK-3β信号通路来降低GSK-3β的活性,进而抑制tau蛋白过度磷酸化。芹菜籽提取物——丁苯酞干预由Aβ1-42诱导的AD模型大鼠后,丁苯酞组大鼠形态学表现介于正常组与AD模型组之间,且丁苯酞中、高剂量组的表现优于低剂量组[18];海马CA1区GSK-3β活性与磷酸化tau蛋白水平降低[19];还能改善脑内炎症及氧化应激反应,改善认知功能[20]。葛根提取物——葛根素干预通过腹腔注射D-半乳糖建立的AD模型大鼠,可削弱因造模引起的GSK-3β强活性与嗅球内tau蛋白的磷酸化[21]。独活提取物——蛇床子素灌胃APP/PS1双转基因小鼠6周后,改善了小鼠学习记忆能力,海马CA3区锥体细胞和尼氏体数量增多,细胞形态学表现较佳,p-GSK-3β/GSK-3β的表达增高,tau蛋白Ser202位点的磷酸化效应受到削弱,但实验中未指出p-GSK-3β的检测位点[22]。Chen等[23]用激活GSK-3β的方式建立AD模型大鼠,建模后用头顶一颗珠(trillium tschonoskii maxim,TTM)水煎液对AD大鼠进行灌胃干预,实验结果显示AD大鼠的学习记忆能力得到改善,TTM中、高剂量能改善海马CA1和CA3区尼氏体的数量与形态,高、中、低剂量均能降低海马内GSK-3β活性并提高GSK-3β在Ser9位点的磷酸化,还能上调蛋白激酶C(protein kinase C,PKC)和Akt活性,抑制tau蛋白磷酸化,改善AD症状。知母提取物——知母皂苷干预Aβ1-42诱导的AD大鼠后,大鼠的空间学习记忆障碍得到改善,胆碱乙酰基转移酶(choline acetyltransferase,ChAT)蛋白表达增加,磷酸化Akt增多,促进GSK-3β在Ser9位点磷酸化,达到抑制GSK-3β活性的目的,进而降低因造模引起的海马区tau蛋白过度磷酸化,但同时发现GSK-3β的表达增多[24]。丹参酮IIA是中药材丹参的脂溶性有效成分,Lin等[8]在注射Aβ1-42建立AD模型大鼠时,发现Aβ1-42具有促进GSK-3β在Tyr216位点磷酸化,并抑制GSK-3β在Ser9位点磷酸化的作用;建模后用丹参酮IIA对AD大鼠进行灌胃干预,实验结果表明丹参酮IIA可逆转由造模引起的学习记忆障碍,可改善脑内细胞形态,且海马区tau蛋白磷酸化程度与丹参酮IIA剂量具有相关性,此外GSK-3β在Ser9位点磷酸化水平升高,Tyr216位点磷酸化水平降低,伴磷酸化ERK增多,tau蛋白的磷酸化水平降低。
1.2 复方对tau蛋白激酶的调控
黄连解毒汤(黄连、黄芩、黄柏、栀子)灌胃干预由Aβ25-35诱导的AD模型大鼠,发现其可改善AD大鼠的学习能力[25],抑制GSK-3β和CDK-5的活性,还可对tau蛋白多个位点的磷酸化进行干预[26],进而起到防治AD的作用。双侧海马注射Aβ25-35建立AD模型大鼠后,用不同剂量的乌芩健脑方药液(制首乌、郁金、黄芪、川芎等)对其实施干预,实验发现该药液可改善AD大鼠的学习记忆能力,能通过弱化CDK5与GSK-3β活性从而减轻tau蛋白过度磷酸化程度[27]。复智散干预Wistar大鼠皮层神经元,采取Aβ25-35养的方式建立AD模型,发现复智散可弱化CDK5活性,同时可在多个位点抑制tau蛋白的磷酸化,实验结果提示调控calpain-p25/CDK5通路进而抑制tau蛋白过度磷酸化或许是复智散抑制tau蛋白过度磷酸化的主要途径[28]。Guo等[29]对两种AD模型小鼠(东莨菪碱腹腔注射小鼠和认知障碍与年龄相关的SAMP8小鼠)展开好忘方(续断、肉苁蓉、茯苓、远志、菖蒲)与盐酸多奈哌齐的随机对照试验,实验结果表明,好忘方可改善AD小鼠的认知障碍,减少记忆丢失,并对PKA/GSK-3β/tau信号通路进行调控,抑制tau蛋白的磷酸化,缓解脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)的下降趋势,增强突触的可塑性。益智聪明汤(人参、肉苁蓉、赤芍、知母、菖蒲等)干预由Aβ25-35诱导的AD模型小鼠,发现小鼠学习记忆障碍得到改善,海马区细胞形态结构较佳,益智聪明汤中、高剂量组抑制tau蛋白的Ser404和Thr231位点磷酸化效果最明显,高剂量组还对tau蛋白的Thr181和Ser396位点的磷酸化有抑制作用,同时强化PI3K在p85位点、Akt在Ser473位点与GSK-3β在Ser9位点磷酸化的表达[30-32]。表明益智聪明汤可通过激活PI3K/Akt/GSK-3β信号通路对tau蛋白的磷酸化进行调控,继而防治AD。
2 中药对tau蛋白磷酸酶的调控
磷酸酶活性降低时,脱磷酸效应随之降低,这将无法扭转磷酸化tau蛋白逐步增多的局面,最终导致tau蛋白过度磷酸化。中药可通过调控磷酸酶的活性达到防治AD的目的,在众多的磷酸酶中,蛋白磷酸酶2A(protein phosphatase 2A,PP2A)的脱磷酸效应强度占总脱磷酸效应的大多数[33],因此PP2A常作为检测磷酸酶效应的指标。
2.1 单味中药对tau蛋白磷酸酶的调控
板桥党参干预冈田酸诱导的AD模型大鼠,实验结果显示板桥党参可提升PP2A活性,降低tau蛋白磷酸化水平,修复神经元损伤[34]。TTM水煎液干预冈田酸诱导的AD大鼠后,AD大鼠的空间学习能力得到改善,且海马内PP2A活性上升,tau蛋白磷酸化水平降低,其中TTM高剂量组的尼氏体含量显著增加[35]。人参提取物——人参皂苷Rb1干预冈田酸诱导的AD模型大鼠,检测海马后发现PP2A活性明显提高,且tau蛋白磷酸化水平下降,神经元形态结构得到改善[36]。山茱萸提取物——山茱萸环烯醚萜苷(cornel iridoid glycoside,CIG)干预tau蛋白过表达的rTg4510转基因AD小鼠,3个月后发现小鼠的认知及记忆力得到改善,对小鼠大脑进行检测后发现CIG增强了PP2A活性,降低tau蛋白过度磷酸化程度和聚集程度[37]。
2.2 复方对tau蛋白磷酸酶的调控
扶正祛邪方(人参、川芎、黄连)灌胃处理SAMP8小鼠,实验结果表明该方可维持海马CA1区内神经元总量变化,提高PP2A活性,抑制tau蛋白过度磷酸化,改善学习记忆能力[38]。柴胡疏肝散(柴胡、枳壳、香附、川芎、白芍、陈皮、甘草)干预通过腹腔注射D-半乳糖联合双侧海马注射Aβ1-42建立的AD模型大鼠,发现柴胡疏肝散可增加PP2A的表达,逆转由造模引起的tau蛋白过度磷酸化状态,改善AD大鼠的认知和学习障碍[39]。
3 中药对tau蛋白激酶和磷酸酶的共同调控
tau蛋白过度磷酸化导致的NFTs是AD的主要病理特征之一[3],用于描述AD患者脑内神经元受损程度。激酶和磷酸酶的活性变化在tau蛋白过度磷酸化的进程中起关键性作用,当激酶对tau蛋白的磷酸化效应与磷酸酶对磷酸化tau蛋白的脱磷酸效应的平衡被打破,在磷酸化效应明显强于脱磷酸化效应时呈现出tau蛋白过度磷酸化的态势。目前研究表明,中药防治AD的优势在于可通过多条途径干预tau蛋白的磷酸化进程。
3.1 单味中药对tau蛋白激酶和磷酸酶的共同调控
目前研究认为锌是导致AD的诱因之一,锌可活化p38丝裂原活化蛋白激酶(p38 mitogen activated protein kinase,p38 MAPK)和GSK-3β[40],间接提高tau蛋白磷酸化水平。一项研究用锌诱导tau蛋白特定位点(Ser262)磷酸化后加以银杏提取物(Ginkgobilobaextract 761,EGB761)进行处理,结果显示EGB761能够防止p38MAPK和GSK-3β被锌诱导活化,表明GBE761具有在Ser262特定位点抑制tau蛋白磷酸化的能力[41]。Zeng等[42]采用高同型半胱氨酸血症模拟AD模型大鼠后使用EGB761,发现EGB761能够纠正PP2A与GSK-3β的活性,还原磷酸化tau蛋白特定位点的未磷酸化状态。由此可知银杏叶有调控激酶与磷酸酶的能力,可抑制tau蛋白的磷酸化。CIG干预rTg4510转基因小鼠,实验结果表明CIG可减少病理性tau蛋白的异常沉积,还可通过上调内源性PP2A激活剂(phosphatase 2A phosphatase activator,PTPA)的表达,进而增强PP2A的活性,改善tau蛋白过度磷酸化现象[43]。山茱萸提取物——山茱萸多糖干预采取腹腔注射D-半乳糖联合双侧海马注射Aβ1-40建立AD模型大鼠后,GSK-3β表达受到抑制,即山茱萸多糖通过弱化激酶的磷酸化效应来缓解tau蛋白过度磷酸化状态[44]。黄芪提取物——黄芪多糖灌胃干预Aβ25-35诱导的AD大鼠后,大鼠定位与学习能力有所改善,且PP2A水平上升,Aβ、磷酸化tau蛋白、GSK-3β和β-分泌酶(β-site amyloid precursor protein-cleaving enzyme,BACE1)水平降低[45]。另一项研究表明黄芪多糖能将tau蛋白磷酸化水平和GSK-3β活性降低,且黄芪多糖能激活Wnt通路从而抑制Aβ引起的神经毒性[46]。何首乌提取物——二苯乙烯苷灌胃干预APP/PS1/tau三转基因小鼠后小鼠学习记忆能力得到改善,GSK-3β和JNK活性降低,PP2A蛋白与蛋白磷酸酶2B(protein phosphatase 2B,PP2B)mRNA的转录及其蛋白表达升高,脑组织中磷酸化tau蛋白在Ser404和Thr205位点的表达下降、聚集度降低、分布范围缩小,认为二苯乙烯苷可通过削弱GSK-3β和JNK对tau蛋白的磷酸化效应,增强PP2B的脱磷酸效应来缓解tau蛋白磷酸化的效应[47-49]。单味中药及其提取物对AD中tau蛋白过度磷酸化的调控见表1。

表1 单味中药及其提取物对AD中tau蛋白过度磷酸化的调控
3.2 复方对tau蛋白激酶和磷酸酶的共同调控
复方金思维干预双侧脑室注射微量链脲佐菌素建立的AD模型大鼠后,进行免疫组化染色观察GSK-3β、蛋白磷酸酶1(protein phosphatase1,PP1)、PP2A,结果显示金思维能调控GSK-3β、PP1、PP2A活性,使之保持在正常范围,进而使tau蛋白磷酸化维持在正常水平[50]。不同剂量的远志散(远志、枳壳、旋覆花、半夏等)灌胃Aβ1-40诱导的AD模型大鼠,实验表明远志散可通过调节PI3K/Akt/GSK-3β信号通路抑制AD大鼠海马CA1区tau蛋白磷酸化表达[51];Li等[52]利用远志散干预Aβ1-40诱导的AD模型大鼠后,检测发现海马区PP2A活性增强,GSK-3β活性减弱,在激酶与磷酸酶效应力的综合作用下,tau蛋白过度磷酸化程度降低。涤痰汤对冈田酸诱导的AD大鼠进行灌胃,实验表明其能降低tau蛋白Ser214、Ser262位点的过度磷酸化,这可能与上调PP2A活性,增强对磷酸化tau蛋白的脱磷酸效应有关[53]。证明涤痰汤可有效缓解AD大鼠临床症状后,对涤痰汤及其拆方继续展开研究,研究表明涤痰汤拆方和全方能够通过上调PP2A、下调GSK-3β活性,进而降低tau蛋白磷酸化水平,并缓解AD大鼠的空间学习障碍[54]。黄精丸灌胃干预采用D-半乳糖联合冈田酸诱导的AD模型小鼠后,小鼠学习记忆障碍得到改善,这可能与激活Wnt/catenin信号通路有关[55];海马CA1和CA3区神经元数量、PP2A蛋白及mRNA表达增强,且CA1区GSK-3β在Ser9位点磷酸化增强,削弱其对tau蛋白的磷酸化效应[56]。酸枣仁汤(酸枣仁、茯苓、川芎、知母、炙甘草)灌胃干预APP/PS1双转基因小鼠,发现酸枣仁汤可有效改善小鼠学习记忆力,海马CA3区神经与尼氏体数量较多,细胞排列密集,神经元树突棘密度与分支数量均优于模型组,GSK-3β表达减弱,GSK-3β的Ser9位点磷酸化后GSK-3β失活,tau蛋白磷酸化程度降低[57]。表明酸枣仁汤可从直接削弱GSK-3β表达与对其Ser9位点磷酸化这两种直接与间接的方式削弱其对tau蛋白的磷酸化效应,达到防治AD的目的。温脾通络开窍汤(黄芪、益智仁、何首乌、三七、绞股蓝、石菖蒲)干预右侧海马注射冈田酸的AD模型大鼠三周,海马检测显示温脾通络开窍汤中、高剂量组GSK-3β活性降低,PP2A活性增高,且与中药剂量组之间存在量效关系[58];温脾通络开窍汤中、高剂量组海马tau蛋白磷酸化水平降低,大鼠认知障碍得到缓解[59],即温脾通络开窍汤从GSK-3β和PP2A两个角度降低tau蛋白过度磷酸化。复方对AD的tau蛋白过度磷酸化的调控见表2。

表2 复方对AD的tau蛋白过度磷酸化的调控
4 总结及展望
尽管目前尚未找到成熟的方式来干预AD的发病及病情进展,大量中药的临床、动物及细胞实验已证实中药在干预阿尔茨海默病tau蛋白过度磷酸化方面有一定效果[60]。中医认为AD病位在脑,与心、肝、脾、肾四脏关系密切[61],在心的统领下,脾运化转运营养物质,肝调畅机体,肾藏纳精微,诸脏配合以保障神机正常发挥。已证实一系列具有补肝肾、益气活血、补髓益智、清热解毒等功效的方药对激酶的调控作用较佳,通过弱化GSK-3β、CDK5、JNK、ERK等激酶活性和调控相应信号通路,抑制tau蛋白相应位点的磷酸化,进而减缓tau蛋白向磷酸化tau蛋白的转化。尽管现在尚不能详尽地检测出磷酸化tau蛋白的磷酸化位点,但已能体现出不同的激酶对tau蛋白磷酸化影响的差异。此外,《血证论》有云:“凡心有瘀血,亦令健忘”认为瘀血是AD的主要致病因素之一,实验证明具有补气活血、温阳化瘀功效的方药对AD疗效较佳,尤其在调控tau蛋白过度磷酸化方面具有一定作用;可直接调控磷酸酶活性,加强对磷酸化tau蛋白的脱磷酸化效应,达到减少产生NFTs,防治AD的目的。更有《石室秘录》有云:“痰气最盛,呆气最深”,清代陈士铎认为“呆”与“痰”有密切关联,实验证实补益肝肾、益气升阳、活血化瘀、化痰开窍等功效的方药对激酶和磷酸酶有共同调节作用,由于激酶中GSK-3β的磷酸化效应最强[62],磷酸酶中PP2A的脱磷酸化效应最强,因此大多数研究以GSK-3β和PP2A为主要检测目标,来揭示中药多途径调控tau蛋白磷酸化的机制。
中药可通过影响激酶、磷酸酶或同时影响二者等途径调控tau蛋白的磷酸化水平,达到防治AD的目的。就目前对中药已开展的研究而言,笔者认为在以下几方面还有待突破:(1)中药治疗具有辨证论治的特点,在大量实验中可体现出辨病的过程,但未能充分展现出辨证的特点,可在动物实验中增加对实验对象进行辨证的内容;(2)中药、复方干预AD疗效确切,但由于成分复杂,目前作用机制尚未阐明,其推广可信度较低,可将现代医学研究技术与中药防治AD进一步结合,一方面纯化并分析中药起作用的有效成分,另一方面探究中药药对调控激酶与磷酸酶的药对配伍规律,尝试从分子水平阐释药对配伍的意义;(3)多类激酶、磷酸酶呈现网络状交互调节tau蛋白的磷酸化水平,但是目前在同一实验中,由于对激酶和磷酸酶种类与磷酸化tau蛋白的磷酸化位点检测不全,不足以构建出中药影响激酶与磷酸酶的全貌,可通过增加检测激酶和磷酸酶的种类,以及磷酸化tau蛋白的磷酸化位点,找到更充足的证据展现中药影响激酶与磷酸酶的网络状调节系统;(4)部分研究仅对tau蛋白与磷酸化tau蛋白进行定量分析,遗漏对中间环节(激酶、磷酸酶或其他指标)的检测,造成证据链缺失,只能展示结果,不能详细阐明原因。在后续研究中可适当添加中间证据的检测,构成完整的证据链;(5)大量临床、动物实验展现出中药疗效较佳,但是中药的毒副作用尚不明确,可增加相关中药的毒理实验,为中药的临床提供更安全的指导。

