基于铝氧键稳定的隧道型钠离子电池正极材料
胡海燕,武源波,刘益峰,唐瑞仁,吴雄伟,肖遥
(1.温州大学,a.化学与材料工程学院;b.碳中和研究院,浙江 温州 325035;2.中南大学化学化工学院,长沙 410083;3.湖南农业大学,化学与材料科学学院,长沙 410128;4.中交(天津)疏浚工程有限公司,天津 300451)
不断增长的能源需求导致全球化石燃料的使用增加,由此排放的大量二氧化碳将导致各种环境问题,如全球变暖和沙漠化[1-4]。为了有效地存储和利用可再生能源(即太阳能、风能、水能、潮汐能和地热能),大规模储能系统的开发成了一个重要的研究领域[5-12]。由于可再生能源的发电通常是间歇性的,并且相对于目前的大规模能源发电设施具有地域限制,电化学储能方式因其成本低、能量密度高、循环寿命长而被视为最优选择[13-17]。在电化学储能方式中,钠离子电池的资源丰富,成本低,安全性高,并且反应机理与锂离子电池相似,因而被认为是一种极具应用前景的锂离子电池的替代品[18-24]。
钠离子电池主要成分包括正极材料、负极材料、电解液和隔膜。正极材料主要包括聚阴离子化合物、普鲁士蓝类化合物、过渡金属氧化物[25-34]。负极材料主要包括碳类、合金类、过渡金属氧化物[35-40]。因为正极材料对电池的能量密度和生产成本有很大的影响,同时,正极材料对于钠离子电池的综合电化学性能表现出更大的提升空间,所以正极材料是电池开发的重要研究对象。在各种正极材料中,聚阴离子化合物具有工作电压高、循环稳定性好、反应动力学快等优异性能,但其电导率比较低,制备条件苛刻,在空气中不稳定,其实用性还需进一步考察[41-42]。普鲁士蓝类化合物具有开放的框架结构,易于容纳Na+,并能使其快速迁移,因而可作为正极材料,但其存在结构不稳定、倍率性能差、首圈库仑效率过低、氰基具有潜在毒性等问题。层状过渡金属氧化物因其易于合成和理论比容量高而成为一种热门的候选正极材料,主要可以分为P2 型和O3 型。P2 型正极材料具有更开放的钠离子扩散通道,更低的迁移势垒,表现出更为优异的动力学性能,但在高电压区域经常发生P2 到O2 的相变和循环过程中出现结构重排,影响了这类材料的循环稳定性和钠离子的扩散。O3 型正极材料是富钠结构,通常有很高的脱嵌钠容量,但O3 型正极材料通常会发生多重相变,空气稳定性很差[43-44]。锰在地壳中的含量高,并且无毒,目前钠锰氧化物正极材料如层状O3-NaMnO2、P2-Na0.67MnO2和隧道结构的Na0.44MnO2成为研究热点[45-48]。在这些钠锰氧化物中,隧道型钠锰氧化物(Na0.44MnO2)因其特殊的隧道型结构、较低的成本和丰富的资源而得到广泛研究,但是由于在长时间的Na+嵌入和脱出过程中材料的结构会坍塌,以及在循环过程中正极材料中的锰离子会发生溶出和迁移,从而影响其实际应用。为解决上述问题,研究者对具有隧道结构的Na0.44MnO2正极材料进行了大量的改性研究。近两年,SHI 等通过Zr 取代策略来优化Na0.44MnO2的隧道结构,得到的Na0.44Mn0.98Zr0.02O2正极材料在充放电过程中体积的变化小,Na+扩散系数高[49]。CHAE 等设计了一种Ca0.07Na0.26MnO2正极材料,钙优先取代Na1 位点,这种取代在Na2 和Na3 位点上产生空位,这些空位改善了正极材料的扩散动力学[50]。ZHONG 等用Co3+取代Mn3+后得到Na0.44Mn0.9925Co0.0075O2正极材料,小的S形通道空间增大,Na+在小通道内扩散的能量势垒降低,使得不活跃的Na+更容易嵌入和脱出[51]。LI 等将Mg2+引入Na0.44MnO2正极材料中小的五边形隧道和大的S 形隧道之间的连接位,调整了钠离子在脱嵌过程中的结构演变[52]。
综上所述,利用化学元素取代的方法可以有效地缓解晶格应变,抑制材料结构退化,得到具有优异电化学性能和动力学性能的正极材料。本文采用固相法制备Na0.44Mn0.95Al0.05O2正极材料,对该材料的晶体结构、形貌、电化学行为、电化学性能和动力学性质进行了深入研究。制备得到的正极材料的电化学性能和动力学性能优异,其原因主要是Al3+结构稳定,其离子半径(0.053 nm)小于Mn3+的离子半径(0.064 nm),而且Al-O键键能(512 kJ/mol)大于Mn-O 的键能(402 kJ/mol),通过Al3+取代部分Mn3+,不仅可以提高Mn 的平均价态,而且能够增强Na0.44MnO2正极材料的结构稳定性,抑制Jahn-Teller 效应[53]。
1 实验过程
在实验室通过高温固相法制备Na0.44MnO2和Na0.44Mn0.95Al0.05O2钠离子电池正极材料,为书写方便,分别将Na0.44MnO2和Na0.44Mn0.95Al0.05O2简写为NaM、NaMA。按照一定计量比准确称量Na2CO3、Mn2O3和Al2O3于研钵中,研磨45 min 使其混合均匀,然后利用压片机将混合物在16 MPa 下压成陶瓷片。最后将得到的陶瓷片在900 ℃的空气中煅烧12 h,升温速度为5 ℃/min。当温度冷却到室温得到正极材料,将其置于研钵中研磨成粉末后装于离心管中,再转移至手套箱中进行保存。
1.1 材料表征
采用日本Rigaku 公司生产D/max—2500 型X射线衍射仪分析确定制备的钠离子正极材料的结构,日本日立公司生产S—4800 型扫描电子显微镜表征正极材料的形貌。
1.2 电池组装及电化学性能测试
将正极材料、导电炭黑(SP)、聚偏氟乙烯(PVDF)按质量比7∶2∶1 放入小研钵中进行混浆,加入一定量的N-甲基吡咯烷酮(NMP)作为溶剂,铝箔(φ10 mm)作为集流体制作正极极片。活性物质的面载量为2~3 mg/cm2。在手套箱中组装CR2032 型扣式电池,钠金属作为对电极,玻璃纤维膜作为隔膜,加入180 μL 电解液(1 mol/L NaClO4(碳酸丙烯酯+5%氟代碳酸乙烯酯))。组装完成后,在2~4 V(versus Na+/Na)下的LAND 蓝电测试通道上进行充放电测试,相应的电流密度为1 C=200 mA/g。对电池先在0.05、0.1、0.2、0.3、0.5、1 C 的倍率下分别循环5 次测试电池的倍率性能,接着在1 C 的倍率下循环50 次测试电池的循环性能。同时,在普林斯顿仪器测试系统上进行了循环伏安法测试。
2 结果与讨论
2.1 材料的结构表征
采用简单易操作的固相法制备了NaMA 正极材料。利用X 射线粉末衍射仪(XRD)表征NaMA 正极材料对应的晶体结构,相应的表征图谱如图1(a)所示,NaMA 正极材料的XRD 图谱与Na0.44MnO2的标准图谱一致,具有隧道型晶体结构。在隧道型结构中,有2 种类型的隧道:在较小的五边形隧道中,只有1 个钠位(Na1)被完全占据;在较大的S 形隧道中,有2 个钠位(Na2 和Na3)被占据一半[54]。对于Mn3+/Mn4+离子,Mn2 和Mn5 由Mn3+占据,其中,四方锥形的Mn5 位置较特殊,它将不规则多面体和较大S 形通道连接起来,可以在钠离子脱嵌过程中起到类似弹簧的作用,缓冲结构应力的变化,从而提升材料在循环过程中的结构稳定性。隧道型NaMA 正极材料沿[001]和[010]轴方向的晶体结构分别如图1(b)和图1(c)所示,铝取代后材料的结构没有发生变化,该正极材料能够实现钠离子的嵌入脱出[55-57]。图1(d)和图1(e)显示了NaMA 正极材料的低倍数和高倍数的扫描电镜(SEM)图像,从图中可以看到颗粒呈棒状。
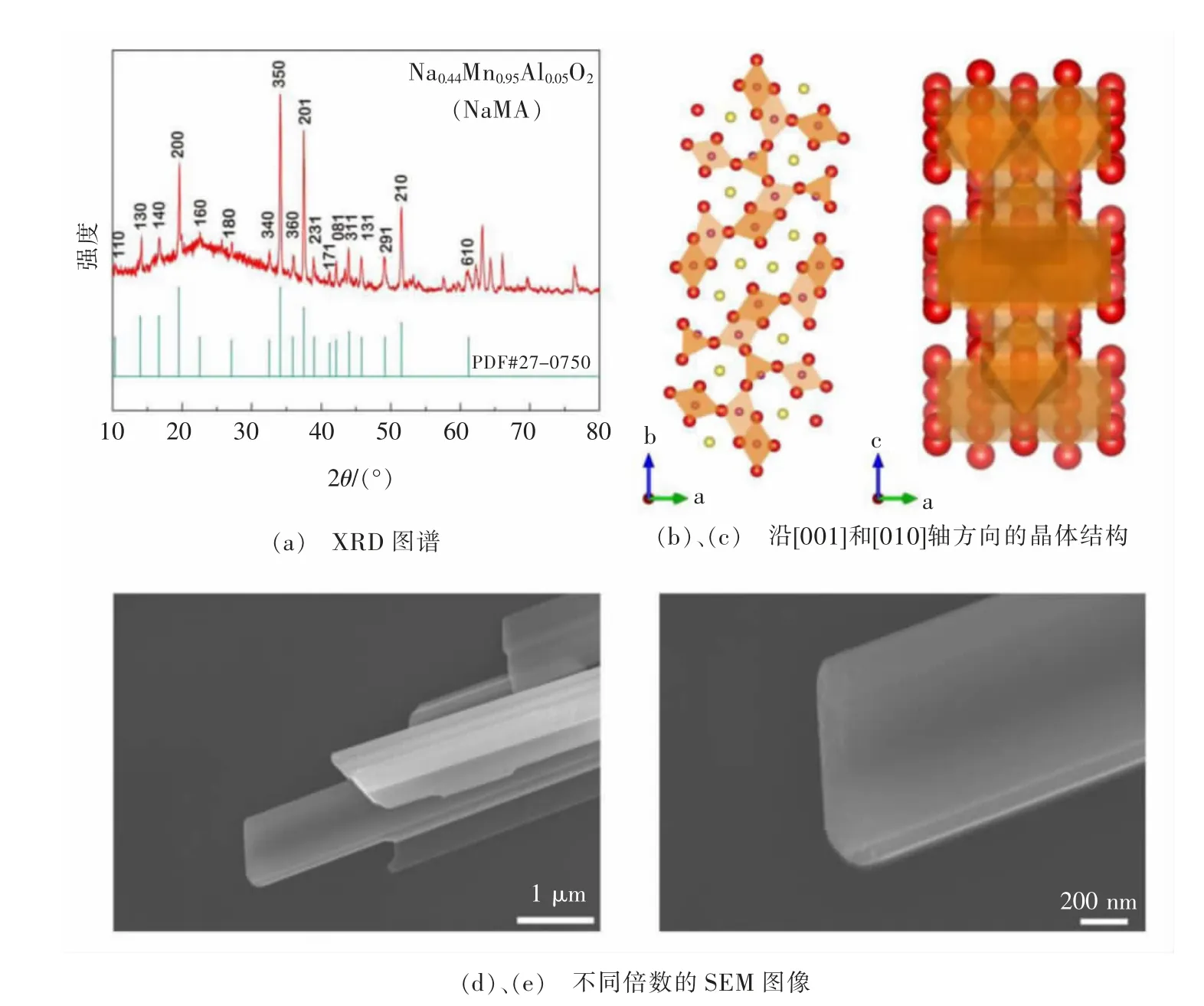
图1 NaMA 正极材料的结构表征Fig.1 Structure characterization of the NaMA cathode material
2.2 材料的电化学行为
采用恒流充放电法和循环伏安法评价NaM 和NaMA 电极的电化学行为。图2(a)和图2(c)显示了NaM 和NaMA 电极分别在0.1 C(20 mA/g)和0.05 C(10 mA/g)下2~4 V 之间的充放电曲线。从图2(a)中可以看到NaM 电极可发挥出120.3 mAh/g 的可逆容量,在整个充放电过程中,会伴随有很多小的电化学平台,这主要对应的是钠离子脱出嵌入过程中复杂的相变过程[52]。铝取代锰后得到的充放电曲线如图2(c)所示,NaMA 正极的恒流充放电曲线变得平滑,说明铝取代锰后可以抑制充放电过程中存在的相变。同时,NaMA 正极的放电比容量可高达127.8 mAh/g。如图2(b)和图2(d)所示,0.1 mV/s 条件下测试得到的循环伏安曲线中的氧化还原峰分别对应钠离子的连续嵌入/脱出,与恒流充放电曲线结果一致。
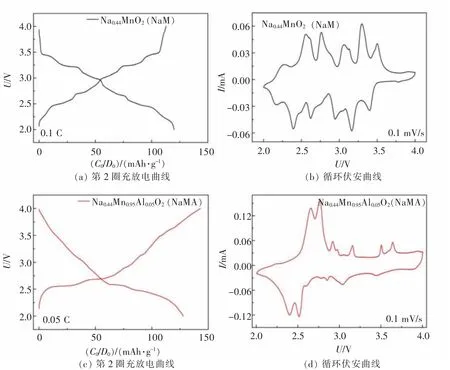
图2 NaM 和NaMA 电极的电化学行为Fig.2 Electrochemical behavior of the NaM and NaMA electrodes
2.3 材料的电化学性能
2.3.1 倍率性能
对NaMA 正极材料进行倍率性能测试。如图3所示,相比于0.05 C,在0.5 C 的电流密度下,NaMA电极可以发挥82.6 mAh/g 的可逆比容量,容量保持率高达65%,同时可以发挥230.3 Wh/kg 的能量密度。在0.1、0.2、0.3、0.5、1.0 C 倍率下放电比容量分别为116.8、100.4、91.0、82.6、70.5 mAh/g。从图3(b)和图3(c)可以看到不同倍率下都具有平滑的充放电曲线,这有利于其得到优异的倍率性能。同时,库仑效率与能量效率及中值电压也都相对比较稳定。
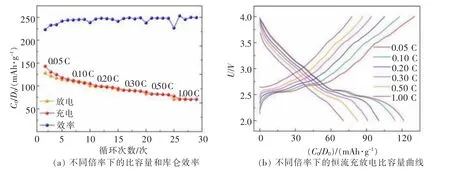
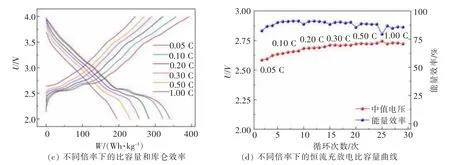
图3 NaMA 电极的倍率性能Fig.3 Rate performance of the NaMA electrode
2.3.2 循环性能
NaMA 电极在0.05、0.1、0.2、0.3、0.5、1 C 下分别循环5 次测试完电池的倍率性能后,接着在1 C的倍率下循环50 次测试电池的循环性能。如图4(a)和图4(b)所示,NaMA 正极在进行50 次循环后仍可以发挥出52 mAh/g 的可逆比容量,容量保持率为79%,而且在后续的循环中表现出较小的极化。不同循环次数的库仑效率与能量效率及中值电压也都相对比较稳定,如图4(c)和图4(d)所示。在循环过程中Na0.44MnO2常会出现正极材料中锰离子溶出和迁移的问题,铝取代锰后可在一定程度上解决此问题,因此该正极材料的循环性能佳,得到的充放电曲线平滑。
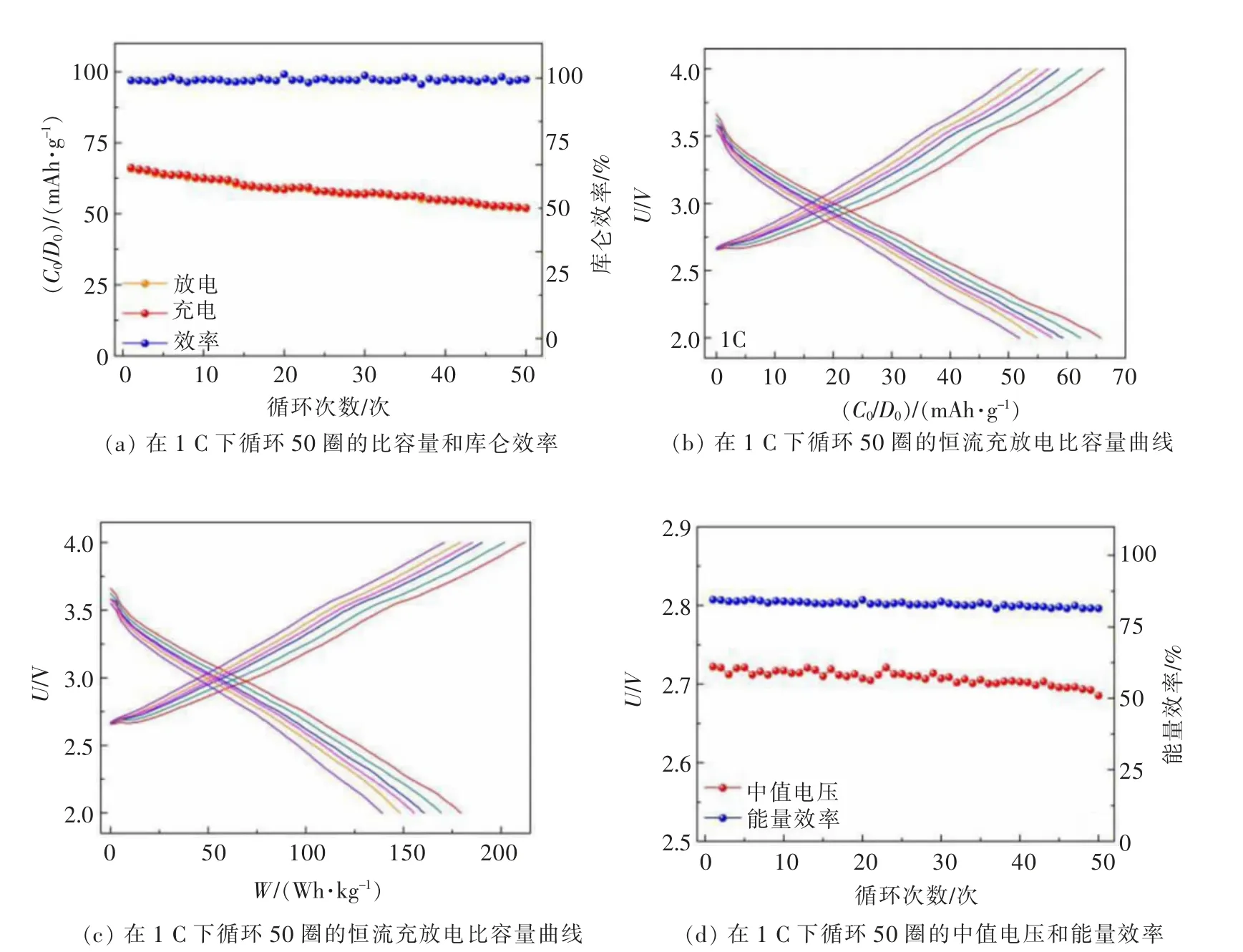
图4 NaMA 电极的循环性能Fig.4 The cycle performance of the NaMA electrode
2.4 材料的动力学性质
为了更加详细地研究NaMA 电极的动力学行为,以不同扫速的CV 测试作为可靠的动力学研究技术定量研究了电容贡献。如图5 所示,分别在0.1、0.2、0.4、0.5、0.8、1.0 mV/s 扫速下对NaMA 电极进行循环伏安测试,为对其动力学行为进行研究,选择图5 中的O1/R1 和O2/R2 这2 对峰电流较大的氧化还原峰进行分析。
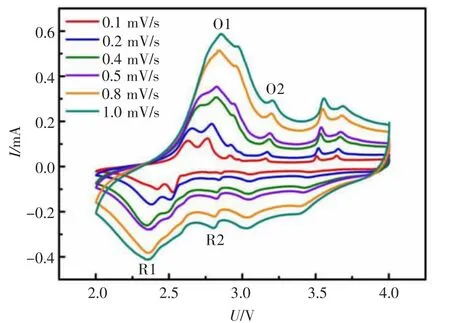
图5 NaMA 电极不同扫速下的循环伏安曲线Fig.5 Cyclic voltammetry curves of the NaMA electrode at different scan rates
图6 所示为峰电流与扫速平方根的线性关系和峰电流对数值与不同扫速对数值的线性关系图,NaMA 电极的储钠机制可通过电容计算公式i=avb进行计算[58-59]。b 值的大小是衡量扩散控制和电容控制的重要指标。当b 值接近1 时,说明此过程主要以电容控制为主;当b 值接近0.5 时,说明此过程主要以扩散控制为主。结合具体计算结果显示,氧化峰O1和还原峰R1 的b 值分别是0.71 和0.57,氧化峰O2和还原峰R2 的b 值分别是0.90 和0.88,说明NaMA电极储钠机制由扩散控制行为和电容控制行为组成,以电容控制行为为主[60-61]。NaMA 电极的动力学性质总结如表1 所列。铝取代锰后形成铝氧键,由于铝氧键的键能高于锰氧键得到较为稳定的结构,从而缓解了晶格应变和锰离子溶出,使其在充放电过程中材料结构保持稳定。因此,NaMA 正极材料的动力学性质优异。
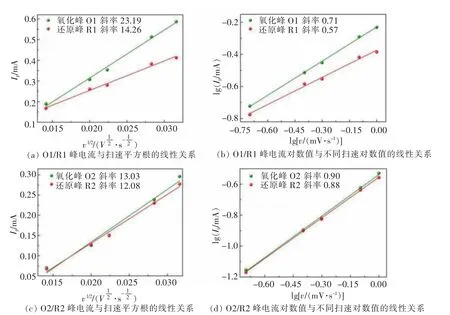
图6 NaMA 电极动力学性质Fig.6 Kinetic properties of the NaMA electrode

表1 NaMA 电极动力学性质Table 1 Kinetic properties of the NaMA electrode
3 结论
1)基于隧道型正极材料Na0.44MnO2存在循环过程中因正极材料发生Jahn-Teller 效应而产生的锰离子溶出和迁移进而导致结构不稳定的问题,设计了一种稳定的Na0.44Mn0.95Al0.05O2正极材料。
2)Na0.44Mn0.95Al0.05O2正极材料的可逆容量高达127.8 mAh/g,充放电曲线变得平滑,说明铝取代锰后可以抑制充放电过程中存在的相变,储钠机制以电容控制行为为主。
3)Na0.44Mn0.95Al0.05O2正极材料电化学性能和动力学性质优异的主要原因是铝取代锰后形成的铝氧键的键能高于锰氧键,从而缓解了晶格应变,减少循环过程中正极材料中锰离子的溶出和迁移。

