新生儿先天性肾上腺皮质增生症筛查切值的影响因素分析
路 遥
大连市妇女儿童医疗中心(集团) 遗传代谢医疗中心 辽宁 大连 116600
新生儿疾病筛查是指在新生儿期通过快速、简便、敏感的检测方法对一些严重影响患儿身体和智力发育的先天性、遗传性疾病进行早期群体筛查,从而使患儿得到早期诊断、早期治疗,避免患儿生长、智力发育障碍,甚至死亡。先天性肾上腺皮质增生症(CAH)是一种常染色体隐性遗传病,由于类固醇激素合成过程中某些酶先天缺陷,导致肾上腺皮质醇的合成过程完全或者部分受阻,使促肾上腺皮质激素增加,导致肾上腺皮质增生,引发以肾上腺皮质功能不同程度减退、性腺发育异常、伴或不伴水盐代谢、高血压等为主要表现的综合征[1]。血17α-羟孕酮(17-OHP)水平测定是CAH诊断和疗效评估的一个重要指标。本研究对大连地区新生儿CAH筛查数据进行分析,探讨大连地区足月儿、早产儿及正常体重儿、低体重儿CAH筛查中17-OHP分布状况及切值。
1 资料与方法
1.1 一般资料 研究对象为2019年12月至2021年4月在我市分娩的活产新生儿,共计45 504例。新生儿出生72 h后,并充分哺乳6次以上由助产机构专业护理人员采集3滴足跟血滴于专用滤纸上,要求每个血斑直径≥8 mm,血斑均匀渗透到滤纸两面,在室温下自然晾干,避免阳光直射,放置于4℃冰箱密封保存,一周内运送或者邮寄到实验室进行新生儿疾病筛查。
1.2 仪器与试剂 全自动打孔仪(Panthera-PuncherTM9,美国PerkinElmer公司);美国PerkinElmer公司全自动荧光免疫分析仪(GSP,Genetic Screening Processor,型 号为2021-0010)及其配套的测定试剂盒。质控品采用第三方质控品,由杭州宝荣科技有限公司生产,生产批号为R1191201-2。检测方法为时间分辨荧光免疫分析法。
1.3 结果判断 测定滤纸血片中17-OHP浓度,初筛切值统一定为11 nmol/L。若标本17-OHP浓度≥11 nmol/L,则判断该新生儿先天性肾上腺皮质增生症初筛为阳性,然后原血片复查,结果仍为阳性则由网络组人员通知患儿家长召回复查,若复查仍为可疑阳性则需到综合性医院进行确诊及分型。
1.4 统计学方法 采用SPSS 23.0软件对新生儿17-OHP浓度结果进行统计学分析。对新生儿的17-OHP筛查结果做正态性检验,由于17-OHP浓度数据属于偏态分布,因此本研究通过百分位数法确定其切值。
2 结果
2.1 17-OHP初筛浓度分析 研究对象中足月儿(≥37 w)42 987例,占比94.5%,早产儿(<37 w)2 517例,占比5.5%;正常体重儿(≥2 500 g)43 770例占比96.2%,低体重儿(<2 500 g)的1 734例,占比3.8%。对45 504例新生儿17-OHP初筛浓度进行正态性检验分析,结果显示45 504例新生儿17-OHP初筛浓度呈偏态分布,见表1。17-OHP总体最小值为0.30 nmol/L,最大值为396.30 nmol/L,95%和99%百分位数分别为8.10 nmol/L和13.20 nmol/L。
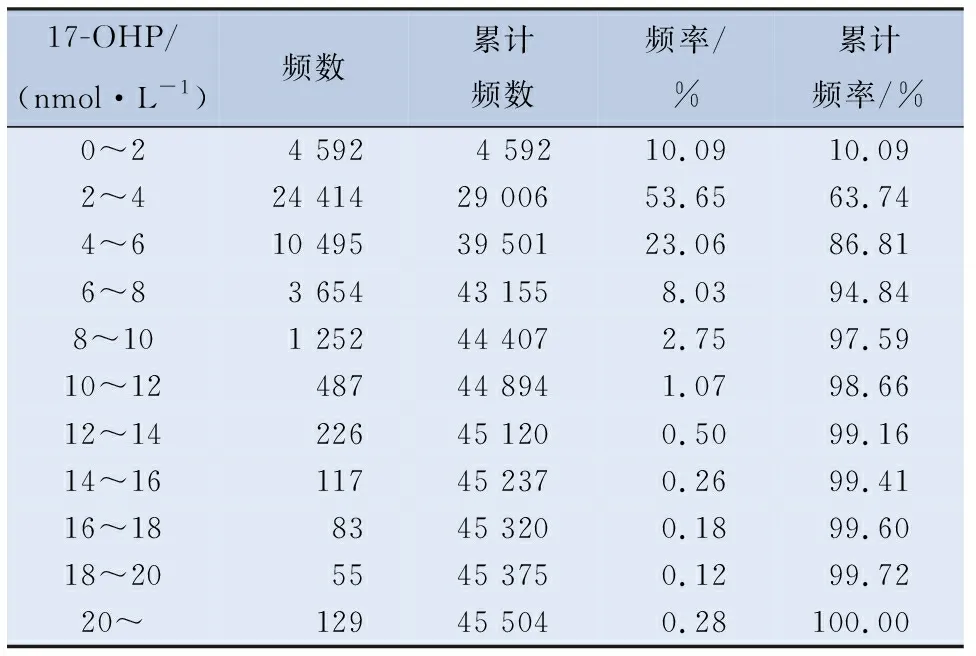
表1 17-OHP浓度频数分布表
2.2 17-OHP浓度与孕周的关系 将45 504例新生儿按出生孕周分为早产儿组(<37 w)和足月儿组(≥37 w)。其中早产儿2 517例,早产儿组17-OHP浓度分布水平为(8.6±6.3)nmol/L。早产儿组17-OHP浓度的95%百分位数和99%百分位数分别为19.12 nmol/L和32.87 nmol/L;足月儿42 987例,足月儿组17-OHP浓度分布水平为(3.8±2.7)nmol/L。足月儿组17-OHP浓度的95%百分位数和99%百分位数分别为7.20 nmol/L和10.01 nmol/L(表2),经统计学分析,早产儿组和足月儿组17-OHP浓度比较,P<0.01。

表2 早产儿与足月儿17-OHP浓度的比较
2.3 17-OHP浓度与体重的关系 将45 504例新生儿按出生体重分为低体重儿组(<2 500 g)和正常体重儿组(≥2 500 g)。其中低体重儿1 734例,低体重儿组17-OHP浓度分布水平为(8.8±6.6)nmol/L。低体重儿组17-OHP浓度的95%百分位数和99%百分位数分别为19.99 nmol/L和33.62 nmol/L;正常体重儿43 770例,正常体重儿组17-OHP浓度分布水平为(3.9±2.8)nmol/L。正常体重儿组17-OHP浓度的95%百分位数和99%百分位数分别为7.5nmol/L和10.7 nmol/L(表3),经统计学分析,低体重儿组和正常体重儿组17-OHP浓度比较,P<0.01。

表3 低体重儿与正常体重儿17-OHP浓度的比较
2.4 新生儿CAH筛查确诊情况汇总分 45 504例筛查标本中初筛阳性共计818例,其中早产儿543例,足月儿275例;低体重儿415例,正常体重儿403例。经召回复查确诊,最终确诊CAH共3例,均为男性患儿。确诊患儿17-OHP初筛值及孕周、体重详情见表4,CAH筛查发病率为1/15 168。

表4 确诊患儿17-OHP初筛值与孕周、体重统计表
3 讨论
CAH是一种常染色体隐性遗传病,主要包括21-羟化酶、11β-羟化酶、17α-羟化酶缺陷等类型,其中21-羟化酶缺陷症所占的比例高达90%~95%,是最常见的一种类型,通过对新生儿17-OHP浓度的检测能筛查出70%未出现临床症状的21-羟化酶缺陷,使患儿及时得到诊断和治疗。21-羟化酶缺陷症根据临床症状可分为单纯男性化型、失盐型和非经典型[2]。我国CAH发病率约为1/14 000~1/16 000[3],大连市2019年12月—2021年4月新生儿CAH发病率为1/15 168。
在新生儿疾病筛查实验中,建立合理的切值十分重要,所采用的切值是否合理将直接影响阳性结果的判断,若切值过高会增加漏诊的风险;若切值过低则会增加假阳性率,浪费人力、物力,并且还会给新生儿家长带来不必要的心理负担。因此,设立合适的阳性切值是CAH筛查的关键点。由于各筛查实验室筛查条件、方法不完全相同,且不同地区人群分布亦不同,因此各地区应建立适合本地区、本实验室的17-OHP合理切值。切值设置常用方法包括均值±标准差法、ROC曲线法及百分位数法。由于17-OHP浓度分布为偏态分布,因此适合使用百分位数法确定其切值。
国内研究表明,新生儿17-OHP浓度水平与新生儿出生孕周及体重有关,早产和低体重新生儿17-OHP浓度可有不同程度的增高[4-5]。因此,要制定与新生儿出生孕周、体重相关的17-OHP切值。本研究显示,两组新生儿17-OHP浓度差异具有统计学意义。本研究显示17-OHP浓度随体重增加而降低;且早产儿17-OHP浓度水平高于足月儿,这与国内其他学者研究报道[6-8]相一致。
胡定波等[9]研究表明,提前采血尤其是新生儿出生后24 h内就采血,会使CAH筛查的假阳性率明显升高。因此筛查的血标本采集时间不宜过早,各采血单位应严格按照采血规范采血、保存以及运输血片,以免造成假阳性或者假阴性。对于CAH筛查,国内多数新生儿疾病筛查实验室都有各自的阳性切值,目前全国并无统一标准。为了防止CAH病例的漏诊及尽可能减少初筛假阳性率,结合以上统计数据同时根据本实验室的实际情况,建议目前大连地区的足月且正常体重儿的17-OHP阳性切值不调整依然为11 nmol/L;而早产儿或低体重儿的17-OHP阳性切值切值适当调高暂定为30 nmol/L,待本实验室早产和低体重新生儿17-OHP数据积累到一定数量再重新计算并校正其切值。

