慢性粒单核细胞白血病合并单克隆免疫球蛋白血症1例*
李天寿,王健琨,刘 琴,黄锦雄
柳州市人民医院血液内科,广西柳州 545006
2008年世界卫生组织(WHO)将慢性粒单核细胞白血病(CMML)归入骨髓增生异常综合征(MDS)/骨髓增殖性肿瘤(MPN)中,MDS/MPN是一组髓系疾病,兼具骨髓发育异常和骨髓增殖的特点。CMML 患者的临床表现和预后具有高度异质性,目前的治疗手段包括去基化治疗及异基因造血干细胞移植术。单克隆免疫球蛋白血症(MGUS)由克隆性B细胞-浆细胞过度分泌单克隆免疫球蛋白所致,常见于浆细胞病及B细胞淋巴瘤。CMML伴发MGUS的病例国内外罕见,现就其报道并进行文献复习。
1 临床资料
1.1病历资料及检查结果 患者男,64岁,2019年7月因“腹胀”在本科住院,既往身体健康,无发热、咳嗽,无头痛,无牙龈出血、血尿、血便不适。查体:贫血貌,皮肤未见瘀斑及出血点,浅表淋巴结、肝、脾未扪及肿大。入院后查血常规及白细胞计数(WBC)手工分类:WBC 72.50×109/L,红细胞计数(RBC)3.68×1012/L,血红蛋白(Hb)72.0 g/L,血小板计数(PLT)77×109/L,中性粒细胞(N)百分比54%,单核细胞(M)百分比30%,幼稚白细胞百分比6%。骨髓细胞学:骨髓增生明显活跃,原始粒细胞占8%,原始单核细胞占1.5%,幼稚单核细胞占6%,成熟单核细胞占12.5%,形态学考虑CMML(图1)。骨髓活检病理:骨髓组织增生极度活跃(>90%),粒系核左移,粒红比例增大,均以中幼及以下阶段细胞为主,巨核细胞不少,分叶核为主;偶见胞体小、分叶少的巨核细胞;网状纤维染色(MF-0级);免疫组化:CD34个别(+)、CD117少许(+)、MPO粒细胞(+),CD3、CD20、CD79a淋巴细胞(+),Lyso散在(+)、TdT(-),形态学改变不除外MDS/MPN可能(图2)。骨髓免疫分型:淋巴细胞约占有核细胞的14%,各淋巴亚群分布大致正常,原始区域细胞约占有核细胞的1%,单核细胞约占有核细胞的35%,表型成熟,粒细胞约占有核细胞的52%,部分考虑存在发育异常,见图3。BCR/ABL融合基因阴性;染色体核型分析:46,XY[20]。
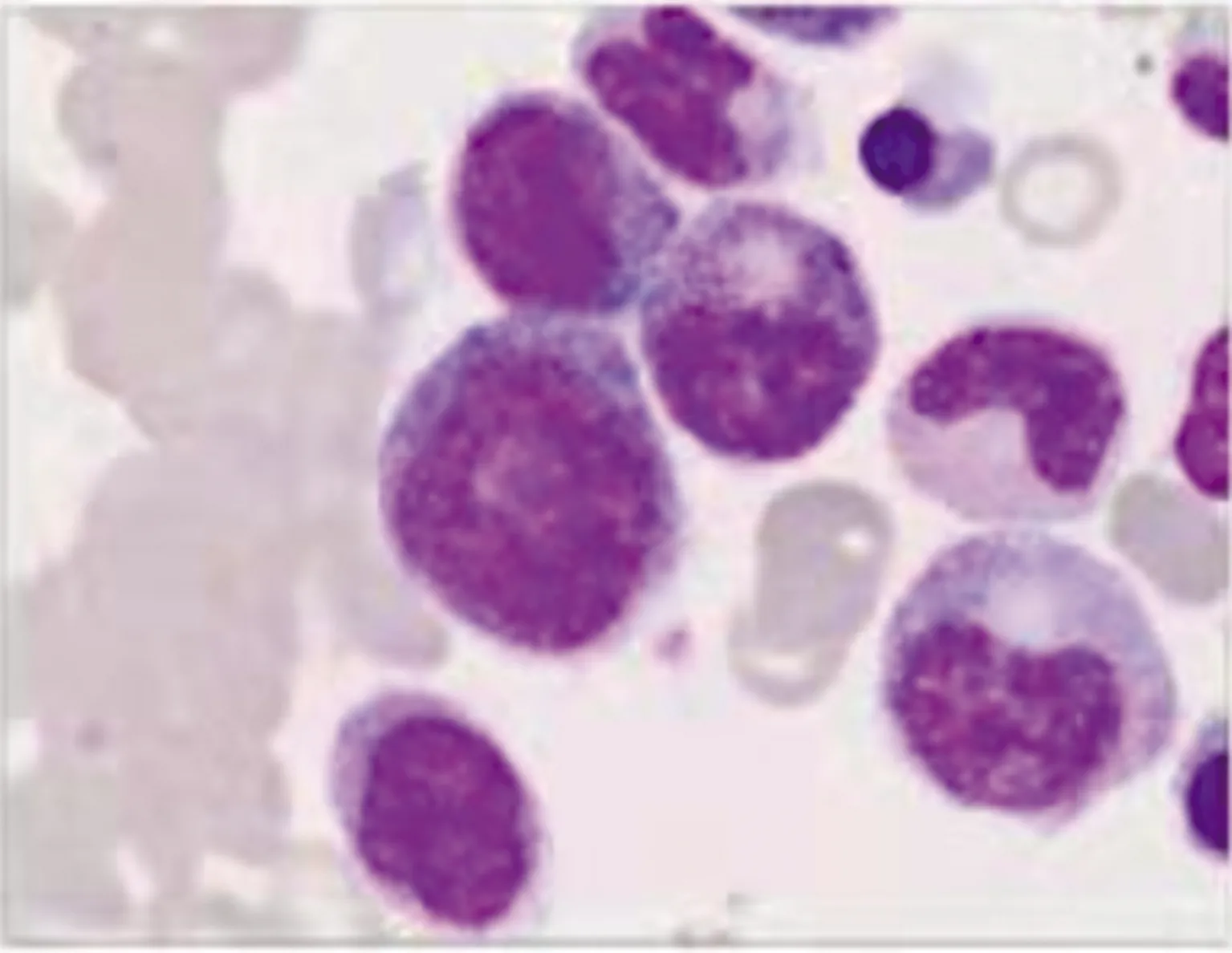
图1 骨髓细胞形态学(×1 000)
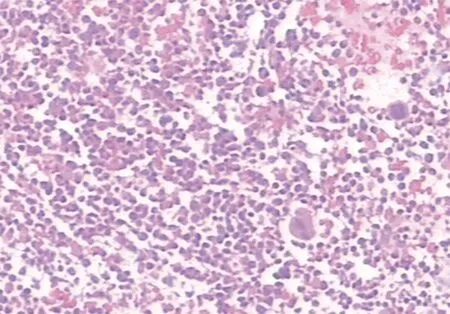
图2 骨髓活检病理(×10)
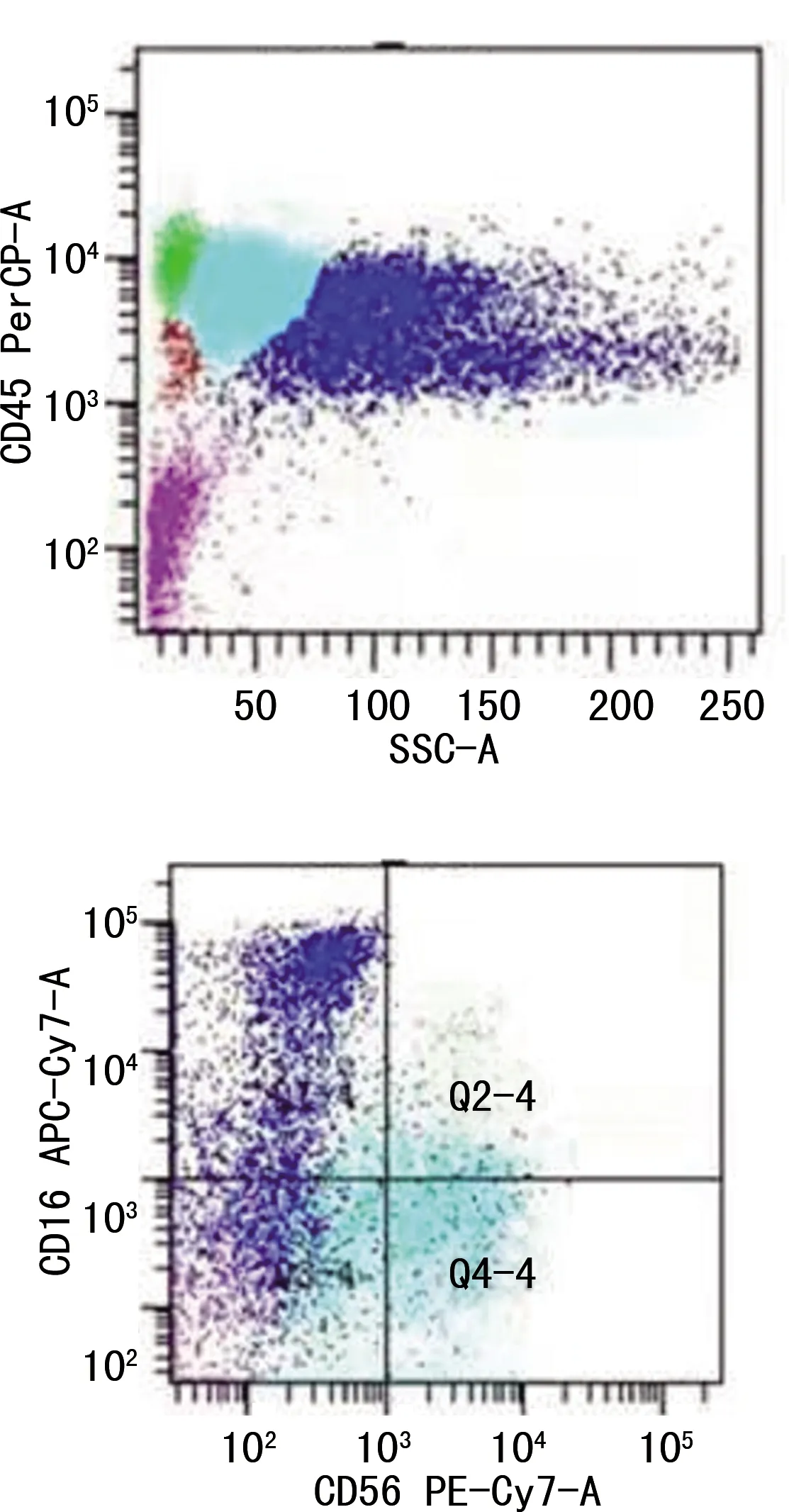
图3 患者骨髓免疫表型
1.2治疗过程 患者分别于2019年8月5日、2019年9月2日接受2个疗程地西他滨(20 mg,第1~5天)化疗。2019年11月再次返院,查血常规:WBC 43.88×109/L,RBC 3.93×1012/L,Hb 73.0 g/L,PLT 90×109/L,N 2.24×109/L,M 29×109/L。肝功能:总蛋白80.4 g/L,清蛋白30.2 g/L,球蛋白50.2 g/L,IgG 29.7 g/L。血清蛋白电泳:在γ区见异常浓染条带,疑为M带。免疫固定电泳:单克隆免疫球蛋白中IgG阳性,游离轻链λ 阳性。β2微球蛋白 5.8 mg/L。骨髓细胞学:原始粒细胞占3.5%,幼稚单核细胞占2.5%。骨髓活检病理:形态学改变不除外MDS/MPN可能。骨髓免疫分型:淋巴细胞约占有核细胞的4%,各淋巴亚群分布大致正常;原始及髓系区域细胞约占有核细胞的83.5%,原始细胞约占有核细胞的1.5%,单核细胞约占有核细胞的40%,部分细胞考虑存在发育异常,粒细胞约占有核细胞的41%,部分细胞考虑存在发育异常,另可见约1%的浆细胞,其cKappa/clambda 比值为1.16;提示单核细胞比例明显升高,伴部分细胞发育异常。随后分别于2019年11月23日、2019年12月20日、2020年4月18日、2020年6月6日、2020年10月12日接受地西他滨(20 mg,第1~5天)化疗,同时持续予以口服沙利度胺(100 mg,每晚一次)治疗。2020年6月6日返院复查血清蛋白电泳及免疫固定电泳为阴性。随访至2021年6月,患者有乏力,无发热、出血、骨痛不适,但因经济原因未返院治疗。
2 讨 论
2008年WHO将CMML归类为MDS/MPN,这类疾病的临床和血液学表现兼有MDS和MPN的特点,即骨髓髓系细胞存在过度增殖,而另外的髓系细胞存在病态造血或无效造血,外周血细胞表现为某类细胞明显升高,而其他类型细胞减少[1]。该患者外周血WBC、N、M均升高,M大于1×109/L;分子遗传学检测未见BCR/ABL融合基因异常,细胞遗传学正常,排除慢性粒细胞白血病;同时患者外周血及骨髓细胞学提示见幼稚细胞,但原始及幼稚细胞比率<20%;免疫分型提示粒系发育异常,故患者诊断CMML明确[2]。CMML目前尚无统一治疗方案,去甲基化药物(如地西他滨、阿扎胞苷)联合小剂量化疗为可能有效的治疗方案[3]。国内外临床血液工作者认为异基因造血干细胞移植是唯一能治愈CMML的手段,但移植后仍有一部分患者死于感染或疾病复发[4-6]。
患者病程中监测肝功能提示球蛋白升高,查IgG升高,电解质、肾功能正常;影像学检查未见骨质破坏表现;进一步完善检查提示血清蛋白电泳见M带,免疫固定电泳提示单克隆免疫球蛋白中IgG和游离轻链λ阳性;但患者复查骨髓细胞学及免疫分型未见浆细胞明显异常增生依据;故患者诊断为CMML合并MGUS。MGUS和白血病属于两种不同来源的疾病,但白血病合并MGUS并不少见。JIN等[7]报道了1例急性髓系白血病合并MGUS的病例,认为合并MGUS是急性髓系白血病独立的预后不良因素。意义未明的MGUS属于浆细胞疾病中的一大类,主要表现为血液中出现大量的单克隆免疫球蛋白,但无异常浆细胞增生及其引起的临床表现。已有的研究表明,MGUS患者可能会进展为骨髓瘤、华氏巨球蛋白血症、淀粉样变性或恶性淋巴瘤[8-9]。关于CMML合并浆细胞疾病的研究较少,杨英等[10]报道了1例CMML合并多发性骨髓瘤的病例;徐敏等[11]报道了1例冒烟型骨髓瘤合并CMML的病例。这些已报道的病例表明,CMML有可能合并恶性浆细胞疾病,但其中机制尚未明确。本例患者骨髓免疫分析提示异常表达CD56(图3),CD56 又称神经细胞黏附分子(N-CAM)。研究认为,CD56(+)细胞起源于髓系/自然杀伤细胞的前体细胞,异常表达CD56的血液恶性肿瘤更具侵袭性,预后更差[12]。蔡梦洁等[13]通过研究流式细胞术检测多发性骨髓瘤循环肿瘤浆细胞免疫表型,发现循环肿瘤浆细胞CD56阳性率占81.7%。丁雅雯等[14]通过检测骨髓瘤免疫表型,发现多发性骨髓瘤浆细胞CD56阳性率占65.71%。这些研究表明,CD56(+)细胞为更早期的祖细胞,CMML患者CD56(+)肿瘤细胞在肿瘤克隆演化过程中存在浆样分化可能。
沙利度胺是一种免疫调节剂,可抑制肿瘤血管新生,目前较多应用于治疗浆细胞疾病及恶性淋巴瘤[15]。SWAMINATHAN等[16]报道了1例慢性粒细胞白血病患者,服用伊马替尼治疗后达到分子学缓解,但停药后复发,复发后检查提示合并MGUS,再次予以伊马替尼治疗后病情得到缓解,随后检查发现合并多发性骨髓瘤,予以沙利度胺、硼替佐米联合地塞米松治疗多发性骨髓瘤,并继续予以伊马替尼治疗慢性粒细胞白血病,后患者病情得到控制。也有相关研究证明沙利度胺可应用于治疗CMML[17]。KENEALY等[17]开展的一项关于沙利度胺联合阿扎胞苷治疗MDS、CMML、低增生急性髓系白血病(AML)的临床研究表明,沙利度胺联合阿扎胞苷治疗MDS、CMML、AML是安全的,且能提高这3类疾病患者的总生存时间。本例患者病程中发现合并MGUS,在原有地西他滨的治疗方案上加用口服沙利度胺治疗。经治疗,患者乏力症状改善,血象WBC得到控制,MGUS转阴。
合并MGUS可能是CMML预后不良的危险因素。CMML合并MGUS罕见,如患者球蛋白升高,且血清蛋白电泳、免疫固定电泳阳性,应完善骨髓形态学、免疫分型以及遗传学检查明确是否合并多发性骨髓瘤、淋巴瘤可能;地西他滨联合沙利度胺治疗可能有效。期待有更多CMML合并浆细胞疾病的研究,以阐明其机制。

