基于实验探究的“溶解度”一课的概念教学
周娜
摘要:分析了“溶解度”在教材中的地位,通过实验探究引发学生的思维冲突,让学生发现问题、解决问题、大胆质疑、勤于反思,学生的核心素养在课堂教学中得到培养。
关键词:实验探究;溶解度;概念教学;核心素养
文章编号:1008-0546(2022)10x-0092-04中图分类号:G632.41文献标识码:B
一、教学主题内容和背景分析
“溶解度”选自沪教版九年级化学下册,[1]这一教学内容安排在物质的溶解性之后,学生有溶质、溶剂、溶液、溶解性、饱和溶液等知识的基础,同时此节内容为后续学习结晶奠定了基础。
本节课主要内容是:溶解度概念的认知,溶解度曲线理解与应用。
课标要求:了解溶解度概念;利用溶解度表或溶解度曲线,查阅物质的溶解性或溶解度;依据给定的数据绘制溶解度曲线;认识溶解度在生活中的重要作用。[2]
溶解度的学习,不仅使学生学会利用溶解度来定量表示物质的溶解性,还使学生认识到定量方法在化学学习中的重要性。
已有的教学设计中的教学思路对概念的建构过程过于弱化,一般是给出概念后,让学生理解,教学重点放在了概念的应用。[3-5]
二、教学思想与创新点
溶解度在生产、生活中有非常重要的应用。比较溶解性的限定条件是什么?笔者选取“茶卡盐湖中的项圈”现象引发思考。“项圈”中的成分很复杂,选取其中的氯化钠、硫酸钠、硫酸钙,通过层层实验对比探究,引发思考,挖掘比较溶解性的限定条件,引出溶解性强弱的定量表示:溶解度。再通过两种表示方式,挖掘信息,体会溶解度表示方法的优缺点。
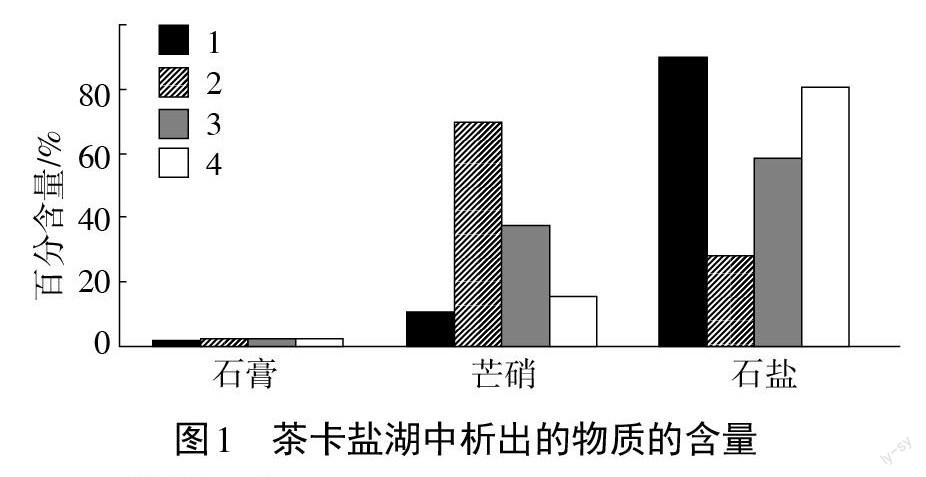
最终回归盐湖中的真实情况,[6]体会溶解度、浓度的重要关系(见图1)。体会到化学可以解决生产、生活中的实际问题。
三、教学目标
1.通过实验探究了解溶解度概念,体会化学实验探究方法,锻炼学生的探究能力。
2.通过溶解度的两种表示方法,学会数据处理,并用溶解度曲线解决实际问题。
3.通过了解溶解度的应用,体会化学与生活的密切关系,体会化学学科价值。
四、教学流程
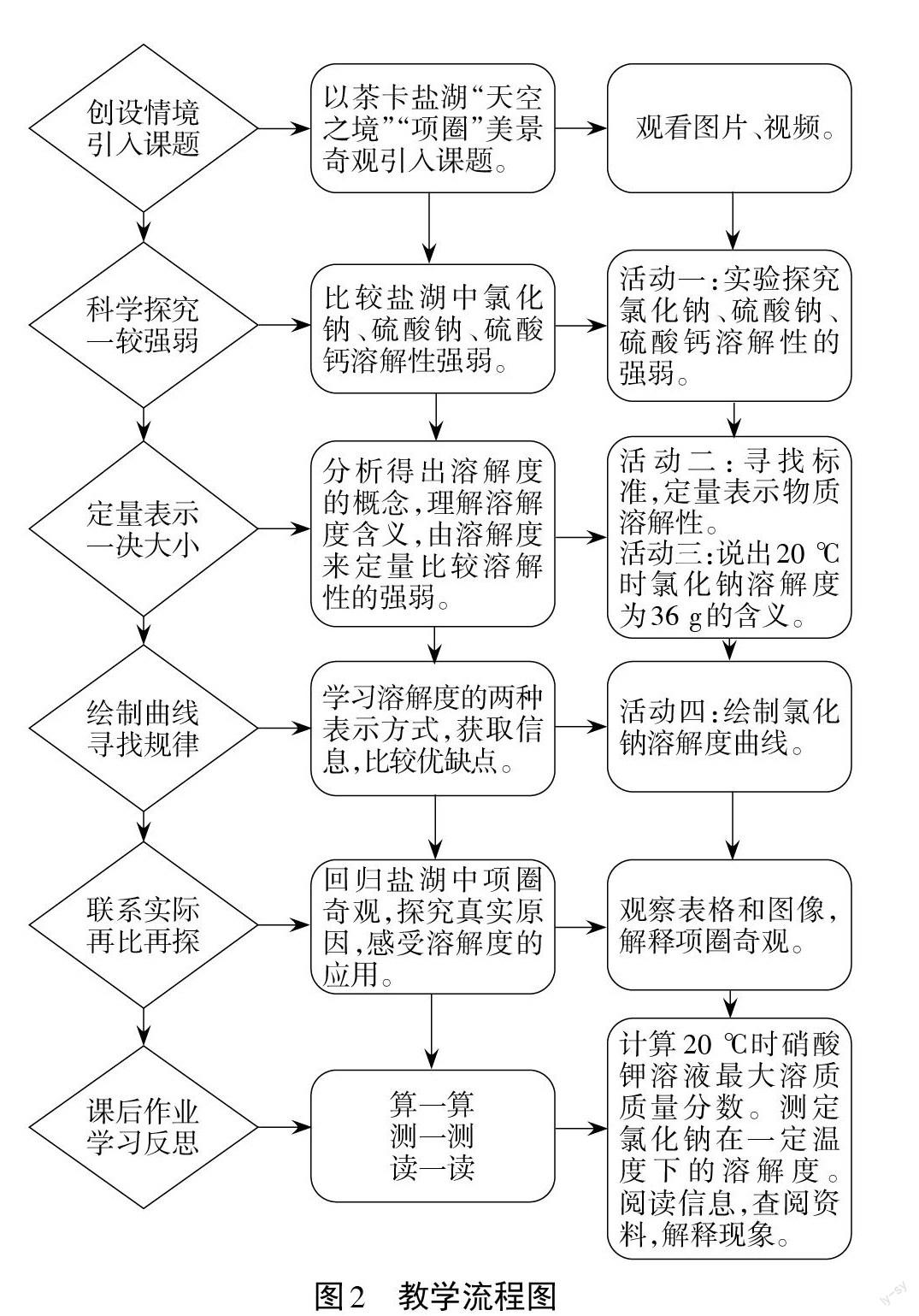
“溶解度”一课的教学流程见图2。
五、教学过程与意图
1.创设情境引入课题
[引入]同学们,请欣赏一组图片,这是位于我国青海省乌兰县的茶卡盐湖,这里被中国旅游地理杂志评为“人一生必去的55个景点之一”。“茶卡”蒙语是盐海的意思,为什么叫盐海?这是因为茶卡盐湖中有多种盐类物质。你们看,多么美丽的景观啊,蓝天白云清晰地倒映在湖中,湖面多么像一面为天空梳妆打扮的镜子啊。所以茶卡盐湖又被誉为中国的“天空之境”。茶卡盐湖还有另外一个奇观,请同学们再来欣赏一段视频。视频中析出的物质一圈一圈挂在湖中,就好像为盐湖戴上了项圈。
[问题1]同学们知道这些美景奇观是怎么形成的吗?这与我们今天要学习的内容有关。今天我们来学习溶解度。
[交流]通过上一课时的学习,我们已经知道物质在水中不能无限溶解。这说明物质在水中的溶解是有极限的,叫溶解限度(板书),物质的溶解限度大小与溶解性有关。溶解性越强,溶解限度越大,也就是说物质在水中溶解的质量也越大。
[问题2]溶解性又受到什么因素影响呢?(板书:温度、溶质、溶剂)当这些条件改变了,溶解性的强弱也就会发生改变。
[陈述]研究发现,茶卡盐湖中溶有许多物质,比如:氯化钠、硫酸钠、硫酸钙等。随着天气的变化,这些物质会争先恐后地析出,析出的物质沉积在湖底,使湖面对光产生强烈的反射。这些物质环湖析出,就会出现一圈一圈的项圈。
[问题3]那么湖水中的物质在什么条件下会析出?谁又更容易析出呢?
[总结]这与物质溶解性的强弱有重要的关系。溶解性越强的物质,也就是越容易溶解的物质,越难析出。溶解性越差的物质越易析出。
设计意图:以茶卡盐湖中的特殊景象引入,从生活走进化学,吸引学生注意力,激发学习思考,养成用化学知识思考问题的习惯。
2.科学探究一较强弱
[问题1]如何比较氯化钠、硫酸钠、硫酸钙溶解性强弱?
[活动一]设计实验,比较氯化钠、硫酸钠、硫酸钙溶解性强弱。小组交流讨论,提出方案。
方案一:相同溫度、等量水,加固体至饱和,比较加入固体质量。
方案二:相同温度、等量固体,加水至恰好溶解,比较用水量。
[问题2]这两种方案,控制了哪些相同条件?不同的条件是什么?
[分组实验]取10mL的水,再分别加0.5g三种物质中的一种,比较它们的溶解性,结论如表1所示。
[问题3]你观察到了什么现象?为什么说硫酸钙的溶解性最弱?
[追问]根据实验的现象,你有什么疑惑?怎么能在刚刚实验基础上进一步比较氯化钠、硫酸钠两者溶解性的强弱?
小组交流讨论。提出方案:继续加药品至溶液饱和,比较加入药品的质量。
[分组实验]在每个小组的实验盒中,老师分别给大家准备了2g的氯化钠和硫酸钠。请分别继续加入药品,继续探究。再次记录实验现象(见表2)。
[总结]通过两组实验探究,发现此温度下氯化钠的溶解性强于硫酸钠强于硫酸钙。
[过渡]我们在比较氯化钠和硫酸钠溶解性强弱的实验中,发现硫酸钠没有完全溶解,怎么才能完全溶解?
提出方案:加水,升温。
我们的实验都是在等量水中进行,下面采用加热的方法看看。
[分组实验]将保温杯中热水倒入大烧杯中至标记处,参照导学案“实验三”对其进行水浴加热。边加热边用玻璃棒不断搅拌。
[追问]加热后硫酸钠固体完全溶解,说明了什么?
现在几种物质的溶解性强弱还是这样一个顺序吗?
[总结]条件改变了,溶解性强弱也改变了,因此要想比较物质的溶解性强弱还要建立统一的标准。
设计意图:从实验中发现不同形成认知冲突,学习应用控制变量实验方法。培养学生实验操作能力、语言表达能力,交流讨论和小组合作解决问题能力,体会科学探究的重要性。
3.定量表示一决大小
[问题1]具体比较溶解性强弱的标准是什么呢?请结合实验分析标准该怎么制定呢?
[活动二]寻找标准,定量表示物质溶解性。
[交流]在一定温度下,我们规定溶剂质量为100g(通常为水),比较溶解的溶质的质量。这个溶质的质量,我们又给了它一个新的名词“溶解度”。
[问题2]你能给溶解度下定义吗?
[追问]有了溶解度的概念,我们又怎么比较物质溶解性的强弱呢?
[活动三]观察与思考:从表3中你能获取哪些信息?说一说,20℃时,氯化钠溶解度为36g的含义是什么?
[学生1]20℃时,100g水中,达到饱和状态,溶解的氯化钠质量为36g。
[学生2]20℃时,100g水中,最多溶解的氯化钠质量为36g。
……
[教师]一定温度下,某种物质的饱和溶液中溶质和溶液的质量比值是一定的,这个值跟溶解度有关。
20℃时,硫酸钠溶解度是19.5g是什么意思?
[总结]有了溶解度的值,可以定量表示物质溶解性的强弱。现在你能说说氯化钠、硫酸钠、硫酸钙的溶解性谁强谁弱了吗?20℃时,氯化钠溶解度是硫酸钙的上百倍。
设计意图:在交流中形成认知冲突,知道控制变量法的重要思想。培养学生归纳总结能力。帮助学生提取有效信息,深层次理解溶解度,知道溶解度可以定量表示物质溶解性。
5.绘制曲线寻找规律
[问题1]当温度改变时,两者溶解性的强弱又如何?
[活动三]观察与思考:从表4中你又能获取哪些信息?
[追问]如何比较25℃时,氯化钠和硫酸钠的溶解性谁强谁弱?
[学生]画图比较?
[教师]怎么画?请以氯化钠为例说一说。
[活动四]学生根据溶解度表绘制氯化钠的溶解度曲线(见图3)。
[问题2]从曲线你能获取哪些信息?点的含义是什么?你能说说列表法和图像法的优缺点吗?
[追问]同样的道理,也可以画出硫酸钠溶解度随温度变化的曲线。如果想直观比较出不同温度下氯化钠和硫酸钠溶解度的大小,怎么办?
从图4你又能获取哪些信息?交点的含义是什么?
现在你能说说25℃时氯化钠和硫酸钠溶解度谁强谁弱了吗?
设计意图:学会通过表格、图像比较溶解度大小,学会分析图像,在图像中提取有效信息。
5.联系实际再比再探
[问题1]通过以上探究,你能试着解释茶卡盐湖的奇景“盐湖项圈”形成的原因吗?其中什么样的物质容易析出?它与溶解度有什么关系?
[追问]是不是溶解度小的物质就一定会析出呢?观察表5,你觉得谁会析出得更多?
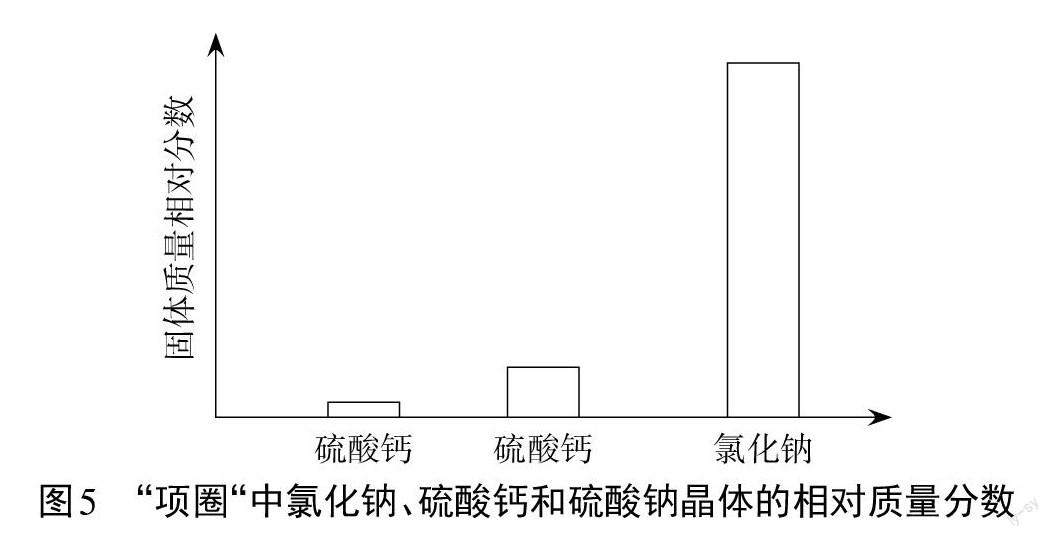
[观察]“项圈”中氯化钠、硫酸钙和硫酸钠晶体的相对质量分数的柱状图(见图5)。
[再追问]为什么溶解度最小的硫酸钙析出得最少,而溶解度较大的氯化钠析出得最多?
[总结]溶液中物质是否析出,什么时候析出,既与物质溶解度有关,又与溶液中该物质的浓度有关,利用这一原理,可以控制温度和浓度来调控物质的析出,从而达到分离、提纯这些物質的目的。
[问题2]通过本节课对溶解度的探究,关于溶解度你有哪些认知?
[总结]课堂小结。
设计意图:知识迁移解释现象;联系实际,形成冲突;综合应用知识,分析解决问题,体会化学与生活息息相关,体现学科价值。
6.课后作业学习反思
[课后作业]
算一算:20℃时,硝酸钾溶液的溶质质量分数的最大值。
测一测:利用身边的物质和用品设计实验,测定氯化钠在一定温度下的溶解度。
读一读:查阅资料,解释“夏天晒盐,冬天捞碱”的现象,并利用查阅的信息对该现象做出解释。
设计意图:培养学生动手能力、阅读能力和分析、解决问题的能力。
六、教学反思
本节课由于概念的限定比较多,学生学习时易产生非胜任感。教学中应重视学生已有认知,强化概念的建构和理解。
1.抓住已有认知,开展实验探究,找寻溶解度定义的限定条件。通过采用科学探究的形式,层层比较,引出限定条件,提出问题,最终解决问题。让学生感知到科学探究对于化学学习的重要性。
2.思维提升,弄清楚概念的内涵。限定溶解度的条件为:一定温度下,饱和状态时,一定量的水中溶解的溶质的质量。弄清楚限定的条件,为什么要限定这些条件?比较的是什么?
3.多重表征,由定性到定量。通过实验,让学生初步感知不同物质在限定条件下溶解度不同。再用溶解度的具体数据比较,定量获知一定条件下物质的溶解度大小,溶解性强弱。用图像表征,粗略获知不同温度下物质的溶解度,比较物质溶解性的强弱。
4.联系生活实际,让学生感受到溶解度与生活息相关。溶解度可以帮助解决生产、生活中的问题,体现化学学科价值。
参考文献
[1]中国化学国家课程标准研制组.义务教育教科书(化学九年级下册)[M].上海:上海教育出版社,2015.
[2]中华人民共和国教育部.义务教育化学课程标准(2011年 版)[S].北京:北京师范大学出版社,2012.
[3]殷志忠.初中化学“溶解度”的改进[J].化学教学,2020(9):94-97.
[4]黄兵.初中化学概念的建立与巩固——以《溶解度》教学设计为例[J].江苏教育研究,2010(11):53-54.
[5]何如涛.初中化学“溶解度概念”的教学与反思[J].化学教学,2013(3):37-38.[6]刘兴起.基于Pitzer模型的茶卡盐湖卤水及盐类矿物形成的地球化学模拟[J].中国科学,2003(3):247-254.

