壳聚糖联合酶诱导碳酸盐沉淀处理铜废水的劣化现象和强化机理研究
徐银龙,郑文杰,王琳,薛中飞,谢毅鑫
(1 西安建筑科技大学土木工程学院,陕西西安 710055; 2 陕西省岩土与地下空间工程重点实验室,陕西西安 710055)
引 言
随着全球经济的迅速发展及工业进程的加快,重金属污染物通过各种途径进入土壤和河水,导致大气和水环境质量进一步恶化[1]。重金属污染是一个国际上环境工程领域的关键问题,关乎人类健康和社会的可持续发展。矿山开采、印刷、电镀、化工等行业产生的废水中含有大量的铜离子(Cu2+),在自然环境中极易发生扩散和运移[2]。铜(Cu)进入人体内会形成富集,导致人体生长发育异常、致癌、智力低下并引发一系列其他疾病[3-4]。
铜废水的主要处理技术包括化学沉淀法、离子交换法、电化学法、吸附法、微生物法等,但化学沉淀法无法形成稳定的沉淀从而产生大量的污泥并容易造成二次污染,离子交换法、电化学法、吸附法处理成本高昂,微生物法所使用的微生物对环境要求较高无法处理高浓度的铜废水[5]。酶诱导碳酸盐沉淀(EICP)是一项主要用于土壤改良的新兴的修复技术,鲜少用于铜废水的处理。相较于上述处理技术,这一方法可形成稳定的碳酸盐沉淀结构从而避免污泥的产生,适应各种环境,操作简单高效,因此备受同领域学者和从业人员关注[6-7]。
EICP 方法的实施原理即利用脲酶催化尿素水解为铵根离子(NH+4)和CO2-3[式(1)~式(3)],进而与铅离子(Pb2+)、锌离子(Zn2+)、铬离子(Cr2+)、铜离子(Cu2+)等结合形成碳酸盐沉淀从而防止重金属离子扩散运移,最终达到处理、固化重金属污染的目的[8-10]。Nam 等[11]应用EICP 技术固化重金属和类金属,研究结果表明砷、锰、锌、铅、铬和铜的浓度分别大幅降低了31.7%、65.8%、50.6%、51.6%、45.1%和49.7%。Moghal 等[12-13]发现EICP 能有效沉淀镉、镍和铅的碳酸盐,同时还引用乙烯二胺四乙酸(EDTA)和柠檬酸对固化后的重金属进行萃取,结果表明EICP技术可以有效降低重金属的解吸水平。
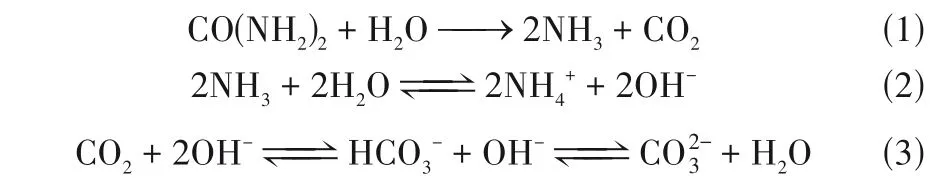
虽然EICP 在重金属固化方面有很好的应用前景,但Wang 等[14]的研究表明在铜废水浓度低于5 mmol/L 时EICP 方法才能发挥出较大作用,而就前人研究来看,实际的污染浓度早已超越这一范围,因此在高浓度铜污染背景下的EICP 修复方法研究甚是缺乏。另外,高浓度的铜离子会显著影响脲酶活性,进一步降低铜废水处理效果[15-17]。因此,需寻找一种材料和方法来保护脲酶免受铜离子毒性作用影响。
壳聚糖是以虾蟹外壳中的甲壳素为原料,经脱乙酰化得到的线性聚阳离子生物聚合物[18-21]。因其优异的吸附性、生物相容性和生物降解性而被广泛应用于蛋白质的吸附与酶的固化[22-24]。以往的研究表明,壳聚糖多与微生物诱导碳酸盐沉淀(MICP)技术联用改善生物矿化的结构[25],却鲜少用于重金属污染的固化。壳聚糖作为一种大分子物质(分子量在5000 以上),Hamdan 等[26-27]进行试验表明生物大分子胶体的加入会使碳酸盐晶体之间的相互作用更紧密,并且可以延长EICP 反应时间,提高沉淀效率使得沉淀结构更为稳定。因此,基于以上研究现状,本研究的主要目的是:(1)研究在酶诱导碳酸盐沉淀处理铜废水中,脲酶活性对处理效率的影响;(2)探求钙源添加对沉淀形态和处理效率的影响;(3)揭示壳聚糖联合酶诱导碳酸盐方法处理铜废水的强化和劣化机理。
1 试验材料和方法
1.1 试剂与主要仪器
1.1.1 化学试剂 本试验所用试剂均为分析纯:尿 素[CO(NH2)2];氢 氧 化 钠(NaOH);钙 源[CaCl2;Ca(CH3COO)2];冰 醋 酸(CH3COOH);无 水 乙 醇(C2H5OH);硝酸铜[Cu(NO3)2];壳聚糖(chitosan,脱乙酰度≥95%);去离子水;干燥刀豆。
1.1.2 试验仪器 粉碎机;电子天平;磁力搅拌器;冰柜;烘干机;pH 计(HANNA HI2003);电导率仪(HANNA HI2314);台式高速离心机(常州市金坛勒普仪器TG16G);分光光度计(上海仪电分析仪器721G);原子吸收分光光度计(北京普析通用仪器TAS-990SVPERF)。
1.2 试验方法
1.2.1 脲酶制备与活性测量 本研究所用脲酶提取步骤为:①将刀豆置于粉碎机中粉碎,过筛备用,储存时应注意低温、密封;②取豆粉溶于乙醇溶液中,置于磁力搅拌器上搅拌10~20 min 至均匀;③将豆粉溶液放入离心机离心30 min;④取离心管上清液,于冷柜中静置4 h;⑤将静置后的溶液再次离心1 h;⑥离心完成后分离上清液,沉淀即为所用脲酶。
电导率法测量脲酶活性:室温下,将1 mol/L 尿素溶液30 ml和0.09 g 脲酶混合,使用电导率仪每隔5 min 测定混合溶液的电导率变化,连续测定3 次,取均值;根据Whiffin[28]提出的电导率法进行脲酶活性测量,即1 mS/(cm·min)的电导率变化对应11.1 mmol/(L·min)的尿素水解量,再乘以稀释倍数,计算脲酶每分钟水解尿素量,为刀豆脲酶活性的量化指标。脲酶活性(每克)=电导率(每分钟)×11.1×稀释倍数/脲酶浓度,得到尿素水解量为1.47 mmol/(g·min)。
1.2.2 壳聚糖胶体制备 将一定质量的壳聚糖加入质量分数为1%的醋酸溶液中,置于磁力搅拌器上搅拌至无肉眼可见颗粒,再加入NaOH 调节pH 至弱酸性即配制完成[29]。本试验所使用的壳聚糖浓度为4 g/L和2 g/L。
1.2.3 铜废水处理过程 将脲酶溶于去离子水中得脲酶溶液,将脲酶溶液与壳聚糖胶体混合搅拌均匀,再加入尿素溶液搅拌均匀即为本试验所用的修复液,将上述修复液加入至不同浓度的硝酸铜和钙源混合的污染液中,反应过后进行剩余铜离子浓度、铵根离子浓度、pH测量。剩余铜离子浓度通过原子吸收分光光度计测量,铵根离子浓度通过纳氏试剂法测量,pH通过pH计测量。本试验方案如表1所示。根据式(4)计算铜废水处理效率:

表1 试管试验方案Table 1 Testing scheme applied to the present work
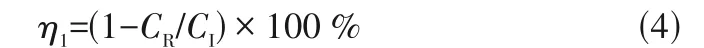
式中,CI为铜离子初始浓度,mmol/L;CR为处理后铜离子剩余浓度,mmol/L。
1.2.4 软件模拟 为了评估脲酶活性和钙源对铜废水处理效率的影响,使用Visual MINTEQ 3.1 软件进行模拟。脲酶催化尿素水解这一生物过程通过添加尿素水解产物,即铵根离子和碳酸根离子来体现,该软件可通过添加由试管试验中所测得的铵根离子和碳酸根离子来重现化学平衡反应的产物。数值模拟输入参数如表2所示。
表2 数值模拟输入参数Table 2 Simulation scheme applied to the present work
2 试验结果与讨论
2.1 脲酶活性对铜废水处理的影响
由式(1)~式(3)可知,氢氧根离子和铵根离子作为脲酶催化尿素水解的产物,可以通过测量铵根离子浓度和pH 来反映脲酶活性和尿素水解程度,即铵根离子浓度和pH 越高,脲酶活性越高尿素水解程度越高。结果表明在未添加壳聚糖的试样中均未检测出NH4+,说明此时脲酶处于失活状态,无法在EICP过程中实现尿素水解,故后续剩余铜离子浓度、处理效率没有再进行测量和计算。脲酶失活的本质是铜离子结合脲酶上的巯基(—SH),从而改变其结构使其失活[28]。
基于前述量测结果,本研究拟添加不同浓度壳聚糖联合酶诱导碳酸盐沉淀技术开展后续试验,结果如图1 所示。在添加壳聚糖的试样中,铵根离子浓度最高达330 mmol/L,并随着壳聚糖浓度增加而增加,随着铜离子浓度增加呈降低趋势[图1(a)]。另一方面,添加壳聚糖的试样中,pH 的测量结果最高达9 以上,并且pH 随壳聚糖浓度的增加而增加,同时随铜离子浓度增加而降低[图1(b)]。此结果说明壳聚糖能稳固脲酶活性进而保证尿素水解。根据剩余铜离子浓度和式(4)计算处理效率。如图2所示,处理效率分布在18%~94%范围,在尿素水解程度较高即铵根离子浓度较高(4 g/L 壳聚糖)和初始铜离子浓度较低(5 mmol/L 和10 mmol/L)的情况下,处理效率却更低。在以往的研究中显示,脲酶的活性越高,重金属处理效率会越高[6]。然而本研究结果显示脲酶活性与铜处理效率不成正比关系。
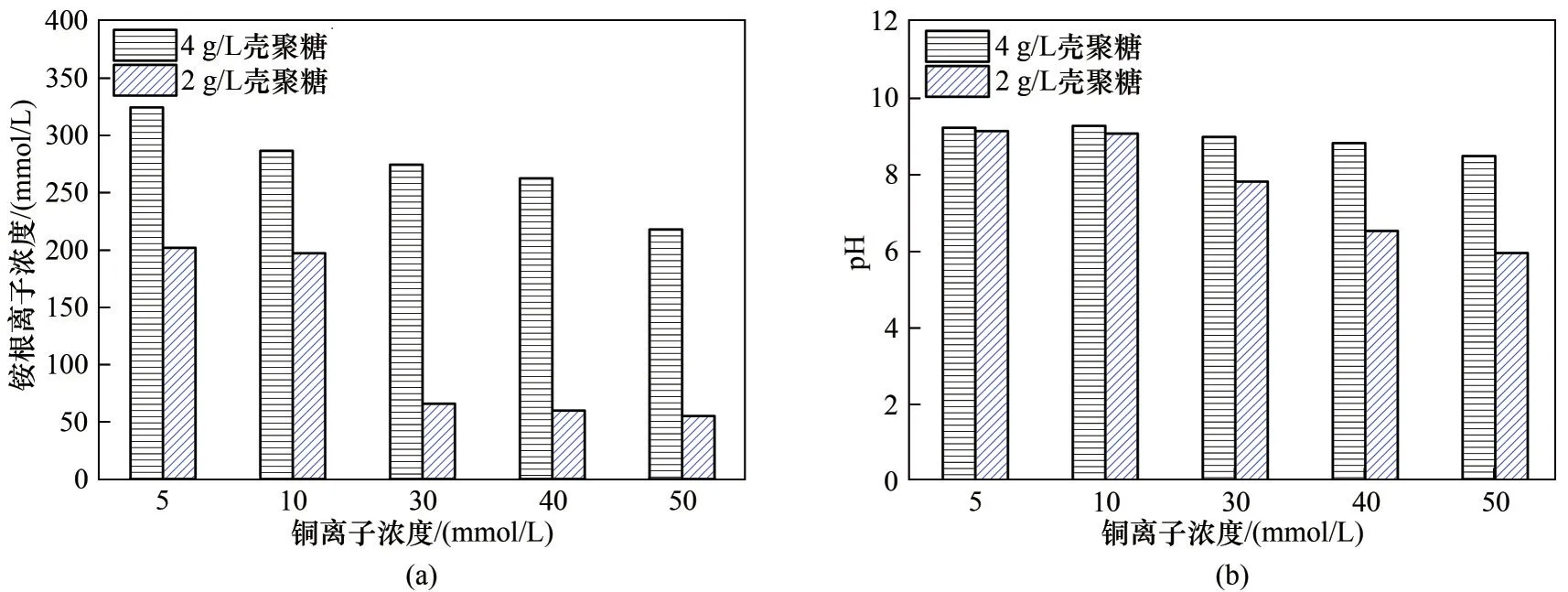
图1 考虑添加壳聚糖铵根离子浓度和pH随铜离子浓度的变化Fig.1 NH4+concentration and pH versus Cu2+concentration using the chitosan-assisted EICP method
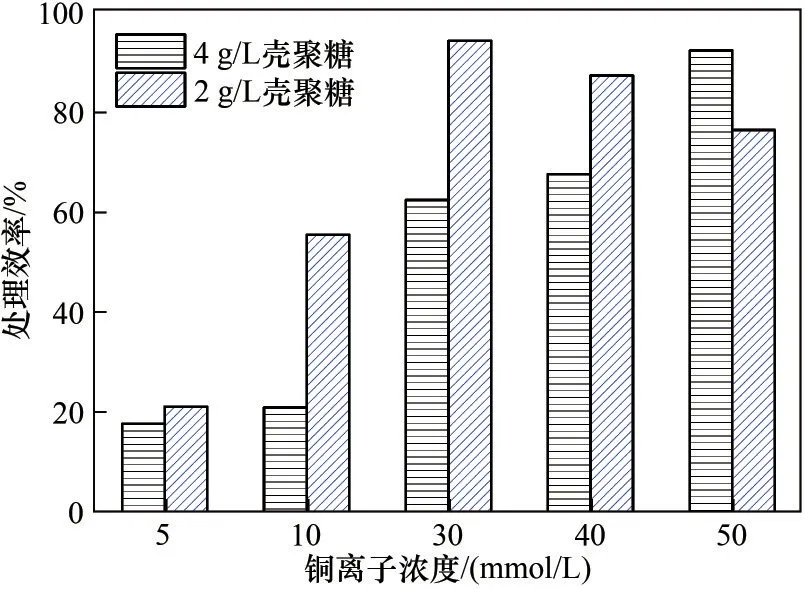
图2 考虑添加壳聚糖处理效率随铜离子浓度变化Fig.2 Treatment efficiency versus Cu2+concentration using the chitosan-assisted EICP method
进一步地,由数值模拟分析讨论壳聚糖联合酶诱导碳酸盐沉淀的相关产物,探究影响铜处理效率的因素。数值模拟通过实际测量得出的铵根离子和碳酸根离子浓度作为输入参数(图1),考虑不同壳聚糖浓度下重现试管试验EICP 过程。由图3 可知,铜的相关产物主要为孔雀石[Cu2(OH)2CO3]、蓝铜矿[Cu3(OH)2(CO3)2]和铜氨络合物[[Cu(NH3)n]2+,n=1~4][式(5)~式(7)]。
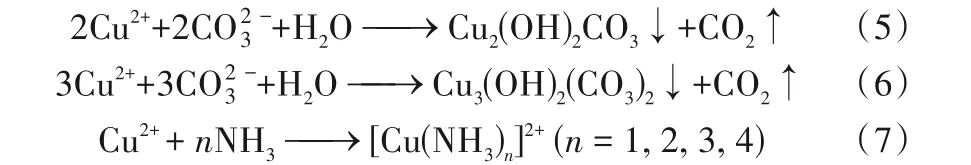
孔雀石和蓝铜矿以沉淀形式存在,形态稳定且不易分解,而铜氨络合物以离子形态存在,易扩散迁移,从而劣化处理效果[30]。由图3(a)得,铜离子浓度为30 mmol/L时,铜相关的产物只有Cu3(OH)2(CO3)2,浓度接近于10 mmol/L,即沉淀了30 mmol/L 的Cu2+,此时处理效率接近100%(图2)。铜离子浓度为5 mmol/L 时,铜产物为[Cu(NH3)n]2+,浓度接近于4 mmol/L,由式(4)计算处理效率低至20%(图2)。由图3(b)得,铜离子浓度为50 mmol/L 时,生成铜的沉淀只有Cu2(OH)2CO3,浓度接近于25 mmol/L,即沉淀了50 mmol/L的Cu2+,此时处理效率约为100%(图2)。以上数值模拟得出的结果与试管试验量测结果一致。由图2 可得,铵根离子浓度越高处理效率反而越低的原因在于形成铜氨络合物,造成游离铜的浓度较高从而劣化处理效率。铜氨络合物的形成与氨的浓度紧密相关,本研究中氨主要来源于尿素水解,而尿素水解程度与脲酶活性密切相关。图1、图2的结果也证明壳聚糖浓度越高,脲酶活性越高,使得尿素水解程度较高,令溶液中的铵根离子和pH 较高,提供铜氨络合物形成的优良条件。基于以上讨论,本研究通过精细化数值模拟探究尿素水解程度以及铜氨络合物的形成条件,以有效提高处理效率。
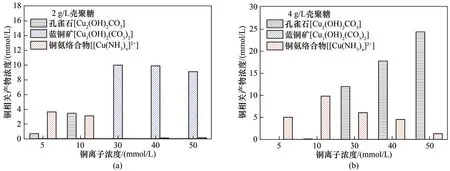
图3 考虑添加壳聚糖碳酸盐沉淀随铜离子浓度的形态分布Fig.3 Speciation of carbonate precipitation versus Cu2+concentration using the chitosan-assisted EICP method
2.2 不同尿素水解程度下沉淀形态分析
2.2.1 未添加钙源 从图1(a)可知,壳聚糖能够显著提高脲酶活性,使铵根离子浓度高达330 mmol/L。为研究不同尿素水解程度对沉淀形态和处理效率的影响,数值模拟中引入铵根离子浓度范围为100~700 mmol/L,对应的碳酸根离子浓度范围为50~350 mmol/L。未添加钙源时不同尿素水解程度下沉淀形态如图4所示,主要沉淀形态包含蓝铜矿、孔雀石和黑铜矿,其余均以铜氨络合物和铜离子等离子形式存在。由分析结果可知铜浓度低于20 mmol/L,铵根离子浓度在300 mmol/L 以上时,形成了大量的铜氨络合物,相应的处理效率接近于0,此时溶液pH在9以上(图4)。铜离子浓度高于50 mmol/L,铵根离子浓度在200~300 mmol/L 范围时,处理效率接近100%,此时铜主要以前述三种沉淀形式存在。由试管试验和数值模拟的结果得,铵根离子浓度随铜浓度增加而减少,当铜离子浓度较低时铵根离子浓度越高且pH越高[图1(b)和图4(c)],这种情况下形成了大量铜氨络合物(图3),说明碱性环境是铜氨络合物形成的优良条件,Duarte-Nass 等[31]研究也发现pH在9以上时,铜离子偏向与氨络合生成铜氨络合物,而不是与碳酸根结合生成蓝铜矿和孔雀石。综合以上分析可知,高活性脲酶会产生一个偏碱性的多氨环境,并且使得溶液pH 超过9 时生成铜氨络合物。由此发现可知,若能研发调控pH 的方法则可避免铜氨络合物的形成,从而提高处理效率。

图4 处理效率和pH与铵根离子浓度之间关系(未添加钙源)Fig.4 Treatment efficiency and pH versus NH4+concentration(without calcium source addition)
尿素水解产生铵根离子和碳酸根,一部分碳酸根与铜离子结合生成碳酸盐沉淀,剩余碳酸根大量水解,产生OH-造成pH 升高[式(8)~式(9)],因此阻止碳酸根水解即可对pH 进行调控。基于此猜想,本研究通过添加钙源,使钙离子与碳酸根结合进而阻止其水解,为了验证此分析,本研究开展添加钙源的数值模拟,相关的结果将在2.2.2 节进行分析讨论。
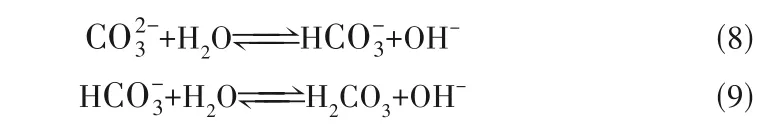
2.2.2 添加钙源 图5为氯化钙作为钙源时,不同尿素水解程度下的沉淀形态分析,其主要包含氯铜矿[Cu2(OH)3Cl]、蓝铜矿和孔雀石三种形态,并且铵根离子在200~500 mmol/L 范围时,各浓度的铜废水处理效率接近100%[图5(b)],此时沉淀主要以蓝铜矿和孔雀石的形态存在[图5(a)],这种形态的沉淀较为稳定,不易分解生成其他物质,是铜最佳的沉淀形态。另外,此时pH 基本在5~7 之间[图5(c)],远小于易形成铜氨络合物的范围。铜离子和铵根离子浓度为100 mmol/L 时,沉淀以氯铜矿的形态存在,这是因为这种条件下pH 过低[图5(c)],尿素水解产生的50 mmol/L 碳酸根离子不足以使所有的铜离子沉淀,只能沉淀66 mmol/L 的铜离子,并由式(4)测算处理效率约为66%[图5(b)]。从图5(c)可以看出此时的pH 接近4,既有的研究表明过酸的环境不利于孔雀石和蓝铜矿形成沉淀[31],故铜的沉淀形式只有氯铜矿一种,未沉淀的铜以铜离子的形式存在。此外,在铜离子浓度5 mmol/L、铵根离子600 和700 mmol/L,以及铜离子浓度10 mmol/L、铵根离子700 mmol/L 时,处理效率测算为0[图5(a)、(b)] ,即无碳酸盐沉淀形成,铜主要以铜氨络合物的形式存在溶液中,此时pH 处于8~9 之间[图5(c)]。添加钙源的数值模拟结果表明,其不仅可以改变碳酸盐沉淀形态,还可对pH进行调控,少部分处理效率的劣化主要是因为尿素水解程度不足(铵根离子浓度为100 mmol/L)而导致,但水解程度过高(铵根离子浓度为600 和700 mmol/L)提高了溶液pH亦会劣化处理效率。
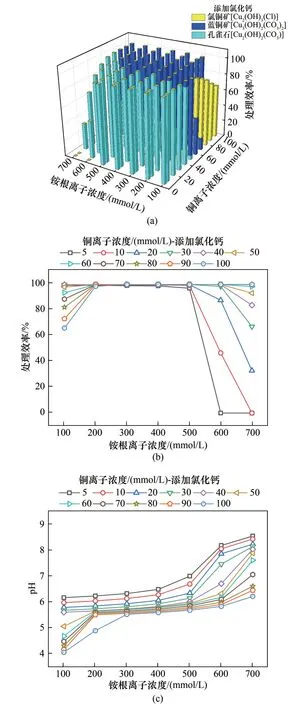
图5 处理效率和pH与铵根离子浓度之间关系(钙源为氯化钙)Fig.5 Treatment efficiency and pH versus NH4+concentration(with CaCl2 addition)
图6 为醋酸钙作为钙源时,不同尿素水解下的铜沉淀形态分析,主要包含蓝铜矿和孔雀石两种形态[图6(a)],并未出现未添加钙源时出现的黑铜矿沉淀[图4(a)],对比蓝铜矿和孔雀石,黑铜矿稳定性较差且易与其他化合物反应[31]。由图6(b),铵根离子在200~500 mmol/L范围,处理效率高达90%~100%,此时pH 介于5~8 之间[图6(c)]。铜离子和铵根离子浓度为100 mmol/L 时,溶液pH 较低,尿素水解产生的50 mmol/L 碳酸根不足,只能沉淀76 mmol/L 的铜离子,由式(4)测算处理效率约为76%[图6(b)]。此时pH 在5 以上,不利于铜氨络合物形成。当铜离子浓度为5 mmol/L、铵根离子600 和700 mmol/L,以及铜离子浓度10 mmol/L、铵根离子700 mmol/L 时,处理效率测算为0[图6(a)、(b)],处理效率劣化的原因与pH接近9时铜氨络合物的形成紧密相关[图6(c)]。
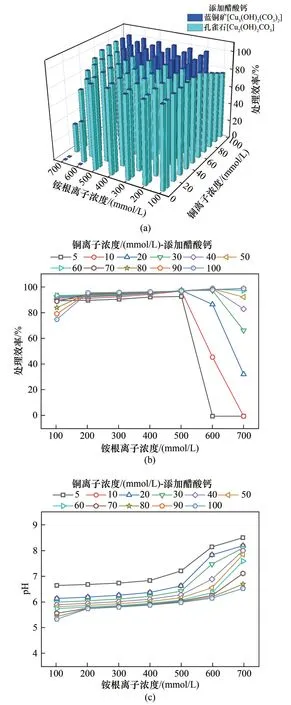
图6 处理效率和pH与铵根离子浓度之间关系(钙源为醋酸钙)Fig.6 Treatment efficiency and pH versus NH4+concentration(with Ca(CH3COO)2 addition)
2.3 钙源对处理效率的影响
由数值模拟结果得知添加钙源能有效调控pH,避免铜氨络合物的形成,且模拟结果与试管试验有较好的一致性。图7为考虑添加钙源时不同壳聚糖浓度下铵根离子和pH 随铜离子浓度的变化,铵根离子浓度随壳聚糖浓度增加而增加,且随铜离子浓度增加而减小[图7(a)、(b)]。另外,醋酸钙作为钙源时,对比氯化钙为钙源时铵根离子浓度和pH 较低,原因是醋酸根水解产生的醋酸是有机酸,会破坏壳聚糖大分子的链式结构,降低壳聚糖对脲酶的保护作用,劣化脲酶活性[32]。当壳聚糖浓度为2 g/L 时,醋酸根水解产生的氢氧根会提高pH,因此图7(c)中醋酸钙作为钙源时pH 高于氯化钙作为钙源时pH。当壳聚糖浓度为4 g/L时,由于两种钙源的铵根离子浓度差距较大,即尿素水解程度差距较大,从而弱化醋酸根水解的影响,导致图7(d)中当醋酸钙作为钙源时pH低于氯化钙作为钙源时pH。

图7 考虑添加钙源时壳聚糖联合酶诱导碳酸盐沉淀方法铵根离子浓度和pH随铜离子浓度变化Fig.7 NH+4 and pH versus Cu2+concentration using the chitosan-assisted EICP method(with calcium source addition)
图8为添加钙源时不同浓度壳聚糖下的处理效率随铜离子浓度变化规律,较未添加钙源时处理效率显著上升。当壳聚糖浓度为2 g/L时,氯化钙作为钙源可使处理效率稳定提高至80%以上,当壳聚糖浓度为4 g/L 时,铜离子浓度为5 和10 mmol/L 时,处理效率显著下降,原因为水解程度过高显著提升了溶液pH,导致铜氨络合物的形成。此外,对比两种钙源,醋酸钙作为钙源时的处理效率较低,普遍在80%以下。值得一提的是当壳聚糖浓度为4 g/L 时,尽管醋酸钙作为钙源时的pH 更低,但其处理效率也较低,主要与壳聚糖絮凝作用有关,将在2.4 节深入讨论。

图8 考虑添加钙源壳聚糖联合酶诱导碳酸盐沉淀方法处理效率随铜离子浓度变化Fig.8 Treatment efficiency versus Cu2+concentration using the chitosan-assisted EICP method(with calcium source addition)
2.4 壳聚糖联合酶诱导碳酸盐沉淀对处理效率的强化机理
试管试验和数值模拟已表明处理效率的劣化现象,原因可归结为:(1)水解程度不足无法沉淀所有铜离子;(2)较高的水解程度产生较多的氢氧根,导致溶液pH 升高从而形成铜氨络合物。本节将深入讨论壳聚糖联合酶诱导碳酸盐沉淀方法处理铜废水的强化机理,如图9 所示,其包含如下几个作用。
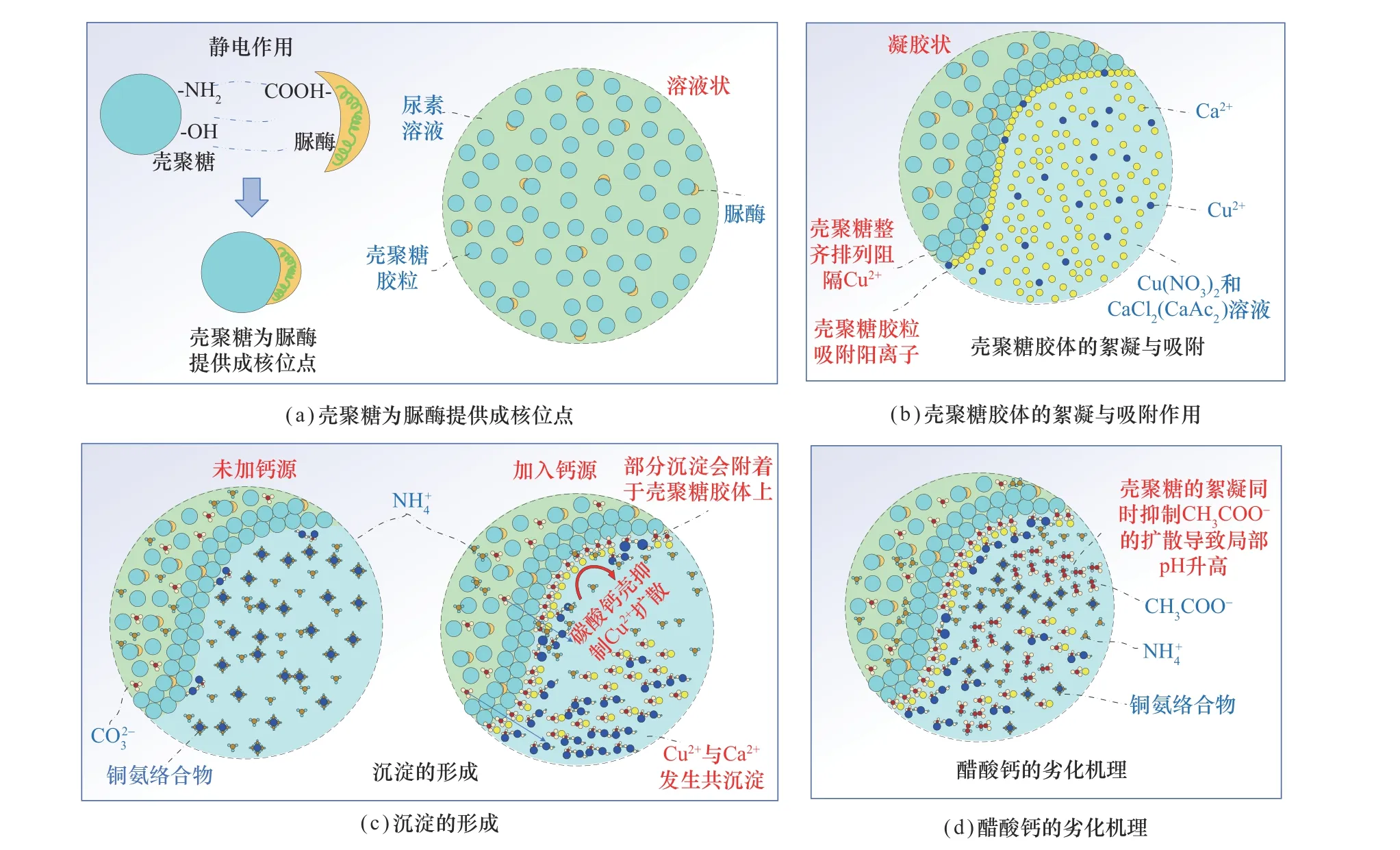
图9 壳聚糖联合酶诱导碳酸盐沉淀处理铜废水强化机理示意图Fig.9 Enhancement mechanism of the chitosan-assisted EICP method for copper wastewater treatment
(1)壳聚糖为脲酶提供成核位点:由于壳聚糖分子中含有大量的氨基(—NH2)和羟基(—OH),可以与蛋白质分子中的羧基(—COOH)等活性基团产生静电作用,所以壳聚糖与蛋白质之间有很好的亲和性,可有效地吸附水中蛋白质分子[33-34]。因此,这种静电作用使脲酶与壳聚糖胶体牢牢地结合在一起,避免其游离在溶液中因其他因素而失活,增强了脲酶的稳定性。
(2)壳聚糖胶体的絮凝与吸附作用:将壳聚糖和脲酶、尿素的混合溶液加入铜和钙源的混合溶液后,壳聚糖胶体会产生絮凝作用,将铜离子和脲酶隔绝开,此时修复液呈凝胶状,壳聚糖胶体会抑制铜离子的扩散并保护脲酶免受其抑制作用,为脲酶催化尿素水解提供足够的时间,并且壳聚糖浓度越高这种絮凝作用就越强,进而尿素水解程度越高。这种絮凝作用的产生,是因为壳聚糖是一种阳离子多糖,在酸性溶液中带正电荷,在接触到含有铜和钙源的混合溶液后,溶液中的反离子(即与带电粒子表面电荷相反的离子)会影响分散系的稳定性,粒子双电层的扩散层被压缩,粒子间排斥位能降低而导致的[35-37]。因此在本文2.1 节中添加壳聚糖后脲酶活性显著提高,为壳聚糖的絮凝作用将脲酶与铜离子隔离开提供了强而有力的证明。
(3)沉淀的形成:壳聚糖是一种线性聚阳离子聚合物,会吸附阳离子,即铜离子、钙离子和尿素水解产生的铵根离子。未添加钙源时,由于pH 范围和铵根离子的缘故,铜离子会倾向于产生铜氨络合物。添加钙源后,钙离子浓度为250 mmol/L,铜离子浓度最高为50 mmol/L,由于钙离子浓度远高于铜离子浓度,因此壳聚糖吸引钙离子的量会高于铜离子的量,并且由于碳酸钙(Ksp=10-8.54)和碱式碳酸铜(孔雀石和蓝铜矿)(Ksp=10-9.86)的平衡常数相近,所以钙离子会和碳酸根离子优先发生反应生产碳酸钙沉淀,并在壳聚糖表面形成一层“碳酸钙壳”,进一步地保护脲酶免受铜离子抑制作用,极大提高脲酶活性。因此,在本文2.3 节中添加钙源后的铵根离子浓度会显著提高。另一方面,碳酸钙的形成会阻止碳酸根水解,pH 得以控制在9 以内,有效避免铜氨络合物的生成。再者,受壳聚糖吸引的铜离子和尿素水解释放的碳酸根离子会在壳聚糖絮凝处与碳酸钙形成共沉淀,从而提高重金属沉淀的稳定性。
(4)醋酸钙作为钙源处理效率降低:醋酸钙作为钙源,壳聚糖浓度为2 g/L 时,修复过程中醋酸根的水解会提高pH,如图7(c),较高的pH 会促进铜氨络合物的产生,因此醋酸钙作为钙源时的处理效率均小于氯化钙作为钙源。对于壳聚糖浓度为4 g/L 的情况下,虽然醋酸钙作为钙源时pH 较低,但由于壳聚糖的絮凝作用更强,抑制了醋酸钙的影响。因此,无论壳聚糖浓度高低,醋酸钙作为钙源时进行铜废水处理的效果都不如氯化钙。
3 结 论
(1)铜离子对脲酶的抑制作用十分明显,未添加壳聚糖时,脲酶处于失活状态,而添加壳聚糖后,脲酶有较高活性,可使得铵根离子浓度最高达到330 mmol/L。但脲酶活性与处理效率不成正比关系,较高的脲酶活性会促使尿素水解产生较高的铵根离子,提高溶液pH,促使铜氨络合物产生,进而降低处理效率。而较低的脲酶活性又无法满足铜离子的完全沉淀,故较高和较低的脲酶活性都会劣化铜废水处理。
(2) 未添加钙源时,尿素水解使得pH 达到9 以上会大量生成铜氨络合物,添加钙源后会抑制pH的升高及铜氨络合物的产生,显著提高处理效率。铵根离子浓度在200~500 mmol/L 之间,pH 在5~8 之间利于产生孔雀石和蓝铜矿这类理想的铜沉淀。相比于氯化钙,壳聚糖的这种强絮凝作用使得醋酸钙不合适作为钙源进行铜废水的处理,因此氯化钙是强化铜废水处理的较好钙源。
(3)壳聚糖和脲酶之间的静电作用使得脲酶吸附于壳聚糖之上,加入铜溶液后,壳聚糖的絮凝作用使脲酶和铜离子隔绝开,脲酶有活性催化尿素水解。壳聚糖作为一种线性聚阳离子聚合物,会吸引阳离子,未添加钙源时,pH 的不断升高会为铜氨络合物的形成提供良好的环境从而劣化处理效率。添加钙源后,会在壳聚糖表面产生“碳酸钙壳”,进一步阻止铜离子的扩散,另外添加钙源能够有效降低pH阻止铜氨络合物生成,有效提高处理效率。

