彩色光刻胶用蒽醌染料的合成及稳定性研究
任玉鑫,徐润峰,王婉颖,陈鹏忠,2,彭孝军
(1大连理工大学精细化工国家重点实验室,辽宁大连 116024; 2大连理工大学宁波研究院,浙江宁波 315000)
引 言
目前薄膜晶体管-液晶显示器(TFT-LCD)因为具有制备工艺路线成熟、色彩丰富等优点[1-4],在平板显示技术领域占据主流地位。TFT-LCD 面板主要由背光模组、驱动模块(IC)、偏光片、配向膜、液晶层、氧化铟锡(ITO)导电膜和彩色滤光片等组分构成。LCD 面板的彩色发光特性需要借助背光模组和彩色滤光片实现,当施加电压于晶体管时,液晶转向,背光源发出的白光通过液晶后产生偏转,进一步经彩色滤光片后变成相应的红、绿、蓝(RGB)色光。通过TFT 阵列调节加在各个子像素的电压值,从而改变各色光的透射强度,不同强度的RGB 色光混合在一起形成不同颜色,最终实现彩色显示。由此可见,彩色滤光片是TFT-LCD 最为关键的组成部分之一[5]。
如图1 所示,彩色滤光片基本结构包括玻璃基板、彩色层、黑矩阵、透明导电膜和透明保护层等。制备过程如图2 所示,首先在玻璃基板上涂覆黑色光刻胶,经过曝光、显影、后烘等工艺后形成黑色矩阵,红绿蓝(R、G、B)彩色光刻胶经过上述工艺后,依次将三原色素填充在黑色矩阵内形成彩色膜层,然后在膜上依次涂覆透明保护层和透明导电膜制成彩色滤光片。
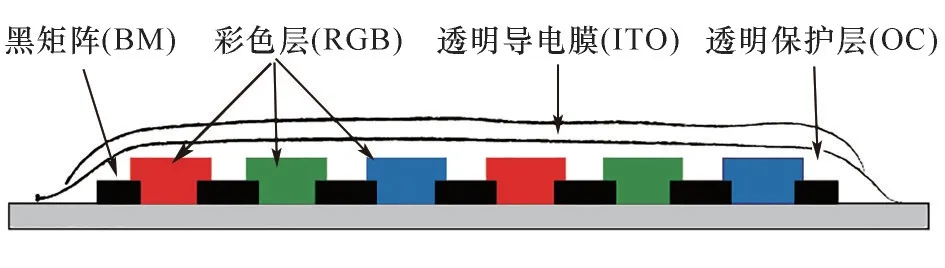
图1 彩色滤光片的基本构造Fig.1 The basic structure of color filter
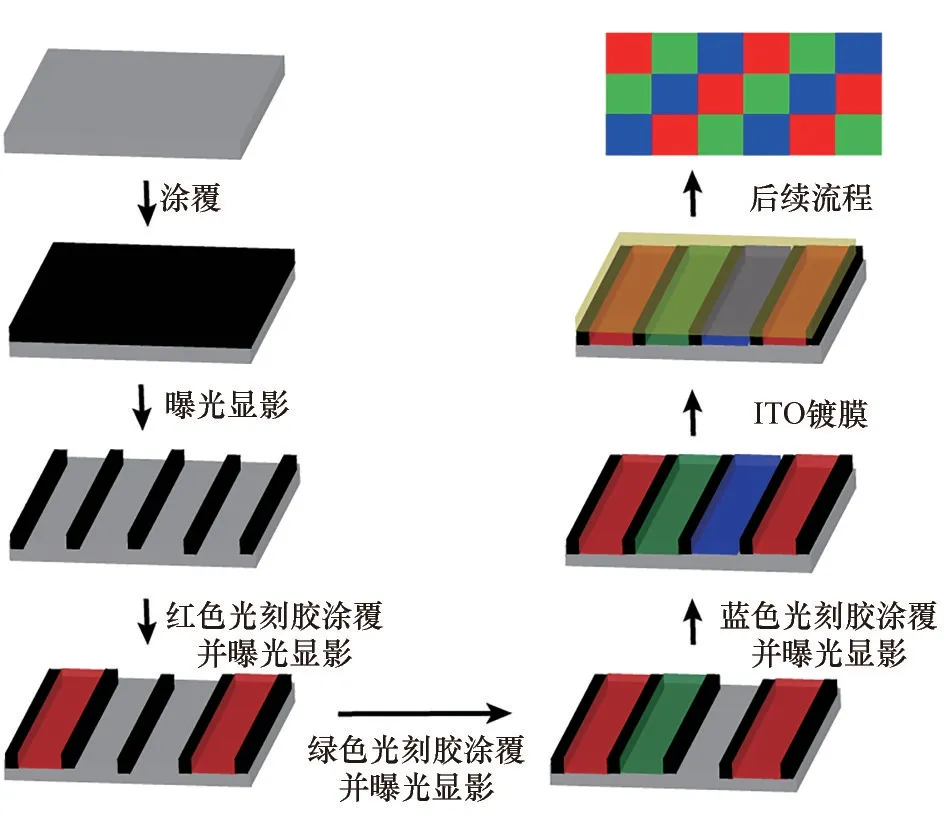
图2 彩色滤光片的制备过程Fig.2 The fabrication process of color filter
目前制备彩色滤光片的主流方法是颜料分散法[6-7],所用色浆中的着色剂为颜料[8]。颜料是具有特定结构的分子聚集体,溶解度低,具有良好的耐光、耐热、化学稳定性等特点[9]。未来LCD 面板向高亮度、高对比度、高色彩饱和度和高分辨率的方向发展。但是颜料颗粒的大尺寸易造成透光率低和光散射严重等问题,从而导致色纯度低,无法在亮度和对比度方面实现更高水平的色彩特征[10]。为解决上述问题,研究者提出两种可行性方案:一是颜料颗粒进一步细化,其需要探索更为复杂精细的研磨工艺,以及颜料分散过程中其他分散助剂对颜料粒径的影响[11];二是开发与之对应的RGB 染料分子代替颜料[12]。相对于颜料体系,分子态的染料在溶解度允许范围内无需分散剂,有利于增大用量提高色饱和度,同时分子态的染料避免了光散射和折射现象引起的透光率与对比度低下等问题,具有透光率高、色纯度好、色彩艳丽等优点[13]。但是染料分子的耐热稳定性和耐光稳定性比颜料差[14],阻碍其产业化应用。因此发展适用于彩色光刻胶的染料体系,并在分子结构水平上探索提高染料光热稳定性的普适性策略,具有重要的意义。
蒽醌是一类性能优异的有机染料,具有耐晒牢度高、色彩鲜艳等优点,广泛用于油墨[15-17]、生物医学[18]及光电材料[19-22]等领域。通过改变取代基的类型与修饰位点,蒽醌染料可产生蓝、紫、黄和红等颜色,是少有的可实现全色谱的染料品种。1,4-二取代的蒽醌染料种类繁多,颜色以蓝色为主,例如溶剂蓝78,其结构为1,4-二甲氨基蒽醌,广泛应用于塑料和高分子树脂的着色。如图3 所示,1,4-二氨基取代的蒽醌染料中氨基与羰基之间形成的激发态分子内质子转移,可耗散激发态能量,提升蒽醌染料的稳定性。因此,探究1,4-位取代基的种类对染料颜色和光热稳定性的影响,对探索染料在彩色光刻胶中的应用基础具有重要意义,而相关工作鲜有文献报道。基于此,本文选用蒽醌作为染料母体,在1、4 位分别引入烷基链、醚链、胺烷基链等柔性基团,合成9 种蓝色染料分子,系统研究染料分子的光物理性质,探讨不同种类的取代基对染料分子光热稳定性的影响。研究可为染料分子在彩色光刻胶中的应用奠定基础。
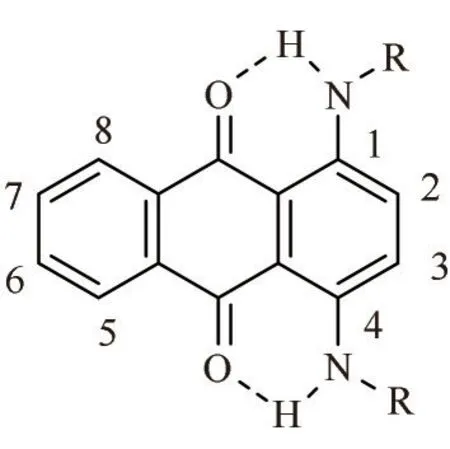
图3 蒽醌的基本结构Fig.3 Basic structure of anthraquinone dyes
1 实验材料和方法
1.1 材料
1,4,9,10-蒽四醇(>99.8%)购自阿拉丁化工有限公司;氨基五甘醇单甲醚(>95%)购自阿尔法化工有限公司;2-乙基己胺(>99.8%),己胺(>99.8%),环己甲胺(>99.8%),2-(2-(2-氨基乙氧基)乙氧基)乙醇(>99.8%),氨基三甘醇单甲醚(>99.8%),2-(2-氨基乙氧基)乙醇(>99.8%),乙二胺(>99.8%),丁二胺(>99.8%),乙二醇甲醚(>99.8%),乙腈(>99.8%)购自安耐吉化工有限公司。上述试剂购买后直接使用,未经纯化。
1.2 测试仪器
核磁共振氢谱和碳谱采用瑞士布鲁克公司Bruker Avance Ⅱ400/Ⅲ500 型核磁共振波谱仪测定;质谱采用美国Thermo Scientific 科技有限公司LTQ Orbitrap XL 型线性离子阱-高分辨液质联仪测定;紫外-可见吸收光谱采用美国Agilen公司Cary60型紫外-可见分光光度计测定;透射光谱与色差采用中国远方公司HACA-2000 型高精度颜色分析仪测定;热重采用美国TA公司Q500热重分析仪测定;平面形貌采用日本奥林巴斯公司CKX53 型光学显微镜测定。
1.3 化合物的合成
1.3.1 化合物A1~A7 的制备 反应如图4 所示,以A1为例,氮气保护下,在25 ml圆底二口烧瓶中加入1,4,9,10-蒽四醇(1 g,4.13 mmol)与10 ml 乙二醇甲醚,加热到80℃后加入2-乙基己胺(2.15 g,16.64 mmol),反应24 h 后,将该反应温度降至50℃,反应体系暴露于空气中氧化2 h。冷却到室温后,将反应液倒入100 ml 的纯水中,析出固体后抽滤得到粗产物,最后将粗产物经柱层析(展开剂为乙酸乙酯)分离得到蓝色固体。
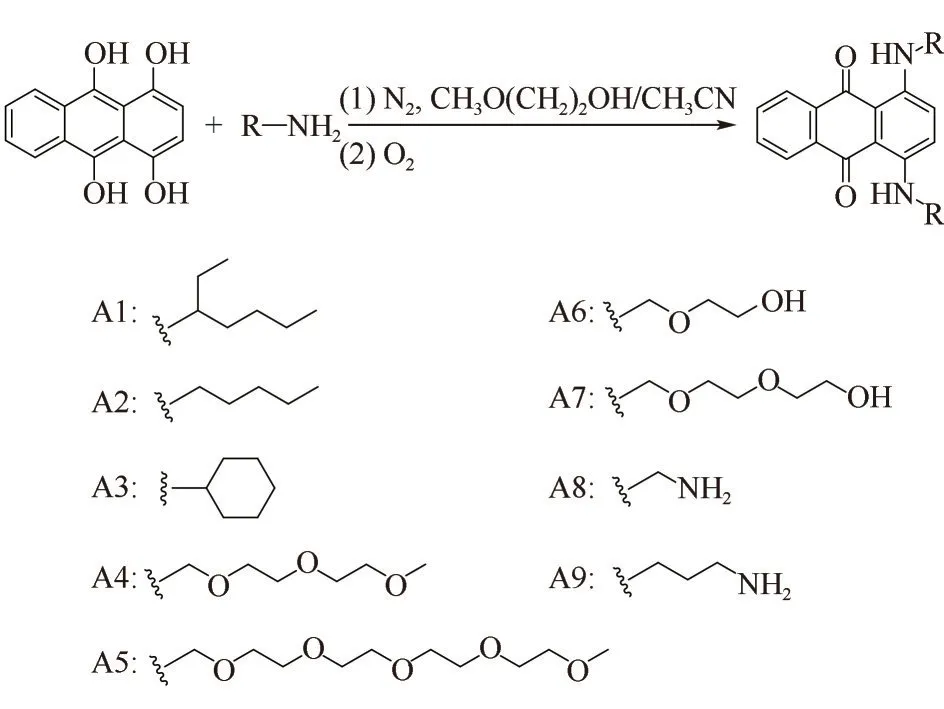
图4 蒽醌类染料A1~A9的合成路线Fig.4 Synthetic routes of anthraquinone dyes A1—A9
1,4-双(2-乙基己胺基)蒽醌(A1):蓝色固体,产率70%。1H NMR (400 MHz, Chloroform-d)δ: 10.97(s, 2H), 8.38 (dd,J= 5.9, 3.3 Hz, 2H), 7.71 (dd,J=5.9, 3.3 Hz, 2H), 7.31 (s, 2H), 3.36(m, 4H), 1.75(m,2H), 1.56(m, 8H), 1.36(m, 8H), 0.95(m, 12H)。13C NMR (126 MHz, Chloroform-d): 181.1, 145.5, 133.5,130.8, 125.0, 122.6, 108.6, 44.9, 38.4, 30.2, 27.9,23.4, 21.9, 13.1, 9.9。 HRMS(ESI): C30H43N2O2([M+H]+),计算值463.3320,测试值463.3312。
1,4-双(己胺基)蒽醌(A2):蓝紫色固体,产率74.8%。1H NMR (400 MHz, Chloroform-d)δ: 8.36(dd,J= 5.9, 3.3 Hz, 2H), 7.71 (dd,J= 5.9, 3.3 Hz,2H), 7.27 (s, 2H), 3.41 (t,J= 7.2 Hz, 4H), 1.79 (m,4H),1.51(m,4H),1.38(dd,J=4.6,3.7 Hz,8H),0.96 ~0.91 (m, 6H)。13C NMR (126 MHz, Chloroform-d):181.1, 145.1, 133.5, 130.8, 124.9, 122.6, 108.6, 41.9,30.5, 28.6, 25.8, 21.5, 13.1。 HRMS(ESI): C26H35N2O2([M+H]+),计算值407.2694,测试值407.2687。
1,4-双(环己甲胺基)蒽醌(A3):蓝色固体,产率69%。1H NMR (400 MHz, Chloroform-d)δ: 11.00(s,2H), 8.38(dd,J= 5.9, 3.3 Hz, 2H), 7.72 (dd,J= 5.9,3.3 Hz, 2H), 7.31 (s, 2H), 3.28 (d,J= 6.7 Hz, 4H),1.96 (m, 4H), 1.77 (m, 8H), 1.31 (m, 7H), 1.11 (m,3H)。13C NMR (126 MHz, Chloroform-d)δ:180.9,145.4, 133.5, 130.7, 124.9, 122.6, 108.4, 48.5, 37.1,30.2, 25.4, 24.9。 HRMS(ESI): C28H35N2O2([M+H]+),计算值431.2694,测试值431.2688。
1,4-双(三甘醇单甲醚胺基)蒽醌(A4):蓝色油状液体,产率79%。1H NMR(400 MHz,Chloroform-d)δ:8.37 ~8.32(m,2H),7.74 ~7.69(m,2H),7.34(s,2H),3.84(t,J=5.7 Hz,4H),3.77 ~3.72(m,8H),3.72 ~3.68(m,4H),3.64 (t,J= 5.7 Hz, 4H), 3.60 ~3.55 (m, 4H), 3.38 (s,6H)。13C NMR(126 MHz,Chloroform-d):181.5,145.0,133.4,131.0,125.0,122.4,109.1,70.9,69.8,69.6,69.5,69.0,58.0,41.7。HRMS(ESI):C28H39N2O8([M+H]),计算值531.2662,测试值531.2691。
1,4-双(五甘醇单甲醚胺基)蒽醌(A5):蓝色油状液体,产率10%。NMR(400 MHz,Chloroform-d)δ:8.32(m,2H),7.68(m,2H),7.27(s,2H),3.79(t,J=5.7 Hz,4H),3.71 ~3.5(m,36H),3.36(s,6H)。13C NMR(126 MHz,Chloroform-d):182.6, 146.0, 134.4, 132.0,126.0,123.4,110.2, 71.9, 70.8, 70.6, 70.6, 70.5, 70.5, 70.4, 70.1, 70.1,58.9, 42.7。 HRMS(ESI): C36H55N2O12([M+H]), 计算值707.3710,测试值707.3739。
1,4-双(2-(2-羟基乙氧基)乙胺基)蒽醌(A6):蓝色固体,产率 75.6%。1H NMR (400 MHz,Chloroform-d)δ: 8.24 (dd,J= 5.9, 3.3 Hz, 2H), 7.61(dd,J= 5.8, 3.3 Hz, 2H), 7.16 (s, 2H), 3.80 ~3.74 (m,8H), 3.66 ~3.62 (m, 4H), 3.52 (t,J= 5.3 Hz, 4H)。13C NMR (126 MHz, Chloroform-d): 181.3, 145.1,133.3, 131.1, 125.1, 122.5, 108.9, 71.7, 68.3, 60.8,41.4。 HRMS(ESI): C22H27N2O6([M+H]+), 计 算 值415.1824,测试值415.1861。
1,4-双(2-(2-(2-羟基乙氧基)乙氧基)乙胺基)蒽醌(A7):蓝色固体,产率77.4%。1H NMR (400 MHz,Chloroform-d)δ: 8.37 (m, 2H), 7.72 (m, 2H), 7.30 (s,2H),3.85(t,J=5.4 Hz,4H),3.80(dd,J=5.2,3.7 Hz,4H), 3.76 (s, 8H), 3.68 (dd,J= 5.2, 3.7 Hz, 4H), 3.63(t,J= 5.4 Hz, 4H)。13C NMR (126 MHz, Chloroformd): 181.7, 145.0, 133.4, 131.1, 125.1, 122.5, 109.1,71.7, 69.7, 69.3, 68.7, 60.8, 41.7。 HRMS(ESI):C26H35N2O8([M+H]+), 计 算 值503.2349,测 试 值503.2390。
1.3.2 化合物A8~A9 的制备 以A8 为例,氮气保护下,在25 ml圆底二口烧瓶中加入1,4,9,10-蒽四醇(1 g,4.13 mmol)与10 ml 的乙腈,加热到50℃后加入乙二胺(2.50 g,4.16 mmol),待反应原料完全消耗后,将反应体系置于空气中氧化1 h。冷却到室温,将反应液倒入100 ml 的乙腈中,抽滤得到粗产物,最后将粗产物用乙醚洗涤得到蓝色固体。
1,4-双(2-氨基乙胺基)蒽醌(A8):蓝色固体,产率50%。1H NMR (400 MHz, DMSO-d6)δ: 8.25 (dd,J= 5.9, 3.3 Hz, 2H), 7.79 (dd,J= 5.9, 3.4 Hz, 2H),7.51 (s, 2H), 3.45 (q,J= 6.1 Hz, 4H), 2.85 (t,J=6.3 Hz, 4H)。13C NMR (126 MHz, DMSO-d6): 180.5,146.0, 133.8, 132.1, 125.6, 124.4, 108.4, 42.2, 35.3。HRMS(ESI): C18H21N4O2([M+H]+), 计算值325.1620,测试值325.1664。
1,4-双(4-氨基丁胺基)蒽醌(A9):蓝色固体,产率54.5%。1H NMR (400 MHz, DMSO-d6)δ: 10.90(t,J=5.5 Hz,2H),8.36(dd,J=5.9,3.3 Hz,2H),7.71(dd,J= 5.9, 3.4 Hz, 2H), 7.27 (s, 2H), 3.50 (q,J= 6.1 Hz,4H), 3.10 (t,J= 6.3 Hz, 4H), 1.43 (m, 8H)。13C NMR(126 MHz, DMSO-d6): 181.1, 145.8, 133.4, 132.0,125.5, 124.3, 108.8, 43.3, 40.7, 26.7, 25.3。 HRMS(ESI): C22H29N4O2([M+H]+), 计算值381.2246,测试值381.2288。
1.4 染料的紫外-可见吸收光谱测定
将上述合成染料配制成30 μmol/L溶液,溶剂为N,N-二甲基甲酰胺(DMF),丙二醇甲醚(PGME)和丙二醇甲醚醋酸酯(PGMEA),在紫外可见分光光度计中测试吸收光谱。用式(1)计算染料的摩尔消光系数:

式中,A是吸光强度;ε是摩尔消光系数,L/(mol·cm);c是浓度,mol/L;l是吸收层的厚度,cm。
1.5 染料的溶解度测试
测试合成染料在PGMEA 与DMF 中的溶解度,分别称取一定量染料与有机溶剂,室温搅拌10 min后静置24 h,使用滤膜过滤3 次,将滤液烘干,用式(2)计算染料的溶解度S:

式中,MS是烘干后染料质量,g;ML是溶液质量,g。
1.6 染料的光稳定性测试
测试合成染料在屏幕背光源连续照射下的耐受性。以PGMEA 为溶剂,将这9种染料分子配制成浓度为33 μmol/L 的溶液,选用波长为365 nm、功率为20 W 的LED 灯,调节溶液与LED 灯的距离,使溶液所接受的光密度为2 mW/cm2,连续光照8 h,每隔1 h 测试溶液的紫外可见透射光谱。用式(3)计算染料光照前后的ΔE值:
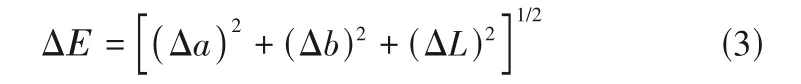
式中,L是明暗指数(亮度轴);a是色品指数(红绿轴);b是色品指数(黄蓝轴)[23-24]。
1.7 染料的热稳定性测试
在制作彩色滤光片过程中要经历200℃或高于200℃的后烘过程[25],工业要求染料分子要在此温度下有良好的热稳定性能。
本文采用热重法评价合成染料的热稳定性,合成染料在氮气保护下,从室温以10℃/min 的升温速度加热到500℃,以确定其热分解温度Td。同样条件下加热至230℃停留30 min,以模拟制造彩色滤光片后烘的加热条件,并计算出此温度下失重率。
1.8 染料薄膜的制备
将0.096 g 合成染料与0.192 g 聚乙烯醇缩丁醛酯树脂(PVB)充分溶于5.4 g PGMEA 中,通过式(4)计算出固体含量(TSC)为5%。玻璃基板选用2.5 cm×2.5 cm×1 mm 石英玻璃片,设置中国科学院微电子研究所KW-4T 型匀胶机转速为1000 r/min,旋涂时间为20 s。然后在100℃下前烘100 s 以蒸出多余溶剂,最后在200℃下进行30 min 后烘坚膜。
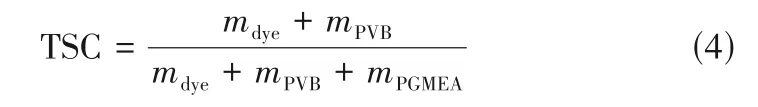
式中,mdye是染料的质量,g;mPVB是PVB 树脂的质量,g;mPGMEA是溶剂PGMEA的质量,g。
1.9 染料薄膜的热稳定性测定
将染料薄膜放入烘箱,调整温度为200℃烘烤30 min,用高精度颜色分析仪测试烘烤前后染料薄膜的透射光谱并计算烘烤前后薄膜的色差。
1.10 染料薄膜的光稳定性测定
根据GB/T 31370.2—2015 的要求,选用波长为365 nm 的LED 灯,调节染料薄膜与LED 灯的距离,使染料薄膜所接受的光密度为20 mW/cm2,照射时间为5 min,用高精度颜色分析仪测试光照前后染料薄膜的透射光谱并计算光照前后薄膜的色差。
1.11 染料成胶均匀性测定
根据1.8 节的方法制备染料-树脂溶液,室温放置24 h 后旋涂成片,然后在100℃下前烘100 s以蒸出多余溶剂,最后在200℃下进行30 min 后烘坚膜。利用光学显微镜(40 倍)测试染料薄膜的平面形貌。
2 实验结果与讨论
2.1 染料的紫外-可见吸收光谱
DMF、PGME 和PGMEA 常用于作为彩色光刻胶的溶剂体系,三种溶剂的Hansen 参数(色散、极性、氢键)为DMF(16.4、11.4、9.2),PGME(15.6、7.2、13.6)和PGMEA(16.1、6.1、6.6)[26]。分别测试了9 种染料分子在三种溶剂中的吸收光谱,结果如图5 和表1 所示。以DMF 溶液为例,从图5(a)、(b)可以看出,合成染料的DMF 溶液呈现蓝色,吸收光谱呈现双峰结构,分别位于590~600 nm 和630~650 nm 范围内,A1~A7的摩尔消光系数为11400~16900 L/(mol·cm),与商业化的染料蓝78 相当,说明合成的染料分子A1~A7 具有较强的吸光能力,而A8 与A9 的摩尔消光系数分别为8300 和7200 L/(mol·cm),吸光能力很弱,不适合应用在彩色滤光片中。如图5(c)、(d)所示,染料分子在PGME 和PGMEA 中的最大吸收峰和摩尔消光系数与在DMF 中无明显差异,表明染料分子的基态性质不受溶剂极性和溶剂-染料分子之间的氢键作用影响。
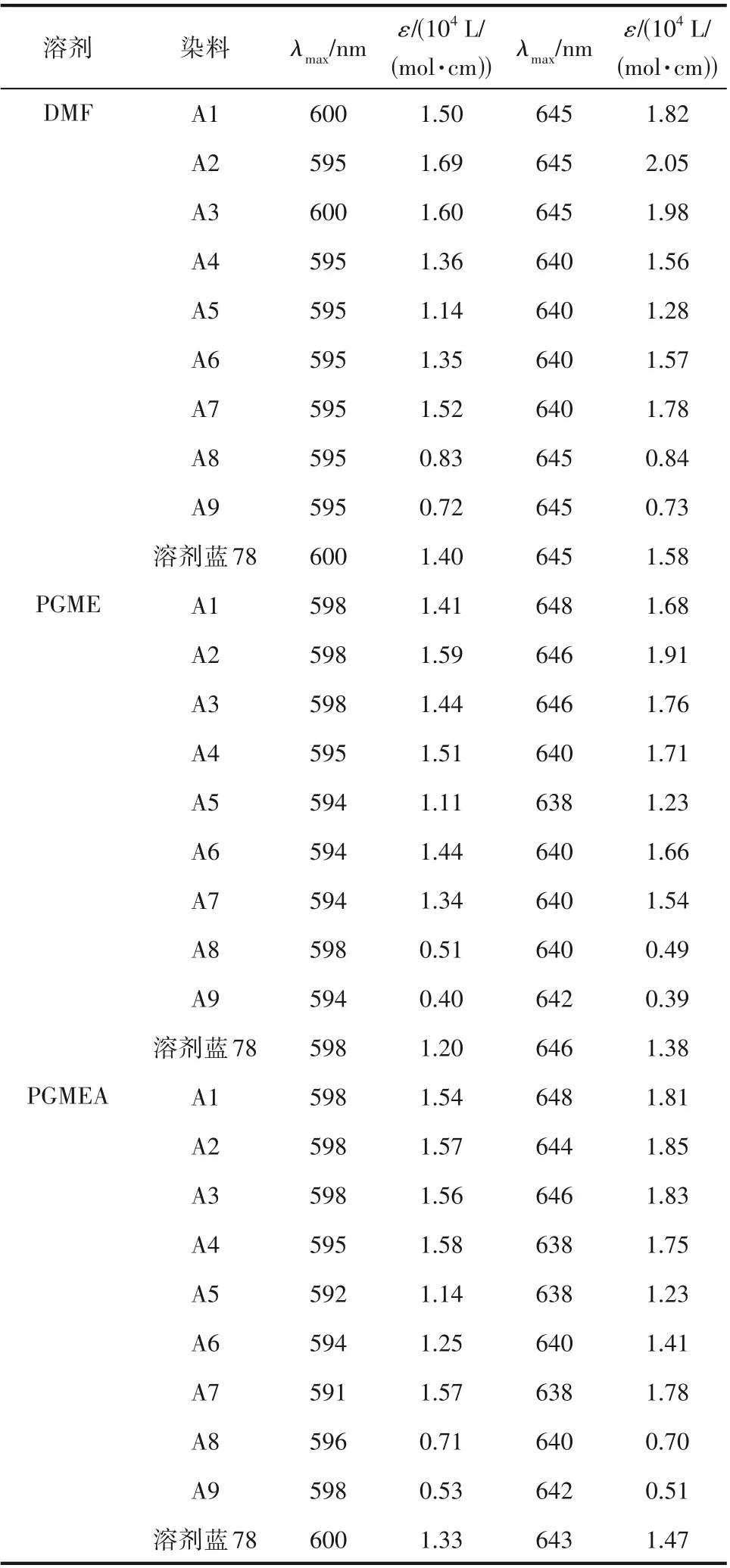
表1 染料在不同溶剂中的光谱数据Table 1 Spectroscopic data of dyes in organic solvents
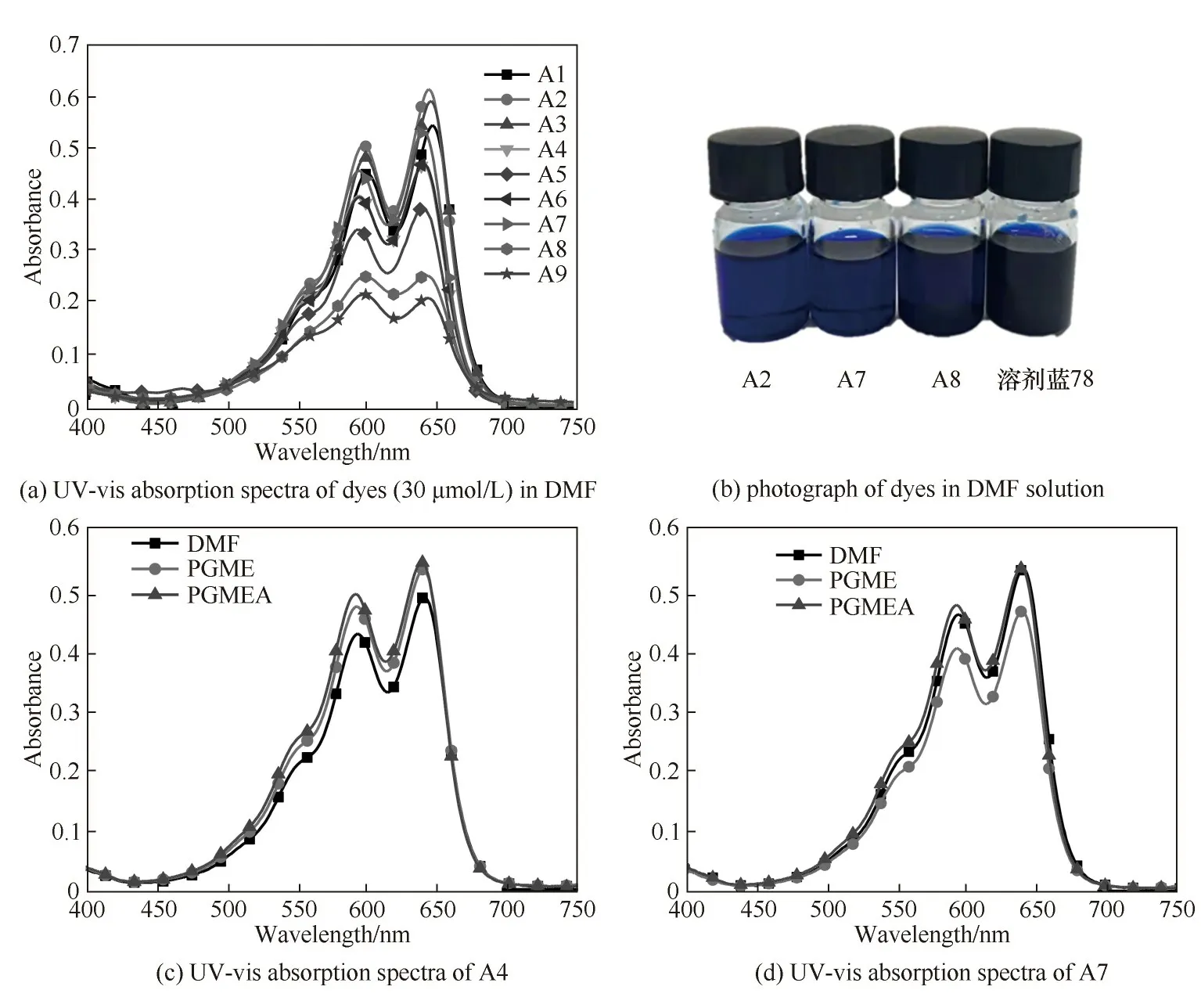
图5 染料分子在不同溶剂中(30 μmol/L)的紫外-可见吸收光谱及溶液照片Fig.5 UV-vis absorption spectra of dyes(30 μmol/L)in different solvents and photograph of dyes
2.2 染料的溶解度
影响物质溶解度的因素主要包括物质结构(离子化合物的晶格能、离子半径、溶质溶剂极性及氢键)和体系条件;通过薄层色谱测得A1、A2、A3 的 比 移 值(Rf)分 别 为0.38、0.26、0.24,流 动相:V(二氯甲烷)∶V(石油醚)=2∶3;A4、A5、A6、A7 的Rf为0.65、0.37、0.50、0.40,流动相:V(乙酸乙酯)∶V(甲醇)=50∶7;DMF 的极性远大于PGMEA,由薄层色谱测试可得出烷基蒽醌的极性比醚链蒽醌小。如表2 所示,在极性相对较小的溶剂PGMEA中,烷基蒽醌A1、A2 的溶解度比醚链蒽醌A4、A5、A6、A7 大;在大极性溶剂DMF 中,醚链蒽醌A4、A5、A6、A7 的溶解度更大;而A8 与A9 的极性与这两种溶剂的极性相差很大,在PGMEA 与DMF 中溶解度均较低。
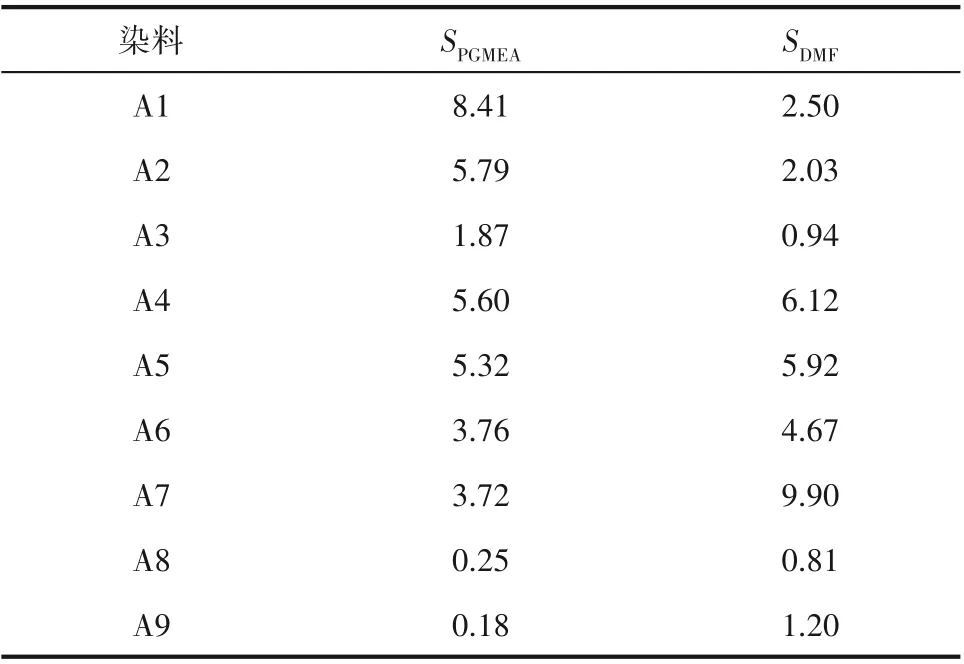
表2 染料在有机溶剂中的溶解度Table 2 Solubility of dyes in organic solvents
比较烷基蒽醌与醚链蒽醌的溶解度,前者在较小极性的溶剂中溶解度较好,后者在较大极性溶剂中溶解度好。
2.3 染料的光稳定性
按照1.6 节的方法,对合成染料进行光稳定性测试。如图6 所示,经8 h 光照后,A4 和A7 透射率分别下降了2.53%、2.7%,与商业化染料溶剂蓝78基本一致。而A8 和A9 透射光谱分别下降了17.66%、15.36%。合成染料的色系坐标(x,y)在光照前后变化如图7 所示。A4 和A7 的色系坐标从(0.2426,0.2928)、(0.2426,0.2852) 变 为(0.2466,0.2948)、(0.2455,0.2860),色系坐标无明显变化。A8和A9 的色系坐标分别从(0.2748,0.3167)、(0.2686,0.3141)变为(0.2936,0.3225)、(0.2845,0.3176),颜色明显变化。从表3 中可以看出,A2、A3、A4、A5、A7的色差变化ΔE分别为1.96、1.56、1.73、1.48、1.36,颜色无明显变化。A1 和A6 的ΔE分别为2.99 和2.16,表现为轻微的颜色变化。A8 和A9 的ΔE分别达到了8.50和7.41,光照前后褪色明显,不适合应用于彩色滤光片。上述结果说明了带有较长醚链和椅式-船式构象的六元环结构的蒽醌染料分子具有较好的光稳定性。
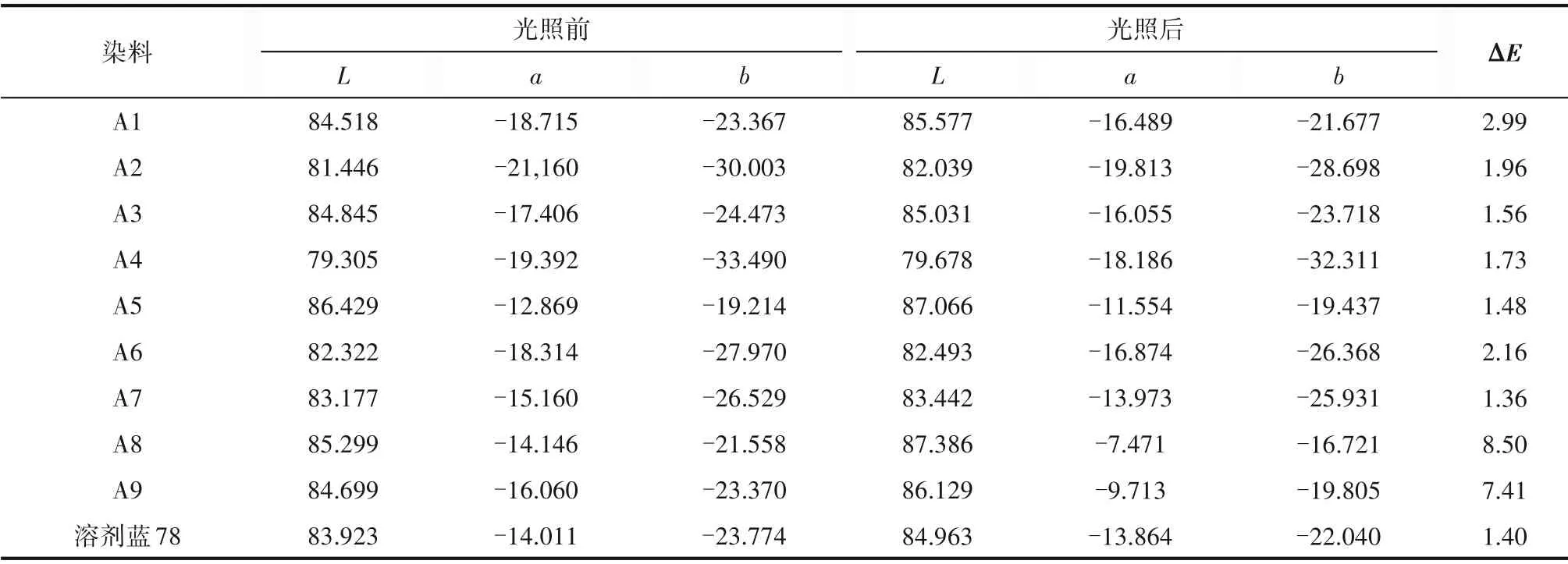
表3 光照前后染料L、a、b数值以及色差变化(ΔE)Table 3 L,a,b data and color difference value(ΔE)of dyes before and after accelerated irradiation
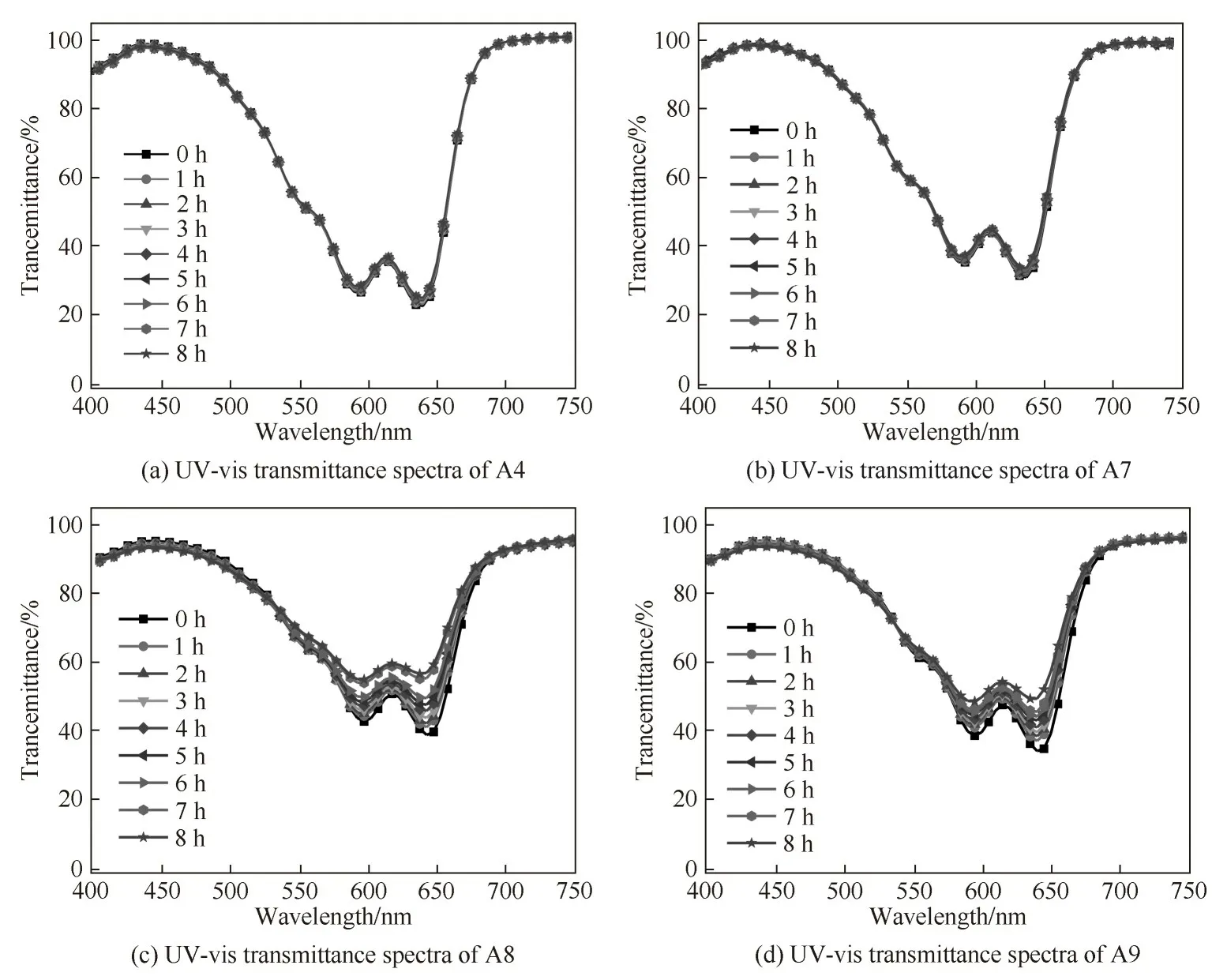
图6 A4、A7~A9染料分子的PGMEA溶液(33 μmol/L)在365 nm波长光下连续光照8 h的透射光谱Fig.6 UV-vis transmittance spectra of A4,A7—A9(33 μmol/L)dyes in PGMEA upon illumination at 365 nm light for 8 h
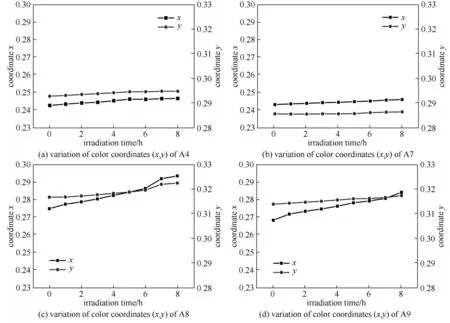
图7 A4、A7~A9在CIE Yxy中的色系坐标变化Fig.7 Variation of color coordinates(x,y)of A4,A7—A9 in CIE Yxy color space
染料分子的光稳定性与其激发态释能过程密切相关[27-28]。1,4-二氨基取代的蒽醌染料通过结构修饰提高光稳定性,其受光激发后,质子给体氨基与受体羰基之间距离和空间取向性合适,可通过分子内氢键形成六元环并且完成质子转移。该过程是可逆循环的过程,并伴随着较大的构型转变,因此可有效耗散激发态能量,提升染料分子的稳定性。与此同时,氨基取代基上的柔性链对消耗激发态能量,同样至关重要。对于含有醚链结构的A4、A5 和A7 染料分子,醚键内旋转位垒较小,分子链的动态柔性较好,因此当染料分子吸收光子被激发后,可以通过柔性链的振动-转动将激发态能量转化为热能而消耗,提高了染料分子的抗光氧化能力[29]。A3 分子的氨基取代基含有六元环环己烷结构,存在椅式-船式互变构象以及a 键和e 键的快速转换,同样可以耗散激发态能量。A8和A9 染料分子烷基链末端含有氨基,伯胺易被氧化而进一步诱导染料分子分解[30],所以A8 和A9 的光稳定性差。
2.4 染料的热稳定性
用热重分析仪(TGA)测试合成染料的热稳定性,测试结果如图8和表4所示。市售蓝色染料溶剂蓝78 的分解温度Td值是250℃,而A4 和A7 的Td值达到了300℃,均满足制作彩色滤光片所要求的温度(>230℃)。A3、A4与A7在230℃下烘烤30 min 后的失重率分别为1.18%、2.13%和1.92%,符合工业要求的失重率(<5%),而其他合成染料的失重率远大于A3、A4和A7。值得注意的是,含有2-乙基己基和正己基的A1、A2 染料分子,含有四缩乙二醇单甲醚的A5 染料分子以及甲基取代的溶剂蓝78在测试条件下失重严重,失重率分别达到了14.56%、55.24%、15.00%和43.95%,甚至高于含有氨基烷基的染料分子。染料分解温度的变化主要与分子间的相互作用密切相关,通常情况下分子间作用力强的染料热稳定性较好[2]。这一结果表明,一定长度范围的醚链取代基和环己基对提升染料分子热稳定性具有重要的作用,而四缩乙二醇取代基易破坏蒽醌分子π-π 堆积作用,使其分子间作用力减小,热稳定性下降。此外,醚链取代基的可修饰性优于环己基,因此通过进一步分子结构修饰,调节含有醚链基团的染料分子在光刻胶中的分散性和与树脂主体的匹配性,表现出潜在的应用前景。

表4 染料在230℃加热30 min后的失重率及分解温度Table 4 The weight loss of dyes at 230℃for 30 min and decomposition temperature
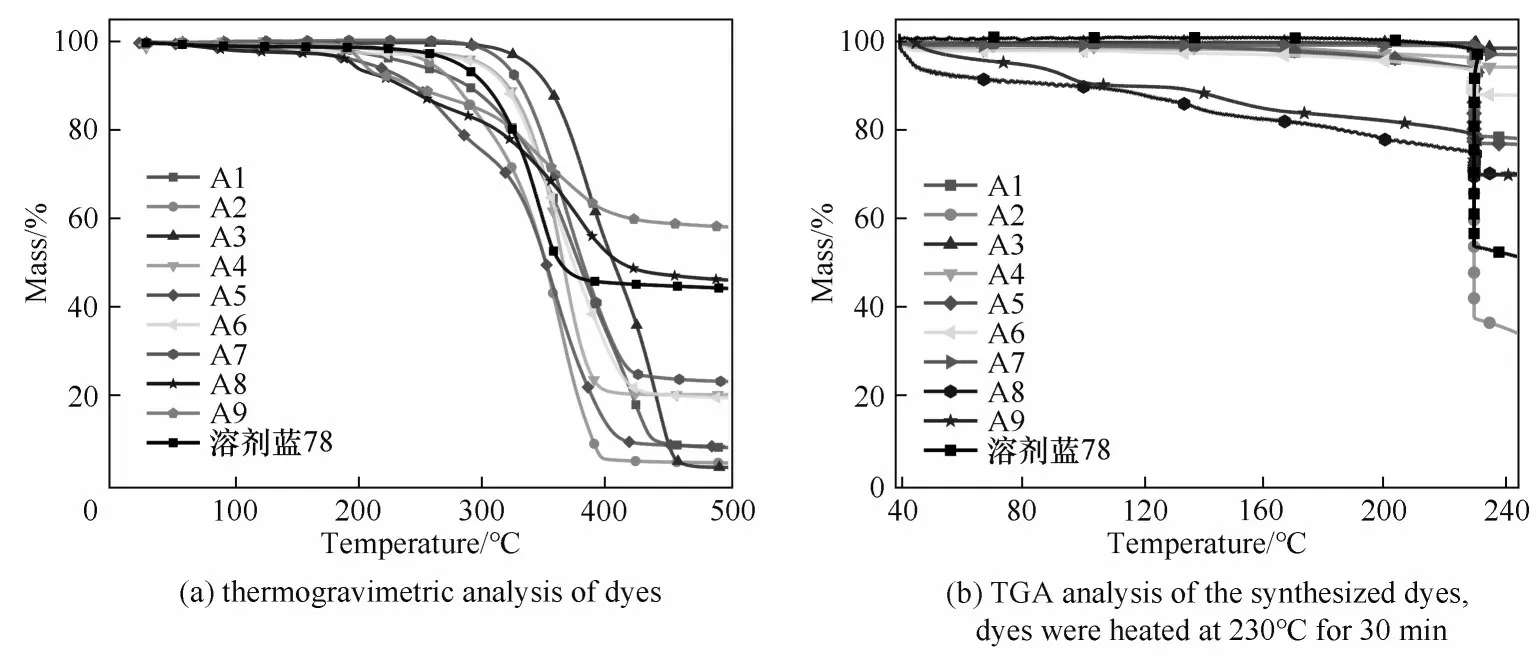
图8 染料的热重分析Fig.8 Thermogravimetric analysis of dyes
2.5 染料薄膜的光热稳定性及成胶均匀性
蓝色染料在玻璃基板上烘烤后的蓝光透过率直接关系到背光源的背光效率,因此处于400~480 nm 波段内蓝光透过率应接近100%。然而无论是染料还是颜料,当光通过玻璃基板时,部分蓝光会被吸收和反射,因此在工业生产上透射率应该超过90%[31]。在本研究中,选择了光热稳定性相对较高的染料A4 和A7 制成染料薄膜,探究这两种染料薄膜的光热稳定性。如图9(a)、(b)所示,两种染料薄膜在400~480 nm 之间的透射率均大于90%,并且在200℃烘烤30 min 后,其在此波段范围的透射率变化很小。如表5 所示,加热前后两种染料薄膜的色差分别为2.66 和0.24,色差均小于3,颜色无明显变化。同样,如图9(c)、(d)所示,两种染料薄膜光照前后的透射光谱无明显变化,且如表6所示,光照前后色差仅为0.16 和0.17,说明两种染料具有优异的光稳定性。

表5 后烘前后染料薄膜的色差Table 5 The color difference of the dye film before and after post-bake
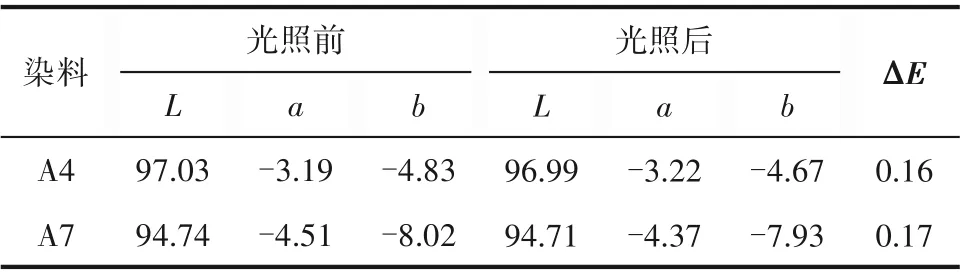
表6 光照前后染料薄膜的色差Table 6 The color difference of the dye film before and after irradiation
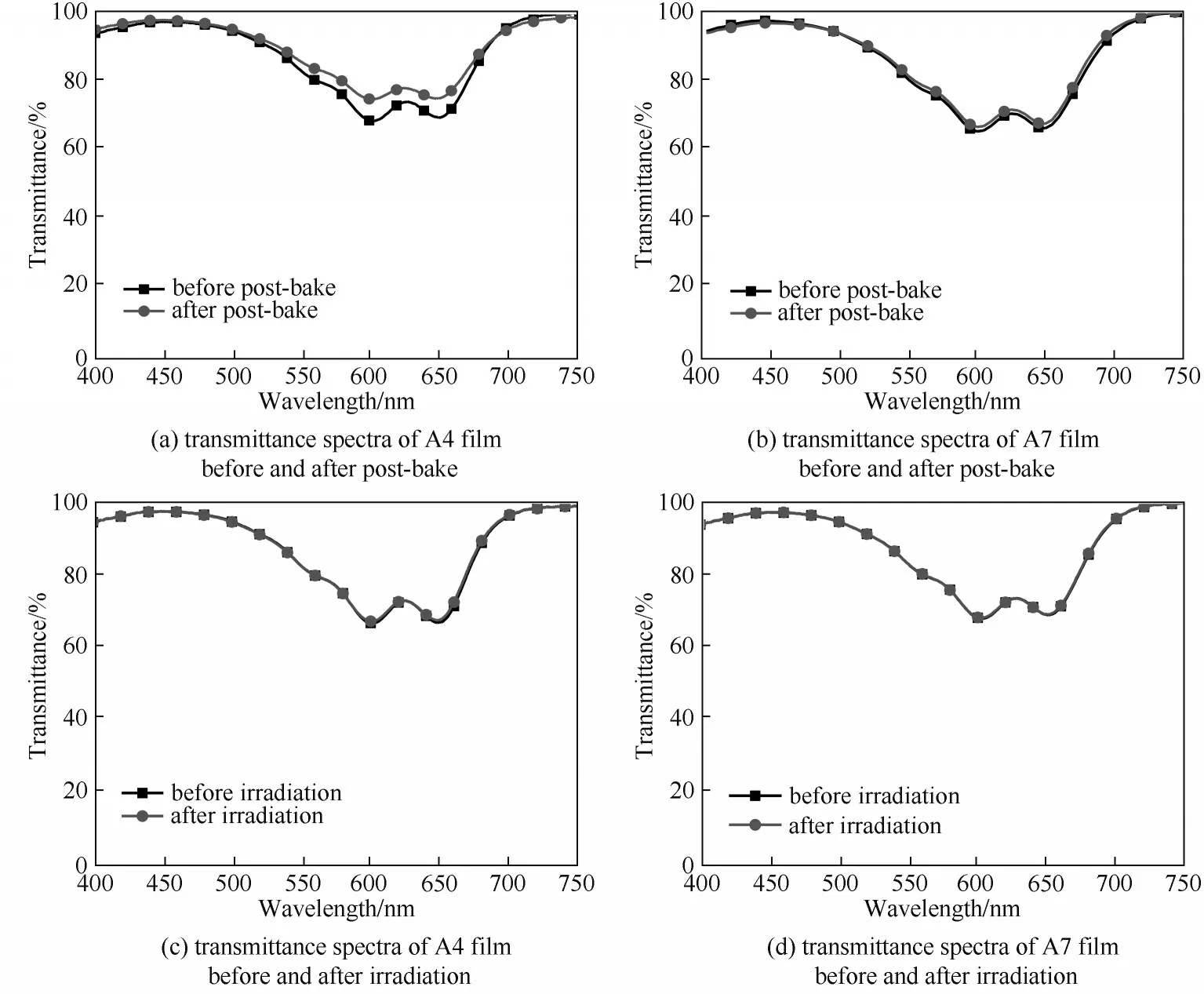
图9 后烘前后染料薄膜的透射光谱及光照前后染料薄膜的透射光谱Fig.9 Transmittance spectra of dye film before and after post-bake and transmittance spectra of dye film before and after irradiation
根据1.11 节的方法制成A4、A7 染料-树脂溶液,经过24 h 放置后观测染料-树脂溶液均无明显聚沉现象。图10(a)、(b)分别为A4、A7染料薄膜在光学显微镜下的平面形貌,可以看出这两种染料薄膜均无明显颗粒感,从而验证了A4、A7 染料成胶过程中均具有良好的抗聚集性及均匀性。

图10 A4、A7染料薄膜在光学显微镜下的平面形貌Fig.10 Planar morphology of A4 and A7 dye films under optical microscope
3 结 论
本文报道了9种含有不同取代基的蓝色蒽醌染料分子,探究了染料分子结构与光热稳定性之间的相互关系。在不同溶剂中,所有染料分子在波长590~600 nm和630~650 nm范围内呈现双吸收峰性质,具有较高的摩尔消光系数。光稳定性测试实验结果表明,含有醚链取代基的A4、A5和A7染料分子在光照前后,色差较小,颜色无显著变化。这是由于碳-氧键相比碳-碳键的内旋转位垒较小,分子链的动态柔性较好,当染料分子吸收光子被激发后,更易通过内旋转将激发能转化为动能而消耗,从而提高了染料分子的光稳定性。与此同时,A4和A7的分解温度均是300℃,在230℃下烘烤30 min后,失重率分别为2.13%和1.92%,满足产业要求;A5分解温度和失重率分别为250℃、15.00%,这是由于过长醚链取代基破坏分子间π-π堆积,减小分子间的作用力,导致热稳定性下降。综上所述,在蒽醌染料分子中引入醚链取代基后,可显著提高染料分子的光稳定性;引入一定范围长度醚链取代基可提高染料分子的热稳定性。在此工作基础上将进一步探究醚链长度对染料光热稳定性的影响规律,以及在染料分子上进一步修饰与光刻胶树脂主体相似基团,以提高染料分子在光刻胶中的分散性和与树脂主体的匹配性,实现染料分子在光刻胶薄膜中良好的均匀性和抗聚集性,从而为染料分子在彩色光刻胶中的应用奠定基础。

