Mn强化Fe/C微电解工艺条件优化及降解油墨废水机理
贾艳萍,丁雪,刚健,佟泽为,张海丰,张兰河
(1东北电力大学化学工程学院,吉林省吉林市 132012; 2长春工程学院能源动力工程学院,吉林省长春市 130012)
引 言
水性油墨在生产和应用过程中产生的油墨废水含有大量水溶性树脂类连接剂、醇基类化合物及染料等物质,具有高COD、高色度、难生物降解等特点[1-4]。铁碳微电解工艺是一种运行简便、成本低、绿色环保的废水预处理方法,它将不同电极电势的金属颗粒或非金属以一定比例浸泡在电解质溶液中,通过两者产生的电位差形成原电池,使水中有机污染物通过氧化还原作用被降解和去除[5-9]。张涛等[10]采用铁碳微电解法处理油墨废水,在反应时间为1 h,初始pH 为4,铁、碳用量分别为填料总投加量的10%和16.67%的条件下,废水色度和COD去除率分别为90%和50%。王顺等[11]采用混凝、热固化和铁屑微电解组合工艺处理水性油墨印花废水,当废水pH 为4,铁屑投加量为1000 g/L,反应时间为1 h时,废水COD去除率可达83%。石键韵等[12]利用曝气式铁碳微电解工艺处理PCB 油墨废水,在Fe/C 为1∶1,pH 为3,反应时间为1 h 的条件下,COD去除率约为60%。这些研究集中讨论了Fe/C 微电解工艺对有机物去除率的影响,但是尚不清楚微电解工艺处理前后水质的变化及有机物降解机理。由于传统微电解填料易出现板结钝化的问题,阻碍电子传输效率,导致其处理效果不理想,因此,亟需优化微电解的工艺条件,解决填料的板结钝化问题。
锰在自然环境中含量丰富、价格低廉,其电极电位为-1.18 V,可与铁、碳产生较高的电位差,形成Fe-C、Mn-C 和Fe-Mn 宏观原电池,提高电子传输效率[13-15]。但有关Fe/Mn/C 微电解处理废水研究尚少,其反应机理尚不明确。本研究拟在铁碳微电解填料中加入金属锰形成Fe/Mn/C 三元微电解工艺,构建响应面模型,以初始pH、填料总投加量、Fe/Mn 质量比和反应时间作为影响因素,采用COD 去除率作为响应值,优化Fe/Mn/C 微电解处理油墨废水的工艺条件。采用三维荧光光谱、紫外可见光谱、气-质联用色谱以及Zeta 电位等分析Fe/Mn/C 三元微电解工艺处理前后油墨废水的有机物成分,采用拉曼光谱仪分析填料表面结构变化,推测油墨废水的降解机理,以期为铁碳微电解的改进工艺提供科学依据。
1 实验材料与方法
1.1 实验用水及材料预处理
实验用水为实际水性油墨废水,取自吉林市某纸箱印刷厂印刷机械设备冲洗工段。废水为淡粉色,无明显刺激性气味,废水COD为(857.8±100)mg/L,氨氮为(50.7±10)mg/L,浊度为(333±15)NTU,色度为(259.9±15)倍,pH为6.6±0.5。Fe/Mn/C微电解处理油墨废水的工艺装置如图1所示。
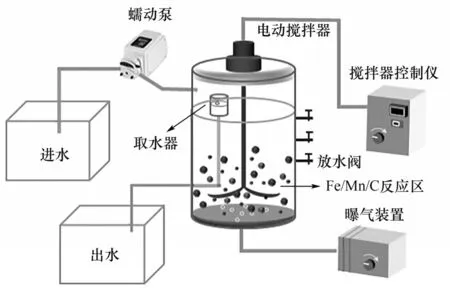
图1 Fe/Mn/C微电解工艺装置示意图Fig.1 Schematic diagram of Fe/Mn/C microelectrolysis process
为去除铸铁屑和金属锰表面油污及氧化物,增强金属活性,采用10% NaOH 溶液和10% HCl 溶液将其浸泡1 h 并冲洗至中性;在活性炭预处理过程中,采用循环吸附法[16]进行吸附饱和,即将活性炭浸泡在废水中,静置吸附24 h,测定吸附前后废水中污染物浓度,然后完全更换废水,再次静置吸附24 h,测定吸附前后废水中污染物浓度,重复操作数次,直至测得吸附前后污染物浓度差小于5 mg/L为止。
1.2 监测指标与分析方法
pH 采用pH 计(pHSJ-3F 型,上海仪电科学仪器有限公司)测定;Zeta 电位采用Zeta 电位仪(JS94K2型,上海中晨数字技术设备有限公司)测定;采用紫外-可见分光光度计(UV1700 型,上海奥析科学仪器有限公司)分析废水处理前后在紫外-可见光区域的物质及含量变化;采用三维荧光光谱仪(RF-5301PC 型,日本岛津公司)分析废水处理前后的荧光物质结构及官能团变化;采用气-质联用仪(QP2010Ultra型,日本岛津公司)分析废水处理前后的有机物变化,采用拉曼光谱仪(DXR3 型,美国赛默飞世尔科技公司)分析反应前后填料表面的分子结构。
1.3 响应面实验设计
Fe+Mn/C质量比为1,初始pH、反应时间、Fe/Mn质量比及填料总投加量对COD去除率的影响如图2所示。

图2 单因素对COD去除率的影响Fig.2 Effects of single factors on removal efficiencies of COD
在图2 单因素实验的基础上,选择中心点及各因素的高低水平,即设定初始pH 为3、反应时间为1.5 h、Fe/Mn质量比为3、Fe/C质量比为3/4及填料总投加量为100 g/L。以COD 去除率为响应值,以初始pH(2~4)、反应时间(1~2 h)、Fe/Mn 质量比(2~4)及填料总投加量(80~120 g/L)为影响因素,通过响应面法建立Fe/Mn/C 微电解处理油墨废水的工艺数学模型。Design-Expert 软件设计的四因素三水平实验如表1所示。

表1 响应面实验因素及水平设计Table 1 The experimental factor and level design for response surface
2 实验结果与讨论
2.1 响应面法
2.1.1 响应面实验设计结果 根据Box-Behnken 中心组合实验原理设计29个实验点,分为五组零点实验(8号、16号、19号、21号和23号)和分析因子实验(剩余24 组),如表2 所示。工艺数学模型的显著性可由F检验和P值表示,如表3 所示,本模型显著性检验F值为22.76、P值小于0.0001,变异系数(CV)为1.23(<10),说明此模型具有较高的可信度和精确度。本模型失拟项值(0.1149)大于0.05,模型与实测数据差异较小,可采用回归方程分析实验结果;本实验信噪比为16.129(>4),说明该模型预测COD 去除率可行。根据F值判断各因素的影响程度:填料总投加量>初始pH>反应时间>Fe/Mn 质量比。反应时间与填料总投加量存在极显著交互作用。
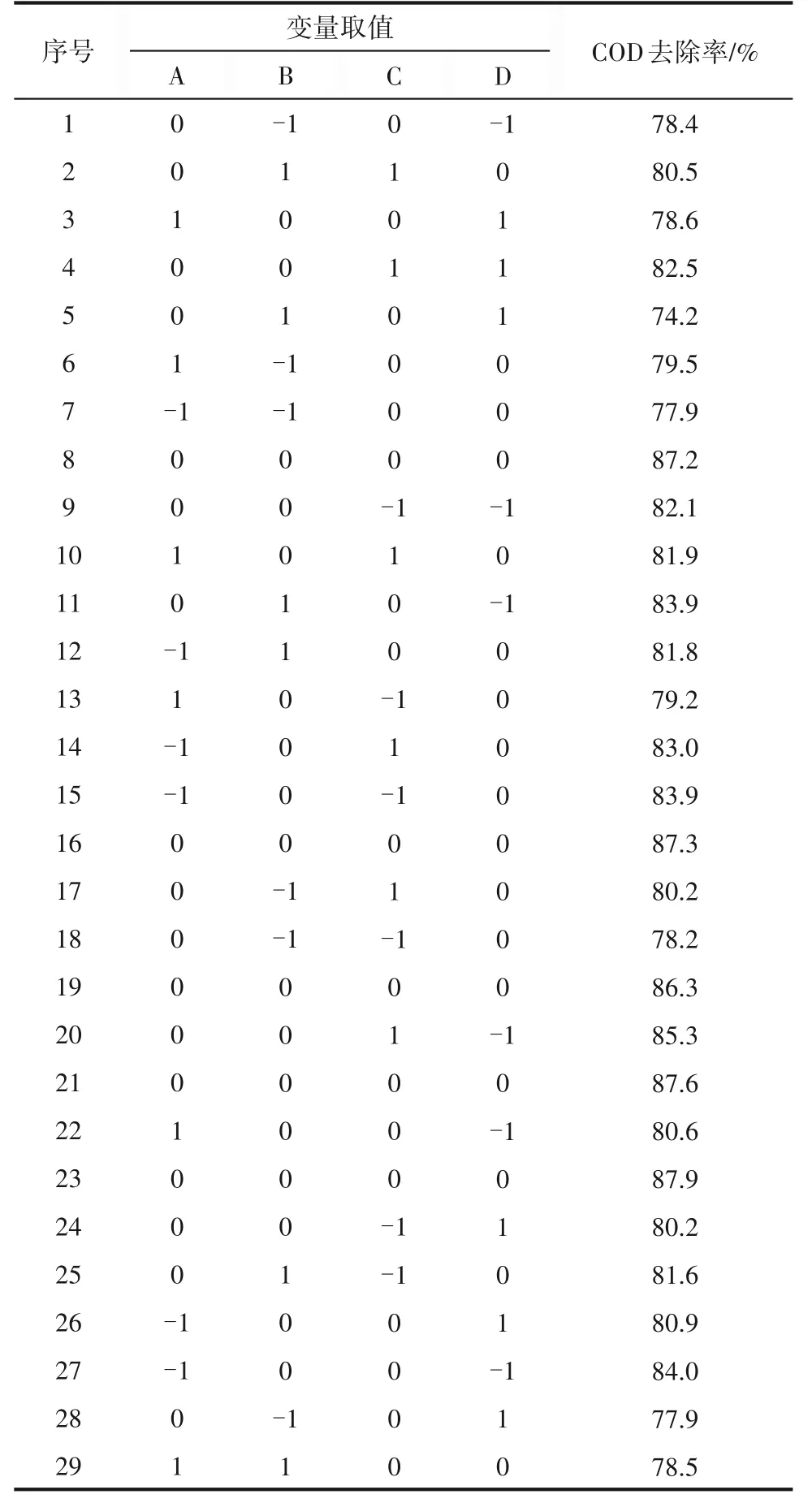
表2 响应面实验组次设计及实验结果Table 2 Experiment design and experimental results of response surface test group

表3 COD去除率(响应值Y)模型方差分析Table 3 Variance analysis of COD removal efficiency(response value Y)model
2.1.2 二次回归模型的建立 实测值与预测值的拟合曲线如图3所示。回归模型的实测值及预测值的残差正态概率在直线两侧相近分布,说明实测值及预测值差异较小。预测值与实测值线性拟合相关系数(0.94969)趋于1,这表明采用该二次回归模型预测COD 去除率的变化可行。各因素回归拟合后,得到COD去除率的二次响应面方程:
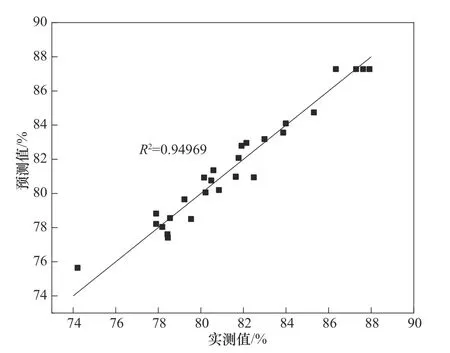
图3 实测值与预测值的对比Fig.3 Comparison of measured value and predicted value

式中,Y为COD 去除率;A 为初始pH;B 为反应时间;C为Fe/Mn质量比;D为填料总投加量。
2.1.3 因素相互作用 由图4 可知,摄动图中各影响因子均为负影响,自变量和响应值呈负相关。初始pH(A)、反应时间(B)、Fe/Mn质量比(C)及填料总投加量(D)的一次项系数分别为-1.10、0.69、0.67及-1.68,影响因素作用大小排序:填料总投加量>初始pH>反应时间>Fe/Mn质量比。
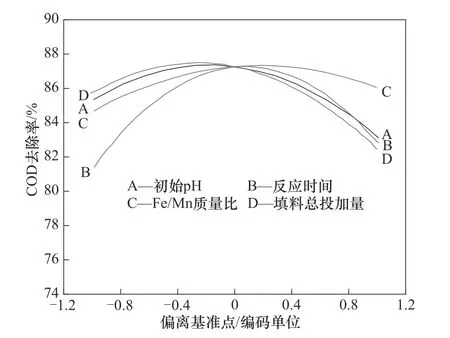
图4 COD去除率摄动图Fig.4 Perturbation graph of removal efficiency of COD
2.1.4 交互作用的响应曲面图 响应面曲线坡度越大,该因素对响应值的影响越显著[17]。根据响应面三维图,分析初始pH、反应时间、Fe/Mn 质量比及填料总投加量对COD 去除率的影响,结果如图5 所示。图5(a)、(e)的曲线坡度较大,表明反应时间与初始pH、反应时间与填料总投加量的两因素相互作用较强,两种组合因素对COD 去除率均有较为显著的影响。图5(b)~(d)、(f)中,曲线较为平缓,对应的两因素相互作用对COD 去除率的影响均较弱。同时,由图5还可知,三维响应曲面开口均向下,各因素在响应曲面中均有最大值,说明该模型存在最优解。

图5 不同因素对COD去除率影响的响应面三维图Fig.5 Three-dimensional graph of the response surface on the effect of different factors on removal efficiency of COD
通过软件分析可知Fe/Mn/C 微电解工艺处理油墨废水的最佳工艺条件:在初始pH 为2.79、反应时间为1.58 h、Fe/Mn质量比为3.11及填料总投加量为93.36 g/L的条件下,COD去除率的预测值为87.8%。
2.1.5 验证实验 在响应面分析法优化得到的最佳工艺条件下,即Fe+Mn/C质量比为1,初始pH为2.79、反应时间为1.58 h、Fe/Mn质量比为3.11及填料总投加量为93.36 g/L,进行3次重复实验。COD去除率达到87.9%,预测值(87.8%)与实测值相差0.1%,可达到《污水综合排放标准》(GB 8978-1996)中二级排放标准,说明该数学模型对Fe/Mn/C微电解工艺条件优化及COD去除率预测拟合度较高,具有可行性。
2.2 Fe/Mn/C 微电解工艺处理油墨废水前后的水质分析
2.2.1 三维荧光光谱分析 在最佳工艺条件下,Fe/Mn/C 微电解工艺处理油墨废水前后的三维荧光光谱如图6 所示。进水存在四个主要特征峰,分别为类溶解性微生物代谢产物荧光峰A(Ex/Em=275/300 nm,荧光强度6481.561)、类芳香族蛋白质荧光峰B(Ex/Em=220/290 nm,荧光强度5164.579)、类富里酸荧光峰C(Ex/Em=230/400 nm,荧光强度14728.527)以及类腐殖酸荧光峰D(Ex/Em=265/580 nm,荧光强度10955.026)。Fe/Mn/C 微电解工艺处理后的出水,荧光峰C(Ex/Em=235/400 nm,荧光强度14449.207)及荧光峰D(Ex/Em=290/580 nm,荧光强度6379.227)均发生红移,说明部分污染物转化为含有羧基、羰基、羟基以及胺基等官能团的有机物质[18-21],荧光峰D 的荧光强度明显降低,但荧光峰C的荧光强度无显著变化,说明Fe/Mn/C 微电解工艺对类富里酸类物质降解效果较差;荧光峰A、B 位置未发生改变,但荧光强度明显减弱,分别为4960.602和3841.881,这说明Fe/Mn/C 微电解工艺对类溶解性微生物代谢产物、类芳香族蛋白质类物质以及类腐殖酸类物质降解效果显著。
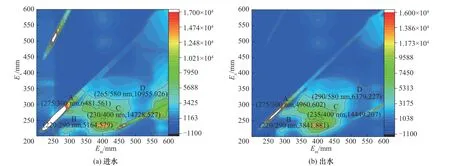
图6 进出水三维荧光光谱图Fig.6 Three-dimensional fluorescence spectrum of influent and effluent
2.2.2 紫外可见光谱分析 废水的成分影响紫外可见光谱在200~400 nm(紫外区)处的吸收强度[22-24],如图7所示。由于油墨废水中溶解性有机物(DOM)种类复杂、浓度高,紫外光区的吸收强度显著,可见光区(400~800 nm)处吸收强度趋于零,处理后的废水吸收强度明显减弱,这说明油墨废水中腐殖质共振能量大[25]。E254、E300和E400分别是254、300和400 nm 处的紫外吸收值,E254反映水中腐殖质类物质的相对含量[26],E300/E400反映腐殖质的腐殖化程度和芳香性[27]。Fe/Mn/C 微电解工艺处理前,油墨废水的E254为0.916,E300/E400为1.58,进水主要以腐殖酸类物质为主。经Fe/Mn/C 微电解工艺处理后,出水E254由0.916 下降至0.295,腐殖质去除率为67.8%;E300/E400为4.38,出水主要以富里酸类物质为主,这是由于Fe/Mn/C 微电解体系对腐殖酸类物质有较好的降解效果,而对富里酸类物质降解效果较差,所以出水腐殖质主要为富里酸类物质,这与上述三维荧光光谱解析结果相吻合。经Fe/Mn/C 微电解工艺处理后,废水的复杂化程度以及芳香性显著减弱,这可能由于Fe/Mn/C 原电池反应产生的Fe2+、Mn2+、[H]以及·OH 等与有机物发生了氧化还原反应,使溶液中苯环及共轭双键等结构遭到破坏,较大程度降低了腐殖质的芳香性。
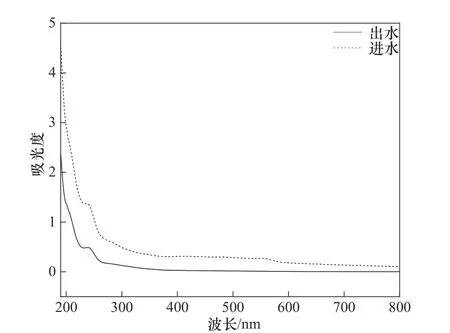
图7 油墨废水的紫外可见光谱图Fig.7 UV-visible spectrum of ink wastewater
2.2.3 拉曼光谱分析 Fe/Mn/C 微电解填料反应前后的拉曼光谱如图8 所示。反应前的铸铁屑、活性炭以及反应后的锰在1350~1590 cm-1范围内存在两个明显的吸收峰,为碳材料的典型特征峰:结构缺陷峰——D 峰(1350 cm-1,1360 cm-1)和sp2碳原子的面内振动峰——G 峰(1580 cm-1,1590 cm-1)[28],这是因为铸铁屑和活性炭在反应过程中,填料消耗和转移,部分转移附着在锰表面,同时由于装置的快速搅拌及填料的碰撞,部分活性炭被破碎成更加细小的炭粒,废水中的带电胶粒会在电极上聚集形成沉淀,Fe(OH)2和Fe(OH)3胶体与有机污染物质发生沉聚作用,在形成沉淀聚集的过程中,细小炭粒易被沉淀去除,C含量显著下降;反应后的铸铁屑,211和271 cm-1处峰可归属为Fe2O3或其他含Fe—O 键化合物的振动[29-32];反应后的锰,在307、361 cm-1处峰为Mn—O 键的弯曲振动信息,653 cm-1处峰为Mn—O键的伸缩振动[33-36];反应后的活性炭,在651 cm-1处可能为Mn—O 键的伸缩振动峰或Fe3O4的振动峰,这说明微电解过程中生成了铁锰氧化物,部分氧化物附着在活性炭表面。

图8 反应前后铁、锰、碳的拉曼光谱图Fig.8 Raman spectrum of iron,manganese and carbon before and after the reaction
2.3 Fe/Mn/C微电解工艺降解油墨废水的机理
利用气相色谱质谱联用仪分析Fe/Mn/C 微电解工艺处理前后油墨废水的有机物种类和含量变化,如图9 所示。Fe/Mn/C 微电解工艺的进水主要存在2,6-二叔丁基对甲苯酚(保留时间为11.255 min)、2,2,4-三甲基-1,3-戊二醇二异丁酸酯(保留时间为12.320 min)、对苯二甲酸二异丁酯(保留时间为15.465 min)、邻苯甲酸二辛酯(保留时间为22.180/23.025 min)等酯类物质;(E)-4-(对氨基苯)乙烯(保留时间为19.700 min)、油酰胺(保留时间为20.540 min)以及直链烃类化合物(保留时间为12.460/14.805/16.935/21.030 min)。其中,经Fe/Mn/C 微电解工艺处理后,2,6-二叔丁基对甲苯酚、2,2,4-三甲基-1,3-戊二醇二异丁酸酯、直链烃类化合物、油酰胺和(E)-4-(对氨基苯)乙烯的含量显著下降,邻苯甲酸二辛酯被转化或降解,出现了浓度较高的2,2′-亚甲基双-(4-甲基-6-叔丁基苯酚)(保留时间为21.170 min),这是因为原水中2,6-二叔丁基对甲苯酚在强酸条件下,与甲缩醛(用于树脂的生成,油墨废水中含有树脂)发生缩合反应,转化为2,2′-亚甲基双-(4-甲基-6-叔丁基苯酚)。这说明Fe/Mn/C 微电解体系可有效降解油墨废水中含双键、苯环、酯类等物质,将复杂高分子有机物分解为易降解的小分子物质,部分有机物转化形成2,2′-亚甲基双-(4-甲基-6-叔丁基苯酚)。

图9 进出水气-质联用谱图Fig.9 Gas-mass spectrometry of influent and effluent
Fe/Mn/C 微电解工艺处理前后油墨废水进水、出水的Zeta电位分别为-11.4681 mV和-3.4148 mV,Zeta 电位绝对值降低,这是由于:(1)带有负电性的水性油墨通常以含有羟基(—OH)、羧基(—COOH)等亲水基团的水溶性或碱溶性树脂作为连接料,油墨粒子由于具有空间位阻效应和静电排斥力的连接料存在而处于稳定状态,反应过程中,H+的加入中和了油墨粒子表面的负电性,同时使连接料的分子链上部分羟基质子化,稳定状态被破坏[37-39];(2)微电解过程产生的Fe2+和Mn2+中和了油墨粒子表面的部分负电荷,同时由于Fe2+和Mn2+的电荷密度较高,压缩了油墨粒子的扩散双电层,溶液的稳定性被破坏,产生凝聚现象;(3)微电解反应产生的Fe(OH)2、Fe(OH)3、Mn(OH)2等氢氧化物在絮凝沉淀过程中,由于网捕、卷扫作用使油墨粒子凝聚,发生共沉降现象,Zeta电位绝对值降低[40-42]。
由前期实验得出,Fe/C 微电解的最佳运行工艺条件为初始pH 为3、铁投加量80 g/L、铁/碳质量比0.8 及反应时间为1.5 h,在此条件下,油墨废水COD去除率为73.7%,远低于Fe/Mn/C微电解对油墨废水的COD 去除率(87.9%);Fe/C 微电解的反应速率常数k为5.7381×10-4min-1,当Mn 加入后,反应速率常数k提高至9.3834×10-4min-1,Fe/Mn/C 微电解对废水的降解速率显著高于Fe/C 微电解,可见,Fe/Mn/C微电解极大地提高了对油墨废水的处理效率。Fe/Mn/C 微电解工艺处理油墨废水的反应机理如图10 所示。Fe/Mn/C 微电解工艺应用于废水处理时,在微观体系中,铸铁屑内部的铁碳构成微观电池,产生无数个细小微电池[43]。在宏观体系中,活性炭与铸铁屑/金属锰分别作为阴、阳极,构成Fe/C 和Mn/C 宏观电池,由于电位差的存在,铸铁屑和金属锰又形成了Fe/Mn 原电池;与传统Fe/C 微电解工艺相比,Fe/Mn/C 微电解工艺增加了原电池的数量,提高了电子传输效率。Fe/Mn/C 反应产生的Fe2+、Mn2+、[H]、H2O2和·OH 等可与有机污染物发生氧化还原反应,Fe2+、Mn2+和[H]等还原性较强的物质可将废水中的卤代基团、碳碳双键、偶氮双键、苯环、硝基等结构断裂,H2O2和·OH 等氧化性较强的物质可氧化分解废水中的难降解有机物[44-46]。微电解体系中,两个电极之间由于原电池作用形成微电场,在微电场作用下,带电胶粒产生电泳现象,在电极上聚集并形成沉淀,从而与废水分离。在中性、碱性条件下通入氧气,Fe2+和Fe3+生成带正电荷的凝胶状沉淀物Fe(OH)2和Fe(OH)3,它们能与带负电荷的一些物质和电解质发生作用,有效吸附水中的污染物质,Mn2+在OH-存在的条件下生成Mn(OH)2,Mn2+和Mn(OH)2易被氧化成性质不稳定的MnO(OH)2,如式(2)~式(4)所示,该物质易被水解成氧化能力较强的MnO2、Mn2O3和Mn3O4[47],增强了微电解反应的氧化还原能力,提高了有机物的降解效率。
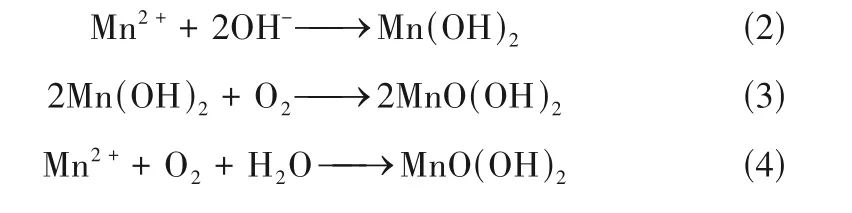
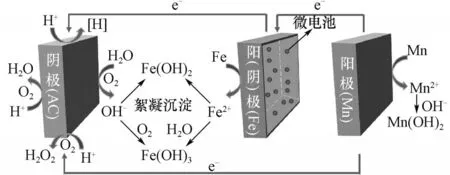
图10 Fe/Mn/C微电解反应机理Fig.10 Reaction mechanism of Fe/Mn/C microelectrolysis process
3 结 论
(1)利用响应面法得出Fe/Mn/C 微电解最佳工艺条件:在初始pH 为2.79、反应时间为1.58 h、Fe/Mn 质量比为3.11 及填料总投加量为93.36 g/L 条件下,COD去除率为87.9%,采用响应面法预测的COD去除率与实测值相差0.1%(<2%),该数学模型具有可行性。
(2)油墨废水主要以腐殖酸类物质为主,腐殖质共振能量大,芳香性高,Fe/Mn/C 微电解工艺对类溶解性微生物代谢产物、类芳香族蛋白质类物质以及类腐殖酸类物质降解效果显著,处理后的废水中部分污染物转化为含有羧基、羰基、羟基以及胺基等官能团的有机物。Fe/Mn/C 三元微电解体系可使溶液中苯环及共轭双键等结构遭到破坏,极大程度使腐殖质的芳香性降低。由于反应过程中铸铁屑和活性炭的消耗和转移,填料C含量显著下降,部分转移附着在锰表面,Fe/Mn/C 微电解过程中生成了铁、锰氧化物,部分氧化物附着在活性炭表面。
(3)进、出水的Zeta 电位分别为-11.4681 mV和-3.4148 mV,Fe/Mn/C 微电解工艺处理后的废水Zeta电位绝对值降低,微电解过程产生的Fe2+和Mn2+可压缩油墨粒子的扩散双电层,并中和其表面的部分负电荷,溶液的稳定性被破坏,产生凝聚现象。Fe/Mn/C 微电解体系可有效降解油墨废水中含双键、苯环、酯类的有机物,部分有机物转化形成2,2′-亚甲基双-(4-甲基-6-叔丁基苯酚)。与传统Fe/C 微电解工艺相比,Fe/Mn/C 微电解工艺处理废水时形成Mn/C、Fe/Mn 原电池,增加了原电池的数量,提高了电子传输效率。Mn2+在OH-存在的条件下生成锰氧化物,有效增强了微电解反应的氧化还原能力。

