微通道内醇胺/离子液体复配水溶液吸收CO2的传质特性
殷亚然,朱星星,张先明,朱春英,付涛涛,马友光
(1纺织纤维材料与加工技术国家地方联合工程实验室,浙江理工大学材料科学与工程学院,浙江杭州 310018;2化学工程联合国家重点实验室,天津大学化学工程学院,天津 300072)
引 言
以二氧化碳(CO2)为主的温室气体过度排放导致全球温室效应日趋明显,引起世界各国的高度关注[1]。我国积极响应国际环保号召,并提出碳中和、碳达峰等一系列战略政策,彰显了我国控制和治理CO2气体排放的坚定决心。工业上常用醇胺溶液化学吸收流程工艺中排放的CO2气体[2-3]。其中,单乙醇胺(MEA)、甲基二乙醇胺(MDEA)、二乙醇胺(DEA)、氨甲基丙醇(AMP)等醇胺溶液对CO2具有反应速率快和选择性高等优点,但存在易降解、解吸能耗大、腐蚀金属管道和设备等缺陷[4]。离子液体(IL)热稳定性高,蒸气压极低,物化性质可调,被视为潜在的绿色溶剂[5-7],但高黏特性限制了其工业应用。将醇胺溶液与离子液体进行复配制备混合溶剂有望实现CO2的高效绿色捕集[8-10]。研究证明,MEA 和MDEA 与1-丁基-3 甲基咪唑四氟硼酸盐([Bmim][BF4])和功能化离子液体1-羟乙基-3-甲基咪唑甘氨酸盐([C2OHmim][GLY])的复配溶液可增强纯醇胺溶液的吸收能力,降低降解和蒸发速率,提高稳定性和再生效率[11-15]。
微反应器技术将流体受限于亚毫米级的微通道内,通过减小扩散距离、增大浓度/温度梯度以及相界面积,在氨化、氧化、硝化、催化等传质受限的气液反应体系中展现显著的强化效果[16-19]。已有研究证明,微通道内醇胺水溶液与CO2的液相体积传质速率(kLa)较传统设备高出1~3 个数量级[20-21]。然而,目前关于微通道内醇胺/离子液体复配溶液吸收CO2方面的传质研究还很缺乏。微通道内气液传质与气液接触形式或流型密切相关。在诸多流型中,弹状流因气泡/液弹分布规整、重复性好和操作可控性高而备受关注,因而阐明液弹内传质机制对过程参数控制与优化、过程强化设计以及传质预测模型的建立十分重要。弹状流气液传质一般包括两部分:泡体向液膜传质和泡头向液弹传质,而这两部分的传质贡献一直存在争议。早期,液膜因易饱和而被认为对整体传质的贡献可忽略[22],两相速度和液弹长度是影响传质的主要参数。随后,诸多研究者论述了液膜不同程度的传质贡献并以此建立传质模型[23-26]。但由于液弹内循环和液膜饱和等复杂因素,明确泡体向液膜传质和泡头向液弹传质的贡献并建立普适的传质模型仍存在巨大挑战。研究表明,毫米级圆管中弹状流内对流通过液弹内的循环涡流和液膜扩散实现[27-28]。基于此实验结果,液弹中循环运动的重要性被进一步揭露,在液膜内扩散传质不限制总传质速率情况下,循环频率与整体液相传质系数存在非常简单的线性关联[29]。然而,这种相关性是否适用于微米级其他截面通道和体系有待进一步实验研究与证实。
本文旨在探究微通道内醇胺/离子液体复配水溶液与CO2的传质性能。将MEA 和MDEA 与亲水性的常规离子液体[Bmim][BF4]和功能型离子液体[C2OHmim][GLY]进行复配,得到四种复配水溶液。在弹状流型下,考察总浓度为1 mol/L 的溶液中醇胺/离子液体浓度比对液相体积传质系数、比表面积和液相传质系数的影响,分析扩散系数和反应速率对传质速率的影响,旨在揭示液相体积传质系数与液弹内循环频率间的关系。
1 实验材料和方法
1.1 材料
实验所用的单乙醇胺(MEA,纯度≥0.995)和甲基二乙醇胺(MDEA,纯度≥0.99)购买自阿拉丁化学试剂有限公司,1-丁基-3-甲基咪唑四氟硼酸([Bmim][BF4],纯度≥0.995)购自河南利华制药有限公司,1-羟乙基-3-甲基咪唑甘氨酸([C2OHmim][GLY],纯度≥0.99)购自上海复捷化学有限公司。以上试剂在使用前未经处理。将二氧化碳(CO2,纯度>99.99%)作为气相,醇胺/离子液体复配水溶液为液相,即MEA/[Bmim] [BF4]、MEA/[C2OHmim] [GLY]、MDEA/[Bmim][BF4]和MDEA/[C2OHmim][GLY]水溶液。醇胺与离子液体的总浓度固定为1 mol/L,醇胺/离子液体浓度比(cAA∶cIL)为5∶5、6∶4、7∶3、8∶2、9∶1和10∶0。实验所用液体密度由振荡管密度计(DMA-4500-M,Anton Paar,Austria)测定,液体黏度由全自动乌氏毛细管黏度仪(iVisc, LAUDA,Germany)测定,表面张力则由表面张力仪(OCAH200,Data Physics instruments GmbH,Germany)测定,相应物性数据见表1。

表1 醇胺/离子液体复配水溶液的物理性质Table 1 Physical properties of various alkanolamine/ionic liquid aqueous solutions
1.2 实验装置
实验所用设备及流程如图1(a)所示。采用两台高精度(0.35%稳定精度)微流注射泵(Harvard PHD 2000, USA)以设定的流率分别将气体和液体送至T型微通道的分支进口和主通道进口。微流注射泵能够精确控制气体流速,并在主通道交叉口附近产生稳定气泡,气泡长度误差小于6%(图2)。液相流率(QL)固定为60 ml/h,气相流率(QG)为20~300 ml/h。在冷光源灯的照明下,高速摄像仪(Motion Pro Y-5,USA)以每秒2000帧的速度采集通道内气液流动图像,并传输至电脑。压差传感器(ST3000,Honeywell,USA)一端连接气体进口,另一端连接大气,用于测量主通道内的总体压力降。实验所用微通道芯片是在聚甲基丙烯酸甲酯(PMMA)板上采用精密铣削工艺进行刀刻,并用另一块薄的PMMA 板通过螺栓密封而成。微通道芯片示意如图1(b)所示,芯片尺寸为80 mm×50 mm×10 mm,T型进口分支和主通道长度分别为5和30 mm,截面均为0.4 mm×0.4 mm的方形。
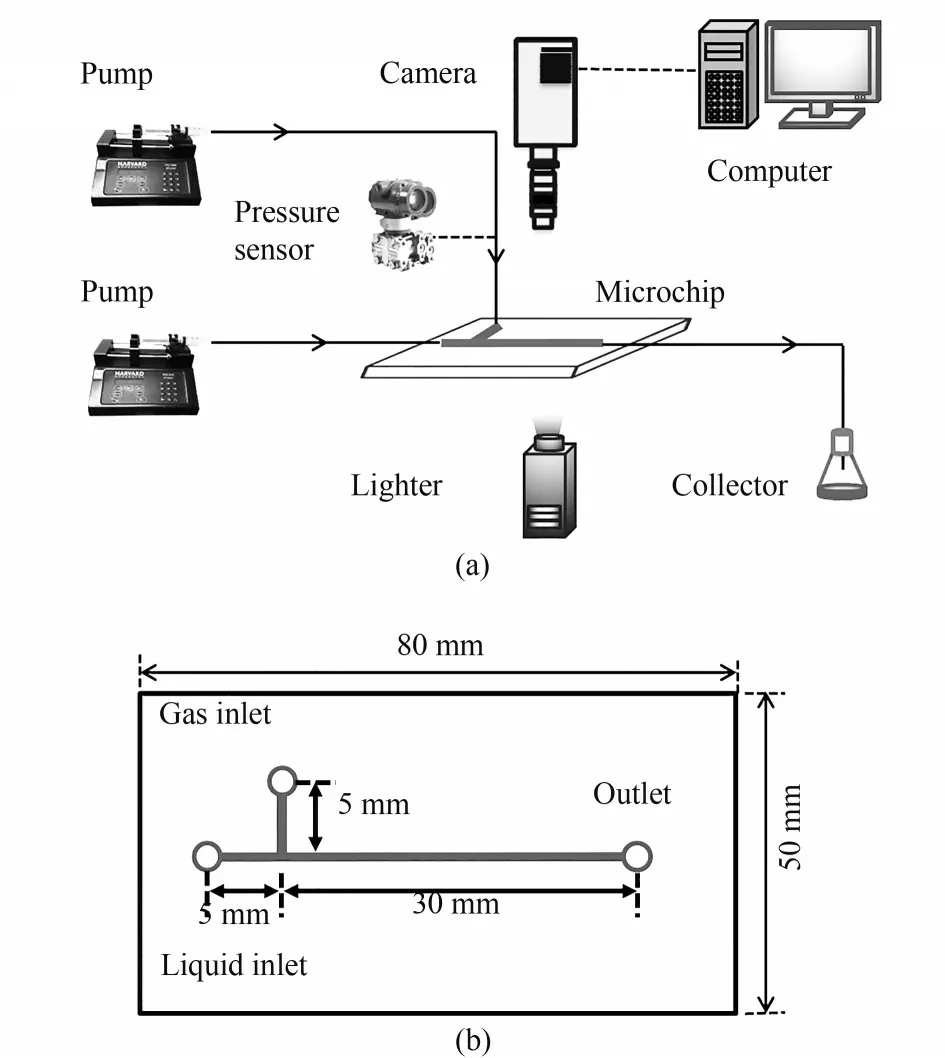
图1 实验装置流程和微通道结构示意图Fig.1 Schematic diagram of experimental device and microchannel structure

图2 气泡初始长度的稳定性分析Fig.2 Stability analysis of initial bubble length
1.3 传质性能参数计算
四种醇胺/离子液体水溶液与CO2的反应均可视为拟一级反应[11-12,15,30],传质为速率控制步骤,反应主要发生在气液界面[31-32]。气相为纯CO2,气膜阻力可忽略不计,传质阻力主要在液膜。液相体积传质系数(kLa)可由式(1)进行计算:

由于气液间反应快速,且醇胺溶剂远远过量,液相主体中CO2浓度可视为零[33-34],则对数平均浓度(ΔcCO2,m)可依据通道进出口CO2界面浓度和进行计算[35]:

根据亨利定律,对数平均浓度可用CO2压力表示:

式中,不同体系的亨利系数可参照文献[11-12,15,30]进行计算,该拟合关联式已被证明具有较高精确度。NCO2,in和NCO2,out分别是通道入口和出口处CO2气体的摩尔流率,采用在线图像分析测定NCO2,out。因微通道内总压力降小于6 kPa,通道进出口处气泡的压缩和膨胀可忽略[36],NCO2,in和NCO2,out均可根据理想气体状态方程进行计算:
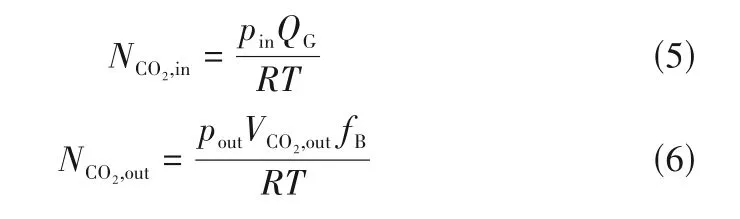
式中,R是理想气体常数;T是温度;fB是气泡的生成频率;VCO2,out是出口处单个CO2气泡的体积;pin,pout分别是气体入口和气泡在通道出口处的压力。微通道内气体因气液界面张力存在而呈现为弹状或泡状,经计算[37],通道出口处气泡两端的拉普拉斯压降为40~800 Pa,远小于大气压。因而,pout可按照大气压处理,对kLa产生的误差在1%以内[38]。
液相传质系数(kL)为kLa与比表面积(a)的比值,而a为主通道内气泡总表面积与通道体积之比:

式中,VC是主通道的体积;AB,i是主通道内第i个气泡的表面积。弹状气泡头尾可视为半球,气泡主体看作伪圆柱[39],如图3 所示,而泡状气泡看作球体。相应气泡表面积和体积可由以下公式获得。

图3 微通道中气液弹状流示意图Fig.3 Schematic of gas-liquid slug flow in the microchannel
弹状气泡:
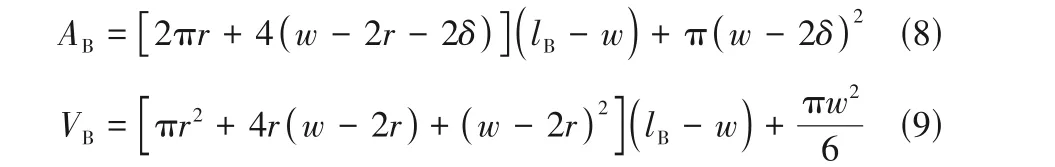
式中,δ是液膜厚度,可根据文献进行计算[40-41]。

其中,Ca是两相毛细管数(Ca=ηLuB/σ,uB为气泡流速),代表黏性力与表面张力的比值。
泡状气泡:

2 实验结果与讨论
醇胺/离子液体浓度比(cAA∶cIL)对kLa的影响如图4 所示。kLa在四种醇胺/离子液体复配水溶液中的变化不尽相同。kLa在MEA/[Bmim][BF4]内随cAA∶cIL的增大而增大,在MEA/[C2OHmim][GLY]内几乎不变,在MDEA/[Bmim][BF4]内略微增大,而在MDEA/[C2OHmim][GLY]内却呈现减小的趋势。对于伴有化学吸收的传质过程,化学反应对气液传质具有强化作用。MEA和[C2OHmim][GLY]与CO2可直接发生化学反应。根据双膜理论,增大MEA 或[C2OHmim][GLY]的浓度可增大化学反应速率,使得吸收到液体中的CO2被迅速反应,主反应区向气液两相界面移动,从而增大界面附近的CO2浓度梯度,加快传质速率,增大kLa。由图4 可判断,[C2OHmim][GLY]与MEA 的CO2传质速率相当,而kLa随MDEA 浓度的增加而增加,说明CO2吸收速率满足MDEA>[Bmim][BF4]。总体而言,吸收剂对CO2的吸收速率满 足MEA≈[C2OHmim][GLY]>MDEA>[Bmim][BF4]规律。

图4 液相浓度比对液相体积传质系数(kLa)的影响Fig.4 Effects of concentration ratio of alkanolamine to ionic liquid on the liquid-phase volumetric mass transfer coefficient(kLa)
微通道内气液流动与反应高度耦合,并与气液接触状态和液相内循环密切相关。与传统设备相比,微通道的尺寸缩小了几个数量级,为气液接触提供了极大的界面面积,如图5 所示,MEA/[Bmim][BF4]、MEA/[C2OHmim][GLY]、MDEA/[Bmim][BF4]和MDEA/[C2OHmim][GLY]体系的比表面积(a)分别为909~3321、909~7385、2419~7500 和1417~7500 m2/m3,比传统泡罩板塔、填料鼓泡塔等设备高出1~3 个数量 级[42]。 此 外,MEA/[C2OHmim][GLY]和MDEA/[Bmim][BF4]中,cAA∶cIL对a几乎不产生影响,而在MEA/[Bmim][BF4]和MDEA/[C2OHmim][GLY]中,a随cAA∶cIL的增大分别略有降低和增大,这是因为吸收增强导致单个气泡长度迅速减小,而液弹长度却未发生明显变化(图6)。由此,醇胺/离子液体浓度比对体积传质系数的影响源于传质系数,而比表面积的影响不明显,因而,四种溶液中kL随cAA∶cIL的变化与kLa规律一致,如图7所示。
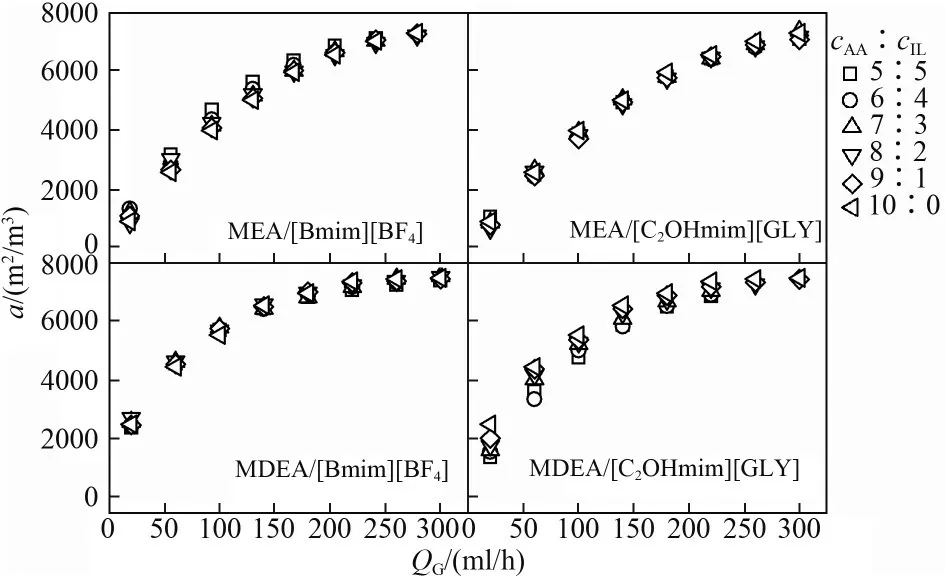
图5 液相浓度比对比表面积的影响Fig.5 Effect of concentration ratio of alkanolamine/ionic liquid on the specific surface area

图6 液相浓度比对气液两相流的影响Fig.6 Effect of concentration ratio of alkanolamine/ionic liquid on the gas-liquid two-phase flow

图7 液相传质系数(kL)随气相流率的变化Fig.7 Variation of the liquid-phase mass transfer coefficient(kL)with the gas flow rate
液相传质系数与CO2分子在液膜内的扩散速率、液相循环以及化学反应速率等紧密相关。根据渗透理论,kL与扩散系数(D)的0.5 次方成正比。CO2在复配溶液中的扩散系数为D= 2.12 ×。由表1 可知,不同浓度间溶液黏度相差甚微,因而扩散系数对kL的影响可忽略不计。液相传质系数依据气泡生成与流动过程的传质总量计算而来[21]。通常,在低流体流速下,通道入口影响气泡生成过程传质,并通过泡/弹生成长度影响主通道内流动过程传质。本实验中气泡生成周期相对较短[44],为0.0043~0.021 s,且cAA∶cIL未对气泡的生成时间和初始长度产生明显影响(图8),说明复配溶液中不同浓度比下气泡生成过程差别不大,液相传质系数可根据气液流动过程进行讨论。
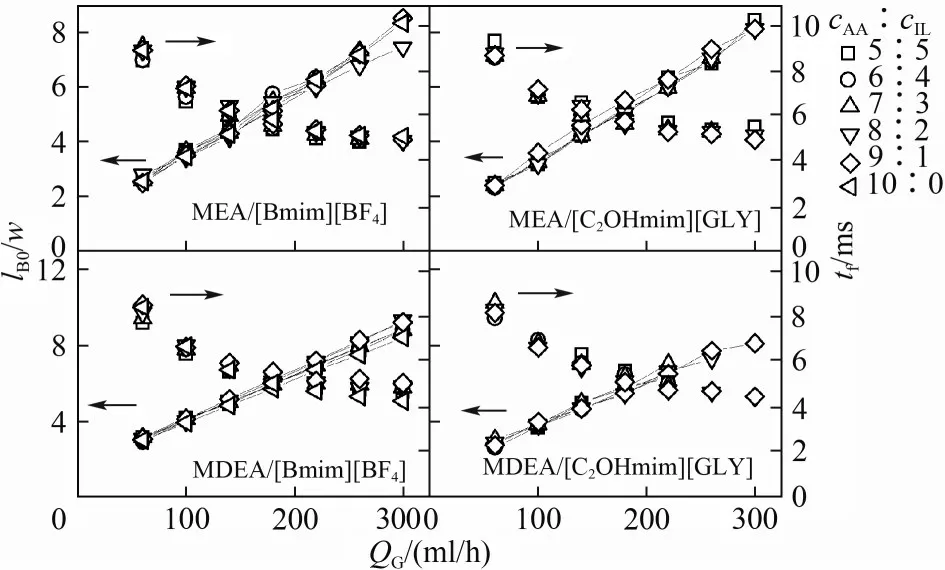
图8 液相浓度比对气泡初始长度和生成时间的影响Fig.8 Effects of concentration ratio of alkanolamine to ionic liquid on the initial length and formation time of bubbles
气液流动过程中,瞬时kL逐渐减小[25],因而气液停留时间减小,kL增大(图7)。实验所用通道较短(30 mm),气液停留时间较短(26~194 ms),且气相为纯CO2气体,无气膜阻力,因而所得kL大于较长微通道内化学吸收体系的kL[26,45]。通常定义增强因子为kL与扩散传质系数kL,diff之比,即E=kL/kL,diff。kL,fill可根据渗透扩散模型表示为kL,diff= 2D/(πtR)(tR为气泡生成和流动的时间总和)。增强因子反映了化学反应和液相循环对气液传质的增强作用。如图9所示,在所有复配溶液中,化学吸收和液相循环产生的传质增强作用随气相流率的增大呈现先增大后减小的规律。MDEA水溶液-CO2体系存在增强因子随较高气相流率的增大而单调下降现象[46]。利用物理吸收过程kL与kL,diff之比定义增强因子,以反映液相循环对传质的增强作用。已有研究表明,增大气相流率可提高液相循环对传质的增强作用[44]。由此可判断,复配溶液中化学反应所产生的传质强化在低气相流率下起主导作用,而在高气相流率下作用减弱。此外,当气相流率一定,增大化学反应速率有助于增强传质速率[42],且当cAA∶cIL一定,增强因子满足MEA/[C2OHmim][GLY]>MEA/[Bmim][BF4]或MDEA/[C2OHmim][GLY]>MDEA/[Bmim][BF4]。

图9 增强因子(E)随气相流率的变化Fig.9 Variation of the enhancement factor(E)with the gas flow rate
弹状流内传质主要包括两部分:一是气泡两端向液弹主体传质,受循环速度影响(如图3所示);二是气泡主体向气泡周围液膜传质,受气泡与液膜的接触时间影响。已有研究证实,液弹内的循环运动可驱动气液界面的整体传质[29,47]。液弹与气泡头部的滑移速度决定了界面传质速率,因而,某种意义上,循环频率(fcir)反映了单位时间内的单元传质量[29]。根据循环长度和循环流速可得到fcir[29,48]:

式中,UTP是两相表观流速;lS是液弹长度。由于气液快速传质,气泡流速和液弹长度不再为定值。为评估和比较不同条件下循环频率大小,用其平均值进行计算,结果如图10 所示。对于四种复配溶液,增大气相流率,液弹长度减小,从而循环频率增大。而不同溶液体系下,浓度比对复配溶液中液弹循环频率的影响存在临界值。当QG大于临界值,fcir在MEA/[Bmim][BF4]、MEA/[C2OHmim][GLY]、MDEA/[Bmim][BF4]体系内随cAA∶cIL的增大而增大,而在MDEA/[C2OHmim][GLY]体系内却呈现减小的规律。已有研究发现,当UTP/uB小于2 时,液弹内部不再产生循环[49],而增强化学吸收可增大UTP与uB间差异[50],进而增大fcir。当QG小于临界值时,化学吸收可显著减小气泡流速[51-52],增大气泡停留时间,但液弹循环长度也相应增加,最终cAA∶cIL的增加未对循环强度产生影响。由上可知,气液传质增强在低流率下主要是由于化学反应增强,而高流率下则是因为液弹内循环增强。当cAA∶cIL和流率一定时,循环频率在四种复配溶液中满足MEA/[Bmim][BF4]≈MEA/[C2OHmim][GLY]>MDEA/[C2OHmim][GLY]>MDEA/[Bmim][BF4]规律。

图10 液相浓度比对循环频率的影响Fig.10 Effect of concentration ratio of alkanolamine to ionic liquid on the circulation frequency
弹状流中液膜处溶质浓度高于液弹中心处浓度时,传质机理被证实为泡体向液膜扩散传质,液膜作为溶质源提供泡头间的液弹,并参与到液弹内的泰勒涡循环[27]。随后,研究发现涡流循环强度在决定整体传质速率上具有重要作用,循环频率与整体kLa满足线性正相关[29]。在较长的螺旋形圆管中也同样发现此线性关系,且强化因子与涡流的增加数量成正比[47]。然而上述研究仅针对圆形毫米级通道内物理吸收体系,且循环频率较低(小于40 Hz)。在方形截面微通道中,伴有化学吸收的kLa与fcir的关系变得复杂。如图11 所示,在kLa-fcir的双对数坐标图中,当cAA∶cIL一定,四种复配溶液的kLa随fcir的演变存在一个临界值fcir,0(约为100 Hz)。当fcir小于fcir,0,循环频率对传质速率的影响显著,两者呈线性关系,而一旦fcir大于fcir,0,循环强度对总传质速率的影响减弱,两者呈指数关系,幂律指数为0.63,且几乎不受液相体系和化学反应速率的影响。这是由于当fcir大于临界值时,气泡均为长气泡(长度大于3 倍通道宽度),气泡长度随气相流速增大而再度增大,液膜与液弹间的质量传递困难。因此,在高气相流率下,尽管液弹内部循环频率增加可增强气泡两端与液弹间传质速率,但对气泡整体传质的驱动作用减弱,从而减弱对kLa的影响。kLa与fcir的关系可总结为:当fcir<fcir,0时,kLa=αfcir;当fcir≥fcir,0时,kLa=αfcir,0+β(fcir/fcir,0-1)0.63。通过线性回归,确定了系数α和β,结果列于表2。系数α反映了液弹内气体浓度增加速率,随化学吸收剂浓度的增大而增大,在吸收剂 中 遵 循MEA≈[C2OHmim][GLY]>MDEA>[Bmim][BF4]规律。系数β与长气泡下液膜与液弹间液体混合的难易程度相关,而增强化学吸收有利于液弹与液膜间液体混合。该拟合结果适用于方形截面(0.4 mm×0.4 mm)微通道,气液流率在20~300 ml/h和60 ml/h,Hatta在5~274范围的条件。
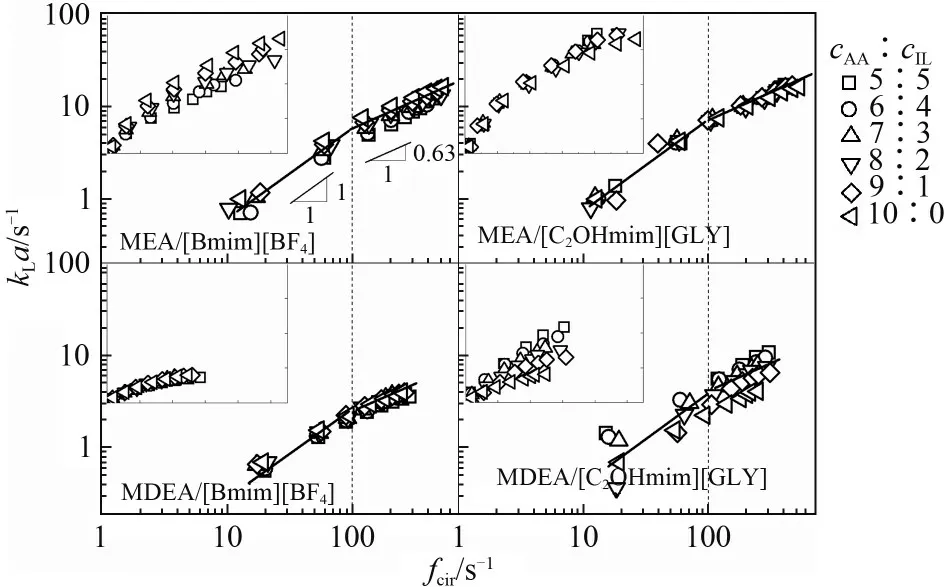
图11 循环频率与液相体积传质系数的关系Fig.11 Relationship of liquid-phase volumetric mass transfer with circulation frequency in the slug

表2 不同复配溶液的拟合系数α和βTable 2 Coefficients α and β for different alkanolamine/ionic liquid solutions
3 结 论
本文研究了方形微通道(0.4 mm×0.4 mm)内MEA/[Bmim][BF4]、MEA/[C2OHmim][GLY]、MDEA/[Bmim][BF4]、MDEA/[C2OHmim][GLY]四 种 复 配 水溶液吸收CO2的传质性能,考察了醇胺/离子液体浓度比(cAA∶cIL)对液相传质系数(kL)、比表面积(a)和液相体积传质系数(kLa)的影响。结论如下。
(1)随cAA∶cIL的增大,kLa在MEA/[Bmim][BF4]和MDEA/[Bmim][BF4]体系中增大,在MEA/[C2OHmim][GLY]中几乎不变,而在MDEA/[C2OHmim][GLY]中逐渐减小。因而,kLa在四种吸收剂中满足MEA≈[C2OHmim][GLY]>MDEA>[Bmim][BF4]规律。kLa的以上结果主要归因于kL,而a的影响起次要作用。
(2)kL主要与液相循环和化学反应速率有关。低流率下,cAA∶cIL对循环频率(fcir)不产生影响,此时化学反应的影响占主导,而高流率下,液相内循环强度起主导作用,循环频率(fcir)在MEA/[Bmim][BF4]、MEA/[C2OHmim][GLY]、MDEA/[Bmim][BF4]体系随cAA∶cIL的增大而增大,在MDEA/[C2OHmim][GLY]体系减小。当cAA∶cIL和流率一定,fcir在复配溶液中满足MEA/[Bmim][BF4]≈MEA/[C2OHmim][GLY]>MDEA/[C2OHmim][GLY]>MDEA/[Bmim][BF4]规律。
(3)方形微通道内fcir和kLa的线性关系在低气相流率下仍然成立,且斜率随化学反应的增大而增大。而在高气相流率下,液弹循环因膜弹混合困难而对总传质速率的影响减弱,kLa与fcir满足指数关系,幂律指数小于1,而指前因子可反映膜弹混合的难易程度。
符 号 说 明
AB——气泡表面积,m2
a——比表面积,m2/m3
Ca——两相毛细管数(Ca=ηLuB/σ)
c——浓度,mol/m3
c*——界面浓度,mol/m3
D——扩散系数,m2/s
E——增强因子
f——频率,s-1
H——亨利系数,Pa/(mol/m3)
kL——液相传质系数,m/s
kL,diff——液相扩散传质系数,m/s
kLa——液相体积传质系数,s-1
l——长度,m
N——摩尔流率,mol/s
p——压力,Pa
Q——体积流率,m3/s
tR——停留时间,s
u——实际流速,m/s
η——黏度,Pa·s
σ——表面张力,N/m
下角标
B——气泡
B0——初始气泡
C——通道
cir——循环
G——气相
in——主通道进口
L——液相
out——主通道出口
S——液弹
0——临界

