纳米分子筛的合成及硫化氢吸附性能
孟祥龙,杨 歌,郭海玲,刘晨光,柴永明,王纯正,郭永梅
(1.中国石油大学(华东)化学化工学院,重质油国家重点实验室,青岛266555;2.闽江学院新型功能性纺织纤维及材料重点实验室,福州350108)
硫化氢是一种具有腐蚀性的剧毒气体,常见于天然气、焦炉煤气等工业生产过程中[1~3],主要有管道腐蚀、催化剂中毒及有毒废气污染等危害[4].对产品气和尾气中含有的硫化氢杂质进行高效、深度脱除是研究其净化问题的热点.目前,硫化氢的脱除技术主要包括湿法和干法两大类.湿法适用于硫含量较高(100 mg/L以上)、规模较大的普通脱硫环境,如溶液吸收法[5]、离子液体法[6,7]和生物脱硫法等[8].对于硫含量极低(1 mg/L以下)的深度脱硫场合,由于反应的传质推动力小,具有高脱硫活性的干法脱硫技术(如吸附法)更可行[9].吸附法具有可操作性强、净化程度高等优势,其技术核心为研发高效吸附材料.常用的吸附材料有金属有机框架(MOFs)[10]、沸石分子筛[9,11~13]、活性炭[14]和金属氧化物[15]等.其中,沸石分子筛因其孔道结构规整、选择性良好、吸附性高和再生性良好而被视为理想的吸附脱硫材料[4].
研究发现,X型分子筛(FAU型)具有较高的穿透硫容,是脱除硫化氢的高效吸附剂[3,16].目前的研究大多针对气氛种类及工艺条件来考察分子筛的吸附脱硫能力,而针对分子筛材料本征吸附性质的研究较少[17,18].Melo等[19]将X型分子筛与商业化吸附材料Zinox(88%ZnO)对比,发现X型分子筛显示出更高的硫化氢吸附能力,但其吸附时间长、吸附效率低.该研究认为吸附剂的吸附性能与材料孔隙率有关,并未做深入研究.Cruz等[20]报道了在室温、分压约0.08 bar(1 bar=0.1 MPa)条件下,X型分子筛的硫容高达5 mol/kg,显著高于其它类型的吸附材料.这是由于X型分子筛具有多级孔结构,同时存在微孔和大孔,并含有大量骨架外钠离子.但X型分子筛也存在吸附时间长、效率低等缺陷.X型分子筛的吸附效率低与其微米尺寸(具有较大的扩散限制)有关,阻碍了硫化氢在全孔道内的快速吸附及脱附[21].此外,分子筛活性中心大多位于孔道内部,吸附活性位利用效率低,从而造成了低硫容和低吸附效率.因此,减小分子筛晶体尺寸、缩短扩散路径和提高活性中心利用率是提高分子筛吸附效率的最直接方法[22].研究证实,当分子筛尺寸小于50 nm时,扩散限制会显著降低,且在原子效应的作用下具有更高的外表面活性(高达20%的四面体配位原子位于外表面)[23].纳米材料的特性为探索和优化X型分子筛对H2S的吸附性能提供了更多选择.同时,分子筛纳米晶的堆积会形成大量晶间介孔,形成类多级孔结构,也有助于吸附性能的提升.此外,利用金属对分子筛进行改性,增加分子筛活性中心数量也是提高硫容的有效手段.Kumar等[24]利用Ag和Cu对X型分子筛进行离子交换改性,发现改性后的分子筛硫容极大提高.但此类研究存在离子交换程度低、所用Ag离子为贵金属和经济效益低等缺点.与之相比,纳米分子筛具有更多暴露的活性位点,可提高离子交换率,从而进一步提高硫容.综上所述,纳米分子筛不仅具有扩散限制低等本征吸附性能优势,还具有更大的金属改性潜力,可以大幅度提高整体硫容.
本文从分子筛材料本征性质出发,对分子筛的吸附脱硫性能进行了考察和优化:通过对比小孔SOD型分子筛和大孔X型纳米分子筛,探究了多孔材料内外表面对吸附脱硫的贡献;通过对比3种不同尺寸X型分子筛的穿透硫容,探究了X型分子筛尺寸对脱硫性能的影响,并筛选出最佳的吸附工艺条件;通过对比Cu、Ni、Fe等改性金属对分子筛脱硫性能的影响,筛选出最优的改性金属.
1 实验部分
1.1 试剂与仪器
氢氧化钠、硅酸钠、偏铝酸钠、三水合硝酸铜、六水合硝酸镍和九水合硝酸铁(Ⅲ)购自国药集团化学试剂有限公司;铝粉(325目,纯度99.5%)购自Alfa Aesar公司;硅溶胶(Ludox-HS 30%SiO2)购自Sigma-Aldrich公司;NaX分子筛(1μm,命名为NaX-1)购自青岛惠城环保科技股份有限公司;硫化氢标气[286 mg/m3(200 ppm),平衡气为N2气]购自青岛天源气体制造有限公司.
Bruker D8 Advance型X射线衍射仪(XRD,德国布鲁克公司),CuKα射线(λ=0.154056 nm),扫描范围3°~80°,工作电压40 kV,工作电流200 mA;JSM-7900F型扫描电子显微镜(SEM,日本JEOL公司),配备Oxford Instruments X-MaxN型能谱仪(EDS,牛津仪器科技有限公司);ASAP 2020 Micro⁃meritics型比表面积及孔隙分析仪(美国麦克仪器公司);NEXUS FT-IR型傅里叶变换红外光谱仪(美国赛默飞世尔科技公司).
1.2 实验过程
1.2.1 纯分子筛的制备 纳米NaX和SOD型分子筛参照Mintova等[25]报道的方法制备.NaX分子筛的母液中各物质的组成为n(Na2O)∶n(Al2O3)∶n(SiO2)∶n(H2O)=9∶1.1∶10∶45,室温下老化24 h,于50℃晶化48 h,命名为NaX-N.SOD型分子筛的母液组成为n(Na2O)∶n(Al2O3)∶n(SiO2)∶n(H2O)=3.5∶1∶2.2∶11.1,室温下老化24 h,于50℃下晶化48 h.大尺寸NaX分子筛参照Lsmna等[26]报道的方法制备.按照n(Na2O)∶n(Al2O3)∶n(SiO2)∶n(H2O)=17∶1∶4.8∶975添加原料,并在90℃下晶化24 h,制备尺寸为3μm的NaX型分子筛,命名为NaX-3.
1.2.2 分子筛的金属改性 室温下,将质量分数为5%的NaX-N悬浮液与0.005 mol/L金属硝酸盐[Cu(NO3)2·3H2O,Fe(NO3)3·9H2O或Ni(NO3)2·6H2O]溶液离子交换1 h[27],然后离心洗涤3次至pH=7,分别得到Cu-NaX-N,Fe-NaX-N和Ni-NaX-N样品.
1.2.3 吸附脱硫性能评价 采用固定床反应器进行吸附剂的脱硫及再生性能评价,尾气处连接GC-456型色谱仪(PFPD检测器),实时检测反应管出口气体中硫化物的含量.吸附剂用量为1 mL.在考察吸附剂对H2S吸附-脱除性能的实验中,出口与入口硫化物浓度之比大于10%时视为穿透.由此计算吸附剂的一次穿透硫容(以下简称硫容),近似硫容(q,mg/g)计算公式如下式所示:

式中:c0和c(mg/m3)分别为进出口气体中硫化物的浓度;Q(m3/min)为气体流量;t(min)为吸附时间;m(g)为吸附剂的质量.
2 结果与讨论
2.1 吸附材料的表征
2.1.1 改性前分子筛的表征 图1为纯分子筛的XRD谱图.SOD,NaX-N,NaX-1和NaX-3样品均具有对应晶体的布拉格特征峰[25],且结晶度高.其中,NaX分子筛的XRD谱图具有明显的Bragg峰宽化现象,说明该沸石晶体的尺寸较小.

Fig.1 XRD patterns of SOD(a),NaX⁃N(b),NaX⁃1(c)and NaX⁃3(d)

Fig.2 SEM images of SOD(A),NaX⁃N(B),NaX⁃1(C)and NaX⁃3(D)
图2为分子筛晶体的SEM照片.可见,SOD分子筛的尺寸约为50 nm,NaX-3,NaX-1和NaX-N分子筛的粒径分别为3μm,1μm和20 nm.NaX-1和NaX-3微米级分子筛可观察到明显的正八面体形貌,而纳米尺寸的NaX-N和SOD分子筛由于粒径小,仅呈现球形.SOD分子筛和不同尺寸NaX分子筛的低温(−196°C)氮气吸附-脱附等温线如图3所示.NaX分子筛的吸附-脱附等温线均为典型的Ⅰ型等温线,在低分压阶段具有高的氮气吸附量,这是微孔材料的典型特征.SOD和NaX-N分子筛在p/p0˃0.8阶段表现出高的氮气吸附量,这归因于纳米分子筛高度堆积形成的晶间介孔.由表1可见,NaX-N分子筛具有更大的外比表面积,从而具有更多暴露的活性位点.
2.1.2 改性后纳米分子筛的表征 从图4中的XRD
图谱可见,经离子交换后的NaX-N分子筛的衍射峰强度均有所减弱,但仍具有FAU型晶体的特征峰,说明离子交换对晶体结构具有一定影响,但是分子筛的整体骨架结构并未受到较大破坏.

Fig.3 N2 adsorption⁃desorption isotherms of SOD,NaX⁃N,NaX⁃1 and NaX⁃3

Table 1 Surface characteristics constants of NaX zeolites,SOD zeolites and ion-exchanged zeolites

Fig.4 XRD patterns of NaX⁃N(a),Cu⁃NaX⁃N(b),Ni⁃NaX⁃N(c)and Fe⁃NaX⁃N(d)
Fig.5 FTIR spectra of NaX⁃N and ion⁃exchanged samples
NaX-N及其离子交换样品的红外光图谱如图5所示,所有样品均可观察到相似的特征峰,分别是位于420~500,550,650~720和950~1250 cm−1处的T—O弯曲振动峰、双六元环(D6R)振动峰、T—O—T对称伸缩振动峰和非对称伸缩振动峰[28].在所有样品的红外光谱中,1630 cm−1处的峰可归属于沸石样品的不完全脱水引起的O—H键的振动.
通过EDS表征了3种改性分子筛中金属离子的含量(表2),发现Cu,Ni和Fe的含量分别为4.58%,6.73%和15.49%.Fe-NaX-N表现出最大的离子交换度,表明Fe3+更易与分子筛进行离子交换[29].
改性前后NaX-N分子筛的氮气吸附-脱附曲线均为Ⅰ型等温线,而且都具有相当的晶间介孔结构(图6).如表1所示,由于较大尺寸的金属离子堵塞了部分微孔,因此改性后分子筛的比表面积和微孔的表面积均有一定程度的下降,但仍保持微孔加晶间介孔的结构.

Table 2 Elemental analysis data of NaX-N and ion-exchanged zeolites determined by EDS
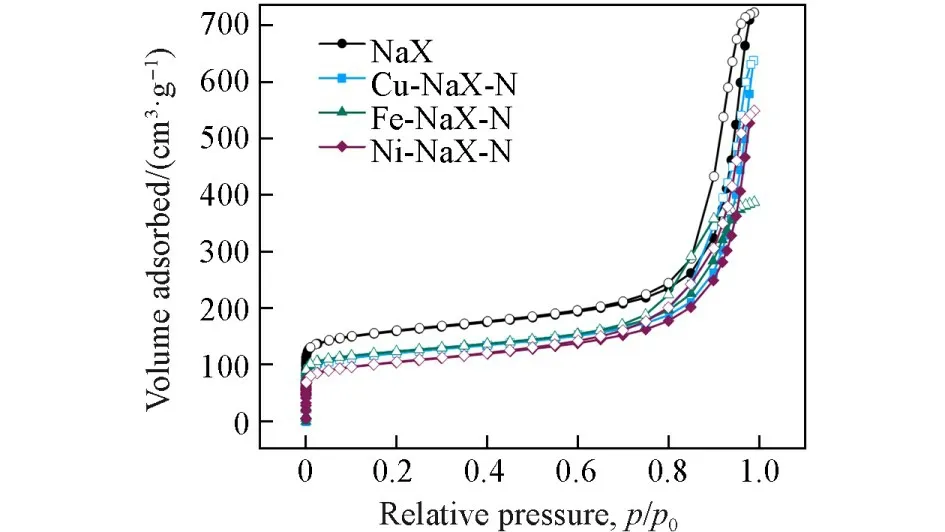
Fig.6 N2 adsorption⁃desorption isotherms of NaX⁃N,Cu⁃NaX⁃N,Ni⁃NaX⁃N and Fe⁃NaX⁃N
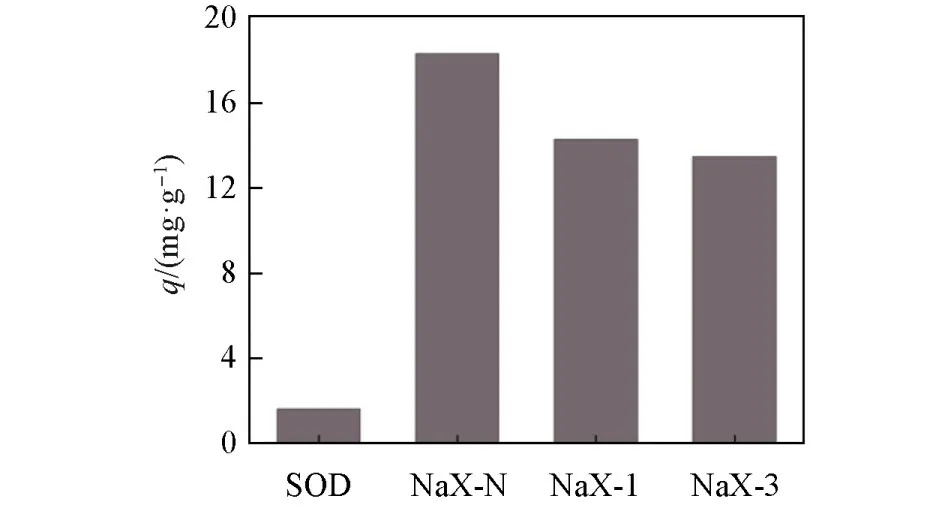
Fig.7 Breakthrough adsorption capacity of SOD,NaX⁃N,NaX⁃1 and NaX⁃3
2.2 分子筛性质对H 2S吸附性能的影响
考察了SOD分子筛和不同尺寸NaX分子筛的吸附脱硫效果,结果如图7和表3所示.可见,SOD的穿透硫容最小,仅为1.61 mg/g.这是由于SOD分子筛的孔径为0.29 nm,而H2S分子的动力学直径为0.34 nm,SOD对于H2S的吸附仅存在于外表面,H2S无法进入孔道内,这也证明了分子筛内部丰富的孔道结构主要贡献于H2S的吸附.通过对比不同尺寸NaX分子筛的硫容可知,晶体尺寸越小,硫容越高,吸附能力越强,NaX-N对H2S的吸附硫容为18.30 mg/g,明显高于微米尺寸的NaX-1和NaX-3分子筛.由于NaX-N具有复杂的微孔和晶间介孔结构、更大的外比表面积和更多可及的活性位点,而且孔道短,更容易克服扩散阻力,因而吸附的H2S气体更多.

Table 3 Breakthrough times and adsorption capacities of all samples
2.3 吸附条件对脱硫效果的影响
考察了吸附温度和空速对于NaX-N分子筛吸附脱硫效果的影响.由图8(A)和表3可知,随着温度的升高,NaX-N的吸附效果下降.当温度从30℃升至110℃后,NaX-N的硫容由18.30 mg/g下降到14.27 mg/g,降低了22%,表明温度升高不利于H2S在NaX-N上的吸附.这是因为分子筛对H2S的吸附主要是物理吸附,是一个放热过程,因此温度升高不利于吸附.
在固定床的吸附装置中,不同的体积流量会改变吸附气与分子筛层的接触时间,从而影响硫化氢的去除效率.如图8(B)和表3所示,随着空速的增加,NaX-N的吸附穿透时间逐渐缩短.当空速由1800 h−1增加到6000 h−1时,穿透硫容由18.24 mg/g降至16.18 mg/g.但NaX-N的穿透硫容的减少和空速的增加趋势并不一致.在1800~3000 h−1空速范围内,NaX-N分子筛与H2S分子具有适宜的接触时间,所以硫容受空速的影响不大.但当空速由3000 h−1增至6000 h−1时,穿透硫容减少了约2.2 mg/g,表明在较大空速下,H2S与吸附剂活性中心相互作用时间较短,不利于二者间的相互作用.由此筛选出最优空速为3000 h−1,此时吸附剂在不损失硫容的情况下穿透时间最短,可减少吸附时间,降低成本.
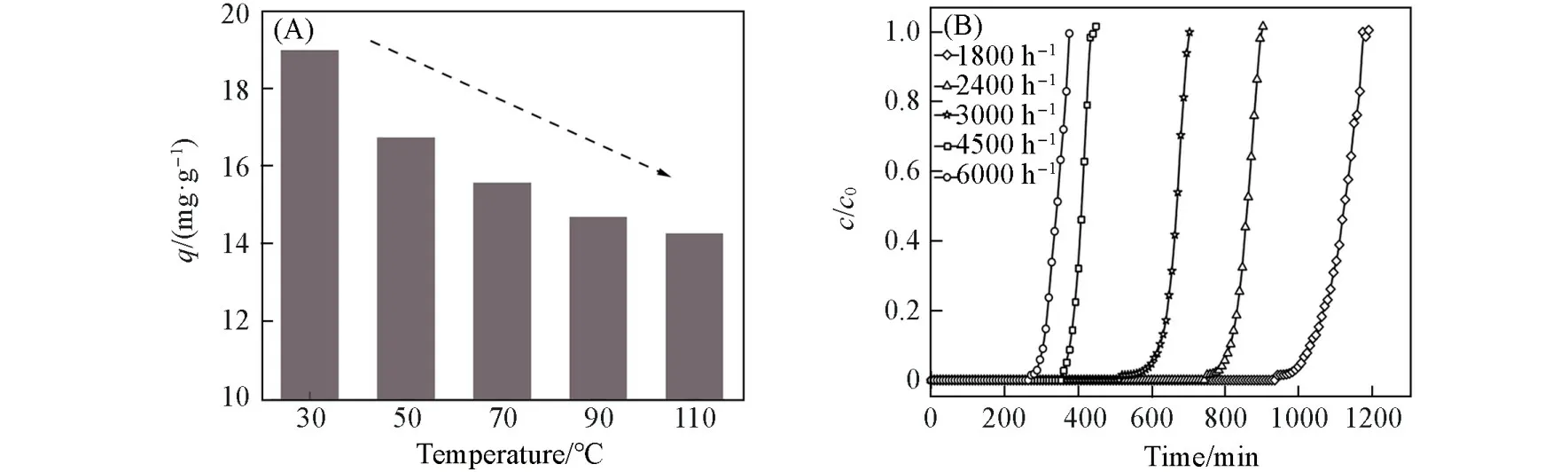
Fig.8 Effect of temperature(A)and space velocity(B)on adsorption of H 2S on NaX⁃N
2.4 改性对NaX-N分子筛吸附H 2S性能的影响
考察了NaX-N分子筛改性前后吸附硫化氢的性能(图9).Cu-NaX-N具有最长的穿透时间(706 min),高于未改性的NaX-N分子筛的穿透时间(622 min),并且其穿透硫容(20.61 mg/g)也高于NaX-N(18.3 mg/g).根据孔结构分析结果,Cu-NaX-N的比表面积和微孔面积均比NaX-N低,其更高的硫容可归因于Cu与H2S通过S—M键的相互作用或π络合的化学相互作用.Ni-NaX-N与Cu-NaX-N的交换量和外比表面积相似,但Ni-NaX-N的硫容仅为11.78 mg/g,可能是因为Ni离子与S2−的作用较弱,由于孔道堵塞,H2S更难进入具有大量活性位的孔道内,导致Ni-Na-X的吸附量较改性前更低.虽然部分孔道堵塞,但由于S—M键的强相互作用,物理吸附占比变低,Cu离子和S2−之间的化学作用贡献更大的硫容量[28].Fe改性的NaX-N分子筛则有最短的穿透时间(246 min)和更小的硫容(5.82 mg/g).虽然Fe的离子交换程度最高,但更高的交换量带来更多的孔道堵塞,使H2S难以进入孔道内与Fe离子活性位接触,硫容降低严重.
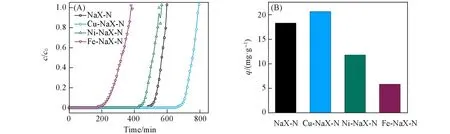
Fig.9 Breakthrough cuves(A)and breakthrough adsorption capacity(B)of NaX⁃N and ion⁃exchanged zeolites
2.5 分子筛的再生性能
考察了NaX-N和Cu-NaX-N分子筛吸附硫化氢后,在氮气、空气氛围(吹扫空速均为3000 h−1)和在350℃下的脱附效果,结果如图10所示.NaX-N和Cu-NaX-N在使用氮气吹扫床层热脱附时的效果较差,其在常压、30℃下的再生穿透硫容分别为3.7和2.5 mg/g,分别为新鲜吸附剂的20%和12.1%.但当使用热空气吹扫床层时,NaX-N和Cu-NaX-N的再生穿透硫容能分别达到11.4和16.2 mg/g,分别为新鲜吸附剂的62.4%和78.5%.原因为对于NaX-N分子筛,其吸附机理可能遵循Sigot[30]提出的保留机理,形成的硫聚合物阻止了吸附剂的热再生,而热空气中的氧气在高温下可以氧化部分S单质,从而被带离吸附位.对于Cu-NaX-N,H2S与Cu2+之间形成较强的Cu—S键,热再生难以将吸附的H2S从活性位上脱附.但在热空气氛围下,空气中的氧可以使被吸附的H2S发生氧化反应,形成SOx分子,从而断开Cu—S键,恢复被占据吸附位的活性.
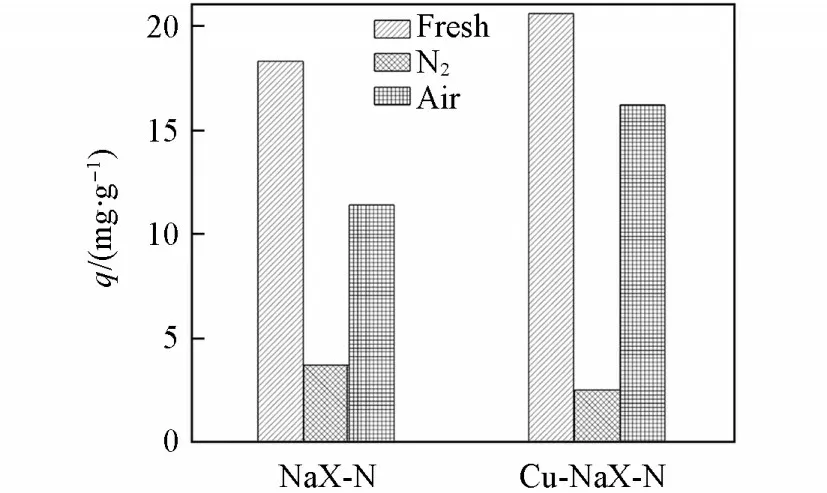
Fig.10 Breakthrough adsorption capacities of NaX⁃N and Cu⁃NaX⁃N for H 2S adsorp⁃tion at different desorption atmospheres
3 结 论
采用无模板水热法合成高结晶度的纳米尺寸的SOD、NaX-N和微米Na-X分子筛,通过对比分子筛吸附硫化氢的性能发现,小孔SOD分子筛由于孔道狭窄,H2S难以进入孔道内与活性位接触,外比表面吸附量低,证实分子筛对于硫化氢的吸附主要集中于孔道内和可及的活性位.相对于微米级NaX(1μm和3μm),纳米NaX具有丰富的微孔和晶间介孔结构、更大的外比表面积和更多可及的活性位,因而具有更高的硫容,体现出纳米分子筛在吸附领域的极大优势.分子筛吸附硫容随温度和空速的升高而显著下降,筛选出最优吸附工艺条件为30℃,空速为3000 h−1.利用离子交换法制备了不同金属改性的Cu-NaX-N、Ni-NaX-N和Fe-NaX-N分子筛,Cu-NaX-N由于更强的S—M键作用和更适宜的离子交换量,具有最高的硫容.用热氮气和热空气吹扫吸附硫化氢后的NaX-N和Cu-NaX-N分子筛,发现热空气中的氧化-脱附再生效果优于氮气中的再生.

