基于心血管保护作用的三七粉质量标志物研究*
李 新,徐 旭,许 浚,林 娟,李晓霞,王德勤,张铁军**,郭海彪**
(1.天津药物研究院/天津市中药质量标志物重点实验室 天津 300301;2.天津药物研究院/中药现代制剂与质量控制技术国家地方联合工程实验室 天津 300301;3.广州白云山和记黄埔中药有限公司 广州 510515;4.华北理工大学研究生院 唐山 063200)
中药质量一直是中药临床需求和产业发展的重要问题。中药区别于化学药的特点主要体现在中药是一个复杂体系,一种中药往往含有结构、性质不尽相同的多种成分,不同性质的成分数量多、结构差异大,而化学药一般由单体或几个化合物组成;由于中药成分复杂,常通过多途径、多成分、多靶点、多层次发挥整体疗效作用,而化学药作用于人体特异性靶点,具有较高的选择性和专一性[1]。由于中药质量缺少系统的理论指导,长期以来,聚焦到中药质量本质和内涵的研究,还处于碎片化状态,是制约中药质量研究的关键瓶颈问题[2]。为解决这一问题,2016 年刘昌孝院士针对中药生物属性、制造过程及配伍理论等自身医药体系的特点,整合多学科知识,提出了中药质量标志物(quality marker,Q-Marker)这一核心质量概念。该概念关联安全性和有效性,着眼于全过程的物质基础特有、差异、动态变化和质量的传递性、溯源性,并且具有整体、多元质控的特点[3]。
中药三七是五加科植物三七Panaxnotoginseng(Burk.) F.H.Chen 的干燥根和根茎,主要产地云南、广西等地区,性温,味甘、微苦,归肝、胃经,功效为散瘀止血、消肿定痛,主要用于治疗外伤出血、胸腹刺痛、跌扑肿痛等[4]。《本草纲目》称三七为“止血之神药、理血之妙品”,三七活血作用广泛用于心脑血管疾病的防治,含三七成分的中药制剂,如血塞通注射液、三七总皂苷片等,已经成为目前中药制剂中年销售额最大的品种之一[5]。通过对130 例急性脑梗死患者的治疗观察,发现以血塞通注射液+阿托伐他汀联合治疗,对患者心电异常发生率,血液流变学具有显著降低作用[6]。通过对慢性心力衰竭大鼠模型的研究,发现三七总皂苷可通过调节慢性心力衰竭大鼠心脏功能指标,改善心室收缩肌舒张功能,并降低利钠肽及血管紧张素Ⅱ水平,有效防止心肌重构[7]。2020 年药典记载三七含量测定以人参皂苷Rg1、人参皂苷Rb1和三七皂苷R1为指标[8]。有文献报道同等剂量三七超微粉的生物利用度优于三七常规粗粉。三七超微粉中主要成分,如人参皂苷Rb1、三七皂苷R1和人参皂苷Rg1的含量均高于三七细粉中的成分,两者间的含量有显著性差异[9]。另外,有研究发现三七中的其他成分也具有心血管保护作用,如人参皂苷Rg3通过调节SIRT1/NFκB 通路抑制NLRP3 炎性小体和氧化应激,从而减轻血管紧张素II诱导的心肌肥厚[10];人参皂苷Rg2通过调节TGF-β1/Smad 信号通路减轻心肌纤维化[11]。由此可见,2020 年药典记载的三七成分人参皂苷Rg1、人参皂苷Rb1和三七皂苷R1,并不能完全代表三七心血管保护的物质基础,而其他相关研究也比较分散,且多集中在个别皂苷类成分研究,甚至有些研究将一些心血管疾病的病因研究,如凝血机制、血脂异常等,与三七粉直接保护心血管的作用相混淆。目前尚未有针对三七粉保护心血管作用物质基础的系统研究报道。本研究在前期网络药理和入血成分研究基础上,采用直接干预心肌细胞、内皮细胞的实验方法,以三七粉中代表成分(包括皂苷类、黄酮类、三七素等)为研究对象,探索三七粉基于心血管保护作用的物质基础,明确质量标志物。
1 实验材料
三七粉由广州白云山和记黄埔中药有限公司负责收集,来源于五加科人参属植物三七Panaxnotoginseng(Burk.)F.H.Chen。三七总皂苷:天津药物研究院制备。三七粉主要成分:人参皂苷Rh1(批号:R26N9F75983)、人参皂苷Re(批号:B04D9S7649 9)、槲皮素(批号:C09S8Y43412)、人参皂苷F2(批号:Z10A9X58128)、人参皂苷Rg1(批号:G16S10Y97436)、人参皂苷Rg3(批号:Z14J10X90607)、人参皂苷Rd(批号Z09A9X67397)、人参皂苷Rb2(批号:P15O10F9498 3)、人参皂苷Rb1(批号:P19S10U98130)、人参皂苷Rb3(批 号:P05M10F87444)、人 参 皂 苷Rk1(批 号:B27J8S39859)、三七皂苷R1(批号:G22D9Y77958)、人参皂苷Rg2(批号:M07N10S102243)、三七素(批号:R05N10F102244)14 种实验样品,均购自上海源叶生物科技有限公司。三七总皂苷和三七素以PBS 配制成储备液,其他单体成分以DMSO配制成储备液。
试剂盒:BCA 蛋白浓度测定试剂盒(批号:010719190624)、SOD 试剂盒(批号:060619190723)、MDA 试剂盒(批号:030819190522),碧云天公司产品;LDH 试剂盒,南京建成公司产品(批号:20191109);ACP试剂盒(批号:FJ2XQKQU6Z):武汉伊莱瑞特生物科技股份有限公司产品。
试剂:CoCl2·6H2O(批号:SLBZ4786),sigma 公司产品;MTT(批号:123A0510),索莱宝公司产品;H2O2(批号:20181205)国药集团化学试剂有限公司产品。
仪器:酶标仪,Thermo Fisher Scientific 公司;倒置显微镜,Leica 公司;低温高速离心机;Thermo 公司;生物安全柜:济南鑫贝西生物技术有限公司。
细胞:大鼠心肌细胞(H9C2)、人脐静脉内皮细胞(HUVEC),购自于赛百慷(上海)细胞库。
2 实验方法
2.1 对心肌细胞的影响
大鼠H9C2 心肌细胞经复苏、传代,取对数生长期的H9C2 细胞接种于96 孔板培养,分别给予三七总皂苷(终浓度为3.125、6.25、12.5、25、50、100、200 mg·L-1)及人参皂苷Rb1、三七皂苷R1、人参皂苷Rb2、人参皂苷Rg1、人参皂苷Rb3、人参皂苷Rg2、人参皂苷Rg3、人参皂苷Re、人参皂苷Rd、槲皮素、人参皂苷F2、人参皂苷Rk1、人参皂苷Rh1、三七素实验样品(每种实验样品设5 个终浓度0.1、1、10、100、200μM),MTT 法测定实验药物对正常心肌H9C2 细胞的作用。计算细胞存活率公式如下:细胞存活率(%)=(实验组OD 值-校正组OD值)÷(对照组OD值-校正组OD值)×100%。
采用CoCl2制备心肌细胞(H9C2)损伤模型。取对数生长期的H9C2 细胞接种于96 孔板,每孔接种100 μL,在37℃、5% CO2条件下培养24 h。根据上述正常H9C2 心肌细胞实验结果,按空白组和给药组给予空白培养液或不同浓度的三七总皂苷/三七单体实验样品溶液各50 μL(共150 μL/孔)继续培养24 h。处理结束后,加入终浓度为500 μM 的CoCl2溶液或空白培养液50 μL 至上述96孔板中(共200 μL/孔),在37℃、5%CO2条件下培养24 h。培养结束后每孔避光加入终浓度为0.5 mg·mL-1的MTT 20 μL,在培养箱中孵育4 h。孵育结束取走上清液后,每孔加入150 μL DMSO,震荡10 min至蓝紫色结晶完全溶解后,酶标仪490 nm 处测定OD值。每组设6个复孔,实验平行重复三次。上清液按照试剂盒要求检测LDH,实验平行重复三次。心肌细胞用预冷PBS 洗2 遍后,每孔加入裂解液60 μL,冰上裂解10min 后,刮下细胞,以12000r 低温离心10 min,取上清进行蛋白定量。随后按照试剂盒要求测定MDA含量和SOD活性,实验平行重复三次。
2.2 对血管内皮细胞的影响
人脐静脉内皮细胞(HUVEC)经复苏、传代,取对数生长期的HUVEC 细胞接种于96 孔板培养,分别给予三七总皂苷(终浓度3.125、6.25、12.5、25、50、100、200、400、800 mg·L-1),以及人参皂苷Rb1、三七皂苷R1、人参皂苷Rb2、人参皂苷Rg1、人参皂苷Rb3、人参皂苷Rg2、人参皂苷Re、人参皂苷Rg3、人参皂苷Rd、槲皮素、人参皂苷F2、人参皂苷Rk1、人参皂苷Rh1、三七素实验样品,(每种实验样品设5 个终浓度0.1、1、10、100、200 μM),MTT 法检测实验药物对HUVEC 细胞存活率的作用。
选取对数生长期的HUVEC细胞,接种于96孔板,密度为6×104cells/mL,每孔中接种100 μL,在37℃、5%CO2条件下培养24h。根据上述正常人脐静脉内皮细胞(HUVEC)实验结果,加入不同浓度的三七总皂苷/三七单体成分50 μL,孵育24h。然后按空白组和造模组分别给予400 μM H2O2溶液或空白培养液各50 μL(共200 μL/孔)继续培养2h。药物处理结束后,每孔避光加入终浓度为0.5 mg·mL-1的MTT 20 μL,在培养箱中孵育4h。孵育结束后,取走上清液,每孔加入150 μL DMSO,震荡10 min 至蓝紫色结晶完全溶解后于酶标仪490 nm 处测定OD 值。每组设3 个复孔,实验平行重复三次。上清液按照试剂盒说明书检测LDH、ACP,实验平行重复三次。
3 实验结果
3.1 对心肌细胞的影响
3.1.1 对正常心肌细胞的影响
三七总皂苷的浓度在3.125-100 mg·L-1时对H9C2 细胞存活率无影响(P>0.05);其浓度在200-400 mg·L-1时表现出轻微的细胞增殖作用(P>0.05),浓度为800 mg·L-1时表现出显著的细胞毒性(P<0.01),因此小于等于400 mg·L-1是三七总皂苷的安全剂量。
单体成分中人参皂苷Rb3、人参皂苷Rb1、人参皂苷Rg2、人参皂苷Rd、人参皂苷Rg3和人参皂苷Rh1具有促进心肌细胞增殖作用。部分成分超过10μM,出现毒性反应,因此各单体成分在0.1-10 μM 范围内均为安全剂量,可进行效应比较。结果详见图1。

图1 三七总皂苷和各单体对H9C2细胞存活率的影响。(A)三七总皂苷对H9C2细胞存活率的影响;(B-C)三七皂苷R1、人参皂苷Rb1、槲皮素、人参皂苷F2等单体对H9C2细胞存活率的影响。
3.4.2 对心肌损伤细胞存活率的影响
选择对H9C2 细胞存活率无毒性影响的三七总皂苷浓度在3.125-200 mg·L-1,观察对CoCl2诱导的心肌细胞(H9C2)损伤模型的影响。实验结果表明,三七总皂苷3.125-50 mg·L-1浓度时,与CoCl2组比较,未见显著差异(P>0.05);100、200 mg·L-1时,可显著增加细胞存活率(P<0.05,P<0.01)。
选择对H9C2 细胞存活率无毒性影响的三七单体成分浓度在在0.1-10 μM,观察对CoCl2诱导的心肌细胞(H9C2)损伤模型的影响。实验结果表明,与CoCl2组比较,三七单体成分人参皂苷Rb3、人参皂苷Rb2、人参皂苷Rg1、人参皂苷Re、人参皂苷Rg3、人参皂苷Rd、槲皮素、人参皂苷F2、人参皂苷Rk1、人参皂苷Rh1、三七素能够显著增加H9C2 细胞存活率(P<0.05,P<0.01)。结果详见图2。

图2 三七总皂苷和各单体对CoCl2诱导H9C2细胞存活率的影响。(A)三七总皂苷对CoCl2诱导H9C2细胞存活率的影响;(B-C)三七皂苷R1、人参皂苷Rb1、槲皮素、人参皂苷F2等单体对CoCl2诱导H9C2细胞存活率的影响。
3.4.3 对心肌损伤细胞LDH的影响
三七总皂苷100 mg·L-1、200 mg·L-1预处理组LDH检测结果分别为104.07±45.06,116.64±27.31,与CoCl2细胞损伤模型组检测结果152.78±6.92比较,具有显著差异,能够减少LDH 活性(P<0.01)。单体成分人参皂苷Rb2、人参皂苷Rb3、人参皂苷Rg2、人参皂苷Rg3、人参皂苷Re、人参皂苷Rd、人参皂苷F2、人参皂苷Rk1和人参皂苷Rh1能够显著降低H9C2 细胞上清中LDH 活性(P<0.05,P<0.01)。结果详见图3。

图3 各单体化合物对CoCl2诱导的H9C2细胞上清LDH含量的影响。(A)三七皂苷R1、人参皂苷Rb1、人参皂苷Rb2等5个单体化合物对CoCl2诱导的H9C2细胞上清LDH含量的影响;(B)人参皂苷Rg1、人参皂苷Rg3、人参皂苷Re等4个单体化合物对CoCl2诱导的H9C2细胞上清LDH含量的影响;(C)三七总皂苷及槲皮素、人参皂苷F2等5个单体成分对CoCl2诱导的H9C2细胞上清LDH含量的影响。
3.4.4 对心肌损伤细胞SOD、MDA的影响
三七总皂苷100 mg·L-1、200 mg·L-1预处理组SOD检测结果分别为0.91±0.07,0.74±0.03,与CoCl2细胞损伤模型组检测结果0.65±0.03 比较,具有显著差异,能够提高SOD 活性(P<0.05,P<0.01)。单体成分人参皂苷Rb3、人参皂苷Rg2、人参皂苷Rg3、人参皂苷Rd、槲皮素和三七素能够显著增加H9C2 细胞SOD 活性(P<0.05,P<0.01)。结果详见图4。
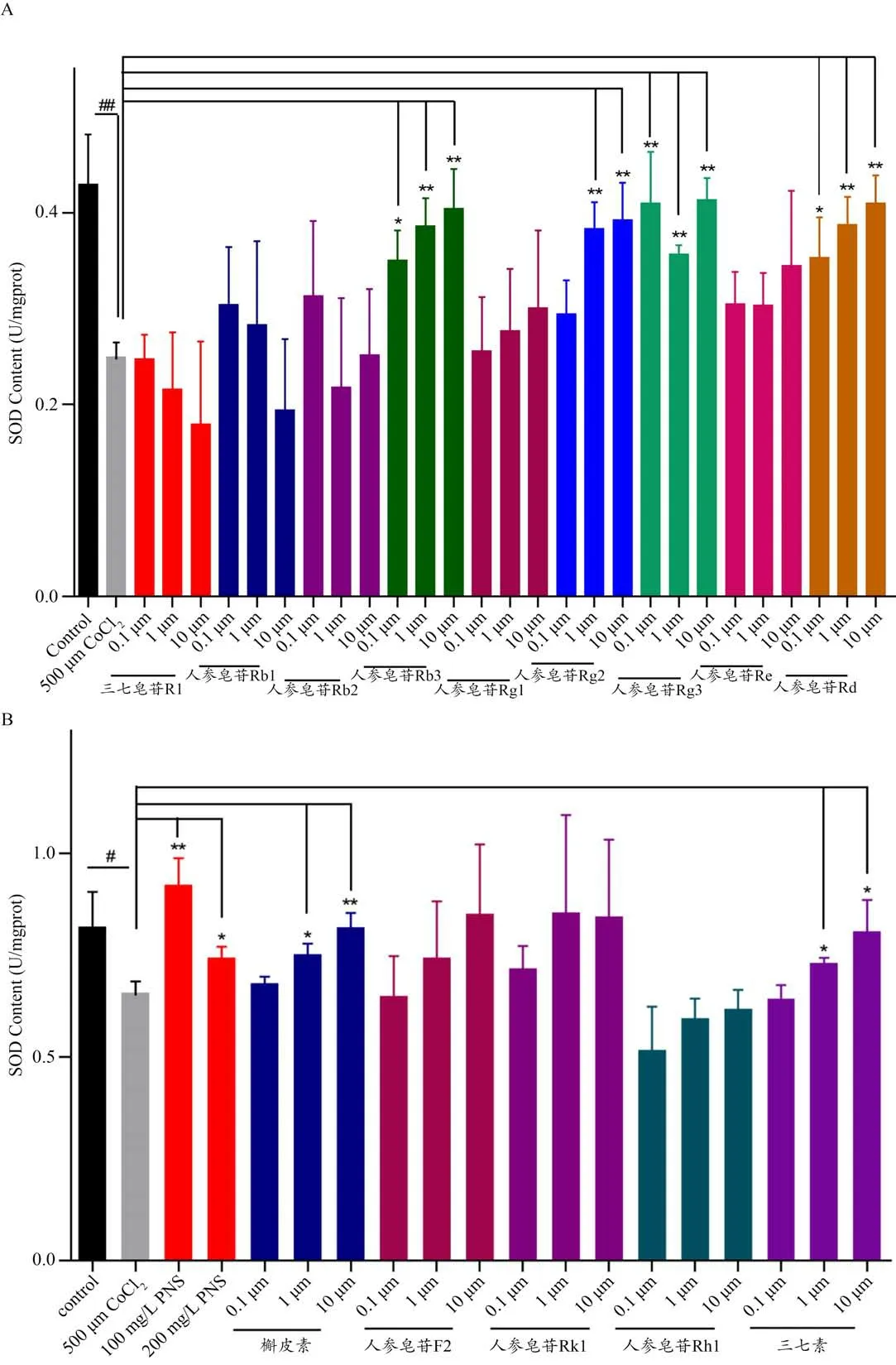
图4 各单体化合物对CoCl2诱导的H9C2细胞SOD含量的影响。(A)三七皂苷R1、人参皂苷Rb1、人参皂苷Rb2等9个单体化合物对CoCl2诱导的H9C2细胞SOD含量的影响;(B)三七总皂苷及槲皮素、人参皂苷F2等5个单体成分对CoCl2诱导的H9C2细胞SOD含量的影响。
三七总皂苷100mg·L-1、200mg·L-1预处理组MDA检测结果分别为14.62±2.01,11.19±0.38,与CoCl2细胞损伤模型组检测结果44.65±2.21比较,具有显著差异,能够减少MDA含量(P<0.01)。
单体成分人参皂苷Rb1、三七皂苷R1、人参皂苷Rb2、人参皂苷Rg1、人参皂苷Rb3、人参皂苷Rg3、人参皂苷Re、人参皂苷Rd、槲皮素、人参皂苷F2、人参皂苷Rk1、人参皂苷Rh1和三七素能够显著降低H9C2 细胞上清液MDA含量(P<0.05,P<0.01)。结果详见图5。

图5 各单体化合物对CoCl2诱导的H9C2细胞MDA含量的影响。(A)三七皂苷R1、人参皂苷Rb1、人参皂苷Rb2等9个单体化合物对CoCl2诱导的H9C2细胞MDA含量的影响;(B)三七总皂苷及槲皮素、人参皂苷F2等5个单体成分对CoCl2诱导的H9C2细胞MDA含量的影响。
3.5 对血管内皮细胞的影响
3.5.1 对正常内皮细胞的影响
三七总皂苷的浓度在3.125 mg·L-1时,对HUVEC细胞存活率无显著影响(P>0.05);其浓度在6.25-100 mg·L-1时其细胞存活率虽有统计学差异(P<0.05,P<0.01),但细胞并未受到明显损伤;其浓度在200 mg·L-1时细胞存活率与空白对照组无显著性差异(P>0.05);其浓度为400-800 mg·L-1时表现出显著的细胞毒性(P<0.01),因此小于等于200 mg·L-1是三七总皂苷的安全剂量。
与溶剂对照组比较,三七皂苷R1在1 μM 剂量下有促进内皮细胞增殖作用(P<0.05);人参皂苷Rb3在0.1-1 μM 剂量下有促进内皮细胞增殖作用(P<0.05)。各单体成分除人参皂苷F2外在0.1-10 μM 范围内均为安全剂量,可进行效应比较。结果详见图6。

图6 三七总皂苷和各单体对HUVEC细胞存活率的影响。(A)三七总皂苷对HUVEC细胞存活率的影响;(B-C)三七皂苷R1、人参皂苷Rb1、槲皮素、人参皂苷F2等单体对HUVEC细胞存活率的影响。
3.5.2 对内皮损伤细胞存活率的影响
选择对正常内皮细胞无毒性作用的三七总皂苷浓度3.125-200mg·L-1,观察对H2O2诱导的内皮细胞(HUVEC)损伤模型的影响。实验结果表明,三七总皂苷3.125-100mg·L-1与H2O2组比较,对H2O2诱导的心肌细胞损伤并未见显著性差异(P>0.05),三七总皂苷200 mg·L-1可显著增加细胞存活率(P<0.01)。
选择对正常内皮细胞无毒性作用的三七单体成分浓度0.1-10 μM,观察对H2O2诱导的内皮细胞(HUVEC)损伤模型的影响。实验结果表明,三七单体成分三七皂苷R1、人参皂苷Rb2、人参皂苷Rb3、槲皮素、人参皂苷F2、人参皂苷Rk1、人参皂苷Rh1、三七素可显著提高HUVEC细胞存活率(P<0.05,P<0.01)。结果详见图7。

图7 三七总皂苷和各单体对H2O2诱导HUVEC细胞存活率的影响。(A)三七总皂苷对H2O2诱导HUVEC细胞存活率的影响;(B-C)三七皂苷R1、人参皂苷Rb1、槲皮素、人参皂苷F2等单体H2O2诱导对HUVEC细胞存活率的影响。
3.5.3 对内皮损伤细胞LDH的影响
三七总皂苷100 mg·L-1、200 mg·L-1预处理组LDH检测结果分别为138.49±13.69,172.48±23.53,与H2O2细胞损伤模型组检测结果175.13±17.28 比较,能够减少LDH活性(P<0.05,P>0.05)。
单体成分人参皂苷Rb1、人参皂苷Rb3、人参皂苷Rg2、人参皂苷Rg3、人参皂苷Re、人参皂苷Rd 和三七素均能不同程度降低细胞上清中LDH 活性(P<0.05,P<0.01)。结果详见图8。
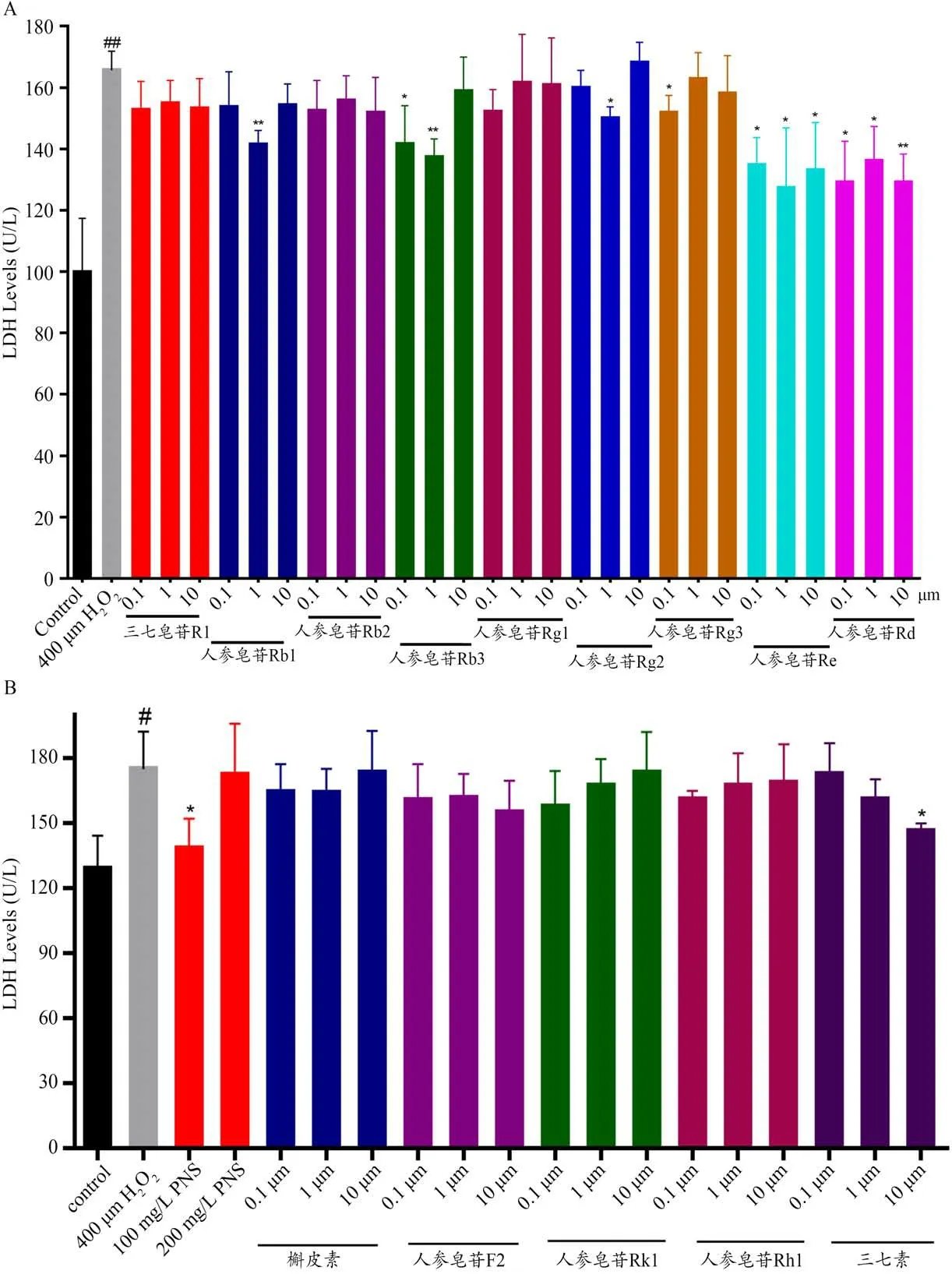
图8 各单体对H2O2诱导HUVEC细胞上清LDH活性的影响。(A)三七皂苷R1、人参皂苷Rb1、人参皂苷Rb2等9个单体化合物对H2O2诱导HUVEC细胞上清LDH活性的影响;(B)三七总皂苷及槲皮素、人参皂苷F2 等5个单体化合物对H2O2诱导HUVEC细胞上清LDH活性的影响。
3.5.4 对内皮损伤细胞ACP的影响
三七总皂苷100 mg·L-1、200 mg·L-1预处理组ACP检测结果分别为0.34±0.21,0.45±0.04,与H2O2细胞损伤模型组检测结果0.67±0.07比较,能够减少ACP活性(P<0.05)。
单体成分人参皂苷Rb1、三七皂苷R1、人参皂苷Rb2、人参皂苷Rg1、人参皂苷Rb3、人参皂苷Rg2、人参皂苷Re、人参皂苷Rg3、人参皂苷Rd、槲皮素、人参皂苷F2、人参皂苷Rh1和三七素均能不同程度降低细胞上清中ACP活性(P<0.05,P<0.01)。结果详见图9。
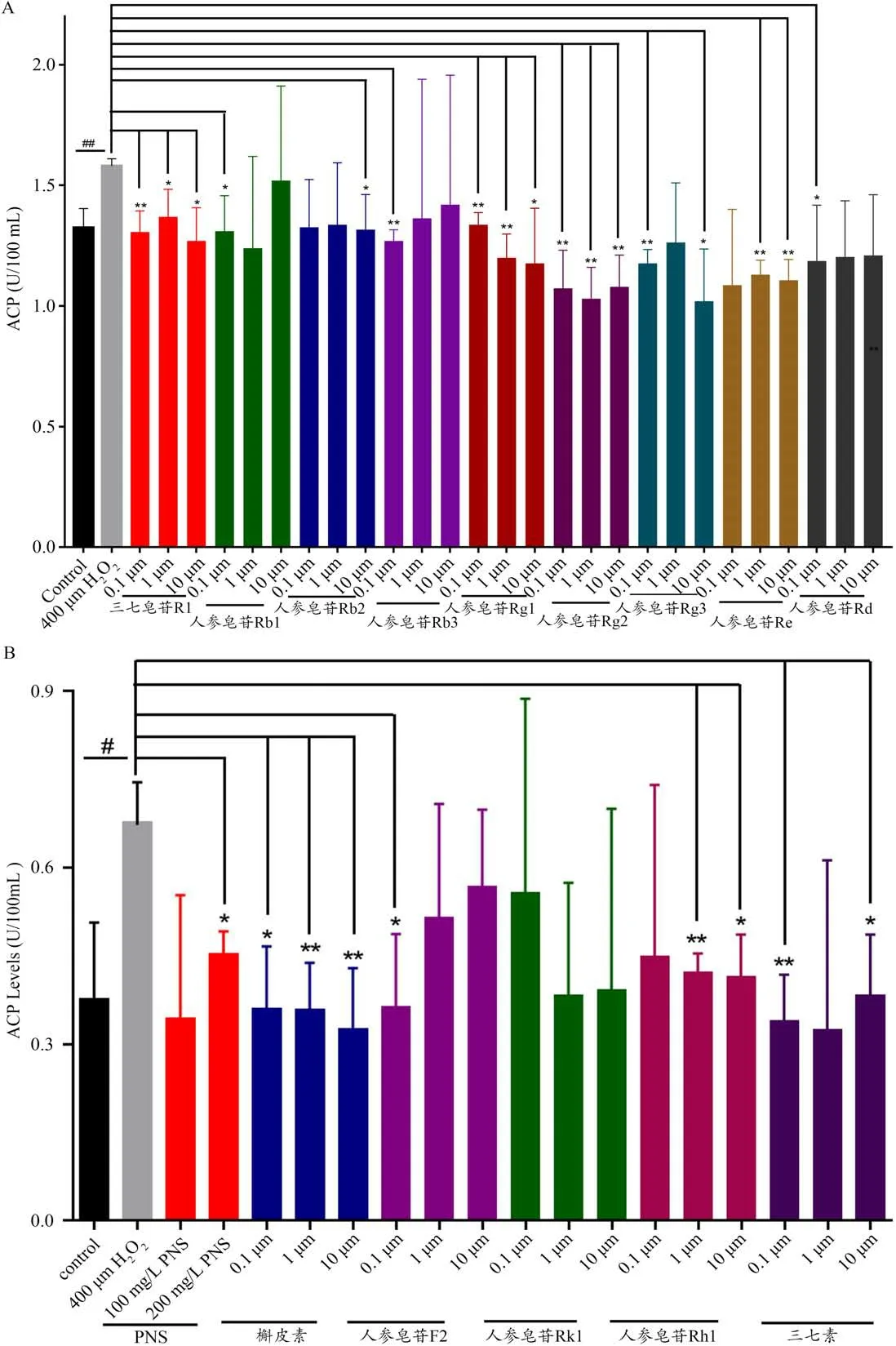
图9 各单体对H2O2诱导HUVEC细胞上清ACP含量的影响(A)三七皂苷R1、人参皂苷Rb1、人参皂苷Rb2等9个单体化合物对H2O2诱导HUVEC细胞上清ACP含量的影响;(B)三七总皂苷及槲皮素、人参皂苷F2 等5个单体化合物对H2O2诱导HUVEC细胞上清ACP含量的影响。
4 小结
三七单体成分对心肌损伤细胞存活率、心肌细胞LDH、心肌细胞SOD、内皮损伤细胞存活率、内皮细胞LDH、内皮细胞ACP 等6 个指标的作用,汇总如下,详见表1。

表1 三七粉中单体成分心血管保护指标汇总
5 讨论
中药三七是五加科植物人参三七panaxnotoginseng(Burk)F.H.Chen 的干燥根,主产于云南、广西等地。三七活血作用广泛应用于心脑血管疾病的防治[12]。其主要作用机制包括,保护心肌,维持心肌正常泵血功能;保护血管内皮,预防动脉粥样硬化斑块形成等。三七化学成分类型多样,主要有皂苷类、黄酮类、多糖类、氨基酸类等。本实验结合血清移行成分结果和文献查证,选取了12个人参皂苷类成分(包括5 个人参三醇类成分和7 个人参二醇类成分),1个黄酮类成分和1 个氨基酸类成分,从中药心血管保护的多种机制方面研究三七的标志性成分。
5.1 保护心肌细胞
冠心病是冠状动脉粥样硬化导致血管腔阻塞,心肌缺血、缺氧而引起的心脏病。心脏对缺血缺氧极其敏感,缺血缺氧造成的心肌细胞损伤较难恢复,因此保护心肌对冠心病患者非常重要[13]。戴红红等将92例心源性脑栓塞患者分为对照组和观察组,对照组(n=46)给予常规治疗,中药治疗组(n=46)在对照组基础上给予黄芪三七汤治疗,结果显示经过治疗后,中药治疗组在生活质量评分方面显著高于对照组,具有统计学意义(P<0.05),在经过治疗7 天、14 天后,中药治疗组在NIHSS 评分、MMP-9 方面均显著比对照组低,具有统计学意义(P<0.05)。因此认为黄芪三七汤治疗心源性脑栓塞能够阻碍患者血浆中MMP-9 的高表达,临床效果较好[14]。
冷雪等采用异丙肾上腺素建立大鼠急性心肌缺血模型,腹腔注射给予人参皂苷Rg110、20 mg·kg-1,连续5天。结果发现,与模型组比较,人参皂苷Rg1组,心肌表面平均血流有显著提升,血清一氧化氮(NO)升高,肌酸激酶(CK)、乳酸脱氢酶(LDH)降低,心肌丙二醛(MDA)含量降低,谷胱甘肽过氧化物酶(GSH-Px)含量升高,内皮型一氧化氮合酶(eNOS)mRNA 表达含量升高,PI3K/Akt 通路蛋白的表达升高,认为人参皂苷Rg1可以通过调控PI3K-Akt-eNOS 信号通路改善急性心肌缺血大鼠心脏变化防治心血管病变[15]。吴惠珍等采用结扎冠状动脉左前支30 min 后再松解手术线的方法制备大鼠心肌缺血再灌注损伤模型,灌胃给予人参皂苷Rb310、20、30 mg·kg-1,连续2 天。结果发现,与模型组比较,人参皂苷Rb3组大鼠心肌梗死面积百分比降低,同工酶、丙二醛、乳酸脱氢酶、内皮舒张因子水平降低,谷胱甘肽过氧化酶、超氧化物歧化酶水平升高,认为人参皂苷Rb3对大鼠心肌缺血再灌注损伤有保护作用,其作用机制可能与抗细胞脂质过氧化、抗自由基、抗炎症反应及影响心肌酶参与体内能量代谢的过程有关[16]。
当机体缺血缺氧时,活性自由基会突然生成增多,超氧化物歧化酶(SOD)和谷胱甘肽过氧化酶(GSH-Px)、过氧化氢酶(CAT)和维生素等内源性物质的活性开始降低,由于难以承受负荷,生成的自由基如MDA,难以清除掉,使得细胞内的生物膜脂质、蛋白质、核酸受到损伤,并引起线粒体受损,因而造成心肌细胞损伤,释放LDH。本研究采用CoCl2诱导的H9C2心肌细胞损伤模型,研究结果发现人参皂苷Rb2、人参皂苷Rb3、人参皂苷Rg1、人参皂苷Rg3、人参皂苷Re、人参皂苷Rd、槲皮素、人参皂苷F2、人参皂苷Rk1、人参皂苷Rh1、三七素可以显著提高心肌细胞存活率,其机制可能与提高心肌细胞SOD活力,降低MDA含量有关。
5.2 保护血管内皮
血管内皮细胞损伤及功能改变是动脉粥样硬化的初始环节。内皮细胞损伤不仅可以促进血管局部血栓的形成,还可促进多种细胞因子的释放,如血管紧张素转换酶、内皮素、5-羟色胺、生长因子、细胞因子、黏附分子等,促进血管的收缩,吸引炎性细胞的趋化和黏附,动脉粥样斑块形成[17]。梁文华等选择109例气虚痰瘀阻络型不稳定型心绞痛(UA)患者,分为治疗组与对照组。对照组患者给予常规心内科监护及规范治疗,治疗组患者在对照组基础上给予自拟的芪蛭三七汤口服治疗。结果显示,对照组总有效率为73.58%(39/53),治疗组总有效率为95.92%(47/49),治疗组总有效率高于对照组(P<0.05),治疗后对照组和治疗组患者在中医证候评分、心绞痛的发作频率及硝酸甘油的用量、血液流变学指标、TXB2、ET-1 等方面均较治疗前显著降低,而且治疗组显著低于对照组(P<0.05);治疗后,对照组和治疗组患者在NO 水平方面显著升高,且治疗组高于对照组(P<0.05)[18]。
陈文明等采用球囊损伤法制备大鼠颈动脉损伤模型,术后次日灌胃人参皂苷Rg35、10 mg·kg-1,每日1次,连续14 天。结果发现,与模型组比较,人参皂苷Rg3组血管内膜增生明显减轻,内膜与中膜面积比明显下降,新生内膜区平滑肌细胞凋亡率明显增加,损伤血管Fas 基因表达水平明显升高,Bcl-2 基因表达水平明显降低,认为人参皂苷Rg3可能通过促进平滑肌细胞的凋亡,从而减轻球囊损伤后血管内膜的增生[19]。邓敏贞等采用四血管阻断法复制血管性痴呆(VD)模型,灌胃给予人参皂苷Rb310 mg·kg-1,每日2 次,连续30 天。结果与模型组比较,人参皂苷Rb3组小鼠的避暗潜伏期显著延长,错误次数均显著减少,4-羟基壬烯酸(4-HNE)、8-羟基脱氧鸟苷(8-OHdG)、活性氧(ROS)含量以及Bax mRNA、蛋白的表达水平均显著降低,Bcl-2 mRNA、蛋白的表达水平均显著升高(P<0.05 或P<0.01),认为人参皂苷Rb3对VD 模型小鼠学习记忆能力具有一定改善作用,其机制可能与抗氧化应激、抗海马组织凋亡有关[20]。
本研究采用了过氧化氢诱导HUVEC 细胞损伤2h内的急性氧化应激损伤,与冠心病、高血压等病理演变的始动环节吻合,可诱导内皮细胞存活率降低,细胞功能标志物LDH 和ACP 分泌增加。研究结果发现三七皂苷R1、人参皂苷Rb2、人参皂苷Rb3、槲皮素、人参皂苷F2、人参皂苷Rk1、人参皂苷Rh1、三七素可明显增高氧化损伤下的细胞存活率,保护内皮细胞。
综上所述,三七具有保护心肌、保护血管内皮等作用,主要活性成分为人参皂苷Rb2、人参皂苷Rb3、槲皮素、人参皂苷F2、人参皂苷Rk1、人参皂苷Rh1、三七素等。

