基于质量标志物的三七粉质量标准提升研究*
刘耀晨,郭海彪,张 杨,王德勤,刘建庭,4,李楚源,张洪兵,4,韩彦琪,4,张铁军,4,5**,许 浚,4,5**
(1.天津医科大学药学院 天津 300070;2.广州白云山和记黄埔中药有限公司 广州 510515;3.天津药物研究院天津市中药质量标志物重点实验室 天津 300301;4.天津药物研究院中药现代制剂与质量控制技术国家地方联合工程实验室 天津 300301;5.天津药物研究院释药技术与药代动力学国家重点实验室 天津 300301)
三七粉具有散瘀止血、消肿定痛的功效[1],在预防及改善心脑血管疾病方面作用显著,且无明显毒副作用,有效性安全性极高,市场需求量极大。2013 年我国提出“一带一路”建设,中医药行业响应“一带一路”倡议,中药在国际市场上的贸易额不断加大。从出口方向上看,主要为亚洲地区,尤其东盟各国由于地理位置及文化背景等原因,用药习惯与我国相近,相对于西方发达国家市场,更加认可中药以药品形式进口,例如泰国、新加坡政府允许中药作为药品合法进口。2010 年中国-东盟自由贸易区建成,对决大多数商品实行“零关税”政策,今年上半年东盟已成为我国的第一大贸易伙伴,东盟正成为我国中药出口最具潜力的市场。由于多数东盟国家经济医疗水平较低,且都已进入老龄化社会,而三七粉在防治慢性疾病方面具有优势,因此,三七粉非常符合东盟国家的需求[2]。三七粉具有有效成分可快速释放的优点,三七粉饮片品牌众多,但缺少统一的三七粉质量标准,掺假的鉴别较为困难[3-4]。对于三七粉的质量评判国内多参考《中国药典》规定指标,三七粉的质量标准主要是测定其中三七皂苷R1、人参皂苷Rg1及Rb1的总量[1],这不能全面反映三七粉的质量。针对三七粉的质量标准研究,刘永利在法定检验的基础上,已围绕重金属检查、有效成分检测等方面进行了初步研究,并建议增加多成分含测指标,防止掺假造假[5]。再看东盟各国的中药质量标准,存在着过于西化、体系混乱等问题,一方面造成假冒伪劣产品流入东盟市场,另一方面导致中药产品注册困难[2]。因此,提升现有三七粉的质量标准,成为未来制定三七粉国际标准和促进三七粉国内外贸易的关键。
中药质量标志物(quality marker,Q-Marker)在解决现在中药质量标准存在的问题和中药质量研究上有很好的指导意义,有利于提高中药在国际上的地位[6-7]。根据中药Q-Marker基本条件,对现行三七粉评价指标做出改善需要明确三七粉中的有效成分群、特有成分群的组成同时兼顾成分的可测性[7]。经过本课题组前期的研究,最终确定三七素、三七皂苷R1、人参皂苷Rg1、Re、Rb1、Rg2、Rd 符合Q-Marker 基本条件,可为三七粉的质量标志物。本实验建立了基于三七粉质量标志物的HPLC 含量测定和指纹图谱方法,对不同厂家三七粉及不同商品规格原料药材进行质量标志物差异分析和质量一致性评价。此外,由于传统的相似度评价方法在中药质量控制中存在一定不足,及为了提高三七粉质量标志物在质量评价上的作用,参考相关文献采用一种新的相似度评价方法-等同系数模型,该模型中权重系数的确定采取层次分析法结合CRITIC 法的方式[8-12]。最后,为了更加全面评价三七药材质量,使用了模式识别进行综合分析。本研究结果可为三七粉的质量标准提升及原料药材的选择提供科学依据。
1 仪器和材料
1.1 仪器
AB204-N 电子天平(德国Mettler 公司);超声波清洗仪(宁波新芝生物科技公司);BT25S电子天平(德国Sartorius 公司);Agilent 1260 高效液相色谱仪(美国Agilent 公司);Waters Alliancee 2695 高效液相色谱仪(美国Waters 公司);Waters Atlantis T3 C18色谱柱(4.6 mm×250 mm, 5 μm,美 国Waters 公 司);Agilent ZORBAX Eclipse C18色谱柱(4.6 mm×250 mm,5μm,美国Agilent公司)。
1.2 材料
三七素(纯度≥90%,批号:R06S8F43250),人参皂苷Rg1(批号:G30N10Y104330)、人参皂苷Rb1(批号:G01O11Y126429)纯度均大于98%,均购自上海源叶生物科技有限公司;三七皂苷R1(批号:110745-201921)、人参皂苷Re(批号:110754-202028)、人参皂苷Rg2(批号:111779-200801)、人参皂苷Rd(批号:111818-201603)均购自中国食品药品检定研究院,纯度均大于98%。纯净水购自杭州娃哈哈集团有限公司,磷酸、乙腈、甲醇均为色谱纯,购自天津市光复科技发展有限公司和康科德科技有限公司。
1.3 样品
三七粉及三七药材均由广州白云山和记黄埔中药有限公司(简称“白云山和黄中药”)负责收集,具体信息见表1-表2。所有样品经天津药物研究院张铁军研究员鉴定均来源于五加科人参属植物三七Panax notoginseng(Burk.)F.H.Chen。

表1 三七粉样品信息

表2 三七药材样品信息
2 方法与结果
2.1 三七素含量测定
2.1.1 色谱条件
Waters Atlantis T3 C18色谱柱(250 × 4.6 mm,5 μm);流动相:0.2%磷酸水;检测波长213 nm;进样量:10 μL;流速:1 mL·min-1;柱温:20℃。0.2%磷酸水洗脱5 min。结果见图1。

图1 (A)对照品色谱图;(B)样品色谱图
2.1.2 对照品溶液制备
取三七素对照品适量,精密称定,置于量瓶中,加入少量纯水溶解后稀释至刻度,摇匀,即得三七素对照品储备液(1.756 mg·mL-1)。精密量取储备液5 mL置10 mL量瓶中,加纯净水稀释至刻度,摇匀,即得。
2.1.3 供试品溶液制备
取三七粉、药材粉末各约1.0 g,精密称定,置具塞锥形瓶中,精密加入纯水20 mL,称定重量,超声45 min,放冷,再称定重量,并用纯水补足减失的重量,摇匀,0.45 μm微孔滤膜过滤,取续滤液,即得。
2.1.4 线性关系考察
取三七素对照品置于量瓶中,配置储备液,将溶液逐级稀释,共配成五个浓度梯度的线性溶液。按“2.1.1”项下色谱条件进行测定,得回归方程,结果见表3。

表3 三七素线性关系考察
2.1.5 重复性实验
取三七粉(YPA8L0004),按照“2.1.3”项下方法制备供试品溶液,平行制成6 份供试品溶液,连续测定,结果表明三七素峰面积RSD 不大于2%,符合含量测定方法学验证要求。
2.1.6 稳定性实验
取同一批三七粉,按“2.1.3”项下方法制备供试品溶液,在室温放置0、2、4、6、8、12 h 后分别进样,记录三七素色谱峰面积,并计算RSD 值。结果显示RSD 不大于2%,表明供试品溶液在室温条件下放置12 h 内稳定。
2.1.7 中间精密度实验
由另一分析人员于不同日期照重复性试验项下方法重新配置6 份供试品溶液,使用不同仪器进样测定,将测定结果与重复性试验结果进行比较,两组测定结果RSD均不大于2%,该方法精密度良好。
2.1.8 准确度实验
取同一批三七粉(含量已通过重复性试验测得,取其含量平均值)约0.5 g 放置于50 mL 锥形瓶内。加入定量的三七素对照品,称重,超声处理45 min,放冷,再称定重量,并用纯水补足减失的重量,摇匀,0.45 μm微孔滤膜过滤,取续滤液。平行制备6份,分别进样于色谱仪,依法测定,计算加样回收率(表4)。结果表明,三七素加样回收率在92%~105%之间,符合方法学验证要求,该方法具有良好的准确度。

表4 准确度实验结果
2.1.9 含量测定
取三七粉及三七药材,按“2.1.3”项下方法制备供试品溶液,并取“2.1.2”项下对照品溶液,依次进样测定(表5)。

表5 三七素含量测定结果
2.2 皂苷成分含量测定
2.2.1 色谱条件
ZORBAX Eclipse C18色谱柱(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-水(B);检测波长203 nm;进样量:10 μL;流速:1 mL·min-1;柱温:25℃。流动相洗脱梯度:0-30 min,20%A;30-40 min,20%-34%A;40-46 min,34%A;46-53 min,34%-39%A。结果见图2。

图2 (A)混合对照品色谱图;(B)样品色谱图
2.2.2 对照品溶液制备
取三七皂苷R1、人参皂苷Rg1、Re、Rb1、Rg2、Rd 对照品适量,精密称定,分别置于量瓶中,用甲醇配成浓度分别为0.253、1.013、0.161、1.051、0.034、0.252 mg·mL-1混合对照品溶液。
2.2.3 供试品溶液制备
取三七粉、三七药材粉末各约1.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定重量,超声45 min,放冷,再称定重量,并用甲醇补足减失的重量,摇匀,0.45 μm微孔滤膜过滤,取续滤液,即得。
2.2.4 线性关系考察
取6种皂苷对照品置于量瓶中,配置储备液,将溶液逐级稀释,共配成五个浓度梯度的线性溶液。按“2.2.1”项下色谱条件进行测定,得回归方程,结果见表6。

表6 皂苷成分线性关系
2.2.5 重复性实验
取三七粉(YPA8L0004),按照“2.2.3”项下方法制备供试品溶液,平行制成6 份供试品溶液,连续测定,结果表明6 种皂苷的峰面积RSD 均不大于2%,符合含量测定方法学验证要求。
2.2.6 稳定性实验
取同一批三七粉,按“2.2.3”项下方法制备供试品溶液,在室温放置0、2、4、8、12、24 h 后分别进样,记录色谱峰面积,并计算RSD 值。结果表明6 种皂苷的峰面积RSD 均不大于2%,表明供试品溶液在室温条件下放置24 h内稳定。
2.2.7 中间精密度实验
由另一分析人员于不同日期照重复性试验项下方法重新配置6 份供试品溶液,使用不同仪器进样测定,将测定结果与重复性实验结果进行比较,两组测定结果RSD均不大于3%,该方法精密度良好。
2.2.8 准确度实验
取同一批三七粉(含量已通过重复性试验测得,取其含量平均值)约0.5g,置于25ml 容量瓶中,加入定量的6 种皂苷对照品溶液,超声处理45min,放冷,即得。平行制备6份,依法测定,加样回收率结果见表7。加样回收率均符合方法学验证要求,该方法具有良好的准确度。

表7 准确度实验结果
2.2.9 相对校正因子计算
取“2.2.4”项下五个浓度梯度混合对照品溶液,以人参皂苷Rb1峰面积为内标,分别计算6种皂苷的相对校正因子(fR),结果RSD<5%,差异较小(表8)。

表8 相对校正因子计算结果
2.2.10 相对校正因子耐用性验证
2.2.10 .1 用不同C18色谱柱测定的耐用性验证
取“2.2.2”项下的混合对照品溶液,在同一台高效液相色谱仪上,分别采用3 根同一厂家不同批号色谱柱进行检测,求算以Rb1作为参照成分时其他4种成分的fR,各相对校正因子RSD 在0.07%-1.74%,fR在使用不同色谱柱时耐用性良好(表9)。

表9 使用不同色谱柱测定并计算得到的各待测成分的相对校正因子
2.2.10 .2 用不同仪器测定的耐用性验证
取“2.2.2”项下的混合对照品溶液,分别在不同厂家高效液相色谱仪上,采用相同色谱柱进行检测,分别计算以Rb1作为参照成分时其他4 种成分的fR,各相对校正因子RSD 在0.20%-1.14%,fR在使用不同仪器时耐用性良好(表10)。

表10 使用不同仪器测定并计算得到的各待测成分的相对校正因子
2.2.11 待测组分色谱峰定位
色谱峰的定位一般可以采用保留时间差或相对保留值,相对保留值计算公式:ras=tRa/tRs;保留时间差计算公式:ΔtRas=tRa-tRs。
考察保留时间差值及相对保留值对6种皂苷成分色谱峰在色谱图上的定位准确度。保留时间差值及相对保留值的RSD 分别为1.62%-12.39%、0.43%-3.32%。由结果可知,相对保留值可以用于待测成分色谱峰的定位(表11-表12)。

表11 使用不同仪器及色谱柱测定的保留时间差值
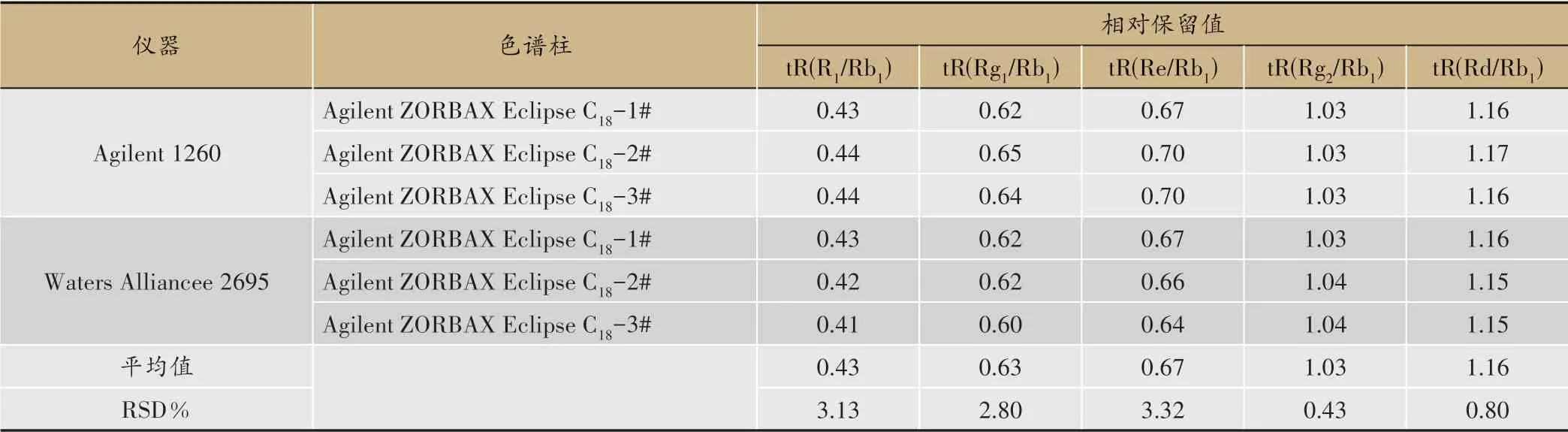
表12 使用不同仪器及色谱柱测定的相对保留值
(1) 不同C18色谱柱及仪器保留时间差重现性
(2) 不同C18色谱柱及仪器相对保留值差重现性
2.2.12 含量测定
以人参皂苷Rb1为参照成分作为“一测多评”法的参照成分,测定样品中6 种皂苷成分的含量(%),“一测多评”法(QASM)测定结果与外标法(ESM)进行比较(表13)。将两种结果进行t 检验,P>0.05,故“一测多评”法测定结果与外标法测定结果不存在显著性差异。

表13 “一测多评”法与外标法测定6种皂苷成分含量的比较
2.3 指纹图谱
对照品溶液及供试品溶液制备方法同“2.2.2”和“2.2.3”项。
2.3.1 色谱条件
ZORBAX Eclipse C18色谱柱(4.6 mm × 250 mm,5 μm);流动相:乙腈(A)-纯水(B);流速1.0 mL·min-1;检测波长:203 nm;柱温为25℃;进样量:10 μL;流动相梯度:0-30 min,20%A;30-40 min,20%-34%A;40-46 min,34%A;46-53 min,34%-39%A;53-65 min,39%-67%A。
2.3.2 精密度实验
取三七粉(YPA8L0006)约1.0 g,制备供试品溶液,连续进样6 次,以人参皂苷Rb1的保留时间和色谱峰面积为参照,计算出各共有峰的相对保留时间及相对峰面积。结果表明,各色谱峰的相对保留时间及相对峰面积的RSD值均不大于5%。
2.3.3 稳定性实验
取精密度下的供试品溶液,室温下分别在0、2、4、8、12、24 h时检测。结果表明,各色谱峰的相对保留时间及相对峰面积的RSD值均不大于5%。
2.3.4 重复性实验
取同一批三七粉约1.0 g,平行制备供试品溶液6份,进样。结果表明,各色谱峰的相对保留时间及相对峰面积的RSD值均不大于5%。
2.3.5 指纹图谱测定和色谱峰指认
对所有样品进行测定,确定三七药材和三七粉的共有峰。将混合对照品溶液注入液相色谱仪进行分析,得到各对照品色谱峰。白云山和黄中药所产三七粉、不同厂家三七粉、三七药材各形成14、23、21 个共有峰,其中指认5个色谱峰(图3~图5)。

图3 (A)白云山和黄中药三七粉指纹图谱;(B)白云山和黄中药三七粉共有模式图

图5 (A)三七药材指纹图谱;(B)三七药材共有模式图
2.3.6 指纹图谱等同系数相似度计算
等同系数相似度结果见表14~表16。根据表中结果,得出质量波动范围的95%置信区间下限分别为0.9797、0.9745、0.9713,以这些值进行评价,实现了白云山和黄中药三七粉中差异批次(表14 中S8、S11、S12)、不同厂家三七粉及冬三七120 头的区分。但未有效区分出冬三七60 头、春三七(筋条)、春三七(须根)、春三七(芦头),同时为了寻找对不同厂家三七粉质量差异贡献度较大的质量标志物,需要结合化学模式识别进行更深入的研究。
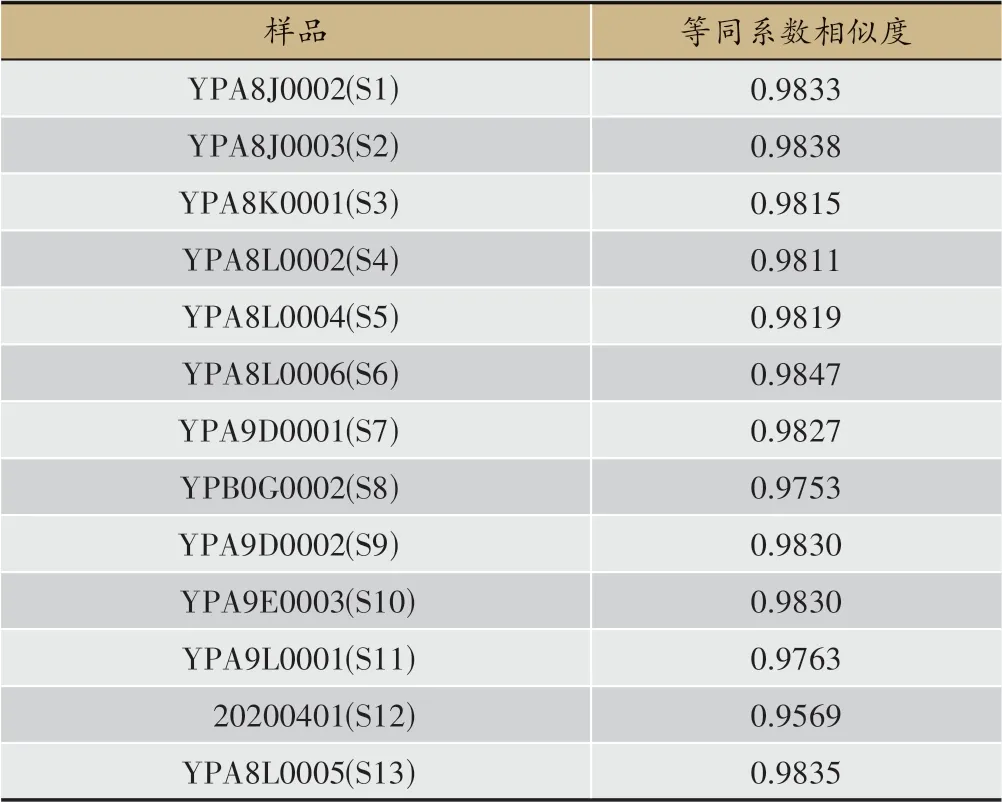
表14 白云山和黄中药三七粉指纹图谱相似度

表15 不同厂家三七粉指纹图谱相似度

表16 三七药材指纹图谱相似度
2.3.7 化学模式识别研究
(1) 主成分分析(PCA)
将三七药材共有峰面积数据导入SIMCA-P 14.1软件中,进行PCA 分析,PCA 得分图见图6。由图可见,PCA 可实现冬三七60 头、冬三七120 头、春三七(芦头)、春三七(须根)的区分,但春三七(筋条)没有得到有效区分。

图6 三七药材PCA得分图

图4 (A)不同厂家三七粉指纹图谱(S1为白云山和黄中药三七粉标准指纹图谱);(B)不同厂家三七粉共有模式图
(2) 聚类分析(CA)
将三七药材共有峰面积数据导入SPSS 26 软件中,以欧式平方距离为测度,采用组间联接法进行CA分析,CA 谱系图见图7。由图可见,CA 可将三七药材聚为五类,冬三七60 头、冬三七120 头、春三七(芦头)、春三七(须根)各为一类,其余样品为一类,所得结果与PCA结果一致。

图7 三七药材CA谱系图
(3) 偏最小二乘回归分析(PLS-DA)
将三七药材共有峰面积数据导入SIMCA-P 14.1软件中,进行有监督的PLS-DA 分析,PLS-DA 得分图见图8。由图可见,春三七主根主要集中于右下象限,冬三七位于左下象限,其他药用部位位于上半部分。

图8 三七药材PLS-DA得分图
通过对不同厂家三七粉进行PLS-DA 分析,发现质量标志物色谱峰中峰5(三七皂苷R1)、峰13(人参皂苷Rb1)、峰14(人参皂苷Rg2)、峰16(人参皂苷Rd)的变量投影重要度(Variable importance for the projection,VIP)值大于1(图9)。

图9 不同厂家三七粉VIP图
3 讨论与结论
本实验在确定三七粉质量标志物的基础上建立了皂苷成分“一测多评”法和三七素含量测定方法,方法更简单快捷,待测成分分离度良好,且降低了含量测定成本,方法学考察符合要求,为三七粉质量控制提供参考。建议三七粉质量标准制定时可考虑增加相关指标性成分。
三七素含量测定结果表明:①三七素含量与头数关系不大,与崔秀明、徐娜等的研究结果一致[13-15];②冬三七三七素含量高于春三七,原因可能与总氨基酸的积累有关[16],而冬三七中多种氨基酸含量高于春三七[17],三七中某些氨基酸可能会参与其生物合成;③芦头、须根、筋条的三七素含量高于主根,与黄海霞等的研究结果相符[18]。有研究表明,三七素作为富氮有机物可能经成熟组织运送至生长分化能力强的组织[19],因此三七素在这三个部位的积累可能多于主根;④白云山和黄中药三七粉中三七素可能为市场上主流厂家产品中的优势指标,这可能与不同厂家的生产工艺或原料药材来源不同有关。拟定优质三七粉三七素含量不小于1.0%并列入质量标准。
三七皂苷含量测定结果表明:①总皂苷及单体皂苷含量和头数关系不大,与王其华、徐娜等的研究结果相同[14,20];②不同药用部位中,总皂苷及单体皂苷含量趋势均表现为芦头>主根>须根>筋条,与已有研究结果基本相符[15,20-21];③冬三七中单体皂苷及总皂苷含量均高于春三七,以往有研究表明春三七皂苷含量高于冬三七[21],但有研究发现种子成熟过程的生理活动可能有利于三七皂苷的形成[23-24],因此冬三七皂苷含量也可能会高于春三七[14,22]。拟定优质三七粉中三七皂苷R1、人参皂苷Rg1、Re、Rb1、Rg2、Rd 含量之和不小于6.5%并列入质量标准。
综合三七素和皂苷成分含量测定结果,考虑应以冬三七为三七粉的原料。目前三七主要的药用部位为主根,建议在三七粉生产中也应提高三七须根、芦头的利用,避免三七药用资源的浪费。
另外,本文在2020年版《中国药典》基础上新增了三七粉HPLC 指纹图谱,并对指纹图谱相关色谱峰进行指认,建议在制定质量标准时增加HPLC 指纹图谱测定。指纹图谱实验对供试品制备方法进行了考察,包括不同提取方法(超声提取和加热回流提取);提取溶剂(水、不同浓度甲醇溶液、不同浓度乙醇溶液);提取时间(30、45、60 min)等对三七粉指纹图谱的影响。对色谱条件进行了考察,包括不同流动相(乙腈-水、乙腈-0.1%磷酸水);不同的柱温(20、25、30℃);波长范围(200-400 nm 全扫描),以色谱峰分离度、峰型、峰数为依据,确定了最优条件。将等同系数模型和模式识别联用应用于三七粉和原料药材质量一致性评价,相似度评价很好地区分出白云山和黄中药三七粉中的三个差异批次和不同厂家三七粉,其原因可能与生产原料来源、车间生产工艺及质量控制方法不同有关。模式识别研究一方面实现了不同三七药材的区分,表明不同采收期、不同部位三七存在差异,不同部位三七的质量评价结果与孟哲研究结果相符[25];另一方面,得出质量标志物中三七皂苷R1、人参皂苷Rb1、Rg2、Rd 可作为不同厂家三七粉的质量差异标志物,对于质量差异的贡献度较大。
综上,本文根据三七粉质量标志物对2020 年版《中国药典》三七粉含量测定项进行修订,新增HPLC指纹图谱测定法。本文研究方法和结果可为以后三七粉的质量标准制定及原料药材选择提供参考。

