经皮雌二醇凝胶与口服戊酸雌二醇在PCOS患者激素替代周期冻融胚胎移植中的临床疗效比较
王安然,乃东红,莫似恩,周莉,黄卡立,王书佳,万江帆,黄晖,李洁
(广西壮族自治区生殖医院,南宁 530029)
冻融胚胎移植(FET)是目前应用较为广泛的辅助生殖技术项目之一[1]。多囊卵巢综合征(PCOS)患者月经周期不规律,激素替代方案(HRT)是目前PCOS患者FET周期中常用的内膜准备方案。目前HRT-FET周期内膜准备方案中最常用的雌激素是口服戊酸雌二醇,其使用方法简单,患者普遍易接受。但临床工作中会发现口服剂量较大时,有部分患者会出现恶心、呕吐、头晕等不良反应,并且可能会增加静脉栓塞的风险[2]。经皮雌二醇凝胶却能避免口服戊酸雌二醇对凝血功能的影响,发生静脉血栓的风险低于口服戊酸雌二醇[3],引起静脉血栓的危险性较小[4]。本研究回顾性分析经皮雌二醇凝胶在PCOS患者HRT-FET周期的临床应用,旨在为生殖临床医师选择何种雌二醇给药途径应用于PCOS患者的HRT方案中提供参考。
资料和方法
一、研究对象
回顾性分析2019年12月至2020年11月在广西壮族自治区生殖医院行HRT-FET的PCOS患者的临床资料。
纳入标准:符合2003年鹿特丹PCOS诊断标准[5];FET周期;HRT准备内膜。
排除标准:子宫腺肌病、宫腔粘连、子宫内膜息肉、子宫粘膜下肌瘤、染色体异常。
共纳入符合标准的PCOS患者82例。根据HRT内膜准备中所用雌激素剂型分为经皮雌二醇凝胶组(A组,31例),口服戊酸雌二醇组(B组,51例)。
二、内膜准备方案及胚胎移植
1.内膜准备方案:A组(经皮雌二醇凝胶组):于月经来潮或黄体酮撤药性出血的第2~5 天起每日外用涂抹经皮雌二醇凝胶(爱斯妥,Besins,比利时)10 g/d,连用7 d后返院行阴道超声检查。如内膜厚度<7 mm,加量至15 g/d再使用5 d后检查如内膜厚度≥7 mm,择期进行孕酮转化,最长时间不超过25 d;如连续使用7 d后内膜≥7 mm,则按照原量(10 g/d)使用,择期进行孕酮转化,最长时间亦不超过25 d。
B组(口服戊酸雌二醇组):于月经来潮或黄体酮撤药性出血的第2~5天起每日口服戊酸雌二醇(补佳乐,拜耳,德国)3 mg/d,连用7 d后返院行阴道超声检查。如内膜厚度<7 mm,加量至6 mg/d,再使用5 d后检查,如内膜厚度≥7 mm,择期进行孕酮转化,最长时间不超过25 d;如连续使用7 d后内膜厚度≥7 mm,则按照原量(3 mg/d)使用,最长时间亦不超过25 d。
经皮雌二醇凝胶(80 g)本医院零售价为132.93元/盒,口服戊酸雌二醇(补佳乐,1 mg×21片)本医院零售价为33.49元/盒。HRT雌激素总价定义为从HRT开始至孕酮转化前一日所产生的雌二醇药物费用。
2.孕酮转化及胚胎移植:两组患者子宫内膜厚度≥7 mm并且<15 mm时,口服地屈孕酮片(达芙通,雅培,荷兰)20 mg,3次/d。卵裂期胚胎于转化第4天移植,囊胚期胚胎于转化第5天移植。移植后继续按原剂量进行黄体支持。
3.胚胎评级:卵裂期胚胎(D3)评分根据 Peter分级标准记录胚胎的分级及卵裂球数,将≥6CG2的胚胎评级为优质卵裂期胚胎;囊胚期胚胎(D5、D6)根据Gardner评分标准观察囊胚形成情况并评分,将≥3BB的胚胎评级为优质囊胚。
三、观察指标及判断标准
患者基本临床资料,包括年龄、不孕年限、体质量指数(BMI)、不孕类型、授精方式等;HRT内膜准备方案相关指标,包括HRT天数、HRT雌激素总价、HRT 7 d后子宫内膜厚度、孕酮转化日内膜厚度、孕酮转化日激素(LH、E2、P)水平;胚胎移植及妊娠结局相关指标,包括平均移植胚胎数、移植优胚率,以及临床妊娠率、胚胎种植率、活产率、流产率、异位妊娠率、多胎率、早产率、极低体重儿出生率、新生儿平均出生体重。
临床妊娠:冻融胚胎移植后4~6周B超下见到孕囊(宫内、宫外、宫内外),或经病理检查证实有绒毛者;流产:临床妊娠后发生的自然流产或胚胎停育;早产:满28孕周至不足37孕周间分娩者。
临床妊娠率=临床妊娠周期数/FET周期数×100%;种植率=B超下见到孕囊数/移植胚胎数×100%;流产率=(早期+晚期)流产周期数/临床妊娠周期数×100%;异位妊娠率=异位妊娠周期数/临床妊娠周期数×100%;多胎率=B超下见到≥2个孕囊数的周期数/临床妊娠周期数×100%;活产率=活胎分娩的周期数/FET周期数×100%;早产率=小于37周活胎分娩的周期数/活产分娩周期数×100%;极低体重儿出生率=新生儿体重<2.5 kg的周期数/活产分娩周期数×100%。
四、统计学分析

结 果
一、患者一般资料
本研究共纳入符合标准的82例PCOS患者的82个FET周期。根据HRT内膜准备中所用雌激素剂型分为经皮雌二醇凝胶组(A组,31例)和口服戊酸雌二醇组(B组,51例)。
两组患者间年龄、不孕年限、BMI、不孕类型、授精方式比较,差异均无统计学意义(P>0.05)(表1)。
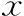
表1 两组患者一般资料的比较[(-±s),n(%)]
二、患者HRT相关资料
两组患者间HRT 7 d后内膜厚度、孕酮转化日子宫内膜厚度、孕酮转化日LH和P水平比较均无统计学差异(P>0.05);然而两组患者间HRT天数、HRT总价、孕酮转化日E2水平比较有统计学差异(P<0.05),A组患者HRT天数、雌激素总价以及孕酮转化日E2水平均高于B组患者(表2)。

表2 两组患者HRT情况比较[(-±s),M(P25,P75)]
三、患者FET结局
两组患者间移植胚胎数、移植优胚率、移植胚胎类型、临床妊娠率、胚胎种植率、流产率、异位妊娠率、多胎率、活产率、早产率、极低出生体重儿出生率、新生儿平均出生体重比较,差异均无统计学意义(P>0.05),但A组的临床妊娠率、种植率、活产率有升高趋势(表3)。

表3 两组患者FET结局比较[(-±s),%]
讨 论
人体内有3种雌激素,包括雌酮、雌二醇和雌三醇,其中以雌二醇的生物活性最强。临床上,雌二醇有多种给药途径,包括口服、经阴道给药、经皮给药等。在各种雌激素制剂中,经皮吸收的雌激素更接近自然状态下雌激素的分泌方式,是目前在临床工作中较常用的雌激素补充剂之一[6]。
经皮吸收雌激素不存在肝脏首过效应,因此可避免一些复杂的生物学作用。在临床工作中,对于一些存在肝功能轻度损害、脂肪肝等疾病的患者,经皮雌激素可能成为临床医生为患者内膜准备的首选药物之一。此外,“对围绝经期妇女心血管疾病危险的处理:欧洲心脏病医生与妇科医生的一项共识声明”[7]中指出:经皮吸收雌激素的使用与静脉血栓危险增加无关。亦有研究表明,对于有冠心病风险的绝经期妇女,C-反应蛋白(C-reaction protein,CRP)水平与冠心病风险增加相关[8],而经皮雌激素不增加CRP水平,可能是绝经期妇女雌激素用药的最佳选择。
宋娟等[2]的回顾性分析显示,在HRT-FET周期中,经皮雌二醇凝胶与口服戊酸雌二醇的妊娠结局相似,并且给药方式安全方便,是可靠的FET周期内膜准备药物。另有研究显示,相比于口服戊酸雌二醇组,经皮雌二醇凝胶组患者的血清E2水平升高可能更为理想,可达到较理想的临床妊娠率,妊娠率为45%~69.1%[9-10]。本研究中经皮雌二醇凝胶组与口服戊酸雌二醇组比较,孕酮转化日血清E2水平升高亦较为明显(P<0.05),而在妊娠结局方面,临床妊娠率(67.74% vs. 58.82%)、胚胎种植率(56.52% vs. 42.68%)、活产率(51.61% vs. 41.76%)也表现为某种升高趋势,但无统计学差异(P>0.05)。
有研究报道,经皮雌凝二醇胶中含有酒精成分,当酒精挥发后,药物逐渐蓄积皮肤,通过皮肤接触可能会转移至其他人出现污染[11-13]。虽然没有大数据的研究证实,但已有个案报道经皮吸收雌激素对家庭亲密接触成员产生严重的不良反应[14-15]。金聪聪等[16]的研究还发现,经皮雌二醇凝胶需要患者每天涂抹在皮肤上,使用量较大的时候可能沾染衣物,亦或吸收不佳,影响其实际用量,使得用药时间延长,给患者造成的心理负担、经济成本增加,从而导致患者依从性较差。本研究的结果也显示经皮雌二醇凝胶组的HRT天数、HRT中雌激素总价均高于口服戊酸雌二醇组,用药时间延长且经济成本增加。我们的研究在病例资料收集过程中就发现有部分病例无法纳入本研究,究其原因就是部分患者依从性较差,对于单用经皮雌二醇凝胶一种雌激素药物来进行内膜准备存在疑虑,会要求采用联合口服戊酸雌二醇用药,因此导致单用经皮雌二醇凝胶组的样本数较少。
本研究的局限性:(1)样本量较少;(2)未能区分季节对于经皮雌二醇凝胶用于HRT的影响:冬季因为天气寒冷,患者对于经皮雌二醇接受度较低,而夏季天气炎热,汗液堵塞毛孔,也可能影响经皮雌二醇的吸收;(3)未能排除实际用药量的影响因素:患者的文化水平差异可能影响药物涂抹的掌握程度,亦不排除衣物沾染,影响实际用药量;(4)未能标准化用药时间和成本量化的影响因素:本中心HRT-FET中孕酮转化的时机会尽量避开移植日在周末或者节假日,因此HRT的用药时间和经济成本的矫正需要加大样本量或者多中心前瞻性随机对照研究来进一步证实。
尽管本研究中经皮雌二醇凝胶组的HRT天数、总价相比口服戊酸雌二醇组而言有所增加,但费用及时间均在合理可接受的范围内,而且相关的FET结局至少与口服戊酸雌二醇组相当(或有某种改善的趋势),可以有效地应用于PCOS患者FET周期的内膜准备。

