纤维素类可吸收止血材料体外效果评价方法
张爽,叶红,朱玉,童琳,曹琛,马征,徐庆华
在临床手术过程中,安全有效的止血方式非常重要,优良的止血材料可以保障患者的生命安全,提高手术效率[1]。可吸收止血材料作为一种可被人体吸收的医疗器械产品,主要适用于手术过程中无法使用常规止血技术的情况,其通过促进局部伤口的血液凝固来实现止血[2]。常见的止血产品依据其材质可以分为纤维素类、胶原蛋白/明胶类、淀粉类、壳聚糖类、纤维蛋白类。材料不同,止血机制也有差异。其中,纤维素类止血产品在市场中占有的比重最大[3]。纤维素是D-葡萄糖残基通过 β-1,4 连接形成的多糖聚合物。纤维素链的线性结构能够满足各种生化需求。纤维素对人体组织具有天然的生物相容性,可以改性成多种形式,如氧化纤维素、氧化再生纤维素、醋酸纤维素、甲基纤维素、羧甲基纤维素、羟乙基纤维素、羟丙基纤维素等,它们的理化性质各有差异。纤维素在其改性后能够表现出优秀的生物效应。
可吸收止血材料直接接触创伤表面,发挥止血功效,需要拥有更加良好的凝血性和组织相容性[4]。国内市场上可吸收止血产品种类繁多,但是临床前的评价标准还比较缺乏,现仅有一部 2016年国家食品药品监督管理总局颁布的《可吸收止血产品注册技术审查指导原则》,导致临床上对于该类产品的选择没有一定的指导标准[2,5]。因此建立可吸收止血材料的评价体系,对规范可吸收止血材料的临床使用具有重要的参考价值。
为此,实验开展了可吸收止血材料评价体系的研究,实验共选取了市售的 3 种不同材质的纤维素类可吸收止血材料,分别对其抑菌性、体外降解性以及体外凝血性进行评价,为筛选出安全、有效的可吸收止血材料提供理论基础以及参考依据。
1 材料与方法
1.1 材料
本实验共选取 3 种市售常用纤维素类止血材料。A 类材料为氧化再生纤维素(oxidized regenerated cellulose,ORC)。ORC 吸收血液后,会形成黑色或褐色的块状,可在很短的时间内达到止血效果,其临床适应证包括伤口修复和组织重建。B 类材料为羧甲基纤维素(carboxymethyl cellulose,CMC)。CMC 是一种半天然聚合物,具有较强的吸水性。它在生理上无毒,与黏膜、骨骼和皮肤相容,可以与组织紧密结合,从而闭合伤口[6]。C 类材料为羟乙基纤维素(hydroxyethyl dellulose,HEC)。HEC 材料本身及代谢产物的 pH 值为中性,HEC 材料最终代谢产物可以分解成人体可吸收的产物,减少血栓的形成,适用于手术、创伤等创面[7]。
1.2 方法
1.2.1 抑菌性 依据《WS/T 650-2019 抗菌和抑菌效果评价方法》[8],实验采用抑菌环法。抑菌片的制备:无菌环境下,将 A 类、B 类、C 类 3 种材料制成直径为 5 mm,厚度不超过 4 mm 的圆片(块),每 4 片为一组。阴性对照样片的制备:将滤纸片制成与实验组大小相同的圆片(块)[8]。
采用的实验菌株为金黄色葡萄球菌 ATCC6538 和大肠杆菌 8099 的冻干株,传代培养,接种于营养琼脂斜面上,37 ℃ 条件下培养 24 h,用磷酸盐缓冲溶液(PBS)将实验菌 24 h 新鲜斜面培养物稀释浓度至 3.0 × 106CFU/ml,用无菌棉拭子蘸取菌液,均匀涂抹在营养琼脂培养基平板表面,盖好平皿,室温放置后备用。用无菌镊子在每个染菌平板上放置 4 片实验样片,中心处放置 1 片阴性对照样片,共 5 片。各样片中心点距离 > 25 mm,与平板的周缘距离> 15 mm。将平板置于 37 ℃ 恒温培养箱中培养 18 h,用游标卡尺测量抑菌环的直径并记录,实验重复 3 次[8]。
1.2.2 体外降解性 实验主要观察 3 种材料在 PBS 缓冲液、生理盐水溶液中的溶解差异。实验在室温 25 ℃、标准气压的条件下进行。将 A 类、B 类、C 类 3 种材料分别处理成 2 cm × 2 cm 大小的试样。在试管中分别加入5 ml 的 PBS 缓冲液、生理盐水溶液备用,将 3 种处理过的止血材料分别加入上述试管中,打表计时,观察样品在 0、1、2、5、10、30 min 时的溶解性。
1.2.3 降解产物的鉴别 分别在饱和 A 类材料生理盐水溶液、1% B 类材料生理盐水溶液、1% C 类材料生理盐水溶液中加入终浓度为 0.2% 的纤维素酶溶液,室温下反应120 h。取 200 μl 反应液,分别加入 200 μl 氢氧化钠溶液(0.1 g/ml)和200 μl硫酸铜溶液(0.05 g/ml)。沸水浴中加热,观察溶液颜色变化[9]。以 1% 葡萄糖溶液为阳性对照,以饱和 A 类材料生理盐水溶液、1% B 类材料生理盐水溶液、1% C 类材料生理盐水溶液、1% 纤维素酶溶液为阴性对照。
1.2.4 终降解产物浓度的测定 采用 3,5-二硝基水杨酸(DNS)法定量测定葡萄糖含量[9]。称取 0.3 g DNS,置于100 ml 烧杯中,用 50 ml 去离子水完全溶解,继续加入氢氧化钠 1.6 g,酒石酸钾钠 3 g,结晶酚 0.5 g,无水亚硫酸钠 0.5 g,搅拌至所有成分完全溶解,转移至 100 ml 棕色容量瓶中,用去离子水定容至刻度,摇匀,常温放置 7 d 后使用[9]。精确配制 2.0、1.0、0.5、0.25、0.125、0.0625 mg/ml的葡萄糖标准溶液。将配制好的 0.5 ml DNS 试剂加入到含有 1.0 ml 标准溶液的试管中,沸水浴中反应 5 min 后,立刻放入冰水浴中冷却,定容至 20 ml,颠倒混匀后室温下静置 20 min。用紫外可见分光光度计在 540 nm 波长下测量,绘制标准曲线[9]。
1.2.5 体外倒置凝血实验 取出 A 类、B 类、C 类 3 种止血材料以及对照组医用纱布,分别处理成 2 cm × 2 cm 大小的试样,放置于无菌培养皿中,37 ℃ 保温 5 min 待用。向待测样品表面滴加 400 μl 37 ℃ 预热抗凝大鼠血液,充分浸润待测样品后,立刻向待测样品表面滴加 45 μl 的氯化钙溶液(0.2 mol/L),将样品放置于 37 ℃ 培养箱中,观察3 种止血材料在反应 5 min 后出现凝血现象的差别。
1.2.6 体外动态凝血 取出 A 类、B 类、C 类 3 种止血材料以及对照组医用纱布,分别处理成 1 cm × 1cm 大小的试样,放置于无菌培养皿中,37 ℃ 保温 5 min 待用。
向待测样品表面滴加 200 μl 37 ℃ 预热抗凝大鼠血液,充分浸润待测样品后,立刻向待测样品表面滴加 25 μl 0.2 mol/L 的氯化钙溶液,将培养皿放入气浴恒温振荡器中以 37 ℃、80 r/min 的条件充分振荡 1、5、10 min,取出培养皿,用 20 ml 超纯水进行淋洗,淋洗出未被止血纱布凝血的红细胞,收集淋洗液后放置于离心机中,以 300 r/min离心 5 min。离心结束后,采用紫外可见分光光度计测量样品的淋洗液在 540 nm 下的吸光度,实验采用普通医用纱布与未加材料的抗凝大鼠血液作为阴性对照组以及空白对照组。实验重复 3 次,观察比较止血材料的凝血性能差异。吸光度值越高,表明材料凝血效果越差,反之说明凝血效果越好[10]。
1.3 统计学处理
采用 SPSS 23.0 软件进行统计分析,计量资料以±s表示,组间比较符合正态分布的采用方差检验,组内两两比较采用 LSD 法,P< 0.05 为差异有统计学意义。
2 结果
2.1 抑菌性
游标卡尺测得抑菌环直径:A 类材料大肠杆菌组为(8.67 ± 0.57)mm,金黄色葡萄球菌组为(8.68 ± 0.64)mm。A 类材料抑菌环直径均 > 7 mm,B 类、C 类材料无抑菌环产生,说明 A 类材料对大肠杆菌和金黄色葡萄球菌均有抑菌作用。而 B 类、C 类材料对大肠杆菌和金黄色葡萄球菌没有抑菌作用(图1)。重复上述实验 3 次,结果相同。
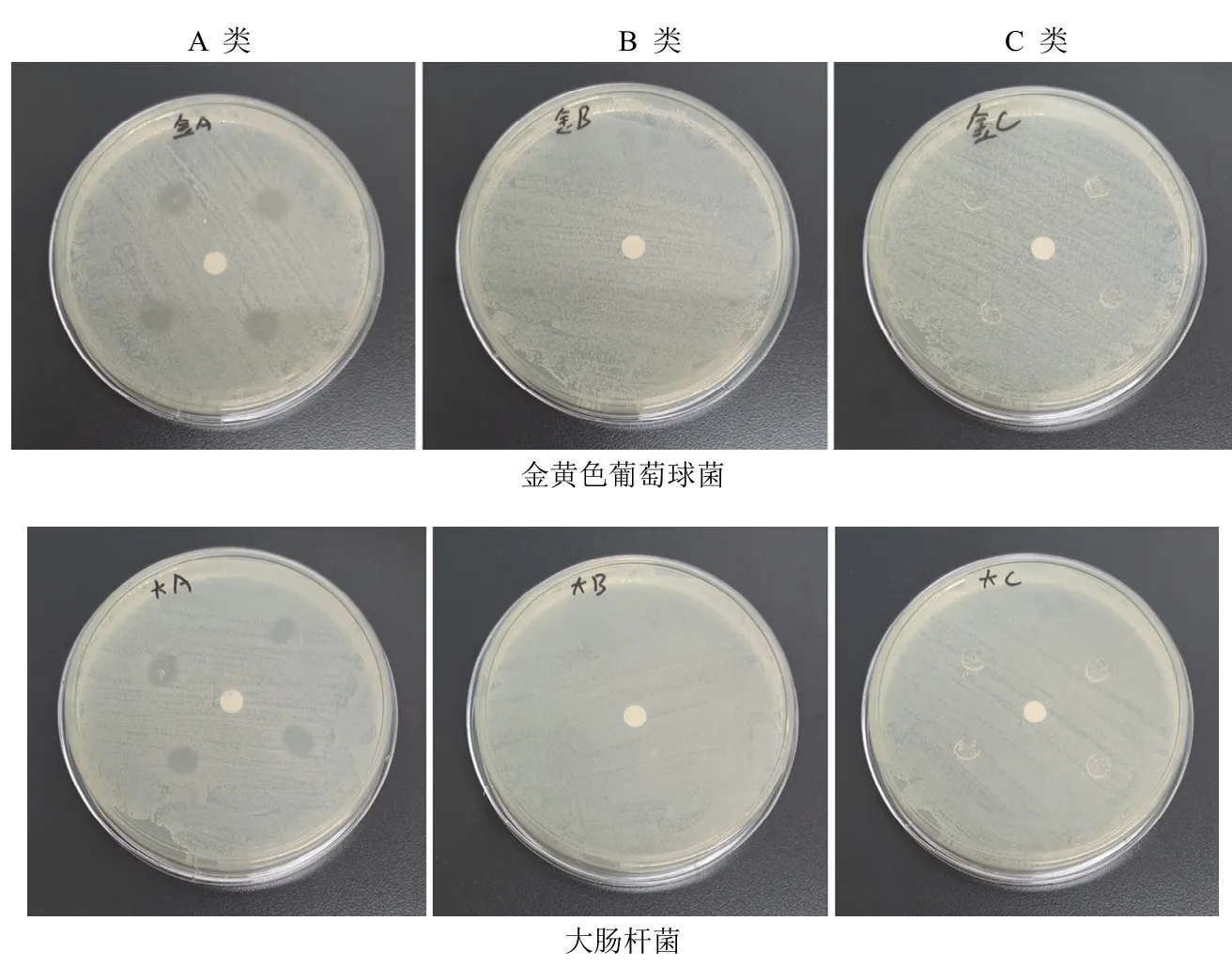
图1 不同种类可吸收止血材料体外抑菌效果
2.2 体外降解性
室温条件下可观察到 B 类、C 类在 PBS 缓冲液、生理盐水这两种溶液中会迅速吸水膨胀溶解,由纤维网眼型织物变为透明的凝胶状物质,然后在较短的时间内完全溶解于溶液中,溶液呈澄清透明状。
由图2 可以看出,3 种止血材料都是纤维素的衍生物,虽具有类似的纤维结构,但是理化性质不同。体外环境下,B 类、C 类材料比 A 类材料具有更好的溶解性。
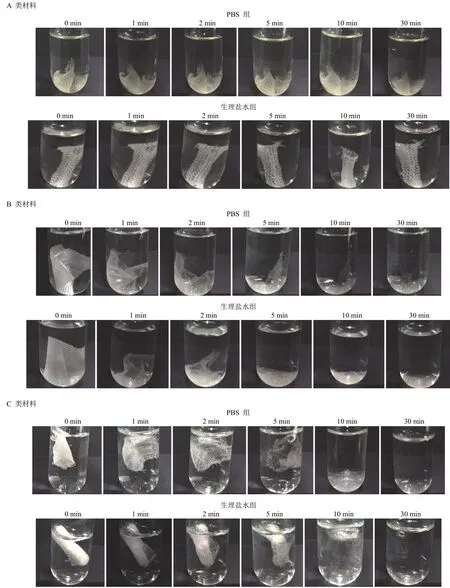
图2 不同种类可吸收止血材料体外降解性比较
2.3 终降解产物浓度的测定
3 种可吸收止血材料在纤维素酶作用下降解产物的显色如图3 所示。A 类材料降解产生葡萄糖不明显,B 类、C 类材料主要降解产物为葡萄糖,A 类、B 类、C 类材料未经纤维素酶处理的溶液均无明显的葡萄糖产生。DNS 法测定葡萄糖的线性方程为 A = 9.99 × 10-3+ 2.05 × 10-2C,相关系数r= 0.998,表明葡萄糖浓度在 0.0625 ~ 2.0 mg/ml内呈良好线性关系。
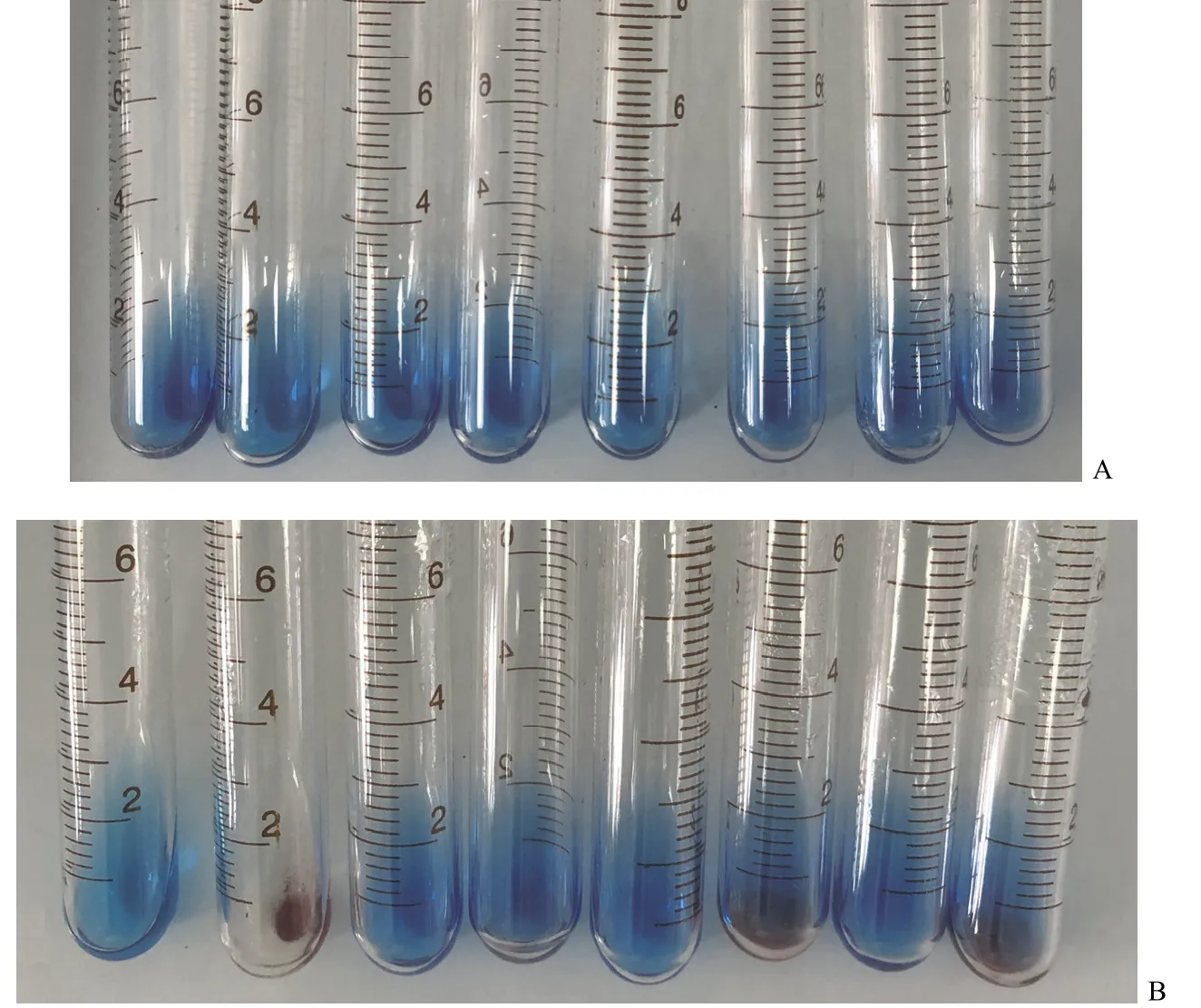
图3 不同种类可吸收止血材料在纤维素酶作用下降解产物的显色(A:加热前显色结果;B:加热后显色结果。从左至右分别为 1% 纤维素酶,1% 葡萄糖,1% A 类材料去离子水溶液,1% A 类材料与纤维素酶作用液,1% B 类材料去离子水溶液,1% B 类材料与纤维素酶作用液,1% C 类材料去离子水溶液,1% C 类材料与纤维素酶作用液)
A 类材料在纤维素酶的催化作用下缓慢降解,如图4A 所示。该降解反应 30 s 内葡萄糖生成速率为0.72 mg/(ml·min),在 5880 min 以后,在降解曲线上发现 A类材料有缓慢的二级降解反应,可能是因为 A 类材料在水中的溶解性较低,纤维素酶吸附到材料后产生了进一步的降解反应,后期葡萄糖生成速率为 1.74 × 10-4mg/(ml·min)。A 类材料降解的终浓度为(0.88 ± 0.14)mg/ml。
B 类材料在纤维素酶催化作用下,生成葡萄糖,如图4B 所示。在此降解反应中,初期葡萄糖生成速率约为2.44 mg/(ml·min),1 min 时达到峰值,峰浓度为 1.26 mg/ml,是 B 类材料初始浓度水平的 42%,葡萄糖终浓度为(1.21± 0.11)mg/ml,是 B 类材料初始浓度水平的 40.3%。
C 类材料在纤维素酶催化作用下,生成葡萄糖,如图4C 所示。在此降解反应中,初期葡萄糖生成速率约为2.22 mg/(ml·min),5 min 时达到峰值,峰浓度为 1.25 mg/ml,是 C 类材料初始浓度水平的 41.7%,葡萄糖终浓度为(1.12 ± 0.10)mg/ml,是 C 类材料初始浓度水平的 37.3%。
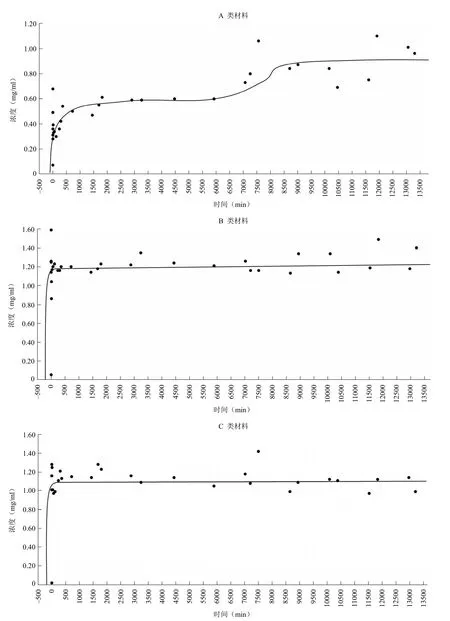
图4 不同种类止血材料降解反应中产生葡萄糖含量与时间关系图
说明B 类、C 类材料在水中的溶解性较好,反应生成葡萄糖的速度较快,葡萄糖是 B 类、C 类材料降解过程中的中间产物,在 B 类、C 类材料的降解曲线上,葡萄糖浓度在 1 min 后未发现明显的增加或降低趋势,说明它们在监测时间内均未发生二级降解反应。
2.4 体外倒置凝血
实验结果(图5)显示,37 ℃ 反应 5 min 后,A 类材料出现明显的血液凝结现象,材料上血样已经开始凝聚,倒置未出现血液下滴现象,凝血效果较好。B 类材料的血液凝结效果其次,C 类材料血样未完全凝固,凝血效果最差。通过观察结果显示:A 类材料的凝血能力优于 B 类、C 类材料。

图5 体外倒置凝血效果图
2.5 体外动态凝血
结果显示不同时间段,各组材料间凝血效果差异均有统计学意义(P< 0.05);10 min 时,3 种止血材料与阴性、空白对照组相比,差异均有统计学意义(P< 0.05),3 种止血材料都表现出促凝血效果。A 类材料的快速凝血能力优于 B 类、C 类材料,5 min 时A 类材料与 B 类、C 类材料出现凝血效果差异,这也与体外倒置凝血实验的结果吻合(表1)。
表1 不同种类可吸收止血材料吸光度(± s )
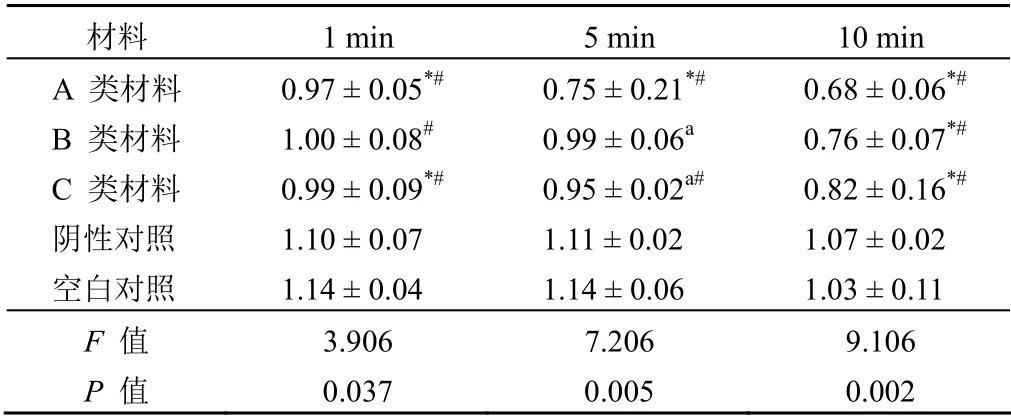
表1 不同种类可吸收止血材料吸光度(± s )
注:a为与 A 类比较,P < 0.05;*为与阴性比较,P < 0.05;#为与空白比较,P < 0.05。
材料 1 min 5 min 10 min A 类材料 0.97 ± 0.05*# 0.75 ± 0.21*# 0.68 ± 0.06*#B 类材料 1.00 ± 0.08# 0.99 ± 0.06a 0.76 ± 0.07*#C 类材料 0.99 ± 0.09*# 0.95 ± 0.02a# 0.82 ± 0.16*#阴性对照 1.10 ± 0.07 1.11 ± 0.02 1.07 ± 0.02空白对照 1.14 ± 0.04 1.14 ± 0.06 1.03 ± 0.11 F 值 3.906 7.206 9.106 P 值 0.037 0.005 0.002
3 讨论
在手术过程中,为了减少出血量、缩短手术时间、避免感染以及二次手术的发生,以提高手术质量和效率,便于患者的恢复,对于可吸收止血材料的合理选择是必要的[4]。目前市场上存在品种多样的可吸收止血材料,但在临床使用中存在各种问题。作为可植入于人体内的第三类医疗器械,对可吸收止血材料的使用具有更高的标准要求[5]。本实验主要研究的是纤维素类可吸收止血材料抑菌性、体外降解性以及体外凝血性。
传统的手术纱布摘除时可能会与皮肤组织等粘连而造成二次创伤,不利于伤口的愈合,增加患者和医护人员的负担。而手术后大量或长期使用抗生素,会对机体产生副作用及耐药性。若止血材料具有抑菌功能,将会更有利于创伤修复[11]。对可吸收止血材料抑菌性能进行评价,对于止血材料的临床使用指导以及医院耗材管理都具有较大的参考价值[2]。因此,可吸收止血材料抑菌性的研究越来越被重视,根据《WS/T650-2019 抗菌和抑菌效果评价方法》结果判定,A 类材料具有抑菌性能,B 类、C 类材料没有显示出抑菌性能,这也和 3 种市售产品的功能宣称相吻合。
可吸收止血材料的体内降解性能是其产品特征之一,体内降解性是评价安全性的指标。而本实验进行的是体外降解性的研究,B 类、C 类材料可以在体外环境下迅速水解,这与材质有关系。体外环境下降解性能快的产品是否会导致材料崩解过快,从而对临床手术中止血有影响,需要进一步的实验验证。由于人体中不含有纤维素酶,所以体内和体外降解性的差异需要进一步的研究。
生理环境止血能力是止血材料最重要的功能,其凝血能力直接反映了止血材料的实用价值。实验中 3 种止血材料都表现出促凝血效果,A 类材料的快速凝血能力优于 B类、C 类材料。
使用此种方式建立可吸收止血材料临床前抑菌性、体外降解性以及体外凝血性评价体系,结果真实可靠,方法简便且稳定,有利于对可吸收止血材料临床前性能进行评价,把控产品质量。局限性在于降解性以及凝血性仅进行了体外实验,并未开展相关体内实验,需要对评价方法进行进一步的验证与完善。
据估计,到 2024年全球医疗器械市场销售额将达到5945 亿美元[12]。国内也有越来越多的可吸收止血材料的研发与上市,利用我国丰富的水产资源研发的海洋材料类止血材料也成为研究热点[13]。而在这些研究评价中,止血功效评价以及抑菌性评价等方面使用了多种模型,如果可以建立较为规范的可吸收止血材料评价体系,对于规范临床使用以及新型材料的开发具有一定的意义。

