抗耐药性结核病新药的先导化合物筛选
刘思含,王潇,关艳,刘忆霜,肖春玲,蒙建州
结核病(tuberculosis,TB)是由结核分枝杆菌(Mycobacterium tuberculosis,Mtb)感染引起的具有高致病性的传染性疾病,是单一性传染源引起的死亡率最高的疾病[1]。全球约有 20 亿人携带有Mtb,其中 5% ~ 10% 的人有可能发展为 TB 患者。直接督导下短程化学疗法(directly observed treatment short course,DOTS)方案的实施,使 85%结核病患者的生命得以挽救[1]。新型抗结核药物及其组合的应用,使得 TB 的感染率和死亡率相对于2000年有了一定程度的降低。但是 TB 的防治形势依然严峻,2019年全球依然有 1000 万新增结核病患者,而死亡患者人数高达 120 万(不包含20 万结核病-艾滋病共感染患者)。这主要是因为TB 治疗周期长而导致患者依从性差、Mtb产生了严重的耐药性,包括单药耐药(single drug-resistant,SDR)、多药耐药(multidrug-resistant,MDR)及广泛耐药菌(extensive drug-resistant,XDR)菌株,近年来甚至出现了完全耐药菌(total drug-resistant,TDR)菌株[2]。常规一线、二线抗结核药物已经不能有效治疗由耐药Mtb引发的 TB,近年来新上市的德拉玛尼和贝达喹啉对多种耐药菌具有良好的治疗效果,但是较大的副作用限制了它们的广泛应用,而且临床应用中也很快发现了对它们具有耐药性的突变菌株[3-5]。可喜的是,2020年 pretomanid(PA-824)成功上市,为治疗由耐药Mtb尤其是XDRMtb感染引起的 TB 提供了新的选择[6]。但是全球依然有超过 50 万株耐药Mtb不能被有效治疗[7],临床对新型抗结核药物的需求依然迫切。
Mtb标准菌株 H37Rv 基因组的注释以及功能研究发现了与菌株生长、增殖以及感染过程相关的必需基因[8-10],它们可能是潜在的抗结核药物靶标。近年来,基于必需基因编码产物建立分子水平的高通量抑制剂筛选模型,获得了大量具有抑酶活性的化合物,但它们由于Mtb的细胞壁、细胞膜的屏蔽作用以及复杂的细胞内部代谢环境而不具有抑菌活性[11-12]。而建立细胞水平的靶向药物筛选克服了这一障碍,排除了不能进入细胞达到作用靶位的化合物[13]。但是必需基因并不等于是药物靶标,靶向筛选、设计抗结核药物成功的案例十分罕见[14]。几乎所有的抗结核药物包括新近上市的德拉玛尼、贝达喹啉、pretomanid 以及利奈唑胺等的先导物都是在细胞水平进行抑制剂筛型获得的[7]。因此在前期研究中,以化合物活性为导向、暂不关注其作用机制的研究策略将更有可能获得结构新颖、作用机制独特且具有成药前景的先导物样品。
本实验中我们将采用基于Mtb标准菌株H37Rv 构建的细胞水平的抑制剂筛选模型,对从上海陶塑生物科技有限公司购买的具有生物活性的化合物样品进行筛选,以期获得结构新颖的活性样品。
1 材料和方法
1.1 材料
1.1.1 菌株MtbH37Rv(ATCC 27294)、临床多药耐药菌株Mtb28 和 1731 由北京市结核病胸部肿瘤研究所(首都医科大学附属北京胸科医院)细菌免疫室保存。其中Mtb28 菌株对异烟肼(INH)、利福平、乙硫异烟胺耐药,对链霉素、乙胺丁醇、阿米卡星、卷须霉素、对氨水杨酸钠敏感;Mtb1731 菌株对 INH、利福平、链霉素、乙硫异烟胺耐药,对乙胺丁醇、阿米卡星、卷须霉素、对氨水杨酸钠敏感。
1.1.2 化合物样品 化合物库 L4000(含有7285 个化合物)购自上海陶塑生物科技有限公司,初始浓度为 10 mmol/L,采用 DMSO 稀释至终浓度为 1 mmol/L;INH 购自美国 Sigma 公司,采用DMSO 溶解配成 1 mmol/L 的溶液,4 ℃ 保存。
1.1.3 培养基 培养Mtb的培养基 7H9、7H10及其添加剂 OADC(油酸、白蛋白、右旋糖和过氧化氢酶)购自美国 BD 公司。
1.2 方法
1.2.1 种子液培养 将保存于 -80 ℃ 的MtbH37Rv 和多药耐药菌株Mtb28 和 1731 接种于7H10 固体培养基(含 10% OADC),37 ℃ 培养直至长出单菌落;挑取单菌落接种于 5 ml 7H9 液体培养基(含 10% OADC 和 0.05% Tween80),37 ℃ 静置培养 10 ~ 14 d。本研究中Mtb标准及临床耐药菌株的培养、药敏实验都在首都医科大学附属北京胸科医院完成。
1.2.2 抑制剂高通量筛选模型建立 为了节约化合物样品的用量,我们需要对前期基于MtbH37Rv构建的细胞水平的抑制剂筛选模型进行修正[15]。以1 μl INH 溶液(终浓度 10 μmol/L)为阳性对照,1 μl DMSO 溶剂为阴性对照,并加入100 μl 含有对数期MtbH37Rv 的 7H9 培养液(终浓度A600≈0.1),以不含溶剂的正常生长组监控溶剂对菌株生长的影响,同时以 7H9 培养基为空白对照,每组3 个平行。将 96 孔板密封后置于培养箱,37 ℃ 静置培养并采用酶标仪每隔一天测定菌株的A600(共测 6 次),计算 Z' 值以评估模型的可靠性。
1.2.3 抑制剂高通量筛选 在 96 孔板建立如表1 所示的筛选体系,对样品库 L4000 进行筛选,初筛浓度为 10 μmol/L。

表1 Mtb H37Rv 细胞水平抑制剂高通量筛选体系Table 1 The assay system of high through-put screening model for searching anti-Mtb inhibitors via Mtb H37Rv
含有培养液的 96 孔板用保鲜膜封闭,于 37 ℃静置培养 9 d 后观察化合物对菌株的抑制情况。在本研究中,我们将在 10 μmol/L 浓度下能完全抑制菌株生长的化合物定义为阳性。
1.2.4 抑制剂抗结核活性测定 采用二倍稀释法测定 1.2.2 中获得的抑制剂对MtbH37Rv 及临床多药耐药菌株 28 和 1731 的最低抑制浓度(minimum inhibitory concentrations,MIC)。在96 孔板中第一排加入化合物样品,最高测试浓度为 10 μmol/L,最低测试浓度为 0.08 μmol/L(8 个梯度,每个样品 3 个平行)。溶剂 DMSO 为阴性对照,INH 为阳性对照。
1.2.5 抑制剂成药性预测 利用免费网络工具Swiss-ADME(http://www.swissadme.ch/)对 1.2.3中获得阳性化合物的药代动力学、类药性质以及化学可合成性进行预测。同时利用 Molsoft L.L.C.(http://molsoft.com/mprop/)的 Drug-Likeness prediction and molecular property prediction 模块对通过 Swiss-ADME 预测的化合物进行验证。
2 结果
2.1 高通量筛选模型构建及评估
本研究中,我们将测试体系由之前的 200 μl降低至 100 μl,因此我们首先测定了实验菌株MtbH37Rv 在此条件下的生长情况。结果如图1 所示,10 μmol/L INH 能完全抑制Mtb的生长,而 1%DMSO 对菌株的生长没有影响,其生长情况与正常生长组一致。根据不同时间点阳性对照组、阴性对照组的A600吸收值计算模型的 Z' 值,第 6、8 及10 天相应的 Z' 值为 0.382、0.723 和 0.819。Z' >0.5 的体系才能满足高通量筛选的要求[16],因此本研究中的筛选体系在 37 ℃ 孵育 8 d 后观测实验结果能保证结果的可靠性和灵敏性。
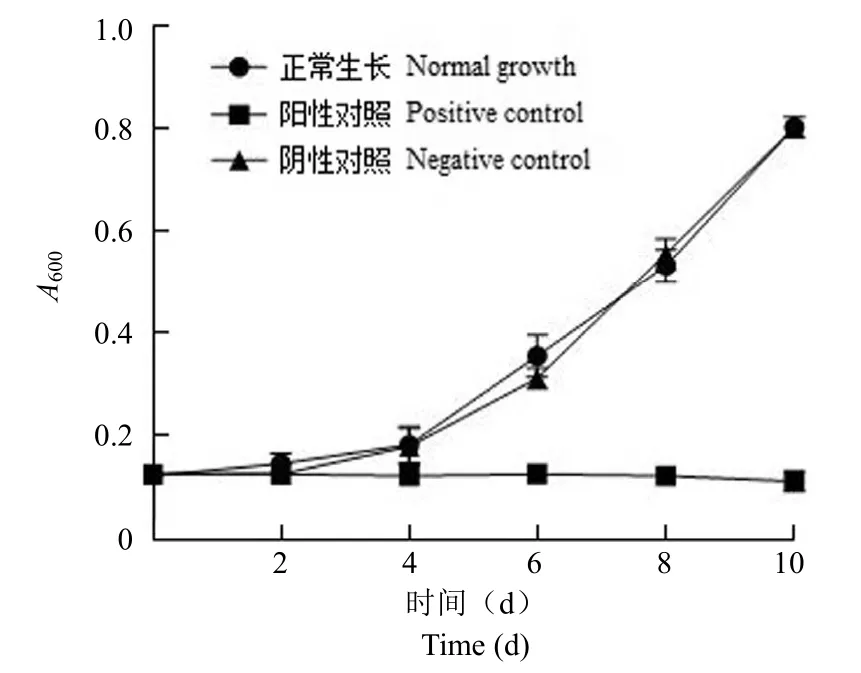
图1 Mtb H37Rv 生长曲线Figure 1 The growth curve of Mtb H37Rv
2.2 抑制剂高通量筛选
利用 2.1 建立的筛选模型,对样品库 L4000的 7285 个化合物进行筛选,并对初筛阳性的化合物进行排重(主要是排除已有抗结核活性报道的化合物)后,得到 411 个阳性样品,阳性率为 5.64%。进一步测定了它们对标准菌株MtbH37Rv 的MIC 值(图2),绝大多数样品对MtbH37Rv 的抑制活性大于 1 μmol/L,而 MIC 值小于 1 μmol/L的样品有 60 个,占比 14.60%。
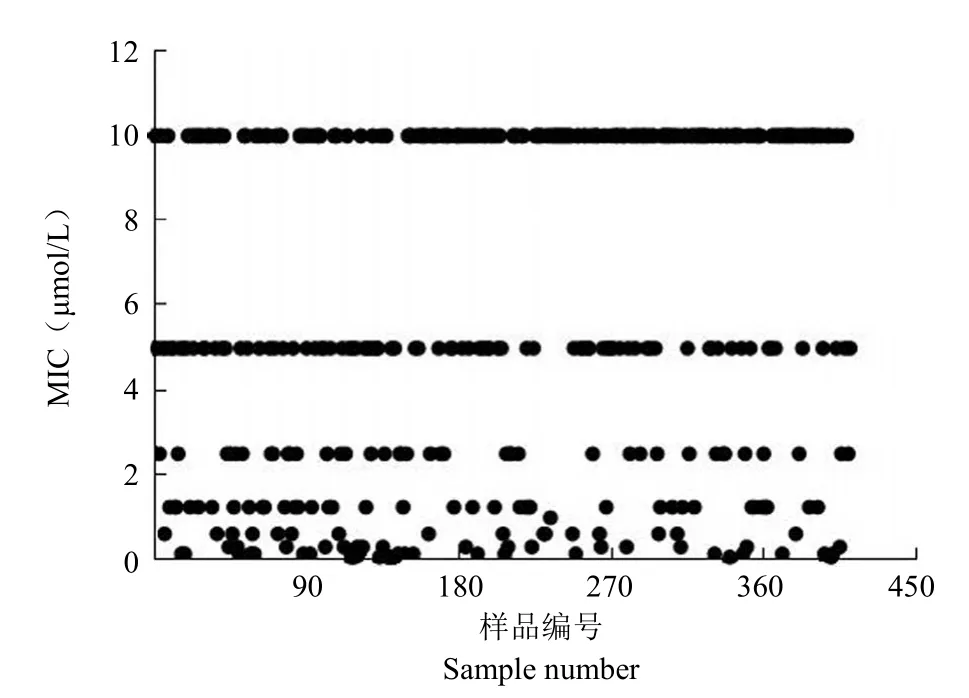
图2 抗结核活性样品对 Mtb H37Rv 的 MIC 值Figure 2 The minimal inhibition concentrations of anti-TB compounds to Mtb H37Rv
2.3 抑制剂对 MDR Mtb 抑制活性测定
在获得抗结核活性化合物的基础上,进一步测定了它们对临床分离的 MDRMtb28和 1731 的抑制活性,结果如表2 所示。从 411 个对标准菌株有抑制活性的化合物中,总共获得 24 个对耐药菌株具有抑制活性的化合物(占化合物库全部样品的 0.33%)。从结果可以看出,绝大多数对标准菌株抑制活性强的样品对耐药菌株也具有抑制效果,极少数样品(如 LBI191 和 LTBI207)对标准菌株抑制活性较弱、对耐药菌株却具有良好的抑制活性。这些化合物中,LTBI118 和 LTBI139 对敏感菌和耐药菌都表现出极强的抑制活性(≤ 0.08 μmol/L),而 LTBI18 等 11 个样品对所有菌株的 MIC 值差异在 8 倍以内。在后续研究中需要对它们予以重视。
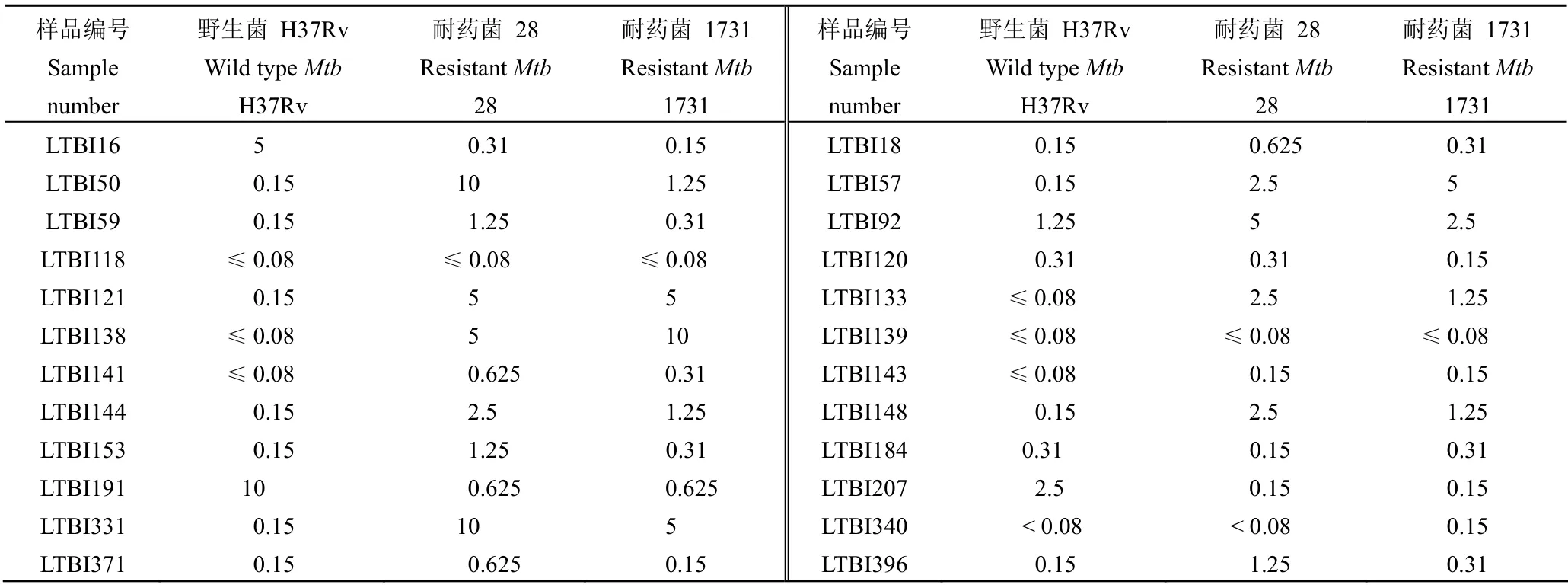
表2 化合物对 Mtb 标准菌株及临床耐药菌株的抑制活性(μmol/L)Table 2 The activities of compunds to the standard and clinical drug-resistant Mtb (μmol/L)
2.4 抑制剂成药性预测
采用 Swisse-ADME 网络工具对获得的 24 个活性样品进行成药性分析,总体分析结果采用WlogPer-TPSA 二维图谱展示(图3),标记为蓝色的化合物可能是 P-糖蛋白的底物,红色的化合物则不是;有 12 个化合物落在允许区域内,其中黄色区域内的样品能够穿透血脑屏障,白色区域内的样品具有较好的肠道吸收性能。这 12 个化合物中,LTBI18、LTBI120、LTBI153 和 LTBI371 对Mtb标准菌株及 MDR 菌株都表现出较强的抑制活性,其余化合物对不同菌株的抑制活性差异较大。而具有最强抗菌活性的化合物 LTBI118 和LTBI139 则落在允许区域以外,不具有成药性。

图3 WlogPer-TPSA 二维图谱展示抗结核化合物的成药性Figure 3 The drug abilities of anti-TB compounds demonstrated via WlogPer-TPSA two-dimensional diagram
进一步查看这 12 个化合物的生物利用度雷达图发现,化合物 LTBI121 和 LTBI371 的药化性质最佳,其中 LTBI121 的药化性质参数几乎都位于粉色的允许区域内,LTBI371 的参数则完全落在粉色区域内(图4)。而化合物 LTBI18、LTBI120和 LTBI153 不饱和程度很高导致生物利用度较差。从图3 可以看出,化合物 LTBI121 能够穿透血脑屏障,LTBI371 能通过肠道吸收。Swisse-ADME 预测的结果还表明 LTBI121 对CYP2C19、CYP2C9、CYP2D6 及 CYP3A4 具有抑制性,而 LTBI371 对所有 CYP 不具有抑制性。表明具有较强抑菌活性的化合物 LTBI371 更具有研究价值。

图4 LTBI121(A)和 LTBI371(B)的生物利用度雷达图Figure 4 The bioavailability radar of LTBI121 (A) and LTBI371 (B)
我们也利用 Molsoft L.L.C. 对 LTBI371 的成药性进行计算(图5),打分为 0.91,接近于大多数药物类药指数的中值,具有潜在的成药性。
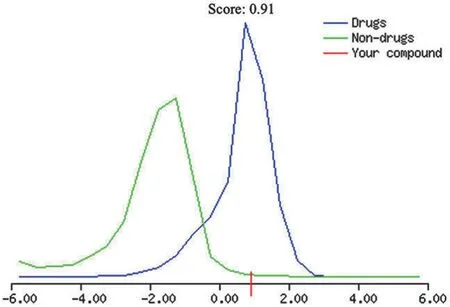
图5 LTBI371 类药性指数Figure 5 The drug-likeness score of LTBI371
3 讨论
耐药Mtb的产生和蔓延使得临床对抗结核药物的需求十分迫切,虽然全球在抗结核药物开发方面投入了大量资金和人力,但是缺口依然很大[1],开发新型抗结核药物依然是全球抗感染药物研究领域的热点之一。我们实验室通过构建分子或细胞水平的抑制剂高通量筛选模型对本单位的合成化合物库样品(约 15 万样次)进行筛选,获得了一批结构新颖的抗结核化合物[15],但没能获得更进一步的研究成果。然而,药物研发成功的案例往往能给作为后来者的我们提供思路及方向。异烟肼在沉睡近 80年之后才发现其具有良好的抗结核活性,并最终成为治疗结核病的一线用药;母核来源于抗疟药氯喹的喹诺酮类药物在抗结核领域也具有一定的研究和应用价值[17-18]。这些例子表明化合物(或药物)新活性的发现或许是药物开发研究的捷径。
本研究中我们从上海陶塑生物科技有限公司购买了具有生物活性的化合物库 L4000(含有7285 个样品),该样品库收藏了近年来新发现的具有抗肿瘤、抗菌、抗病毒以及衰老、凋亡、自噬和人体代谢调节功能的化合物。考虑到采用模式菌株进行活性样品筛选会产生不同程度的阳性样品丢失、L4000 的库容量也比较小,我们直接采用基于MtbH37Rv建立的细胞水平的抑制剂高通量筛选模型对这些样品进行筛选。通过实验的开展,我们总共得到 411 个具有抗结核活性的化合物,通过测定它们对Mtb标准菌株、临床分离的多药耐药菌株的最低抑菌浓度,总共获得了 24 个对它们都有抑制活性的化合物样品,总体阳性率为0.33%,远高于对一般样品库进行活性筛选的阳性率(0.1%)[19]。表明化合物的生物活性可能具有广泛意义,这也是老药新用开发成功概率比较高的原因。SIB(Swiss institute of bioinformatics)分子建模小组开发和维护的 SwissDrugDesign 是基于网络的综合性计算机辅助药物设计网站,我们采用其Swiss-ADME 模块对 24 个化合物进行成药性分析,包括分子量、氢键供(受)体、旋转键、脂溶性、水溶性、CYP 酶抑制活性、P-糖蛋白结合能力及可合成性等。这些参数的优劣对于合成化合物能否开发成为药物至关重要,但是这些评判标准对于天然产物并不适用[20]。本研究中,我们得到 12 个具有成药前景的抗结核化合物。但是,我们并没有对这些活性样品按照来源进行分类,这就使得部分具有研究前景的化合物可能因为成药性参数较差而被排除。因此,在后续研究中需要重点关注具有抗结核活性的天然产物。在 12 个具有成药性的活性化合物中,腺苷激酶抑制剂 LTBI371 的成药性最好,该化合物具有广泛的生物学活性[21-24],我们也首次发现了它具有抗结核活性。然而由于抗感染药物的特殊性,很多抗生素的药化性质参数根本不能满足 Lipinski、Ghose、Veber 或 Egan 等限定的成药规则。因此,后续研究中需要采用实验手段对这 24 个抗结核活性样品的毒性、药代动力学及体内、外药效学进行研究,最终从这些化合物中筛选得到药学性质优良的药物先导物。

