阿片类物质成瘾者服用美沙酮口服液的群体药动学研究
唐晓欢,王 鲸,彭 澎,孙荣基,吴天辉,邓 媛,顾 悦
(1.云南中医药大学中药学院,云南 昆明 650500;2.云南省药物依赖防治研究所,云南 昆明 650228)
据中国毒情形势报告,截至2020年底,全国现有吸毒人员180.1万,滥用阿片类毒品73.4万(占现有吸毒人员总数40.8%),海洛因滥用仍维持较大规模[1]。根据2021年世界毒品报告,美沙酮(methadone)和丁丙诺啡(buprenorphine)是最常用于治疗阿片类物质使用障碍的2种阿片类药物[2]。美沙酮为人工合成的阿片类镇痛药[3],在我国主要被用于阿片类物质成瘾的脱毒治疗[4]。2004年以来,为有效遏制艾滋病在吸毒人群中蔓延,美沙酮维持治疗在我国迅速推广。截至目前,全国已有超过700个美沙酮维持门诊,在治约10万人[5]。
在我国虽然美沙酮已被广泛用于海洛因成瘾者的脱毒和维持治疗,但缺乏对美沙酮维持治疗患者的药动学研究,相关药动学参数只能借鉴国外的研究结果,很大程度上造成了美沙酮在我国临床用药中的经验性和盲目性,使临床合理用药受到很大限制。
本研究选取部分既往研究中符合条件的受试者,回顾性收集受试者日常服用美沙酮期间的血药浓度数据及临床资料,通过非线性混合效应模型法(nonlinear mixed effects model approach,NONMEM)进行数据分析处理[6],得出美沙酮在维持治疗患者体内的群体药动学参数,包括半衰期(T1/2)、吸收速率常数(Ka)和消除速率常数(Ke)等[7],分析美沙酮维持治疗中血药浓度达到稳态人群的药动学特点及其影响因素,为我国美沙酮维持治疗的合理用药提供药理学理论基础和进行临床用药指导。
1 资料与方法
1.1 资料来源
本研究经云南省药物依赖防治研究所伦理委员会批准。回顾性收集既往研究中进行了美沙酮血药浓度检测的患者资料。纳入标准:①年龄≥18岁,保留完整知情同意书;②病例资料完整,包括身高和体重等个人基础信息、血尿常规及疾病状态、治疗药物等;③血样采集期间美沙酮剂量处于稳定期,即之前7 d内未进行剂量调整;④进行了血药浓度检测,并记录了美沙酮服用时间和血样采集时间。排除标准:①依从性不佳的患者;②无法提供知情同意书;③美沙酮服药时间不规律;④病史资料不全者。本研究去除个人标识,保护个人隐私[8-9]。
1.2 血药浓度测定方法
患者血药浓度达稳态后,分别采集患者服药后0.5 h至下一次服药之间的任意时间点的血样6 mL,准确记录服药及采血时间。用肝素锂抗凝管采集血样,并在8 h内离心分离血浆,分离的血浆2~8℃保存,采用高效液相色谱法进行美沙酮血药浓度测定。色谱条件:C18 ODS色谱柱(3.9 mm×150 mm,5 μm);流动相:乙腈-磷酸二氢钾溶液(0.033 mol·L-1)(32∶68,V/V);流速:1 mL·min-1;柱温:32℃;检测波长:220 nm;进样量:10 μL。定量范围 40~1280 μg·L-1,方法回收率为 96.98%~103.63%,日间精密度和日内精密度均<4%。
1.3 数据收集
收集患者的年龄、性别、体重、身高、美沙酮治疗情况、成瘾物质使用情况、肝肾功能、传染性疾病感染情况、联用艾滋病抗病毒药物情况等[10]。根据记录的服药及采血时间,得出与血药浓度一一对应的采血时间间隔,用于药动学参数处理。
1.4 群体药动学模型的建立
1.4.1 基础药动学模型
通过NONMEM法对临床采集的有效数据进行建模[11-12]。文献显示,美沙酮药动学特征符合一室模型[13-14],且本研究为稀疏采样,不支持复杂模型的构建,故采用一级吸收和消除的一室模型进行拟合,估算表观清除率(CL/F)、表观分布容积(V/F)和Ka等药动学参数。个体间变异采用指数模型,个体内变异采用加法、比例和比例加法混合模型拟合,取目标函数值最小的模型[15-16]。
1.4.2 固定效应模型
固定效应的选择主要考察目标函数的变化。将可能影响药动学参数的各个变量按不同模型分别加入药动学模型中对CL,V和Ka进行修正,观察对目标函数的影响[17-19]。若某一变量引入模型后,基础模型目标函数值和新目标函数值的差值>3.84或5.99(分别对应卡方自由度为1和2,P<0.05),表示该因素的加入使模型拟合优度显著改善[20]。首先采用前进法,将所有协变量加在CL,V和Ka3个变量上分别拟合,将目标函数下降值由大到小排序,取影响最大的模型作为新的模型,再加入除选定外的所有协变量进行拟合,再取影响最大的模型作为新的模型,如此直至无显著影响的协变量出现作为全量模型,最后再进行协变量逆向剔除。首先将全量模型协变量一一剔除,对剔除每个协变量引起目标函数变化进行排序,取目标函数增加最小的,考查目标函数差值是否>6.63(对应卡方分布自由度为1,P<0.01),若<6.63则剔除,作为新的模型。再在这新的模型基础上重复前一步骤,直至目标函数增加最小值均>6.63,作为最终模型[21-23]。
1.4.3 模型验证
首先通过模型诊断图法对所建模型的拟合优度进行评价。模型诊断图包括观察值和群体预测值散点图,观察值和个体预测值散点图,个体加权误差和个体预测值散点图,条件权差和采血时间点散点图,以及个体拟合图等。采用自举法(Bootstrap)对最终模型进行评估,对实验数据进行1000次可放回的重复采样获得模型参数分布的中位数和95%置信区间,并将其与原数据集获得的模型参数进行比较,若两者基本重合,提示模型较为稳健[24-25]。
2 结果
2.1 患者的数据特征
本研究共纳入150例美沙酮维持治疗患者896个血样浓度数据进行分析。患者的基本资料见表1。肝肾功能指标谷丙转氨酶异常77例,谷草转氨酶异常78例,总胆红素异常20例,血清肌酐异常4例,尿素氮异常7例。一部分患者合并使用了以下艾滋病抗病毒药物:司他夫定(stavudine)44例、奈韦拉平(nevirapine)50例、拉米夫定(lamivudine)79例、齐多夫定(zidovudine)36例和依非韦伦(efavirenz)30例,多采取三药联用的方式,其中最常用的是拉米夫定。
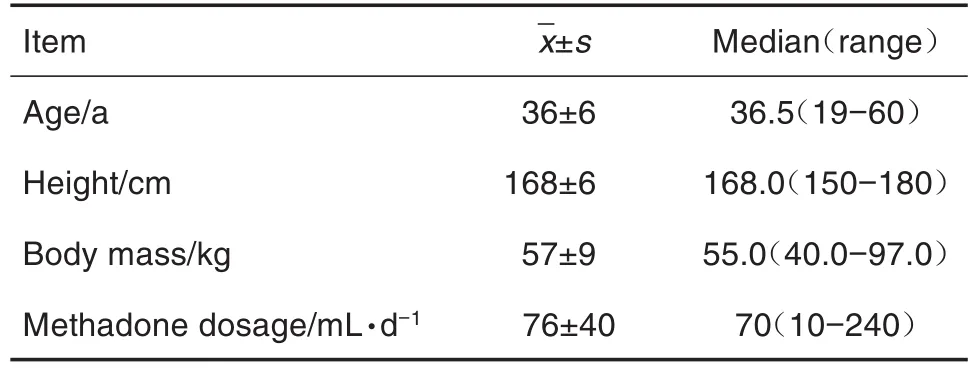
Tab.1 Demographic and clinical characteristics of patients
2.2 群体药动学模型分析
2.2.1 基础模型
个体内变异加法模型目标函数(8643)远大于比例模型(8369)和比例加法模型(8369),后两者目标函数值相同,但比例模型参数更少,因此本研究中选用比例模型。
2.2.2 固定效应选择
考察的协变量包括合并抗病毒药物、年龄、性别、身高、体重、教育程度、是否确诊艾滋病、吸烟和饮酒及谷丙转氨酶、谷草转氨酶、总胆红素、血清肌酐和尿素氮水平。协变量筛选结果为联合用药对清除率有显著影响,即在基础模型的CL上加入group,得到最终模型表达式,用于估算药动学参数。
其中i为第i名受试者;η1为个体差异,符合均数为0、方差为ω2的正态分布;CLgroup的值为-0.5418。group=1为联合用药组,group=0为单用美沙酮组,联合用药组与单用美沙酮组的CL比值为22.32/22.32×(1-0.5418)=2.18,可见联合用药导致清除率提高>2倍。联合用药对清除率的影响非常显著。
联合用药的T1/2=0.693×V/CL1=0.693×446/22.3=13.86(h);单用药的T1/2=0.693×V/CL0=0.693×446/22.32×(1-0.5418)=30.21(h)。
由最终模型得到的药动学参数及参数变异估计值见表2。所有药动学参数的标准误均低于30%,个体间变异的百分比标准误最大值为36%。当group=1时,对应联合用药组,清除率为22.3 L·h-1;当group=0时,对应单用药组,清除率为22.32×(1-0.542)=10.22(L·h-1)。

Tab.2 Parameter estimates from the final model
2.2.3 模型验证
最终模型评价图(图1)显示,群体预测值与观测值有较好的相关性,趋势线同对角线接近,模型能很好地拟合观测值。同时条件权重残差和个体预测值、时间的散点图中散点较均匀分布于0线周围,且基本在±4内,表明模型拟合较为理想。

Fig.1 Fitting evaluation diagrams of the final model.A:scattergram of observed concentration vs population predictions;B:scattergram of observed concentration vs individual predictions;C:scattergram of absolute individual weighted residual vs individual predictions;D:scattergram of weighted residual vs sampling time.
以Bootstrap法对实验数据进行重新采样1000次,对这1000个Bootstrap数据集进行拟合,结果有1个样本数据集未拟合成功,2个样本拟合参数接近边限。余下997次均拟合成功,成功率达99.7%,说明模型稳定。对997次拟合的结果进行统计,并将结果与原样本的参数估计进行比较,发现参数的估计中位数与均值相近且与原样本的参数估计值基本一致,且95%可信区间均在合理范围之内,说明该参数估计稳定可靠,受样本分布影响较小。
群体药动学结果显示,联合用药对美沙酮药动学参数CL有显著影响,对Ka和V无影响。联合用药CL为单用美沙酮的2.18倍。联合用药与单用美沙酮群体药动学参数典型值表3。联合用药Ke为0.05 h-1,单用美沙酮Ke为 0.02 h-1。联合用药T1/2为13.86 h,单用美沙酮T1/2为30.21 h。
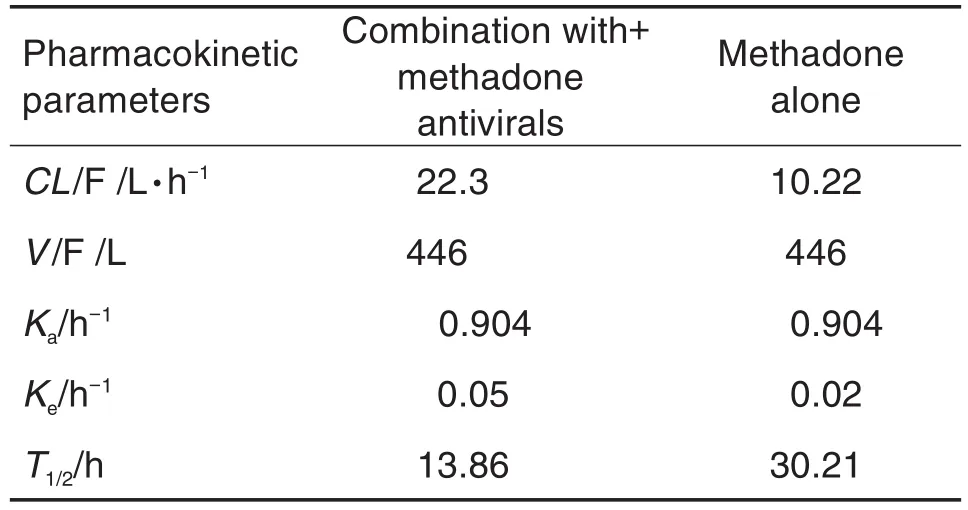
Tab.3 Typical values of population pharmacokinetic parameters for methadone alone and in combination with antivirals
美沙酮单用和与抗病毒药物联用的多次给药药时曲线的比较见图2,其中药动学参数为群体典型值,因建模用数据的给药剂量平均值约为80 mg,故以此为典型剂量。美沙酮单用和联用在开始给药时吸收相表现基本一致,但消除相差异明显,经过几个给药周期后,美沙酮单用组血药浓度明显高于联用组。
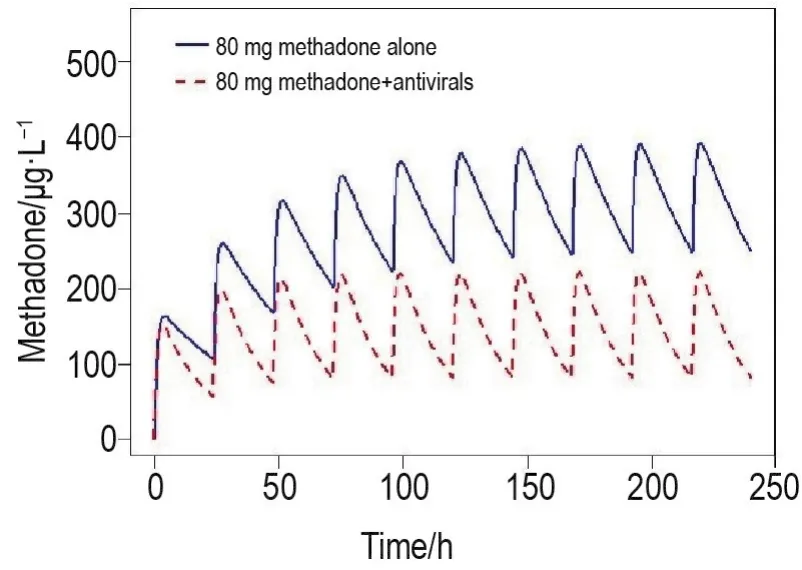
Fig.2 Plasma drug concentration-time curves of multiple administration of methadone 80 mg alone and in combination with other antivirals.The pharmacokinetic parameters were typical values of the population.
3 讨论
美沙酮是一种药动学性质高度可变的药物,日剂量和血清浓度有相当大的个体间差异,因此很难通过治疗药物监测来设计标准的给药方案[26]。美沙酮药动学-药效学关系的大部分信息来自于慢性疼痛患者和给予美沙酮单次口服剂量的健康受试者或动物研究。群体药动学研究方法虽已被证实适用于美沙酮维持治疗患者,但尚无来自大规模或多样化人群的研究[27-28]。已有研究表明,阿片类药物的药动学-药效学研究可能受到耐受性发展和交叉耐受性等因素的阻碍,所以单用药后发现的药动学-药效学关系不能充分预测连续服药后的药动学-药效学关系,且由于之前接触过阿片类药物,在停药期间药物有效性和(或)药效可能会发生改变[29-30]。因此,维持治疗的患者和单次服用患者之间的代谢特征还存在明显差异[31]。阿片类物质成瘾者长期注射使用毒品,血管坏死采血困难[5],按经典药动学研究方法难度较大,运用群体药动学方法对美沙酮维持治疗人群进行血药浓度分析具有很大优势[32]。
文献报道,美沙酮易从胃肠道吸收[33],服药后30 min可在血中检测到,4 h血药浓度达峰值[34-35],血中峰浓度可维持 2~6 h[33,36]。美沙酮治疗血药浓度为480~860 μg·L-1,中毒血药浓度为2000 μg·L-1,致死血药浓度>4000 μg·L-1[4,37]。其T1/2约15 h(10~18h),长期使用者T1/2相应延长,约25h(13~47h)[33-35]。本研究结果表明,联合用药T1/2为13.86 h,单用美沙酮T1/2为30.21 h,与文献数据存在一定差异,可能是由于美沙酮的药动学数据大部分来源于慢性疼痛患者、给予美沙酮单次口服剂量的健康受试者或动物研究,与维持治疗患者在用药剂量和时间上均有很大差异。维持治疗患者需每天规律服药,本研究中美沙酮日剂量接近80 mg,长期大量用药后会在组织中蓄积并缓慢释放,使作用持久。美沙酮的代谢还受妊娠、蛋白结合、尿pH、饮食、联用药物和肝药酶等各种因素的影响,导致个体差异较大[38];且药动学参数多为国外研究结果,也不排除存在人种差异。
本研究对象为美沙酮维持治疗中处于治疗稳定期的患者,采样点包含了吸收相、分布相和消除相,吸收相数据均为2~4 h,属于理论峰浓度时间段,结果显示浓度范围在480~860 μg·L-1的样本数为31例(占21%),另外119例(占79%)的浓度低于文献报道的 480 μg·L-1治疗浓度[38],提示美沙酮维持治疗中日常的给药量偏低,使患者的血药峰浓度未达到治疗范围;谷浓度可能更低,<50 μg·L-1则易出现戒断症状[39]。这可能与美沙酮维持治疗门诊给药多依靠患者主诉及医师经验有关,且由于治疗对象的特殊性,健康状况大多较差,且患者有时候偷吸海洛因,如用足量美沙酮则存在合并用药过量中毒风险,这也造成了医师用药时的谨慎。所以如何使患者达到有效治疗浓度,“抑制心瘾”,减少偷吸海洛因,需要门诊医师思考更为有效的治疗方式和方法。
150例样本中,119例(79%)美沙酮血药浓度低于文献报道的480 μg·L-1治疗浓度,其中有64例(54%)正在接受抗病毒治疗,而总体150例样本中只有65例正在接受抗病毒治疗,提示仅有1例联合用药者达到有效治疗浓度。揭示联用艾滋病抗病毒药物显著增高美沙酮清除率,使其代谢速度加快,更易出现血药浓度过低情况。对于这些代谢加快的患者,一般采取加大美沙酮给药剂量并缩短给药间隔的方法,但一次给足剂量则有可能出现峰浓度过高,超出治疗范围引起过量反应,分为2次给药后既能降低不良反应又保证治疗效果。

