中西医结合治疗心肾综合征的Meta分析*
徐 霞 宋庆桥 吴华芹 张并璇 李雨濛 王亚娇
(中国中医科学院广安门医院,北京 100053)
心肾综合征(CRS)是心脏和肾脏互相作用导致的一系列复杂的疾病状态[1]。Ronco等[2]根据两者发病的急、慢和先、后将其分为5型。心脏和肾脏疾病常常共同存在,一项Meta分析对80 093例心力衰竭患者随访1年发现38%具有肾损伤[3],同时有调查研究发现近800万美国人肾小球滤过率(GFR)<60 mL/min,且心肌梗死、心力衰竭等心脏因素导致死亡的风险较GFR正常者显著增加[4]。慢性肾脏病和心力衰竭的同时存在会显著增加患者的住院率和死亡率[5]。
目前由于对CRS的认识有限,发生机制了解不多,因而缺乏具有针对性的治疗措施,该病仍然是一个临床难题。CRS可归属于中医学“喘证”“水肿”“心悸”等范畴,病位在心、肾,涉及脾、肺功能失司;其病机可概括为“本虚标实”,“本虚”主要为心肾阴阳两虚,心肾不交,“标实”主要为病理产物瘀血、水湿、痰饮等的蓄积[6]。因此,临床上根据症状表现的不同,常采用益气、养阴、温阳、化痰、活血、利水等方法进行辨证治疗。既往关于中医治疗CRS临床试验的系统评价多是探讨温阳利水、益气活血等改善CRS患者的临床症状及心肾功能[7-8]。本研究纳入中西医结合治疗CRS的随机对照试验,以期正确运用辨证论治,抓住疾病关键采用适宜的方药治疗,从而取得更好的临床疗效。
1 资料与方法
1.1 文献选择 研究类型:中西医结合治疗CRS的随机对照临床研究。研究对象:原始文献中明确诊断为CRS[9],对诊断标准与疗效评定标准描述准确,年龄、性别不限。干预措施:对照组采用常规西医治疗;试验组在此基础上加用中医治疗。结局指标:有效率、心功能、肾功能评价指标和炎症因子。结局指标中必须同时具有至少一项心功能和肾功能评价指标才可纳入。排除标准:非随机对照试验、自身前后对照试验、个案报道、临床基础研究、理论探讨、综述、研究进展、细胞或动物实验等文献;诊断不明确或不符;临床数据或重要资料存在异常或缺失,无法进行数据分析的文献;重复发表的文献;无法提取或存在其他较混乱标志的文献;无必要结局指标的文献。
1.2 检索策略 检索方式为计算机及人工检索;检索时间为建库至2021年5月;检索数据库包括:中国知识基础设施工程(CNKI)、万方数据知识服务平台(Wanfang Data)、维普中文期刊服务平台(VIP)、PubMed和Webofscience数据库。检索式包括主题词和自由词,中文检索式为:(“中西医”OR“中医”OR“中药”)AND(“心肾综合征”OR“肾心综合征”)等。英文检索式为:(“Traditional Chinese Medicine”OR“Traditional Chinese Medicine”OR“Traditional Chinese Medicine”)AND(“Cardiorenal Syndrome”OR“Renal Heart Syndrome”)。
1.3 纳入文献筛选 本研究挑选2名研究人员筛选文献,采用独立筛选,交叉核对的方式,遇到分歧与第三方协商决定;筛选时首先通过NoteExpress初筛,删除重复文献;然后阅读标题和摘要,删除明显无关的文献;随后进行全文阅读确定是否纳入;最后提取入选文献的作者、年份、观察例数、性别、干预措施、疗程、结局指标等信息。
1.4 纳入文献质量评价 质量评价采用Cochrane协作网推荐的风险偏倚评估条目进行评价。
1.5 统计学处理 采用RevMan5.3软件进行统计分析。二分类变量采用比值比(OR)作为效应分析统计量,计量资料采用加权均数差(MD)或标准化均数差(SMD)为效应值,各效应值均提供其95%可信区间(CI)。应用CochraneQ进行异质性检验,I2<50%用固定效应模型,反之用随机效应模型。P<0.05认为两干预措施差异有统计学意义,进行敏感性分析,评价结果稳定性。对无法进行Meta分析的研究进行描述性分析,用漏斗图进行发表偏倚分析。
2 结 果
2.1 文献筛选流程及结果 见图1。共检出299篇文献,经过逐步筛选,最终纳入随机对照研究28篇[10-37]。
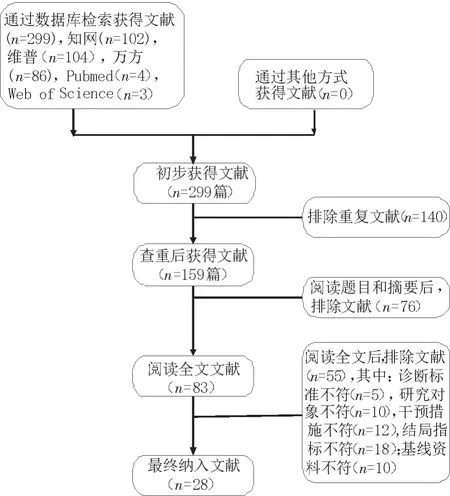
图1 文献筛选流程图
2.2 纳入文献基本特征 见表1。本研究纳入的28项随机对照试验。

表1 纳入文献基本特征
2.3 纳入文献质量评价 见图2。纳入文献中,24项提及随机分配,其余4项[13,28,33,37]中2项未提及分配方法2项按入院时间分组;2篇文献[29,32]报告了病例脱落情况及原因;23项报告了设定的结局指标,5项[14,25,29-30,32]不完整;所有文献研究方法与结果一致,未描述其他偏倚及可能来源,未提及是否采用分配隐藏、是否实施盲法。

图2 偏倚风险比例图
2.4 临床总有效率Meta分析结果 见图3。23项研究[10-18,20-21,24,26-35,37]报告了临床总有效率,共 2 027 例患者,试验组1 013例,对照组1 014例。各研究间不存在异质性(P<0.00001,I2=0%),采用固定效应模型进行Meta分析,结果试验组的临床总有效率明显高于对照组,OR=3.33,95%CI(2.62,4.22),P<0.00001。

图3 临床总有效率的森林图
2.5 对心功能影响的Meta分析 见图4~图6。22项研究[10,12,14,17,19-33,35,36,37]报告了LVEF,共1 971例患者,其中试验组986例,对照组985例。各研究存在显著异质性(P<0.00001,I2=87%),故采用随机效应模型分析,结果显示中西医结合治疗组LVEF水平优于对照组,SMD=0.96,95%CI(0.69,1.23),P<0.00001。
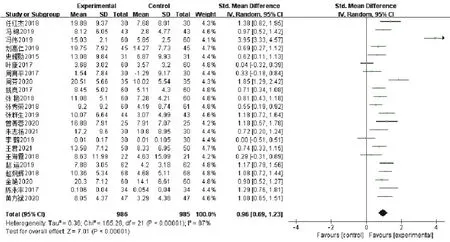
图4 对LVEF影响的森林图
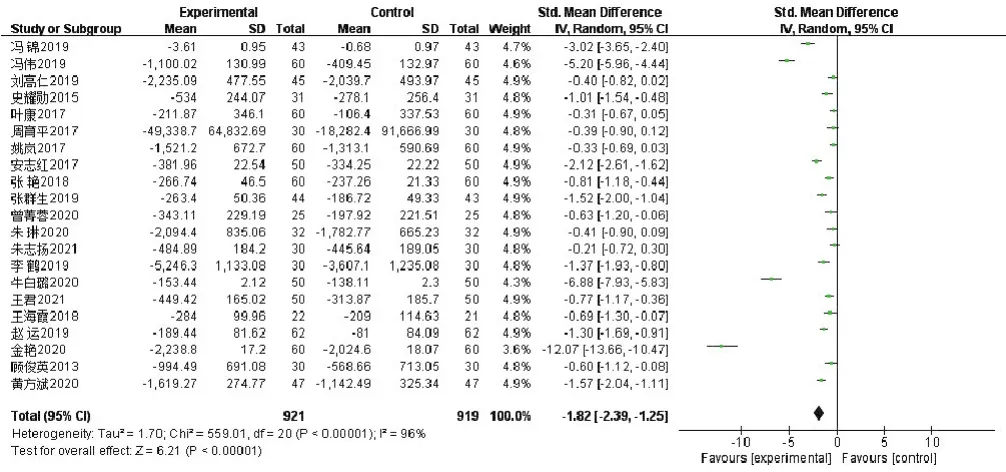
图5 对NT-proBNP/BNP影响的森林图

图6 对LVEDD影响的森林图
21项研究[10-11,13-23,25-29,31,33-34,36,37]报告了NT-proBNP/BNP,共1 840例患者,其中试验组921例,对照组919例。各研究存在异质性(P<0.00001,I2=96%),故选用随机效应模型,结果显示治疗组降低NT-proBNP/BNP 更显著,SMD=-1.82,95%CI(-2.39,-1.25),P<0.00001。
8 项[17,20-21,25,27,31,35,37]研究报告了 LVEDD 指标,包含患者772例,两组各386例。根据异质性检验结果(P<0.00001,I2=94%),选择随机效应模型,结果显示中西医结合试验组改善患者LVEDD优于单纯西药治疗组,MD=-4.65,95%CI(-6.85,-2.46),P<0.00001。
2.6 对肾功能影响的Meta分析 见图7~图10。12项研究[10,12,17,19,22,24-25,27,31-32,36-37]提到了对 Scr的影响,共纳入患者985例,治疗组493例,对照组492例。各研究存在高度异质性(I2=89%,P<0.00001),故选用随机效应模型进行分析。总体合并后治疗组降低CRS患者Scr优于对照组(Z=5.33,P<0.00001)。
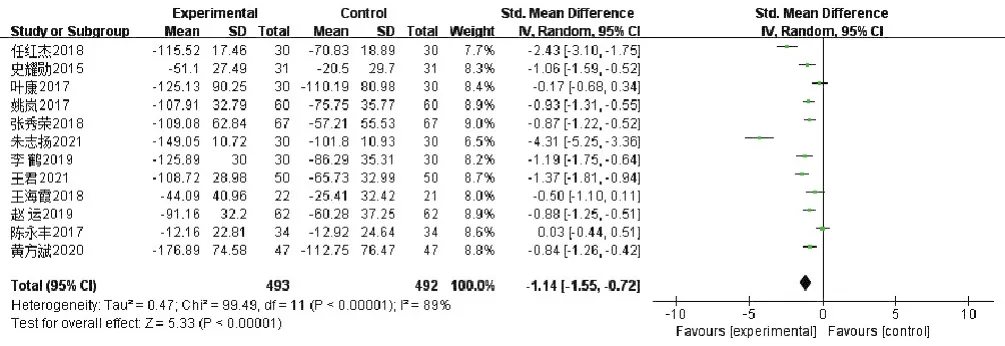
图7 对Scr影响的森林图
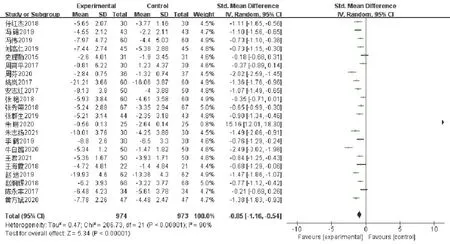
图8 对BUN影响的森林图

图9 对eGFR影响的森林图
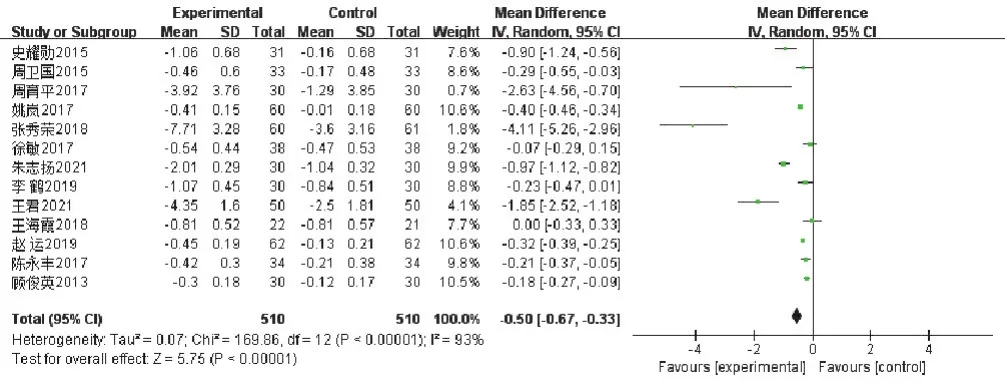
图10 对CysC影响的森林图
22 项研究[10,12,14-15,16,19,21-27,29-37]比较了两种治疗方法对BUN的影响,共纳入患者1 947例,治疗组974例,对照组973例。各研究存在高度异质性(I2=90%,P<0.00001),故采用随机效应模型。结果显示,总体合并后,SMD=-0.85,95%CI(-1.16,-0.54),差异显著(Z=5.34,P<0.00001),治疗组改善CRS患者的BUN更优。
14项研究[10-11,14,16,18-19,21-23,26-27,29,32-33]提到了对患者eGFR的影响,共纳入患者1 278例,治疗组640例,对照组638例。研究存在高度异质性(I2=91%,P<0.00001),故采用随机效应模型。结果总体合并后,MD=5.68,95%CI(3.02,8.35),说明加用中药更有助于改善eGFR(P<0.00001)。
13 项[11,13-14,18-19,22,24-25,27,31-32,36-37]研究报告了CysC,共1 020例患者,两组均510例。根据异质性检验结果(P<0.00001,I2=93%),采用随机效应模型进行Meta分析,结果显示中西医结合治疗组降低CysC优于单纯西药治疗组,MD=-0.50,95%CI(-0.67,-0.33),P<0.00001。
2.7 对炎症因子影响的Meta分析 见图11。提及对hs-CRP 影响的研究共 7 项[20-22,30-32,34],共计 606 例患者,每组303例。异质性检验提示(I2=83%,P<0.00001),故采用随机效应模型进行分析。总体合并后,MD=-0.78,95%CI(-1.20,-0.37),差异具有统计学意义(Z=3.70,P=0.0002),故中西医结合治疗组降低hs-CRP优于单纯西药治疗。
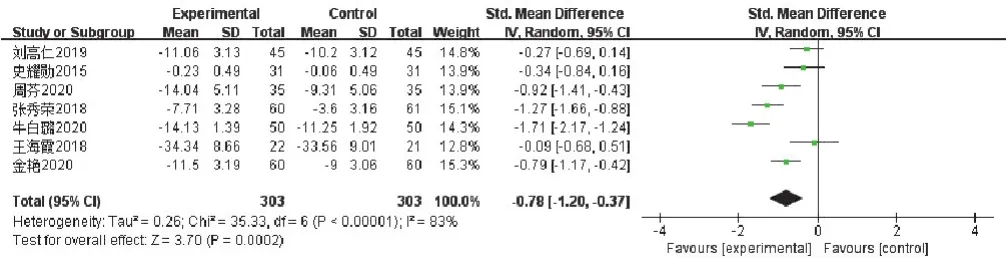
图11 对hs-CRP影响的森林图
2.8 发表偏倚分析 见图12。对以临床总有效率为结局的 23 项研究[10-18,20-21,24,26-35,37]进行漏斗图分析,显示左右不对称,提示可能存在发表偏倚。

图12 临床总有效率发表偏倚分析
3 讨 论
Meta分析结果表明:中西医结合组在提高总有效率、提高LVEF、减小LVEDD、降低NT-BNP或BNP、降低Scr、BUN、CysC和提高eGFR及改善炎症反应方面均优于单纯西药组。但是由于各个试验的条件不一致,这可能为分析研究带来异质性,因此需更大样本、高质量的随机对照试验来得到更加可靠准确的结果。
CRS发病机制可能与血流动力学改变、神经和(或)肾素-血管紧张素-醛固酮系统激活有关,局部和全身性炎症、代谢改变等也会加速HF和CKD进展[1]。因而治疗主要包括:调整血流动力学、治疗液体超负荷、肾脏替代疗法RRT、肾素-血管紧张素-醛固酮系统(RAAS)等,但临床疗效并不十分理想,对患者心肾功能保护作用并不明确[20]。
中医学中将CRS归于“喘证”“水肿”“心悸”“痰饮”进行论治,其病机主要是由于心肾阴阳两虚、心肾不交、瘀血、水湿、痰饮等有关,病位主要在心肾。心为阳脏而主神明,心之阳气推动心脏搏动、温通全身血脉、兴奋精神,以使生机不息的作用。肾阳是人生命活动的根本动力,具有促进生长发育与生殖,温煦和推动脏腑生理活动的作用。在生理状态下,心主血,肾藏精,精血同源,同时心肾阳气相温,共筑一身元阳,肾藏精、心藏神,精神互用。在病理状态下,心肾也互相影响,心病日久,心损及肾,心血瘀阻、心血不足,肾精生化不足,继而出现了心肾阳虚、水湿运化失司的表现。本研究纳入治疗CRS的清上温下,交媾阴阳,交济水火的交泰丸;温阳补元、利水消肿之温阳利水类方剂;益气升阳、祛瘀逐饮、化浊通络之通脉复力汤等文献,经系统分析得出中西医结合治疗CRS较单纯西医常规治疗取得了更显著的效果。因此临床治疗上可依据“同病异治”的原则,治疗CRS不拘泥于温阳利水益气活血的治法,根据患者的临床表现,判断其病机及证候,选择合适的治法方药进行治疗,才能取得良好的治疗效果。
本研究存在一定的局限性,从纳入文献的基本特征来看,均为单中心随机临床试验,缺乏大规模多中心随机临床试验;其次纳入研究文献质量欠佳,28篇文献均未记录分配方案隐藏,而且最后筛选后外文文献数量为0篇,且在疗程控制等方面异质性较大。最后,纳入文献中关于不良反应的记录甚少,对中药治疗CRS的安全性缺乏系统评价。
综合上述,中西医结合治疗不管是在提高临床有效率,还是改善心肾功能方面,作用都更显著。在临床中应注重运用中医辨证论治思想,根据患者的具体情况来选择治疗药物。

