急性缺血性卒中替奈普酶静脉溶栓治疗中国专家共识☆
中国医师协会神经内科医师分会脑血管病专家组
静脉溶栓是目前急性缺血性卒中(acute ischemic stroke, AIS)恢复血流灌注的最主要手段[1]。临床使用的静脉溶栓剂历经了三代药物研发:第一代以链激酶(streptokinase)和尿激酶(urokinase)为代表,此类药物在溶栓的同时,降低血液中纤维蛋白原及凝血因子,缺乏纤维蛋白特异性,易导致出血事件发生;第二代为重组组织型纤溶酶原激活剂(recombinant tissue plasminogen activator,rt-PA),具有高度的纤维蛋白特异性,是目前国际上唯一被批准用于治疗AIS的溶栓药物[2],但由于半衰期(<5 min)短[3],静脉注射后需静脉滴注维持用药;第三代主要是对第二代药物进行基因改构而获得的变异体,例如替奈普酶(tenecteplase,TNK)、瑞替普酶(reteplase,rPA)和去氨普酶(desmoteplase,bat-PA)等,药理及药代动力学特性得到进一步优化,提高了与纤维蛋白结合的特异性,又延长了半衰期。其中TNK是目前国际上AIS静脉溶栓研究的热点药物,已积累了较多临床证据,提示疗效和安全性与rt-PA类似,但半衰期(20~24 min)长[4],只需单次静脉注射给药而不必静脉点滴维持用药,使用方便。在新冠疫情流行高峰期间,由于TNK给药便捷,全球许多卒中中心已超说明书使用TNK治疗AIS[5]。我国自主研发的TNK,多项临床研究证实了其对急性心肌梗死的疗效和安全性[6-7]。2015年国家食品药品监督管理总局(China Food and Drug Administration, CFDA)批准其用于发病6 h内急性心肌梗死的静脉溶栓治疗[8],针对AIS静脉溶栓的多项临床试验也证实了其有效性和安全性[9-10],其中Ⅲ期临床试验结果已在2022年于新加坡召开的世界卒中大会(World Stroke Conference,WSC)上公布,正式论文待发表。
然而,在临床实践中如何选择和合理使用TNK治疗AIS,至今国内外尚缺乏具体指导建议。为帮助和促进临床医师合理、规范地使用第三代溶栓药物TNK,由中国医师协会神经内科医师分会牵头,组织国内脑血管病领域权威专家成立本共识制定委员会,通过系统检索 Medline、PubMed、OVID、EMBase、CNKI和万方数据库,对TNK治疗AIS研究证据进行评阅和审议,基于循证医学证据评价标准并结合中国AIS临床需求,撰写并制定本共识供临床应用参考。推荐强度和证据等级标准参考了《中国脑血管病指南制定方法及应用》[11]。本共识在国际实践指南注册与透明化平台注册(注册号:PREPARE-2022CN723)。
1 替奈普酶药理特性
TNK为rt-PA的变构体,通过取代rt-PA的三个结构位点氨基酸而来,其中103位点(T)的苏氨酸被天冬酰胺替代,通过新增一个糖基化位点延长了半衰期;117位点(N)的天冬酰胺被谷氨酰胺替换后,血浆清除率降低、半衰期延长,4个丙氨酸在296-299位点(K)取代了赖氨酸、组氨酸和2个精氨酸,提高了其对于内源性纤溶酶原激活物抑制物-1 (plasminogen activator inhibitor-1,PAI-1)的抵抗能力和对纤维蛋白结合的特异性,因而又称TNK-tPA或TNKase,简称TNK。与rt-PA相比,TNK血浆初始半衰期由短于5 min提高至约24 min,纤维蛋白特异性提高14倍[4]。用药时以无菌注射用水溶解后5~10 s内静脉注射完毕。TNK经肝脏代谢,体重和年龄明显影响其血浆分布和清除率,给药时须随体重调整剂量。TNK在2000年已被美国食品药品监督管理局(Food and Drug Administration,FDA)批准用于治疗急性ST段抬高型心肌梗死(ST-elevation myocardial infarction,STEMI)[12],随后,世界各国又广泛开展了 TNK静脉溶栓治疗AIS的临床研究。
2 替奈普酶静脉溶栓治疗急性缺血性卒中
基于国外已完成的临床研究证据,TNK主要用于AIS发病4.5 h内的静脉溶栓治疗[13-14]。《中国急性缺血性卒中诊治指南2018》[1]和美国《2019AHA/ASA急性缺血性卒中早期管理指南》[15]推荐TNK可用于轻型卒中和轻度神经功能缺损且不伴有颅内大血管闭塞的患者静脉溶栓治疗,《欧洲卒中组织(ESO)急性缺血性卒中静脉溶栓指南2021》[16]推荐用于大血管闭塞患者桥接取栓前的静脉溶栓治疗,但证据和推荐级别均不高。近年研究将TNK作为新型溶栓药物,从药物剂量、有效性和安全性等各方面,与标准剂量rt-PA静脉溶栓治疗AIS做了一系列对照研究,而且溶栓前后的管理要求和措施与rt-PA静脉溶栓一致,所得研究结果为 TNK静脉溶栓治疗AIS提供了循证医学新证据。
2.1 适应证与时间窗 目前AIS患者临床治疗中采用rt-PA静脉溶栓的时间窗通常为发病后4.5 h以内[17-18]。因此评估TNK静脉溶栓治疗AIS的临床研究,现阶段主要纳入了发病4.5 h以内的患者,并与标准剂量rt-PA进行了有效性和安全性比较。英国一项rt-PA对比TNK卒中溶栓评估研究(Alteplase-Tenecteplase Trail Evaluation for Stroke Thrombolysis,ATTEST)评价 0.25 mg/kg TNK 和0.9 mg/kg rt-PA在AIS发病4.5 h内(基线年龄中位数71岁,NIHSS评分中位数11~12分)的安全性和有效性,最终104例入组患者中,71例(TNK组35例和rt-PA组36例)达到了主要终点,两组挽救半暗带的比例基本一致(TNK组68%vs.rt-PA组68%,平均差异1.3%,95%CI: 9.6~12.1,P=0.81)。两组人群症状性颅内出血(symptomatic intracranial hemorrhage,sICH)发生率和总颅内出血事件无统计学差异[13]。另一项加拿大开展的TNK对比rt-PA静脉溶栓治疗AIS研究(Alteplase Compared to Tenecteplase in patients with acute ischemic stroke, AcT),在1600例发病4.5 h以内AIS患者(基线年龄中位数74岁,基线NIHSS评分中位数为9.5分)中,采用前瞻性、随机、开放标签和盲法结局评价的方法,对比0.25 mg/kg TNK与0.9 mg/kg rt-PA静脉溶栓治疗AIS的有效性和安全性,结果表明90~120 d mRS为0~1分的比例TNK组36.9%不劣于rt-PA组34.8%(未调整风险差异2.1%,95%CI: 2.6~6.9);安全性分析显示,TNK组溶栓后24 h内sICH发生率为3.4% (27/800),与rt-PA组的3.2%(24/763)比较,差异无统计学意义(95%CI: -1.5~2.0),表明TNK 0.25 mg/kg治疗效果不劣于rt-PA 0.9 mg/kg,且安全性相当[19]。对发病4.5 h内的AIS患者,使用TNK与rt-PA静脉溶栓具有类似获益和安全性。
此外,TNK由于使用方便,在院前急救方面也开展了研究。一项比较在救护车上TNK与rt-PA溶栓疗效的临床研究(Tenecteplase versus Alteplase for Stroke Thrombolysis Evaluation trial in the Ambulance,TASTE-A),将发病4.5 h内且符合rt-PA溶栓治疗条件的104例AIS患者(基线年龄中位数为73岁,基线NIHSS评分中位数8分),在配备车载CT的救护车(移动卒中单元)上,随机接受0.25 mg/kg TNK 或0.9 mg/kg rt-PA静脉溶栓治疗,然后送至卒中中心进行后续影像检查和治疗,主要终点为到院时CT灌注成像评估的低灌注体积。结果发现TNK组低灌注体积为12 mL(中位数),显著小于rt-PA组的35 mL(中位数,P=0.003)。在安全性方面,两组均没有发生sICH,TNK组90 d死亡率为9%(5/54),与rt-PA组10%(5/50)比较没有统计学差异[20]。提示TNK凭半衰期长和单次静脉给药的特点,在卒中院前静脉溶栓中比rt-PA更具优势,但其远期临床预后仍需更多大样本量临床研究加以验证。
中国开展的前瞻性、随机、开放标签、盲法结局评价的TNK Ⅱ期多中心临床研究(Tenecteplase Reperfusion therapy in Acute ischemic Cerebrovascular Events, TRACE),入组240例发病3 h内的AIS患者(年龄≥18岁,基线NIHSS评分5~12分),结果发现,0.1 mg/kg、0.25 mg/kg和 0.32 mg/kg TNK 与0.9 mg/kg rt-PA 在14 d时 NIHSS改善率分别为63.3%、77.2%、66.7% 和 62.7%,差异无统计学意义;溶栓后36 h内sICH发生率也无统计学差异。提示TNK可能与rt-PA静脉溶栓具有相似的安全性,TNK 0.25 mg/kg剂量组的早期神经功能改善可能更明显[10]。后续在中国开展的随机、开放标签、盲法评价结局、非劣效设计的Ⅲ期多中心临床试验(Tenecteplase Reperfusion therapy in Acute ischaemic Cerebrovascular Events-Ⅱ,TRACE Ⅱ)中,纳入1430例(基线NIHSS评分5~25分)发病4.5 h内的AIS患者,使用0.25 mg/kg TNK对比0.9 mg/kg rt-PA。结果发现TNK的主要疗效终点90 d mRS评分0~1分的受试者比例为62.7%(421/671,95%CI:58.96~66.41),非劣于 rt-PA 组 59.2%(380/642,95%CI:55.28~63.02)。该结果已在2022年在新加坡召开的世界卒中大会(WSC)公布[21]。该研究评价了在中国卒中患者人群中,使用0.25 mg/kg TNK对比标准剂量rt-PA静脉溶栓的安全性和有效性,结果与国际多项研究一致。
另外,对于大血管闭塞且发病6 h内的卒中患者,使用TNK替代rt-PA静脉溶栓是否能获得更好的再灌注水平和血管再通率?澳大利亚的一项TNK对比rt-PA的ⅡB期临床试验 (a randomized trial of Tenecteplase versus Alteplase for Acute Ischemic Stroke,TAAIS),将75例发病6 h以内影像评估为大血管闭塞且存在灌注不匹配的AIS患者(基线NIHSS评分均数为14分),分别接受TNK 0.1 mg/kg或0.25 mg/kg或rt-PA 0.9 mg/kg静脉溶栓治疗,以24 h再灌注率和24 h NIHSS评分作为主要终点,结果显示24 h后TNK组再灌注率为79.3%而 rt-PA组为55.4%(P=0.004); TNK组24 h NIHSS评分下降8分,而 rt-PA组下降3分(P<0.001),其中TNK 0.25 mg/kg组各项功能结局最佳,安全性方面各组无明显差异[22]。我国开展的多模式影像指导下扩大时间窗溶栓的安全性及有效性研究——替奈普酶治疗超时间窗急性缺血性卒中大血管闭塞患者的前瞻性、多中心、随机、开放标签、单盲(评估者盲)、探索性临床试验(CHinese Acute issue-Based imaging selection for Lysis In Stroke -Tenecteplase,CHABLIS-T),利用多模式CT影像筛选发病4.5~24 h,或发病时间不明但距最后功能正常24 h内的大血管闭塞或重度狭窄且存在灌注影像不匹配的AIS患者(年龄≥18岁,基线NIHSS评分不限),使用TNK治疗,以早期再灌注且未发生sICH作为主要终点,发现对于发病4.5~24 h的伴大血管闭塞和缺血半暗带的AIS患者,使用0.25 mg/kg或0.32 mg/kg TNK进行静脉溶栓均安全且初步有效,其中TNK 0.25 mg/kg组疗效更佳。该研究结果2022年在美国召开的国际卒中大会(International Stroke Conference,ISC)上公布[23]。随着超时间窗溶栓循证证据积累,TNK有望在影像技术的辅助下,将卒中溶栓治疗窗口期从4.5 h延长至24 h,更大规模的临床试验正在进行中。
醒后卒中约占卒中患者人群14%~27%,由于卒中发病时间不明,患者通常难以按照现有时间窗概念采取静脉溶栓治疗[24]。一项TNK治疗醒后缺血性卒中的研究(Tenecteplase in Wake-up Ischemic Stroke Trial,TWIST)采用随机、开放标签、盲法评价结局的方法,在醒后4.5 h内基于CT平扫结果给予溶栓治疗[25]。研究纳入578例患者(基线 NIHSS评分3~25分,中位数6分),比较TNK 0.25 mg/kg静脉溶栓和标准治疗(不给予静脉溶栓,但允许血管内治疗)的疗效和安全性,以90 d mRS位移分析作为主要终点,但因样本量较小且对照组有更多的患者接受了血管内治疗,最终两组90 d mRS位移分析无统计学差异(校正OR=1.18,95%CI:0.88~1.58,P=0.27),两组的安全性终点也无统计学差异,TNK组的sICH比例在数值上高于对照组(3.1%vs.1.0%,P=0.09)。该研究结果在2022年法国举办的欧洲卒中组织大会(European Stroke Organization Conference,ESOC)上公布[26]。提示在醒后卒中患者中,采用TNK 静脉溶栓治疗的获益仍需进一步研究。
推荐意见:
①发病4.5 h内符合rt-PA静脉溶栓适应证的AIS患者,静脉注射TNK有效且安全性好(I级推荐,A级证据)。
②TNK静脉溶栓治疗AIS前后的管理措施与rt-PA静脉溶栓相同(I级推荐,A级证据)。
③ 在移动卒中单元院前静脉溶栓治疗AIS,可使用TNK静脉注射(Ⅱ级推荐,B级证据)。
④对发病4.5~24 h,或起病时间不明、但距离最后正常时间小于24 h,伴有大血管闭塞且存在灌注不匹配的AIS患者,TNK静脉溶栓治疗的有效性和安全性有待进一步研究证实(Ⅲ级推荐,C级证据)。
2.2 静脉溶栓桥接血管内取栓 由于TNK给药方式便捷,在桥接取栓时可能具有一定优势。血管内取栓前TNK对比rt-PA静脉溶栓的多中心随机对照研究(Tenecteplase versus Alteplase before Endovascular Therapy for Ischemic Stroke,EXTEND-IA TNK)的第一部分,纳入202例拟行血管内治疗、发病4.5 h内伴颈内动脉、基底动脉或大脑中动脉闭塞患者(卒中前mRS≤3分,无年龄上限,NIHSS评分不限,无静脉溶栓禁忌症),随机给予0.25 mg/kg TNK或0.9 mg/kg rt-PA静脉溶栓,然后以基线DSA再灌注率或血栓消除作为主要终点,0.25 mg/kg TNK使大血管闭塞患者获得再灌注的比例是rt-PA的2倍(22%vs.10%,P=0.002),各组都有1% sICH发生率[14]。随后ALEMSEGED等[27]将基底动脉治疗 (Basilar Artery Treatment and MANagement,BATMAN)登记研究和EXTEND-IA的TNK试验数据进行汇总分析后发现,与0.9 mg/kg rt-PA相比,取栓前接受0.25 mg/kg或0.4 mg/kg TNK静脉溶栓的发病4.5 h内基底动脉闭塞患者,动脉穿刺时间更短,且再通率更高。EXTEND-IA TNK第二部分研究目的是探索TNK桥接血管内治疗AIS的最佳剂量。研究纳入了300例大血管闭塞AIS患者,随机给予TNK 0.25 mg/kg 或0.4 mg/kg,同样以基线DSA再灌注率或血栓消除作为主要终点,结果显示TNK 0.4 mg/kg与0.25 mg/kg两组再灌注率相同(19.3%vs.19.3%,P=0.89),sICH发生率数值上增加,但无统计学差异(4.7%vs.1.3%,P=0.12)[28]。提示TNK 0.4 mg/kg相较于0.25 mg/kg,未能提高再灌注率,但可能增加出血风险。一项前瞻性队列研究将接受TNK治疗卒中患者(n=234)与rt-PA治疗者(n=354)进行比较,TNK转运到动脉穿刺的时间相对于rt-PA组节省了45 min[29]。可见,对于拟采用静脉溶栓桥接血管内取栓的AIS患者,采用0.25 mg/kg TNK静脉溶栓可能优于标准剂量rt-PA。
推荐意见:
对于发病4.5 h内伴有大血管闭塞并拟行桥接取栓的AIS患者,0.25 mg/kg TNK较标准剂量rt-PA静脉溶栓显著提高再灌注率,并缩短动脉穿刺时间(Ⅱ级推荐,B级证据)。
2.3 剂量选择 在TNK剂量选择方面,目前国际上普遍以0.1~0.4 mg/kg(一般采用0.25 mg/kg、最大剂量不超过25 mg,或0.4 mg/kg、最大不超过40 mg)单次静脉注射治疗AIS开展临床研究。一项多中心、无对照、剂量递增、Ⅱ期临床试验(Tenecteplasetissue-type plasminogen activator Evaluation for Minor ischemic stroke with Proven Occlusion,TEMPO-1),纳入了50例发病12 h内轻型卒中(NIHSS≤5分)伴有颅内大血管闭塞的患者,随机接受0.1 mg/kg或0.25 mg/kg TNK,结果显示0.25 mg/kg比0.1 mg/kg组再通率更高[30]。挪威替奈普酶卒中试验(NOR-wegian TEnecteplase Stroke Trial, NOR-TEST)是一项Ⅲ期、随机、开放标签、盲法评价结局、优效性设计临床试验,在挪威13家中心纳入了1100例发病4.5 h内和醒后卒中症状出现在4.5 h内以及适合桥接取栓的急性卒中患者(基线NIHSS评分中位数为 4),随机给予0.4 mg/kg TNK或标准剂量rt-PA溶栓,以90 d mRS 0~1分作为主要终点,因入组的患者症状较轻,且17.3%患者最终诊断是类卒中,7.3%患者最终是短暂性脑缺血发作,导致研究样本量低于预期,最后两组主要终点无统计学差异(64%vs.63%,P=0.52),未能证实优效或非劣效,两组sICH发生率相仿(3%vs.2%,P=0.70)[31]。新近发表的NOR-TEST 2 A部分是一项Ⅲ期、随机、开放标签、盲法评价结局、非劣效性设计临床试验,旨在明确0.4 mg/kg TNK与0.9 mg/kg rt-PA在中重度卒中(基线NIHSS≥6分,发病4.5 h内)患者中的疗效和安全性。该研究在挪威11家中心纳入216例患者,发现0.4 mg/kg TNK组sICH发生率明显高于0.9 mg/kg rt-PA组,0.4 mg/kg TNK组90 d mRS 0~1分的比例(32%)低于0.9 mg/kg rt-PA 组( 51%,P=0.0064),任何颅内出血和3个月死亡率均显著高于rt-PA,试验提前中止。提示TNK 0.4 mg/kg安全性差,可能需要降低用药剂量[32]。结合TAAIS研究以及我国开展的TRACE和CHABLIS-T研究结果,提示TNK 0.25 mg/kg(最大剂量不超过25 mg)是安全有效的,0.4 mg/kg疗效不优于0.25 mg/kg,反而增加出血风险,而0.25 mg/kg比0.1 mg/kg有更好的血管再通效果。EXTEND-IA TNK研究显示,静脉溶栓桥接血管内取栓时,TNK剂量为 0.25 mg/kg和0.4 mg/kg的再灌注率相似,但前者安全性更好。因此,对于符合rt-PA静脉溶栓适应证的AIS患者,静脉注射0.25 mg/kg TNK能获得与标准剂量rt-PA类似的疗效和安全性。
推荐意见:
AIS静脉溶栓推荐使用TNK剂量为0.25 mg/kg静脉注射,最大剂量不超过25 mg(I级推荐,A级证据)。
2.4 安全性 静脉溶栓药物均可能增加出血风险,sICH是导致AIS静脉溶栓治疗早期死亡的主要原因,目前已有多个临床研究对sICH风险进行了评价(表1),发现0.25 mg/kg TNK与标准剂量rt-PA的sICH风险类似。一项纳入4个随机对照临床试验、共433例大血管闭塞卒中患者的meta分析显示,不同剂量的TNK与标准剂量rt-PA,在sICH及3个月全因死亡率方面均无显著差异[33]。另一项纳入6项临床研究、共1820例患者的meta分析显示,不同剂量TNK与标准剂量rt-PA在3个月sICH发生概率之间未发现统计学差异(粗OR=0.97,95%CI: 0.44~2.16)[34]。但 NOR-TEST 2 A研究发现0.4 mg/kg TNK的颅内出血发生率、3个月死亡率均显著高于标准剂量rt-PA,EXTEND-IA TNK 研究和TRACE研究也显示TNK 0.25 mg/kg组的sICH发生率要显著低于0.4 mg/kg组,AcT研究和TRACE Ⅱ研究显示0.25 mg TNK在安全性方面(sICH发生率或死亡)与标准剂量rt-PA没有差异。

表1 症状性颅内出血发生率汇总表
推荐意见:
TNK 0.25 mg/kg与标准剂量rt-PA静脉溶栓治疗AIS的安全性相似,未增加颅内出血风险(A级证据)。
3 总结与展望
目前TNK静脉溶栓治疗AIS已经积累了大量的证据,包括TAAIS、ATTEST、NOR-TEST、EXTEND-IA TNK和 AcT等研究。这些研究表明,TNK疗效不逊于rt-PA,且可能具有更高地安全性,在大血管闭塞患者中可能实现更快更完全地再灌注,尤其TNK单次静脉注射的给药方式,方便快捷,适合转运患者,缩短静脉溶栓至股动脉穿刺时间,显示了良好的应用前景。表2列举了目前注册在研(https://clinicaltrials.gov/)的多项Ⅱ和Ⅲ期随机对照临床试验以及真实世界研究,包括:①标准时间窗内研究,TASTE(ACTRN12613000243718)、ATTEST-2(NCT02814409)等将为TNK在发病4.5 h内AIS中的应用提供更高级别的证据;②超时间窗研究,CHABLIS-TⅡ(NCT04516993)、TRACE Ⅲ(NCT05141305)与 TIMELESS(NCT03785678)、ETERNAL-LVO(NCT04454788)等将为 TNK超时间窗溶栓提供重要证据;③血管内治疗研究,DIRECT-TNK(NCT05199194)和 BRIDGE-TNK(NCT04733742)等将为其在桥接取栓治疗中提供进一步高质量证据;④后循环静脉溶栓研究,POST-ETERNAL(NCT05105633)为基底动脉闭塞卒中患者TNK静脉溶栓治疗提供数据。作为新一代溶栓药物,TNK便捷的给药方式及优越的药理学特性,使其成为目前更具前景的一线溶栓药物。期待更多的临床研究能为TNK静脉溶栓治疗AIS提供更确凿的证据,也期待更多新型溶栓药的研发为AIS的救治提供更有力手段。

表2 在研和拟启动的TNK随机对照临床试验(来源自clinicaltrials.gov)

续表
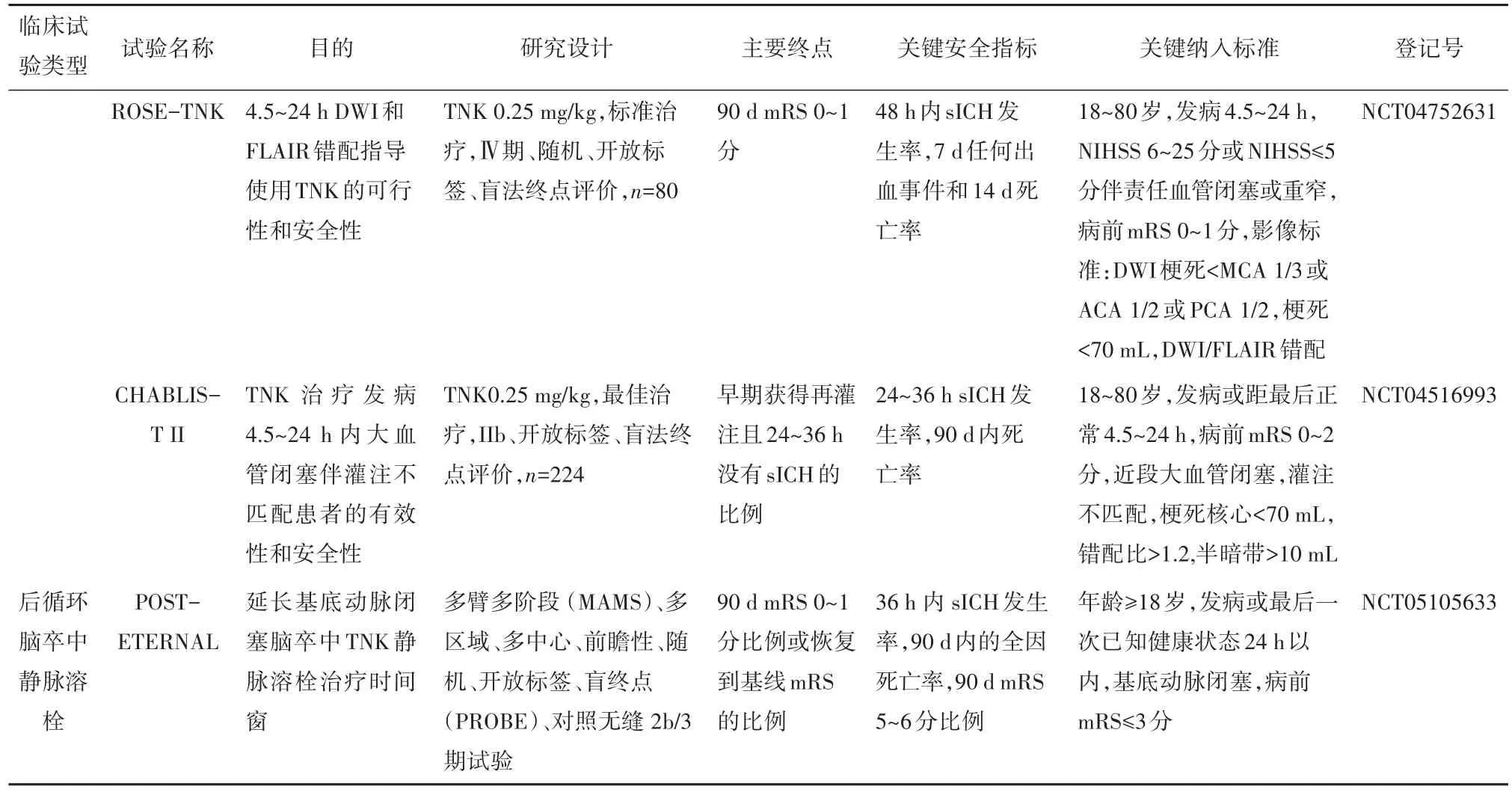
续表
编写专家组成员(按姓名笔划排序):
于生元(解放军总医院第一医学中心神经内科医学部)、马建华(新疆医科大学第一附属医院)、马桂贤(广东省人民医院)、马爱军(青岛大学附属医院)、王伟(华中科技大学同济医学院附属同济医院)、王满侠(兰州大学第二附院)、文国强(海南省人民医院)、田成林(解放军总医院第一医学中心)、成江(宁夏医科大学总医院)、朱润秀(内蒙古自治区人民医院)、刘芳(中国医科大学附属第一医院)、刘俊艳(河北医科大学第三医院)、刘竞丽(广西医科大学附属第一医院)、刘尊敬(北京大学人民医院)、米东华(首都医科大学附属北京天坛医院神经病学中心)、许予明(郑州大学第一附属医院)、李长清(重庆医科大学附属第二医院)、李常新(山西医科大学第一医院)、李新(天津医科大学第二医院)、杨弋(吉林大学第一医院)、杨清武(陆军军医大学新桥医院)、吴波(四川大学华西医院)、吴钢(福建医科大学附属第一医院)、余剑(中山大学附属第一医院)、谷文萍(中南大学湘雅医院)、宋水江(中南大学湘雅医院)、宋海庆(首都医科大学宣武医院)、张拥波(首都医科大学北京友谊医院)、张忠玲(哈尔滨医科大学附属第一医院)、张莉莉(陆军军医大学第三附属医院)、张清秀(南京大学医学院附属鼓楼医院)、陆正齐(中山大学附属第三医院)、陈会生(沈阳军区总医院)、陈晓春(福建医科大学附属协和医院)、周志明(皖南医学院弋矶山医院)、郑昆文(云南省第一人民医院)、屈新辉(江西省人民医院)、赵玉华(西藏自治区人民医院)、胡波(华中科技大学同济医学院附属协和医院)、侯倩(青海省人民医院)、党超(中山大学附属第一医院)、秦新月(重庆医科大学附属第一医院)、徐安定(暨南大学附属第一医院)、徐运(南京大学医学院附属鼓楼医院)、郭毅(深圳市人民医院)、资文杰(陆军军医大学新桥医院)、曹勇军(苏州大学附属第二医院)、龚涛(北京医院)、彭斌(中国医学科学院北京协和医院)、董强(复旦大学附属华山医院)、程忻(复旦大学附属华山医院)、曾进胜(中山大学附属第一医院)、谢鹏(重庆医科大学附属第一医院)、楚兰(贵州医科大学附属医院)、蔡坚(上海交通大学医学院仁济医院)、魏东(西京医院神经科)、魏微(解放军总医院第七医学中心)

