AECOPD患者血浆中性粒细胞水平与住院时间的关系
景琴 侯琳琳 付爱双 闵沛 刘洋 孙晔 戈艳蕾
华北理工大学附属医院呼吸内科 河北唐山 063000
慢性阻塞性肺疾病(COPD)是老年人呼吸系统常见的疾病。根据全球慢性阻塞性肺疾病行动计划(GOLD) 2020年报告,COPD是全球发病率和死亡率最高的肺部疾病形式[1-2],是一种异质性疾病,其特征为气道和肺部对有害颗粒或气体的慢性炎症反应增强,严重危害公共健康,给家庭和社会带来沉重的经济负担[3],是一个全球性的医疗问题。预测2030年COPD将成为全球第三大死亡原因[4]。在发达国家,发展为COPD的最大风险因素是吸烟,而室内污染物是发展中国家的主要致病原因。中国>60岁人群的患病率高达13%~30%;且随着老龄化社会的到来,发病率还将持续上升[5]。COPD急性加重(AECOPD)是本病自然发展的一部分[6],病因主要是以中性粒细胞(NEU)为主的病毒和细菌感染的潜在炎症,但也有10%~25%的病因以嗜酸性粒细胞 (EOS)为主[7]。AECOPD表现为COPD临床症状恶化,包括呼吸困难增加、执行日常任务能力降低、痰量及咳嗽增加、高热等[8]。AECOPD与全身和气道炎症反应增加有关,炎症反应加重患者的临床症状、降低其生活质量和肺功能,需要住院治疗[8],同时造成更大的社会经济负担并加速疾病进展。COPD患者的治疗费用与疾病严重程度具有较强相关性,住院费用在直接治疗成本占比很高,患者住院时间(LHS)延长则增加疾病控制的成本[9]。
气道炎症的急性加重因个体体质而异。少数患者气道炎症加重与嗜酸性气道炎症有关。既往研究表明,外周血EOS计数是EOS相关AECOPD的替代生物标志物[10],可作为AECOPD患者LHS的预测因子。同时,相当比例的COPD病情恶化表现为NEU 气道炎症[11]。研究表明,NEU是COPD患者肺功能持续下降的关键免疫反应调节因子。当NEU被激活时,会释放出一些蛋白水解物酶,如弹性蛋白酶和基质金属蛋白酶,有利于肺实质的渐进破坏和刺激黏液的分泌,促进了肺气肿的发展。气道NEU增多与肺功能下降相关[12]。COPD患者的血液、痰液和支气管肺泡灌洗液(BAL)分析显示,血液循环和外周气道中NEU数量增加。此外,吸烟等外部因素刺激白细胞介素-8和干扰素-α的分泌,这反过来又促进了中性粒细胞炎症、免疫抑制加重[13]。然而,NEU是否是AECOPD患者LHS的主要或独立影响因素尚不清楚。
本研究旨在评估NEU与AECOPDH患者LHS之间是否存在相关性。
1 资料与方法
1.1研究对象 华北理工大学附属医院2018年1月~2019年12月收治的AECOPD患者548例。男333例,女215例,平均年龄69.85岁。纳入标准:①符合GOLD制定的COPD诊断标准[2];②因COPD急性加重住院;③年龄>40岁。排除标准:血液病、活动性肺结核、肺栓塞、尿毒症、晚期肺癌、顽固性心力衰竭、风湿性疾病、放疗、免疫抑制剂、移植及病历和辅助检查不完整者。本研究符合《赫尔辛基宣言》,并获得华北理工大学附属医院伦理委员会批准。
1.2资料收集 收集548例AECOPD患者的一般临床资料,包括性别、年龄、吸烟史、饮酒史、体质量指数(BMI)、高血压、糖尿病、LHS。记录入院时收缩压(SBP)和舒张压(DBP)及白细胞(WBC)、EOS、NEU、淋巴细胞(LYM)、中性粒细胞与淋巴细胞比率(NLR)、甘油三酯(TG)、低密度脂蛋白胆固醇(LDL-C)、肌酐(Cr)、前白蛋白(PALB)等实验室检测指标。
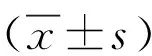
2 结果
2.1患者临床特征和实验室数据 见表1。

表1 548例AECOPD患者一般临床特征
2.2影响LHS的单因素分析 单因素分析显示BMI、WBC、NEU、LYM、NLR、TG、Cr、PALB与LHS相关(P<0.05) ,其中WBC、NEU、NLR与LHS呈正相关,BMI、LYM、TG、Cr、PALB与LHS呈负相关。见表2。
2.3多因素回归分析LHS与NEU水平的独立相关性 多因素回归分析结果显示年龄、性别、舒张压、BMI、LYM、NLR、TG、LDL-C、Cr、PALB、糖尿病符合筛选标准。在对模型I(根据年龄和性别调整) 和模型II(根据年龄、性别、DBP、BMI、LYM、NLR、TG、LDL-C、Cr、PALB和糖尿病调整)的潜在混杂因素进行调整后,分析发现LHS随着NEU水平的增加而增加。此外,以NEU最低四分之一作为参照组,Q2、Q3和Q4的β值(95%CI)分别为-0.49(-1.75~0.78)、1.01(-0.33~2.34)和1.54 (-0.20~3.29),P均<0.05。见表3。
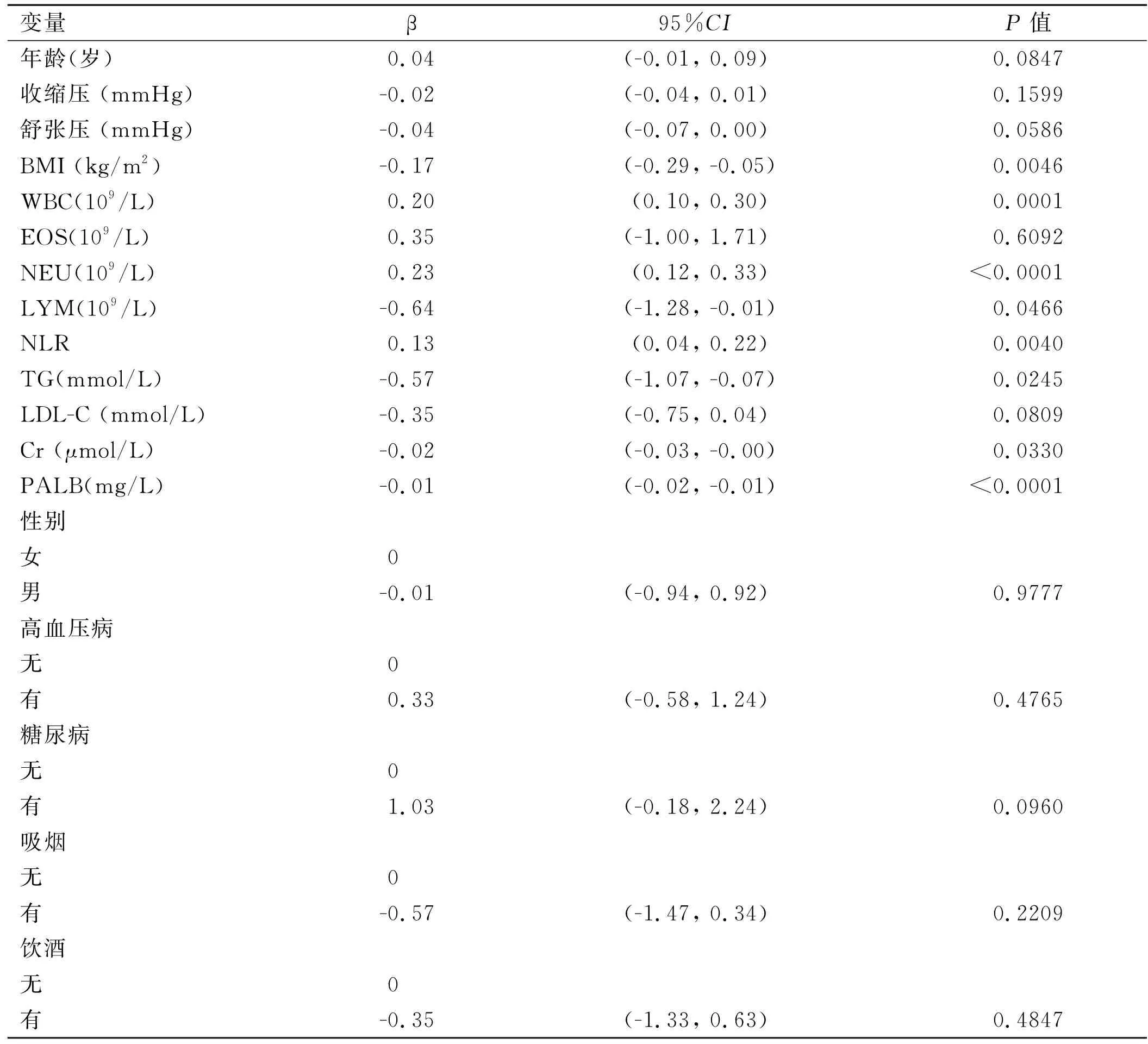
表2 影响LHS的单因素分析
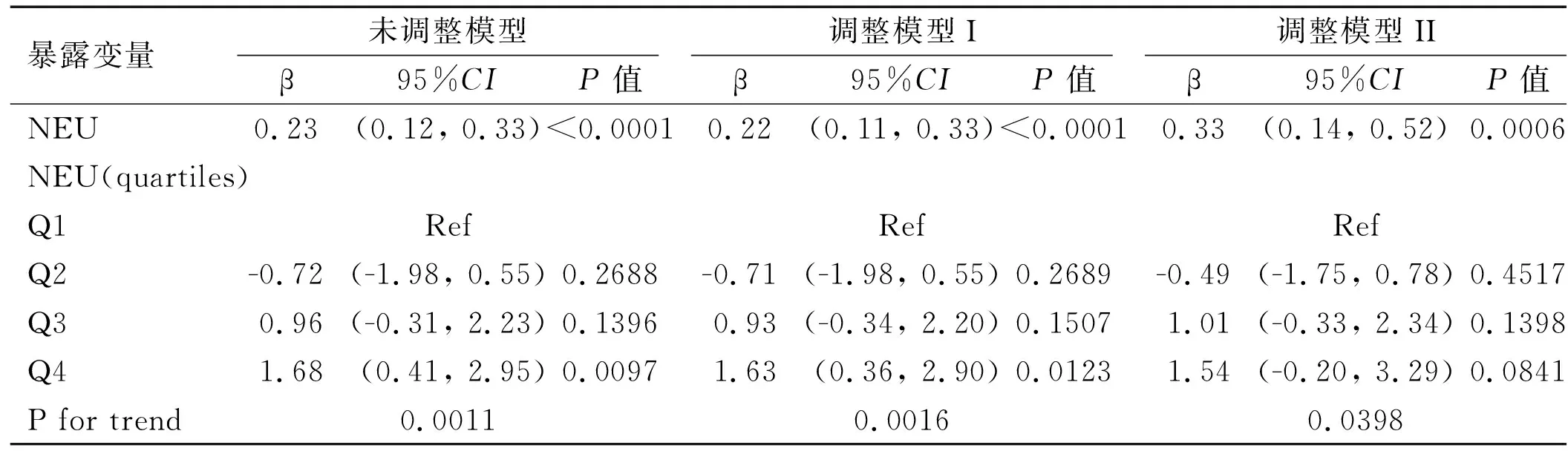
表3 多因素回归分析LHS与NEU的独立相关性
2.4各亚组NEU水平对LHS的影响 在亚组分析中,性别、年龄、BMI、高血压、糖尿病、吸烟、饮酒、LDL-C差异均无统计学意义(P> 0.05)。结果在调整了潜在的混杂因素后,多元回归分析显示LHS随着NEU的增加而增加。见表4。
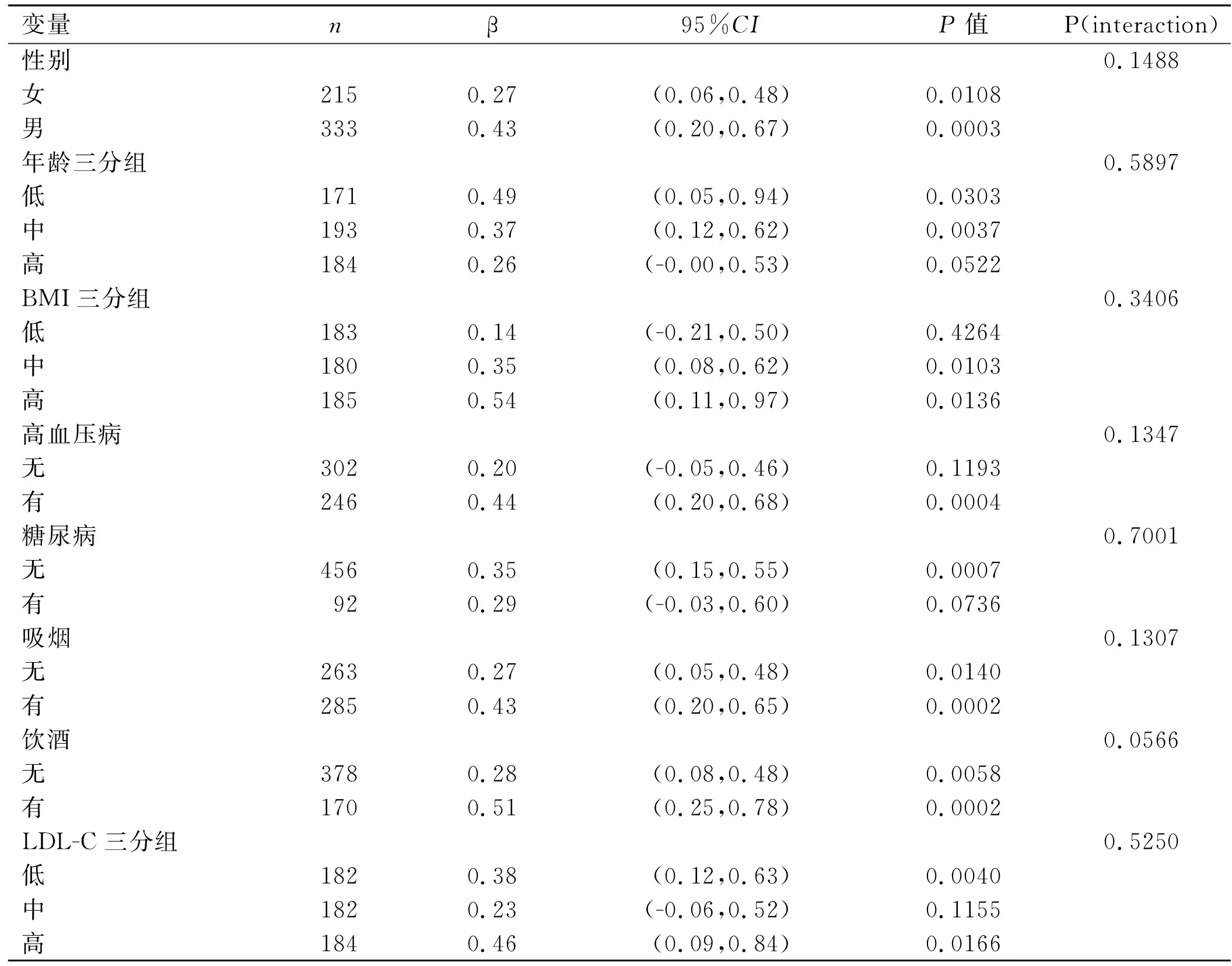
表4 各亚组NEU水平对LHS的影响
3 讨论
AECOPD是COPD发展过程中常见的事件,是COPD患者的主要健康问题,是影响住院率和死亡率的重要原因。AECOPD的出现可能导致身体炎症反应加重,引起血液循环中感染指标的变化,包括红细胞沉降率(ESR)、C反应蛋白(CRP)、WBC计数和中性粒细胞百分比(NE%)等,这些炎症指标的变化对于AECOPD的诊断和治疗至关重要[14]。需要住院治疗的急性加重期患者其治疗费用很大一部分取决于LHS,故本次研究LHS的影响因素可以提高资源利用和效率。大量研究表明,AECOPD患者LHS长短与多种因素有关。Wang Y等报道了心力衰竭、糖尿病、中风、高二氧化碳分压和低血清白蛋白水平与LHS相关[15]。Quintana JM等报道了LHS与基线呼吸困难指数、体力活动水平和医院变异性相关[16]。Wong AW等认为婚姻状况等社会因素与LHS有关[17]。其他因素包括肺心病、BMI、MRC评分和呼吸频率[18]。这些发现是AECOPD患者LHS的定性预测因子,尚无定量指标描述与LHS相关。目前普遍认为AECOPD最常见的病因是病毒和细菌感染,而15%~20%是由其他微生物或未指定的原因引起的,它们刺激促炎因子和趋化因子的产生,进而导致NEU募集和急性炎症[19]。在COPD急性加重期间,气道分泌物和支气管活检标本中观察到NEU增加。空气污染是AECOPD的一个常见诱因。研究表明,健康人暴露在柴油尾气颗粒环境中,通过产生粒细胞-巨噬细胞集落刺激因子(GM-CSF)和白细胞介素8(IL-8)因子等促炎细胞因子,导致NEU数量增加[20]。
NEU已被确定为COPD发病机制中的一种效应细胞[21],可以直接由血常规检查中获得,在稳定期COPD患者循环血液中以更高的浓度存在[22]。NEU是血液循环中最丰富的白细胞,通过吞噬、颗粒产生、炎症细胞因子和趋化因子释放参与多种免疫和炎症过程[23]。气道炎症是COPD病理生理学的核心,导致组织损伤和破坏。NEU介导的气道炎症是COPD病程中的一个重要阶段。在细菌感染引起的AECOPD,NEU显著增加,但不仅存在于细菌感染的情况下。在COPD患者中,大量NEU在IL-8、白三烯B4等NEU趋化因子的作用下,粘附于气道内皮细胞并迁移到呼吸道。细胞因子刺激增加了呼吸道中NEU的数量,进而释放氧自由基和蛋白水解酶,导致肺泡塌陷和肺气肿。COPD患者的肺组织可在烟草、细菌、病毒和细胞外基质裂解液的作用下产生获得性免疫[5]。有越来越多的证据表明COPD患者血液循环中以及中央和外周气道中NEU数量均增加[24]。NEU水平越高提示炎症越重,间接导致LHS延长。此外,COPD加重期间EOS水平可增加[21],较高的EOS计数与较短的LHS相关[11]。在本研究中,我们发现血浆NEU每增加一个单位,LHS就会延长0.33d(见表3)。本研究首次发现NEU计数可作为LHS长短的定量预测因子,但需要进一步的研究来验证这一假设。这一发现可能有助于识别LHS较长的AECOPD患者。随着临床医生对COPD潜在的炎症过程有了更详尽的了解,NEU有望成为一个新的治疗靶点,以改善疾病并控制和降低恶化率,最终减少LHS和费用。
本研究局限性如下:首先,本次研究为单中心回顾性研究,虽已严格调整以尽量减少残留的混杂因素,仍不可避免地受到混杂因素的影响。其次,对于AECOPD患者,我们无法提供一个定量的出院标准,无法准确量化LHS。此外,本研究仅限于中国人,有一定的地域和民族限制。最后,本研究为横断面研究,目前的结果仅显示NEU水平和LHS之间的线性关系。因此,需要前瞻性的基础和临床研究来进一步证实其因果关系。尽管存在上述局限性,但本研究首次明确揭示了AECOPD患者血浆NEU水平与LHS之间的关系。
综上所述,本研究首次揭示了AECOPD患者血浆NEU水平与LHS之间的明确关系,即其呈正相关;且血浆NEU每增加一个单位,LHS延长0.33d。因此,这间接表明NEU水平较高的COPD患者具有更严重的病情恶化倾向。这一发现可能有助于临床医生识别LHS较长的AECOPD患者,以改善疾病控制和减少恶化率,最终减少LHS和费用。

