拉米夫定联合阿德福韦酯治疗LAM 耐药慢性乙型肝炎患者的疗效分析
马晓,薛娟
(河南科技大学第一附属医院检验科,河南 洛阳 471000)
慢性乙型肝炎是感染乙型肝炎病毒引起的肝功能进行性障碍的传染性疾病[1]。 我国是慢性乙型肝炎高发国家,拥有众多的乙型肝炎携带者,近年来随着乙型肝炎疫苗使用的普及,慢性乙型肝炎的发病率得到一定程度的控制[2]。 由于乙型肝炎病毒感染后发病隐匿且病程较长,乙型肝炎病毒本身不具有侵袭性,主要由于自身免疫反应对抗乙型肝炎病毒的同时,对机体自身正常的组织发挥细胞毒性作用,介导炎症反应,引起进行性肝细胞损伤,最终导致肝硬化和肝癌是患者死亡的重要原因[3,4]。抗病毒治疗是控制慢性乙型肝炎病情的关键,拉米夫定(LAM)是临床上第一个抑制DNA 聚合酶合成的核苷酸类似物,其临床疗效得到认可,但长期服用可引起病毒变异,降低病毒对LAM 的敏感性[5,6]。阿德福韦酯(ADV)联合LAM 是治疗LAM 耐药慢性乙肝的补救方案[7],效果优于单纯使用ADV,本研究选取2017年1月至2019年1月于我院治疗的LAM 耐药慢性乙型肝炎患者86 例,回顾性资料分析,分为观察组和对照组,对照组给予ADV 治疗,观察组患者在常规基础上进行LAM 联合治疗,观察LAM 联合ADV 治疗的LAM 耐药慢性乙型肝炎患者治疗效果,对比分析两组患者血清IL-17水平表达的影响以及治疗后生活治疗评分,以确定LAM 联合ADV 治疗LAM 耐药慢性乙肝的临床价值。 报告如下。
1 资料与方法
1.1 一般资料 选取2017年1月至2019年1月于我院治疗的LAM 耐药慢性乙型肝炎患者86例,回顾性资料分析,分为观察组和对照组,对照组给予ADV 治疗,对照组患者43 例,其中男23例,女20 例,年龄18~58岁,平均年龄47.48±9.17岁。 发病时间3~12年,平均发病时间6.31±1.17年。 观察组患者在常规基础上进行LAM 联合治疗。 观察组患者43 例,其中男22 例,女21 例,年龄18~58岁,平均年龄46.51±9.21岁。发病时间3~12年,平均发病时间6.19±1.22年。 纳入标准:⑴均符合慢性乙型肝炎防治指南(2015年更新版)中关于慢性乙型肝炎的诊断标准; ⑵患者曾接受LAM治疗6 个月以上,HBV DNA 由阴性转为阳性,或者HBV DNA 水平曾出现下降后又升高>2 log10 copies/ml 或者明确为YMDD 变异,且HBV DNA 载量>5 log10copies/ml,ALT 升高超过正常;⑶受试者知情同意。 排除标准:⑴合并有恶性肿瘤、自身免疫性疾病、甲状腺疾病等其他疾病;⑵其他类型慢性肝炎患者。 各组受试者一般资料比较差异无统计学意义(P>0.05)。
1.2 实验方法 将血浆标本提取核算和实时荧光定量检测技术,提取标本制备同时进行靶DNA PCR 扩增及靶序列特异性双标记寡核苷探针检测过程, 在离心管加入100μl 待测血浆标本与100 μlDNA 提取液, 振荡混匀后离心10min, 加入25 μlDNA 提取液混匀进行沉淀溶解,离心10s 后在100℃干浴10min,离心10min 后取2μl 上清液加入PCR 反应液,采用罗氏公司Lightcycle PCR 仪和上海复星实业股份有限公司提供的试剂检测HBV DNA,采用Abbott 公司提供的试剂检测HBeAg;采用BeckmanDxC800 全自动生化分析仪检测ALT;采用ELISA 法检测IL-17 水平,所需试剂盒购自苏州露水生物科技有限公司。
1.3 治疗及随访方法 两组患者人院后均给予肝细胞保护药物葡醛酸钠注射液(山东圣鲁制药有限公司生产,国药准字H37023334)等,同时加强补液营养支持以及对症治疗。 对照组患者在常规治疗的基础上,加用LAM 片[葛兰素史克制药(苏州)有限公司,国药准字H20030581]口服,每次服用0.1 g,每天1 次。 观察组患者在对照组的基础上,加用ADV 片(齐鲁制药有限公司生产,国药准字H2008 0032),每次服用10mg,1 次/d。 两组患者均共治疗48 周。 医院定期复查随访。
1.4 统计学处理 统计分析采用SPSS19.0 软件,计量资料采用(±s)表示,多组间比较使用方差分析,两两比较采用LSD-t 检验; 计数资料比较使用χ2检验。 检验水准α=0.05。
2 结果
2.1 治疗前后两组HBV DNA 的变化情况比较 对两组患者治疗前后的HBV DNA 载量进行比较发现,治疗前两组患者的HBV DNA 载量无明显差异,治疗后虽均有下降,但是观察组患者的HBV DNA载量明显低于对照组患者,且随着治疗时间的增加其HBV DNA 载量差距越来越大(P<0.05),见表1。

表1 治疗前后两组患者HBV DNA 情况比较
2.2 两组患者血清IL-17、ALT 水平比较 对两组患者治疗前后血清IL-17、ALT 水平比较,发现治疗前两组患者的IL-17、ALT 水平无明显差异,治疗3个月检测发现,观察组患者的IL-17、ALT 水平明显低于对照组患者(P<0.05),见表2。

表2 治疗前后两组血清APN、RBP- 4 水平比较
2.3 治疗后两组患者HBeAg 血清转换率比较 观察两组患者治疗后HBeAg 血清转换率发现,随着治疗时间的增加两组患者的HBeAg 血清转换率增加,同时观察组患者的HBeAg 血清转换率明显高于对照组患者(P<0.05),见表3。
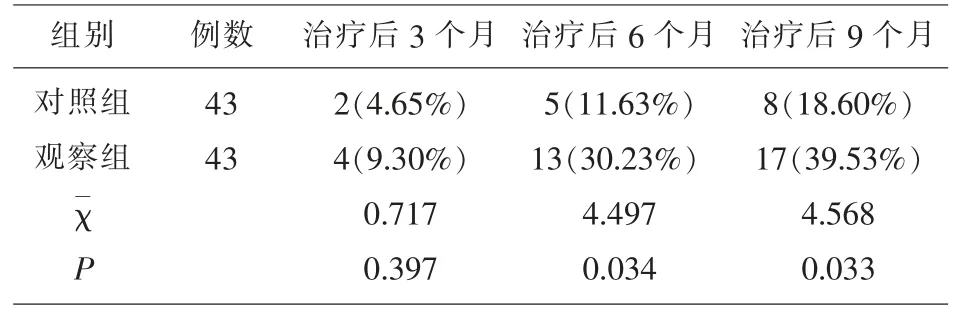
表3 治疗后两组患者HBeAg血清转换率比较
2.4 两组患者服药后不良反应比较 对两组患者治疗后不良反应比较发现,观察组患者中有1 例患者出现恶心呕吐,1 例患者出现头晕头痛;而对照组患者有2 例患者出现恶心呕吐,1 例患者出现头晕头痛的情况,差异无统计学意义(P>0.05)。
3 讨论
慢性乙型肝炎是我国常见的传染性疾病之一,在我国有众多的乙型肝炎感染者,近年来随着乙型肝炎疫苗的引入,慢性乙肝发病率呈逐年下降趋势,但目前仍成为威胁人类生命安全的公众健康问题。 据报道[8]HBV 本身并不引起组织损伤,而是HBV 通过诱导机体过度免疫应答在对抗入侵的HBV 病毒的同时损伤肝脏组织和细胞,最终导致肝脏炎性损伤甚至坏死,肝功能表现为进行性障碍,是肝纤维化和肝硬化的重要诱因。 目前治疗慢性乙型肝炎的药物主要是通过抑制病毒复制的核苷酸类似物,以此改善乙肝患者的肝功能状态,延缓乙型肝炎病情进展。 拉米夫定(LAM)是世界上第一个通过竞争性抑制乙型肝炎病毒DNA 链的合成和延长而达到抗病毒作用[9]。 大量研究均已证实[10,11]LAM 抗病毒的确切疗效及较少的不良反应,但长期使用LAM 容易引起乙型肝炎病毒变异,大大增加5年耐药率,降低HBV 病毒对抗病毒药物的敏感性[12]。 有报道显示[13]LAM 治疗慢性乙型肝炎前四年的YMDD 耐药突变率分别为:14%、38%、49%、66%。 由此可见,随着使用LAM 时间的延长其耐药突变率逐渐升高,治疗效果显著降低。 LAM虽然长期使用存在一定的耐药性,但是对于慢性乙型肝炎患者仍是临床最为常用的基础治疗药物,本研究联合阿德福韦酯(ADV)开展治疗,该药物是新一代可抑制HBV 病毒DNA 聚合酶和逆转录酶活性的核苷酸类似物,在体内通过磷酸化转化为二磷酸盐发挥抗病毒效应[14]。 二磷酸阿德福韦是HBV 多聚酶的天然结构类似物,可与HBV 多聚酶竞争脱氧消耗三磷酸底物,抑制HBV 多聚酶的激活,进而阻断HBV DNA 链的延长,使HBV DNA 的复制终止,进而达到抗病毒的目的[15]。 与LAM 不同的是,ADV 本身含有磷酸基团,更易磷酸化,ADV 在多种细胞内均具有较强的活性,是比LAM 更强效的HBV 病毒抑制剂。 有研究显示[16]ADV 不仅对HBV 野毒株具有抑制作用,同时还能抑制LAM 耐药的突变株。 国外有研究证实[17]LAM联合ADV 并无交叉耐药现象,对HBV 野毒株和YMDD 突变株均有显著的抑制作用。 本研究结果显示,观察组(LAM 联合ADV)、对照组(单独使用ADV)治疗后HBV DNA 载量均较治疗前均显著降低,且观察组降低程度显著高于对照组,说明LAM、ADV 均具有显著的抗HBV 疗效,LAM+ADV联合使用不仅不增加交叉耐药,反而提高病毒抑制作用。
慢性乙型肝炎的肝损伤主要由于过度免疫应答清除入侵HBV 病毒的同时,清除自身正常组织细胞等。 其中参与免疫清除过程的主要为Th1 细胞,而抑制免疫清除的主要为Th2 细胞,故Th1/Th2 失衡是导致机体感染HBV 后不同转归结局的重要影响因素。 IL-17 隶属于Th1 型细胞因子,是近年来新发现的完整性细胞因子,IL-17 通过与其受体形成复合物介导信号传导而发挥免疫增强、细胞毒性作用等生物学效应,主要表现为[18-20]:⑴直接诱导Th1 细胞、NK 细胞、B 细胞、巨噬细胞等产生TNF-α、IL-2 等促炎性细胞因子水平,促进由IL-17、IL-2、IFN-γ、IFN-α 共同组成的炎症级联反应。 ⑵加强FasL 介导的细胞毒作用,增强NK 细胞的杀伤活性,上调NK 细胞穿孔素分泌所致的细胞毒作用。 ⑶IL-17 是重要的内毒素致肝损害的诱导因子,使肝功能进行性衰退。 本研究结果显示,经治疗3 个月后观察组较对照组血清IL-17、ALT 水平显著降低。 说明LAM+ADV 抗HBV 病毒疗效更优,更有效改善慢性乙肝患者的肝功能状态。
另外,本研究结果显示,随着治疗时间的延长,观察组HBeAg 血清转换率显著高于对照组,再次肯定LAM 联合ADV 抗病毒的显著疗效。 且本研究还发现,LAM+ADV 增加抗病毒疗效的同时,并不提高药物不良反应发生率。 说明,LAM+ADV具有HBV 病毒强抑制活性且无交叉耐药现象。
综上所述,LAM 联合ADV 可以有效降低HBV-DNA 的载量,增加患者HBeAg 血清转换率,同时降低血清内IL-17、ALT 水平,值得临床进一步探索。 本研究创新处,确定LAM+ADV 治疗LAM耐药慢性乙型肝炎的临床疗效和安全性,为LAM耐药的慢性乙肝患者提供新的有效的治疗方法,具有重要的临床意义。

