腹腔镜完全腹膜后修补术治疗原发性腰疝2例分析
陈 嘉 戚 腾 屠义梅
(江苏省苏北人民医院疝外科,扬州 225000)
腰疝是一种少见的发生在腰背侧的腹壁疝,位于第12肋和髂嵴之间,患病率占所有腹外疝的1.5%~2.0%。腰疝分为先天性(20%)、原发性(55%)和继发性(25%)[1]。原发性腰疝更为常见,可以发生在腰上三角(Grynfeltt)或者腰下三角(Petit)。目前,治疗腰疝的手术方式众多,尚无金标准术式,常用的是开放式或者腹腔镜使用人工材料进行腹膜前无张力修补术[2,3],腹腔镜手术需要进入腹腔分离腹膜前间隙。在国内,后腹腔入路腹腔镜下完全腹膜后腰疝修补的报道目前仍较少。2021年4~5月我科对2例原发性上腰疝行腹腔镜完全腹膜后修补术,取得良好效果,现报道如下。
1 临床资料
病例1:女,65岁,因发现左侧腰背部可复性包块6年于2021年5月16日入住我科。BMI 25.5。查体:左侧腰部可扪及包块大小约4 cm×4 cm,质地软,无压痛,按压后可还纳,直立位时包块明显,右侧卧位时肿块接近消失。术前CT提示左侧上腰三角处筋膜缺损,腹膜外脂肪疝出(图1A)。术前诊断原发性左侧腰疝。拟行后入路腹腔镜完全腹膜后修补术。全麻,右侧卧位,手术床摇至左侧腰部过伸位,术者站于患者右侧。常规消毒铺巾。平脐与左侧腋前线交界处做切口长约12 mm,逐层切开皮肤、皮下组织,显露腹外斜肌腱膜,纵行切开腹外斜肌腱膜。血管钳钝性分离肌层(腹内斜肌和腹横肌)与腰背筋膜,进入后腹腔,甲状腺拉钩拉开各层肌筋膜组织,从切口探入食指,紧贴腰背筋膜向上下和侧后方钝性分离,推开腹膜及腹膜外脂肪,初步推开空间后将12 mm trocar置入腹膜后间隙作为观察孔,建立气腹后,压力维持在11~14mm Hg(1 mm Hg=0.133 kPa)。直视下分别于腋中线肋缘下3cm处,腋中线髂嵴上缘处1 cm做5 mm切口,置入5 mm trocar作为操作孔。观察无明显出血,电钩及分离钳分离扩大腹膜后间隙,分离范围上至肋弓深面,向下至髂前上嵴,向前到达腋前线,向后显露腰方肌,分离过程中可见腹膜外脂肪从腰上三角疝出(图1B),将疝内容物还纳,可见缺损约2 cm×2 cm(图1C),用倒刺线将疝环缺损缝合关闭,分离过程中注意保护腰方肌表面的髂腹下和髂腹股沟神经。选取大网孔聚丙烯轻量型补片,裁剪成12 cm×10 cm后置入后铺平,覆盖整个缺损区域,补片边缘需超过疝环3~5 cm(图1D),确认补片平整后放气,完成手术,术中未放置引流。手术时间90 min,术中出血量10 ml。术后不受麻醉限制即可下床活动,6 h后恢复半流质饮食,术后腹带加压包扎。术后第1天疼痛轻微,视觉模拟评分为2分。术后切口愈合可,术区未出现血清肿、血肿,无慢性疼痛(图1E)。术后第3天复查CT术区补片放置良好,腰部未见疝内容物突出(图1F),顺利出院。术后随访3个月,术区无疼痛,未出现血肿,无复发。
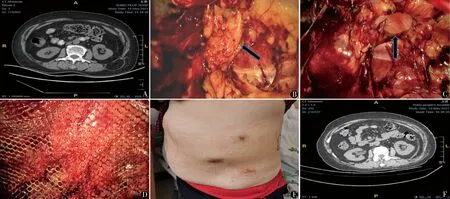
图1 病例1:女,65岁。A.术前CT示左腰上三角缺损,腹膜外脂肪组织疝入;B.疝内容物为腹膜外脂肪;C.腰上三角缺损;D.将补片放置在腹膜前间隙;E.手术后外观;F.术后第3天复查CT,补片放置良好,无内容物疝出
病例2:女,68岁,发现右侧腰背部可复性包块1年于2021年4月7日入住我科。BMI 19.4。术前CT提示右侧上腰三角处筋膜缺损,腹膜外脂肪疝出。查体:右侧腰部可扪及包块大小约5 cm×4 cm,质地软,活动度可,站立或咳嗽时明显,按压后可还纳。既往无特殊病史。术前诊断原发性右侧腰疝。全麻,左侧卧位,手术床摇至右侧腰部过伸位,术者站于患者左侧。手术方法及器械与病例1相同。手术时间为100 min,术中出血15 ml。术后6 h后恢复半流质饮食,术后腹带加压包扎。术后第1天疼痛视觉模拟评分为2分,术后第4天顺利出院。术后随访3个月,恢复良好,切口愈合可,术区未出现血清肿、血肿,无复发。
2 讨论
腰疝是指从腹壁或者后腹膜在第12肋和髂嵴之间突出的疝[4],分为先天性和后天性,先天性腰疝多发在婴儿,约占20%,多为腰背肌或筋膜发育不良所致。后者根据发病原因又可以分为原发性和继发性,其中原发性腰疝最常见,约占55%,常见病因包括高龄、长期体力活动及慢性咳嗽等;继发性腰疝约占25%,多由手术或外伤引起[5,6]。解剖学上原发性腰疝由可分为腰上三角疝(Grynfeltt疝)及腰下三角疝(Petit疝),腰上、下三角为腰背部薄弱区,缺少肌肉保护,因此,在腹压增加情况下局部组织可经此区域突出,而腰上三角间隙较腰下三角间隙大,其底部仅由薄弱的腹横筋膜,故更容易发生疝[7]。本组2例均是腰上三角疝。
腰疝通过临床表现及体格检查明确,多数腰疝可以有明显临床症状,主要表现为腰部包块,俯卧或者健侧卧位时消失,有些患者会出现疼痛症状,疝内容物可以是脂肪、结肠,甚至是腹腔其他器官[8],严重者会发生肠管嵌顿,形成肠梗阻。本组2例疝内容物均是脂肪组织。CT或者MRI可以显示腰部肌群缺损的部位、范围及疝内容物性质,以便排除其他疾病,应作为术前常规检查[9]。
老年原发性腰疝一旦确诊,应及早手术,以免发生潜在的嵌顿和肠梗阻[10]。腰疝手术方式众多。①开放手术:传统Dowd手术利用缺损周围的筋膜或者肌肉做叠瓦状缝合疝环,但手术创伤大,复发率高,已很少使用。目前,较多采用肌后间隙或腹膜前间隙对缺损进行修补(即Sublay或Stoppa),在腹压的作用下使腹膜前间隙内的补片更贴紧于腹壁,不易移位卷曲。杜华栋等[7]报道21例采用部分可吸收补片经腹膜前间隙修补治疗原发性疝。林荣贵等[11]报道采用Kugel补片在腹膜前间隙行原发性腰疝修补。可见,Sublay修补术可能是目前开放手术中应用最广泛的方式[12]。②腹腔镜手术:随着腹腔镜技术的普及,腹腔镜技术也逐步应用到各种疝修补。1996年Burick等[13]报道腹腔镜腰疝修补术,王雷等[14]报道3例采用腹腔镜腹腔内补片植入术(intraperitoneal onlay mesh,IPOM)治疗腰疝,李俊生等[15]报道1例采用腹腔镜经腹无张力修补术(transabdominal preperitoneal,TAPP)治疗原发性腰疝,Sun等[16]报道采用经腹部分腹膜外修补术(transabdominal partial extraperitoneal, TAPE)完成腹腔镜腰疝修补是完全可行的。
我们认为IPOM是治疗腹壁疝的主要方式,在治疗腰疝时存在一定难度,因为腰疝属于边缘腹壁疝,疝环的内侧往往被结肠挡住,不能完全覆盖缺损,而且需要昂贵的防粘连补片及钉枪固定,增加术后出现肠梗阻、肠漏和腹膜炎等并发症的可能性。TAPP需要切开侧腹膜,游离结肠,避免损伤输尿管,放置补片后再缝合腹膜。我们认为腹腔镜完全腹膜后修补术相当于开放的Sublay手术,治疗原发性腰疝优点在于:①腹腔镜创伤小、恢复快;②只需要使用普通聚丙烯补片,节约成本;③可以避开结肠的阻挡,直接进入腹膜后间隙这个天然解剖层面,减少对腹腔的干扰。汤睿等[17]介绍全腹膜囊分离(total visceral sac separation,TVS) 技术时提出:腹横肌后方,越往后腹膜越厚、腹膜外脂肪越多,操作越容易。因此,采用TVS技术腰疝通常较脐疝、白线疝更容易。
根据我们的经验,腰疝修补和切口疝及腹股沟疝相似,越接近腹膜的修补越牢固。根据Pascal流体静力学说,利用腹内压均匀分布在整个补片上,使其贴附固定在腹壁上,摩擦阻力大,修补牢靠,效果好[11]。技术要点:①直视下建立3个trocar孔,熟练掌握腹膜后间隙的解剖结构,充分游离腹膜后间隙,在关闭疝环缺损后保证补片边缘超过缺损范围3~5 cm。②如有腹膜破损时及时关闭,防止补片与腹腔接触。③注意保护穿过腰上三角前方走行的肋下神经、髂腹下神经和髂腹股沟神经。④保证补片充分铺平,缺损较大时可以用医用胶或者缝线悬吊固定补片。⑤术中彻底止血,术后加压包扎,腹带包扎半年。当然,此技术也有一定局限性,对于有手术史的继发性腰疝,腹膜外间隙往往粘连严重,难以建立手术空间,操作难度大,目前我们也仅用于原发性腰疝患者。
因为腰疝的患病率较低,没有诊疗指南及治疗金标准。从本组2例经验来看,对于原发性腰疝,实施腹腔镜完全腹膜后修补术是安全可行的。但本组病例少,随访时间较短,远期疗效有待进一步观察和总结。我们认为腰疝具体的手术方式需要综合评估患者的情况,结合腰部缺损的大小、患者自身心肺功能情况及经济因素等多方考虑,最终达到个体化治疗。

