不同剂量氨甲蝶呤治疗急性淋巴细胞白血病的疗效及对患者造血功能、免疫功能的影响
孙琳,陶有为,张会娜,李现金
解放军联勤保障部队第九九〇医院血液内科,河南 驻马店 463000
急性淋巴细胞白血病(acute lymphocytic leukemia,ALL)是临床常见的血液系统恶性肿瘤,发病因素至今仍未明确,多认为ALL的发生可能与遗传易感性、化疗、机体免疫状态等多种因素有关。对患者进行个体化治疗可有效改善预后。化疗是临床常用的ALL治疗手段之一,但有研究发现,化疗对患者临床疗效的影响较大。但由于化疗剂量把握较为困难,化疗不足或过度,均不利于患者康复,甚至会加重病情,增加死亡风险。化疗药物剂量过大可在杀灭肿瘤细胞的同时损伤正常细胞,影响患者的造血功能和免疫功能,影响患者的预后。氨甲蝶呤是ALL化疗方案中的关键组成药物,但该药有一定的毒性,用药不当可能导致治疗指数低,患者因药物排泄缓慢,导致血药浓度高,导致多种不良反应。目前,对ALL患者采用何种剂量的氨甲蝶呤治疗,仍未有明确定论。本研究旨在探讨不同剂量氨甲蝶呤联合长春新碱+柔红霉素+醋酸泼尼松(VDP)方案治疗ALL的疗效,及对患者造血功能、不良反应的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2015年3月至2021年3月解放军联勤保障部队第九九〇医院收治的ALL患者。纳入标准:①经临床、血常规确诊为ALL;②病历资料完整;③治疗依从性好。排除标准:①纳入研究前1个月内,服用过影响激素水平的药物或接受过相关治疗;②合并心、肝、肾等器官、系统严重疾病;③合并恶性肿瘤;④合并慢性髓系白血病、慢性骨髓增殖性疾病、淋巴系统增殖性疾病。依据纳入和排除标准,本研究共纳入98例ALL患者,根据氨甲喋呤剂量不同分为大剂量组(n
=48)和小剂量组(n
=50),大剂量组患者给予5.0 g/m氨甲蝶呤,小剂量组患者给予3.0 g/m氨甲蝶呤。大剂量组中男30例,女18例;平均年龄(43.44±6.55)岁。小剂量组中男31例,女19例;平均年龄(43.35±6.71)岁。两组患者性别、年龄比较,差异均无统计学意义(P
>0.05),具有可比性。1.2 治疗方法
两组患者均给予VDP方案化疗:长春新碱2 mg静脉注射,每周1次;柔红霉素45 mg/m静脉滴注,每天1~3次;醋酸泼尼松60 mg静脉注射,每天1次。第15天开始减量,1~2周内减停,以28天为1个治疗周期。大剂量组患者给予氨甲蝶呤5.0 g/m,小剂量组患者给予氨甲蝶呤3.0 g/m治疗,于30 min内快速静脉滴注突击量(总剂量的1/6),剩余剂量在23.5 h内滴注完成,同时,完成突击量后鞘内注射氨甲蝶呤、阿糖胞苷、地塞米松三联药物1次。大剂量氨甲蝶呤用药1~4天内对患者进行水化和碱化,水化量3000 ml(/m·d),碱化采用5%碳酸氢钠3~5 ml/kg静脉滴注,使尿液pH≥7。两组进行VDP+氨甲蝶呤治疗期间密切监测血浆氨甲蝶呤浓度,血浆氨甲蝶呤浓度≤0.1 μmol/L时,可停止治疗。
1.3 观察指标和评价标准
①治疗前及治疗2个疗程后,清晨抽取两组患者空腹静脉血5 ml,抗凝、离心处理后,分离血清,-80℃保存待检,检测两组患者造血功能指标,包括血红蛋白(haemoglobin,Hb)、血小板(platelet,PLT)计数。②治疗前及治疗2个疗程后,清晨抽取两组患者空腹静脉血5 ml,检测两组患者免疫功能指标,包括 CD4、CD8,计算CD4/CD8。③化疗2个周期后,根据《中国成人急性淋巴细胞白血病诊断与治疗指南》中ALL治疗反应定义判定疗效分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)与疾病进展(progressive disease,PD)。总有效率(%)=(CR+PR)例数/总例数×100%,疾病控制率(%)=(CR+PR+SD)例数/总例数×100%。④比较两组患者的不良反应发生情况,包括消化道反应、骨髓抑制、肛周炎、口腔黏膜炎。
1.4 统计学方法
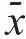
2 结果
2.1 造血功能指标的比较
治疗前后,两组患者Hb、PLT水平组间比较,差异均无统计学意义(P
>0.05)。治疗后,两组Hb、PLT水平均高于本组治疗前,差异均有统计学意义(P
<0.05)。(表1)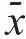
表1 治疗前后两组患者造血功能指标的比较(±s)
2.2 免疫功能指标的比较
治疗前,两组患者CD4、CD8水平和CD4/CD8比较,差异均无统计学意义(P
>0.05)。治疗后,两组患者CD4水平和CD4/CD8均高于本组治疗前,CD8水平均低于本组治疗前,且大剂量组患者CD4水平和CD4/CD8均高于小剂量组,CD8水平低于小剂量组,差异均有统计学意义(P
<0.05)。(表2)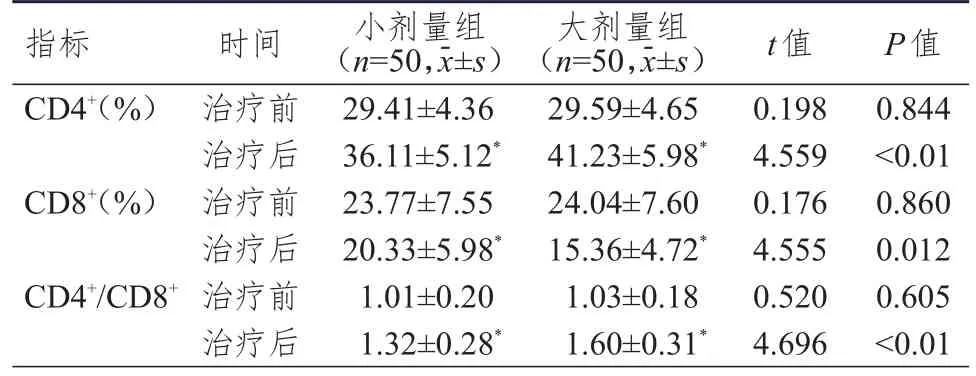
表2 治疗前后两组患者免疫功能指标的比较
2.3 疗效的比较
小剂量组患者的治疗总有效率为50.00%(25/50),低于大剂量组患者的70.83%(34/48),差异有统计学意义(χ
=4.436,P
=0.035);小剂量组患者的疾病控制率为76.00%(38/50),低于大剂量组患者的91.67%(44/48),差异有统计学意义(χ
=4.400,P
=0.036)。(表3)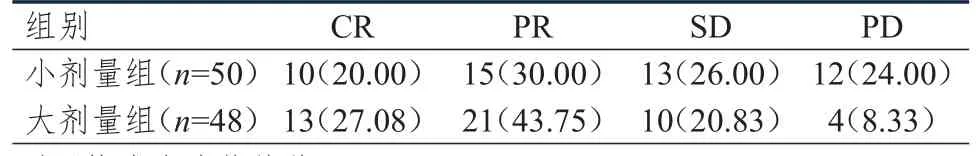
表3 两组患的临床疗效[ n(%)]*
2.4 不良反应发生情况的比较
小剂量组患者的不良反应总发生率为28.00%(14/50),低于大剂量组患者的47.92%(23/48),差异有统计学意义(χ
=4.134,P
=0.042)。(表4)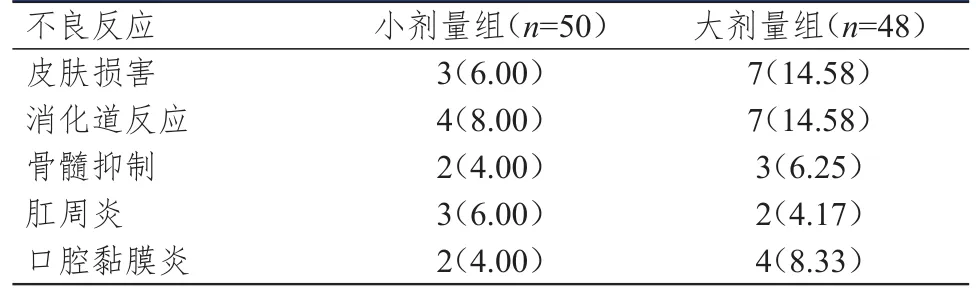
表4 两组患者的不良反应发生情况[ n(%)]
3 讨论
ALL发病时骨髓中异常的原始细胞及幼稚细胞大量增殖并可抑制正常的造血功能,可广泛侵犯患者的肝、脾、淋巴结等多种脏器。研究发现,若不对ALL患者进行针对性的治疗,患者平均生存期仅为3个月左右,甚至可在确诊数天后即死亡。ALL的根治难度较大,给患者家庭及社会带来沉重的经济负担,不利于社会发展。以氨甲蝶呤为主,结合VDP的解救治疗方案成为治疗ALL的主要方案之一。虽然关于氨甲蝶呤的最佳使用剂量的相关研究较多,但最佳的使用剂量仍未明确。
氨甲蝶呤是一种与叶酸结构相似的抗代谢药物,具有抑制DNA合成的作用。血液中的氨甲蝶呤达到一定浓度后会进入细胞内,但由于不同个体对氨甲蝶呤的吸收、生物转化及排泄存在差异。因此,ALL患者接受氨甲蝶呤治疗后,会出现不同程度的毒性反应,影响了治疗效果。且氨甲蝶呤的使用剂量决定了不良反应的发生率,大剂量氨甲蝶呤可在机体蓄积,使药物在体内的消除减慢,增加了不良反应的发生风险。本研究将氨甲蝶呤的使用剂量分为小剂量(3.0 g/m)和大剂量(5.0 g/m)两种,结果显示,治疗后,两组患者的Hb、PLT水平均明显升高,但组间比较无明显差异,表明无论是小剂量氨甲蝶呤+VDP治疗还是采用大剂量氨甲蝶呤+VDP治疗,均对维持ALL患者的正常造血功能发挥了较好的治疗疗效。本研究结果显示,大剂量组CD4水平和CD4/CD8高于小剂量组,CD8水平低于小剂量组,表明大剂量氨甲蝶呤+VDP方案对ALL患者的免疫功能改善效果更好。
本研究结果显示,小剂量组患者的治疗总有效率为50.00%,低于大剂量组患者的70.83%,小剂量组患者的疾病控制率为76.00%,低于大剂量组患者的91.67%。表明大剂量氨甲蝶呤+VDP方案治疗对ALL患者的病情控制效果更好,临床疗效更佳,与既往文献报道结果基本相符。本研究结果显示,小剂量组患者的不良反应总发生率为28.00%,低于大剂量组患者的47.92%。表明小剂量氨甲蝶呤+VDP方案治疗的安全性更高,患者的耐受度更好。本研究采用小剂量氨甲蝶呤+VDP治疗ALL的不良反应发生率更低。也有研究发现,中剂量氨甲蝶呤(4.0 g/m)+VDP方案治疗ALL的临床疗效与大剂量氨甲蝶呤+VDP方案治疗的疗效相近,且可明显降低因氨甲蝶呤用药剂量过大而引起的诸多不良反应。对于年老体弱的患者也需减少氨甲蝶呤的给药剂量,提高患者的机体耐受性,获得最佳的抗肿瘤疗效。同时,临床需积极监测患者的血药浓度,对ALL患者采取对症治疗,选择合理剂量的氨甲蝶呤,尽可能减少不良反应的发生风险。后续将进一步深入分析小剂量(3.0 g/m)、中剂量(4.0 g/m)、大剂量(5.0 g/m)氨甲蝶呤在ALL患者中的应用效果,以更好地指导临床治疗。
综上所述,不同剂量的氨甲蝶呤对ALL患者造血功能的影响类似,大剂量氨甲蝶呤+VDP方案治疗ALL的疗效更佳,改善患者免疫功能的效果更好,但小剂量氨甲蝶呤+VDP治疗不良反应更少。

