MRSA对万古霉素和替考拉宁的异质性耐药情况及分子分型
蓝锴 钟国升 刘宇阳 陈瑶 伍众文 余学高 陈茶★ 黄彬★
作者单位:1.广东省中医院检验医学部,广东,广州510120
2.广东医科大学医学技术学院,广东,东莞523770
3.中山大学附属第一医院检验医学部,广东,广州510080
异质性耐药(heteroresistance,HR)意指同一克隆菌株中同时存在对某种抗生素耐药和敏感亚群的现象,可能是导致临床上患者用药失败甚至诱导耐药菌株产生的重要原因[1]。多种临床常见致病菌已被报道存在异质性耐药现象[2]。长期以来,万古霉素(vancomycin,VAN)是治疗甲氧西林金黄色葡萄球菌(Methicillin-resistant Staphylococcus aureus,MRSA)的首选药物,随着其在临床中的广泛应用,MRSA对VAN 的敏感性逐渐下降,异质性万古霉素中介金黄色葡萄球菌(heterogeneous vancomycin-intermediateStaphylococcus aureus,hVISA)的检出率愈来愈高,但异质性耐药的机制尚不清楚,因此研究MRSA 异质性耐药的机制显得极其重要。葡萄球菌染色体mec 盒基因遗传元件(staphylococcal cassete chromosome mec,SCCmec)分型是目前临床较常用的分子分型方法。目前,国内外研究发现MRSA 耐药机制与SCCmec 元件整合mecA、mecC等相关耐药基因、双组分系统的调控以及生物膜的形成[3]等有关,但MRSA 异质性耐药的机制尚不十分清楚。替考拉宁(teicoplanin,TEC)与VAN 同属于糖肽类抗生素,广泛应用于临床,其治疗效果与VAN 相当,但是MRSA对TEC 的异质性耐药情况并不清楚。因此,本文拟研究MRSA对VAN 和TEC 的异质性耐药情况,对其进行SCCmec 基因分型,并研究SCCmec 基因型是否与MRSA 的异质性耐药有关,为MRSA 异质性耐药的流行病学研究及防治提供实验室依据,为MRSA 复杂的异质性耐药机制研究奠定基础。
1 材料与方法
1.1 菌株来源
收集2016年1月至2020年12月间中山大学附属第一医院临床分离的MRSA 305 株,剔除同一患者重复分离的菌株,冻存于-80℃备用。菌株分离自血液、脓液、痰液标本。质控菌株金黄色葡萄球菌ATCC 25923 购自卫健委全国临床检验中心;SCCmec 分型标准菌株由上海肺科医院检验科余方友教授惠赠。
1.2 主要仪器与试剂
VAN 粉末购自上海麦克林生化有限公司,TEC 粉末购自上海源叶生物科技有限公司,Brain Heart Infusion Agar 脑心浸液琼脂、Brain Heart Infusion Broth 脑心浸液肉汤购自青岛高科园海博生物技术有限公司,Vitek 2 全自动微生物检测系统购自法国生物梅里埃公司,Veriti 扩增仪购自美国Life Technologies 公司。Vilber Fusion FX7 凝胶成像仪购自法国VILBER 公司,DYY-6C 电泳仪购自北京市六一仪器厂,PCR 引物由生工生物工程(上海)股份有限公司合成,2×Accurate Taq预混液购自湖南艾科瑞生物工程有限公司。
1.3 菌株复苏
将临床分离的MRSA 从-80℃冰箱取出,解冻后用接种环挑取一环菌液,分区划线接种于血平板,37℃培养18 h,得到MRSA 单个菌落。
1.4 SCCmec 分型
采用广州达安基因股份有限公司核酸提取与纯化试剂盒提取细菌的DNA。按照参考文献[4]合成引物见表1,采用多重PCR 进行SCCmec 分型。多重PCR 反应条件:预变性94℃5 min;变性94℃45 s,退火65℃45 s,延伸72℃90 s 共10 个循环;变性94℃45 s,退火55℃45 s,延伸72℃90 s 共25 个循环;最后延伸72℃10 min。取3 μL 反应产物在1.2%琼脂糖凝胶上电泳,在120 V、55 mA 条件下电泳40 min 后用凝胶成像系统观察结果并拍照保存。

表1 SCCmec 基因分型所用的引物Table 1 Primers of SCCmec genotyping
1.5 异质性耐药初筛
以菌群谱型分析微量滴定法(microtitration population analysis profiling,MPAP)[5]对MRSA 进行异质性耐药表型初筛,分别配制7 个倍比稀释浓度2-2~24mg/L 含VAN 和TEC 的BHI 平板。挑取复苏的单个克隆菌落接种于3 mL BHI 肉汤培养基,37℃过夜增菌后,用BHI 肉汤调节菌液浓度分别为101、102、103、104、105、106、107CFU/mL。取10 μL 菌液滴定于梯度抗生素平板,每个克隆重复两滴,每块板滴10 株菌的菌液。实验重复三次。37℃孵育48 h 后观察细菌生长情况,菌落数量随着抗生素浓度升高而缓慢下降,最低抑菌浓度(minimum inhibitory concentration,MIC)与最高不抑菌浓度(the highest noninhibitory concentration,HNIC)的比值大于8,则为异质性耐药初筛阳性。
1.6 异质性耐药确证
采用菌群谱型分析法(population analysis profiling,PAP)[6]对MRSA 异质性耐药表型初筛阳性菌株进行确证。分别配制7 个倍比稀释浓度2-2~24mg/L 含VAN 和TEC 的BHI 平板。挑取HR 阳性的单个克隆菌落接种于3 mL BHI 肉汤培养基,37℃过夜增菌后,用BHI 肉汤调节菌液浓度分别为101、102、103、104、105、106、107CFU/mL。取20 μL 菌液滴定于PAP 梯度抗生素平板,均匀涂布,重复三次。37℃孵育48 h 后菌落计数,并使用Graph-Pad Prism 软件将菌落数量与抗生素浓度作图,若MIC与HNIC 比值大于8,则为异质性耐药确证阳性。
1.7 统计学分析
利用SPSS 25.0 统计软件进行统计分析;计数资料采用n(%)表示,采用χ2检验;P<0.05 为差异有统计学意义。
2 结果
2.1 MRSA 的临床特征
305 株MRSA 主要分离自患者痰液36.4%(111/305)、血液30.8%(94/305)、脓液32.8%(100/305)。分离科室主要为重症监护室26.6%(81/305)、外科26.9%(82/305)、内科10.5%(32/305)、急诊区7.5%(23/305)、皮肤科7.5%(23/305)。
2.2 SCCmec 分型
79 株为SCCmec Ⅱ型25.9%,31 株为SCCmecⅢ型10.2%,109 株为SCCmec Ⅳa 型35.7%,6 株为SCCmec Ⅳb 型2.0%,1 株为SCCmec Ⅳc 型0.3%,2株为SCCmec Ⅳd 型0.7%,17 株为SCCmec Ⅴ型5.6%,剩下60 株未能分型19.7%。部分MRSA SCCmec 分型电泳结果见图1。血液和脓液标本中分离的MRSA 主要为SCCmec Ⅳ型;痰液标本中分离的MRSA 主要为SCCmec Ⅱ型(P<0.05)。见表2。

表2 来源于不同标本类型MRSA 的SCCmec 分型结果[n(%)]Table 2 SCCmec typing results of MRSA from different types of specimens[n(%)]
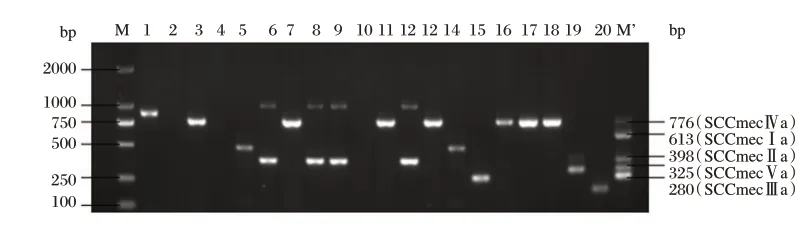
图1 部分MRSA SCCmec 分型结果(多重PCR)Figure 1 SCCmec typing results of partial MRSA(multiples PCR)
2.3 MRSA 异质性耐药初筛
305 株MRSA 中有12 株对VAN 耐药,33 株对TEC 耐药,6 株同时对两者耐药,后续实验分别剔除对VAN 和TEC 耐药的MRSA,剩下对VAN 敏感的MRSA 293 株,对TEC 敏感的MRSA 272 株。分别对VAN、TEC 敏感的MRSA 进行MPAP 异质性耐药初筛,见图2。MPAP 结果显示对VAN 异质性耐药MRSA(MRSA-VAN-HR)阳性菌114 株(114/293,38.9%),对TEC 异质性耐药MRSA(MRSA - TEC - HR)阳性菌166 株(166/272,61.0%),差异有统计学意义(P<0.05);MRSA对VAN 和TEC 同时异质性耐药(MRSA-VAN-TECHR)阳性68 株。

图2 MRSA-TEC-HR 与MRSA-VAN-HR 初筛的MPAP 结果Figure 2 The preliminary screening results of MRSA-TECHR and MRSA-VAN-HR by MPAP method
2.4 MRSA 异质性耐药确证
PAP 法显示,114 株初筛对VAN 异质性耐药阳性菌中有104 株确证对VAN 异质性耐药阳性(MRSA-VAN-HR),异质性耐药率为35.5%(104/293);166 株初筛对TEC 异质性耐药阳性菌中有163 株对TEC 异质性耐药阳性(MRSA-TEC-HR),异质性耐药率为59.9%(163/272),MRSA对VAN与TEC 的异质性耐药率比较,差异有统计学意义(P<0.05)。62 株MRSA 表现为VAN 和TEC 同时异质性耐药(MRSA-VAN-TEC-HR)。见图3。

图3 MRSA-TEC-HR 与MRSA-VAN-HR PAP 法确证结果Figrue 3 The results of MRSA-TEC-HR and MRSA-VANHR by PAP method
2.5 SCCmec 分型与MRSA 异质性耐药情况的相关性分析
不同SCCmec 型别的MRSA对TEC 的异质性耐药率比较,差异有统计学意义(P<0.05),SCCmec分型与MRSA-TEC-HR 有一定相关性(r=0.22)。不同SCCmec 型别的MRSA对VAN 的异质性耐药率比较,差异无统计学意义(P>0.05),SCCmec 分型与MRSA-VAN-HR 不存在相关性。见表3。

表3 MRSA 的SCCmec 型别与异质性耐药相关性分析Table 3 Correlation analysis between SCCmec typing and heteroresistance of MRSA
3 讨论
SCCmec 分型是临床常用的分子分型方法,可根据多重PCR 后电泳条带的位置进行分子分型。SCCmec 元件也被称为“耐药岛”,携带的多种耐药基因可能也与MRSA 的异质性耐药现象存在一定的关联。
本院2016 至2020年五年间临床分离的MRSA 流行菌株以SCCmec Ⅳ型为主(38.7%),其次为SCCmec Ⅱ型(25.9%),提示临床分离的MRSA 以SCCmec Ⅳ型为主要流行菌株,可能与SCCmec Ⅳ型元件相对较短更容易在不同遗传背景的MRSA 中转移有关[7]。本院2008年至2011年四年间560 株MRSA 分型主要为SCCmec Ⅲ型(占66%)[4],提示这几年间本院发生了MRSA 菌株从以SCCmec Ⅲ型为主到以SCCmec Ⅳ、Ⅱ型为主的转变。国内有关文献报道MRSA SCCmec分型主要以Ⅲ型为主[8],主要为院内感染。本次研究有60 株(19.7%)未能分型,可能是除了SCCmecⅠ~Ⅴ型以外的SCCmec Ⅵ-ⅩⅣ型,但是否存在新的型别还有待进一步研究。本研究中来源于不同标本类型MRSA 的SCCmec 分型结果不同,血液和脓液标本都以SCCmec Ⅳ型为主,而痰液标本则以SCCmec Ⅱ型为主;提示SCCme Ⅳ型MRSA 更容易经血源性及化脓性感染途径传播,而SCCmec Ⅱ型MRSA 更容易通过呼吸道传播。
目前,有关MRSA 异质性耐药情况的报道相对较少,已有的研究主要为MRSA对VAN 的异质性耐药。VAN 作为临床上治疗MRSA 的最后一道防线,随着其广泛使用,全球MRSA-VAN-HR检出率逐渐增高,2004年的一项研究[9]曾经报道中国局部地区h-VISA 检出率为6.7%;2009年济南地区的h-VISA 分离率为13.4%[10];2012 至2017年5年间郑州大学附属第一医院h-VISA 检出率为17.9%[11]。本研究结果显示,中山大学附属第一医院2016 至2020年5年间MRSA-VAN-HR 检出率为35.5%,相比于已有报道的检出率更高,提示MRSA对VAN 的异质性耐药现象愈发严重。
TEC 与VAN 都作为糖肽类抗生素被广泛应用于临床,TEC 治疗效果与VAN 相当,但还未见MRSA-TEC-HR 检出率的相关报道。研究结果显示本院MRSA-TEC-HR 的检出率为59.9%,提示MRSA对TEC 有较高的异质性耐药水平。
SCCmec 型别与MRSA 异质性耐药的相关性分析中,SCCmec 型别与MRSA-TEC-HR 存在一定的相关性,相关强度偏弱。SCCmec Ⅳ型MRSATEC-HR 阳性率高达69.7%,提示相对于其它SCCmec 分型,SCCmec Ⅳ型MRSA 更容易出现对TEC的异质性耐药。SCCmec 型别与MRSA-VAN- HR不存在相关性。
综上所述,本院临床分离MRSA 的流行菌株可能存在以SCCmec Ⅲ型为主到以SCCmec Ⅳ型为主的转变,SCCmec Ⅳ型MRSA 的逐渐流行提示应注重社区环境的卫生检测与卫生习惯的培养,防止其暴发流行。MRSA对VAN 与TEC 都存在较高的异质性耐药水平,有必要定期监测MRSA耐药性的变化用于指导临床用药,以避免低剂量抗生素对MRSA 的长时间无效作用。MRSA 的SCCmec 型别与MRSA对TEC 的异质性耐药情况存在一定的相关关系。MRSA对TEC 与VAN 异质性耐药的分子机制值得深入探讨,以防止异质性耐药菌株发展为耐药菌。

