罗汉果质量标准提高研究*
张 萌,黄华花,陈景海,吕诗诗
(1.厦门医学院药学系/厦门市中药生物工程重点实验室/福建省中药精加工与健康产品开发重点研究室,福建 厦门 361023;2.厦门大学附属妇女儿童医院/厦门市妇幼保健院,福建 厦门 361003)
罗汉果为葫芦科植物罗汉果[Siraitia grosvenorii(Swingle)C.Jeffrey ex A.M.Lu et Z.Y.Zhang]的干燥果实。罗汉果是一种传统中药,应用历史悠久,是首批被国家卫生部公布的药食两用中药材。罗汉果中含有皂苷、黄酮和多糖等成分,研究表明罗汉果皂苷具有调节血糖[1]、止咳祛痰[2]、润肠通便[3]、抗炎[3]、抗过敏[4]、提高免疫[5-6]等作用,罗汉果黄酮具有抑菌[7-8]、调节血糖[9]、抗疲劳[10]等作用,罗汉果多糖具有抗氧化作用[11]。因此,罗汉果皂苷和黄酮为罗汉果的主要活性成分。
目前关于罗汉果质量控制研究情况如下:《中华人民共和国药典》(2015年版)一部收载的该药材的质量标准[12]、张彦东等[13]建立的该药材配方颗粒的质量标准和屠寒等[14]研究的罗汉果复方制剂质量标准中均仅检测了罗汉果苷V;钟名诚等[14-15]建立的该药材质量标准中增加了多糖、总糖的含量测定。由此可见,罗汉果的质量控制存在着检测指标单一、专属性不强的问题。故本研究拟在现有研究[15-16]基础上,以黄酮、皂苷类成分为指标,建立多成分的定量和定性方法,使罗汉果的质量标准得到完善和提高,有利于对其质量进行有效地控制。
1 仪器与试药
1.1 仪器 Waters Acquity型UPLC仪(美国Waters公司);BS224S型、CPA225D型电子天平(德国赛多利斯公司);KQ5200E型超声波清洗器(昆山市超声仪器有限公司);WD-9403C型紫外仪(北京市六一仪器厂)。
1.2 试药与试剂 11批罗汉果样品信息见表1。罗汉果黄素(批号:181227)、山奈酚-3,7-O-α-L-二鼠李糖苷(批号:190319)、罗汉果皂苷V(批号:190126)纯度均>98%,均购自上海融禾医药科技有限公司;乙腈为色谱纯,水为超纯水,其余试剂均为分析纯。
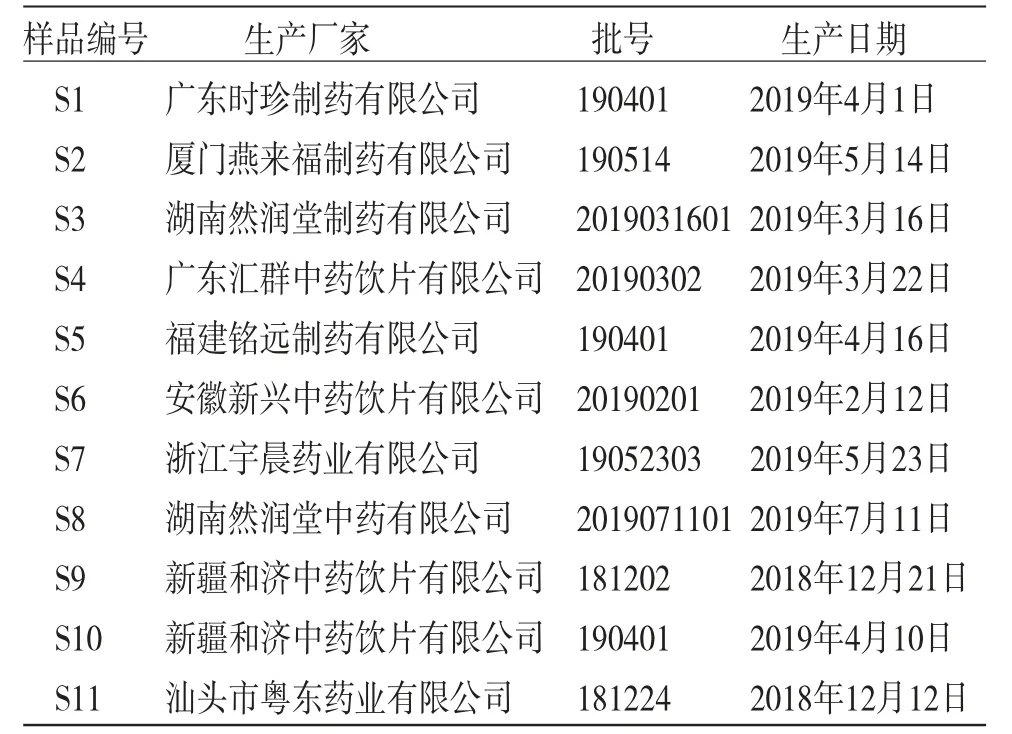
表1 样品信息
2 方法与结果
2.1 薄层鉴别 取罗汉果粉末1 g,加水50 mL,超声(40 kHz,900 W)提取30 min,滤过,取滤液20 mL,加正丁醇萃取2次,每次20 mL,得正丁醇液,合并,回收,残渣以1 mL甲醇复溶,作为供试品溶液。另取罗汉果皂苷V、罗汉果黄素和山奈酚-3,7-O-α-L-二鼠李糖苷对照品,分别加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。按照薄层色谱法(TLC)2015年版《中华人民共和国药典》[16-17]操作,吸取上述4种溶液各2 μL,点于同一硅胶G板上,以正丁醇-乙醇-水(8∶2∶3)为展开剂,展开,晾干,喷以5%AlCl3乙醇液,105 ℃加热1 min,紫外光365 nm下检视。结果供试品色谱中,在与罗汉果黄素和山奈酚-3,7-O-α-L-二鼠李糖苷对照品色谱相应的位置上,显相同颜色的斑点,见图1A;再喷以2%香草醛溶液(以10%硫酸乙醇为溶剂),加热至斑点显色清晰,再检视,结果供试品色谱中,在与罗汉果皂苷V对照品色谱相应的位置上,显相同颜色的斑点,见图1B。
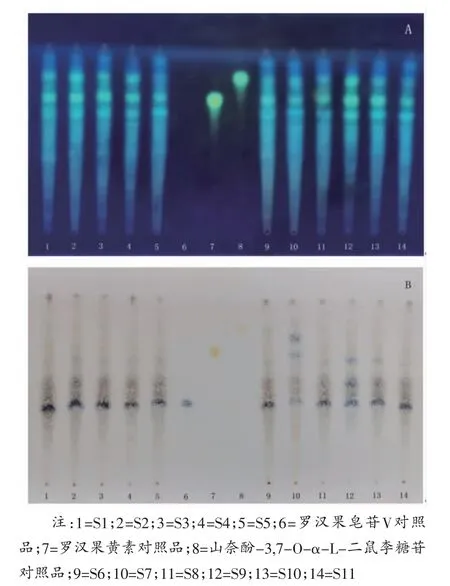
图1 TLC 色谱图
2.2 含量测定
2.2.1 色谱条件 色谱柱:Waters Acquity UPLC BEH C18(100 mm×2.1 mm,1.7 μm);流动相:乙腈(A)-0.2%磷酸(B),梯度洗脱及流速见表2;柱温:35 ℃;检测波长:203 nm;进样量:5 μL。

表2 流动相梯度洗脱及流速表
2.2.2 混合对照品溶液的制备 分别取罗汉果黄素、山奈酚-3,7-O-α-L-二鼠李糖苷和罗汉果皂苷V对照品适量,精密称定,加50%甲醇溶解并制成质量浓度分别为0.047 2、0.032 9、1.342 0 mg/mL的混合对照品溶液。
2.2.3 供试品溶液的制备 取罗汉果粉末约1.0 g,精密称定,置于具塞三角瓶中,精密加入50%甲醇10 mL,称定质量,超声(40 kHz,900 W)提取30 min,放冷,补足质量,摇匀,滤过,即得。
2.2.4 系统适用性试验 取上述混合对照品溶液、供试品溶液按上述色谱条件进样分析,记录色谱图(见图2)。结果3个成分的理论塔板数均不低于5 000,分离度均大于1.5。
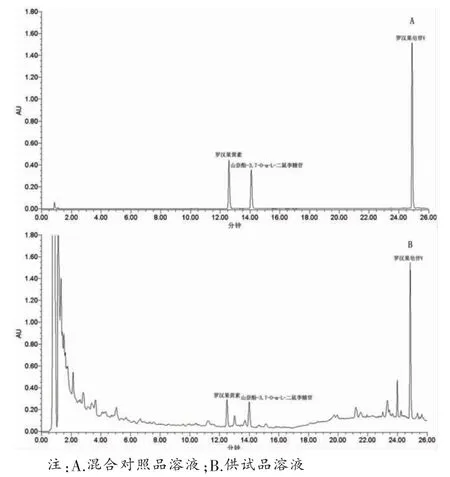
图2 UPLC 色谱图
2.2.5 线性关系考察 分别精密吸取“2.2.2”项下混合对照品溶液1.3、2.5、5.0、7.5、10.0 μL,按上述色谱条件进样分析,以峰面积为纵坐标(Y),质量浓度为横坐标(X,mg/mL)进行回归分析,结果见表3。

表3 3 个成分标准曲线及线性范围
2.2.6 精密度试验 精密吸取同一份供试品溶液,按上述色谱条件连续进样6次。结果罗汉果黄素、山奈酚-3,7-O-α-L-二鼠李糖苷和罗汉果皂苷V峰面积的RSD分别为0.69%、0.91%、0.69%,表明仪器精密度良好。
2.2.7 稳定性考察 取同一份供试品溶液,分别在0、2、4、8、12、24 h按上述色谱条件进样分析。结果罗汉果黄素、山奈酚-3,7-O-α-L-二鼠李糖苷和罗汉果皂苷V含量的RSD分别为1.81%、1.32%、1.50%(n=6),表明供试品溶液在24 h内稳定。
2.2.8 重复性考察 取同一批号供试品,共6份,分别按“2.2.3”项下方法制成供试品溶液,按上述色谱条件进样分析。结果罗汉果黄素、山奈酚-3,7-O-α-L-二鼠李糖苷和罗汉果皂苷V含量的RSD分别为1.83%、2.07%、1.77%,表明本法重复性良好。
2.2.9 加样回收率试验 取已知含量的供试品(批号:190401)6份各0.5 g,精密称定,分别加入一定量的混合对照品溶液,按“2.2.3”项下方法制成供试品溶液,按上述色谱条件进样分析。结果见表4。
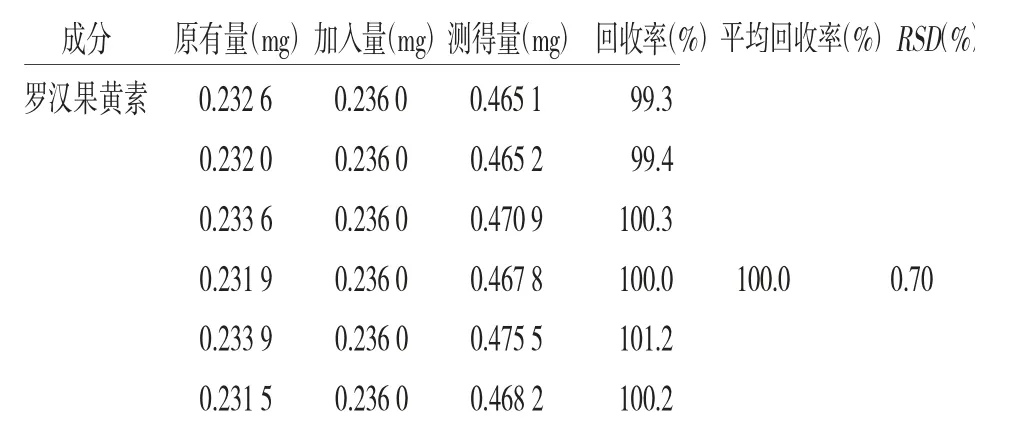
表4 3 个成分的加样回收率试验(n=6)
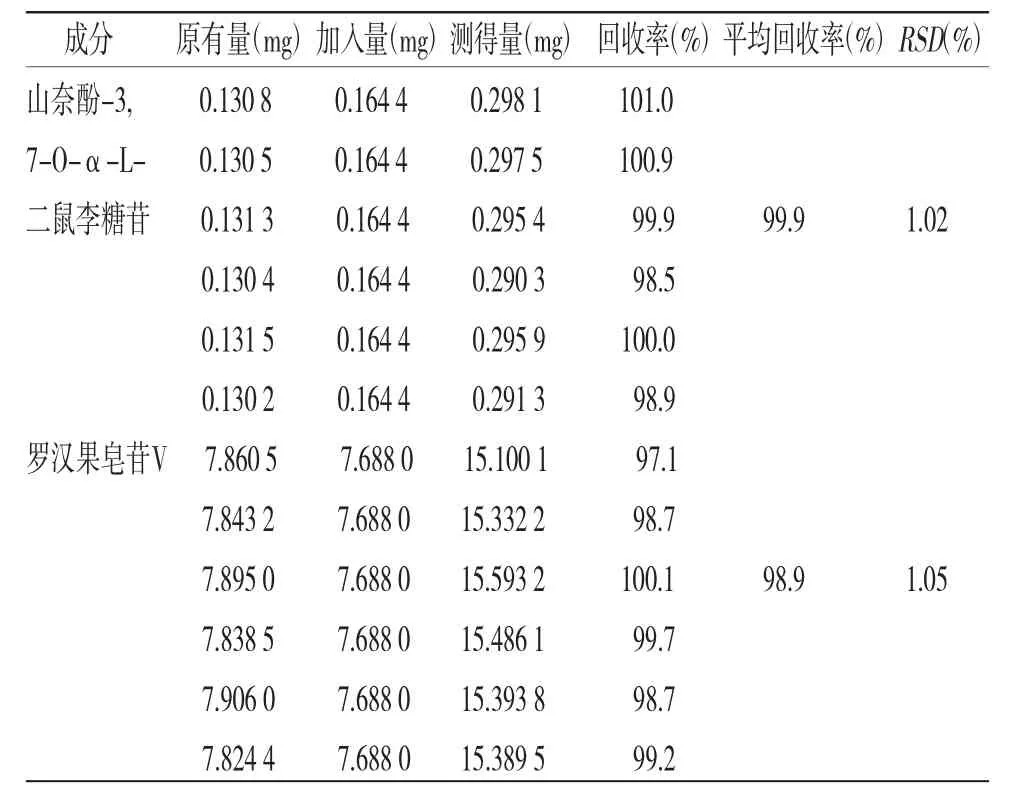
续表4:
2.2.10 含量测定 取11批罗汉果样品,按“2.2.3”项下方法制成供试品溶液,每批样品平行制备3份。按上述色谱方法进样分析。(见表5)
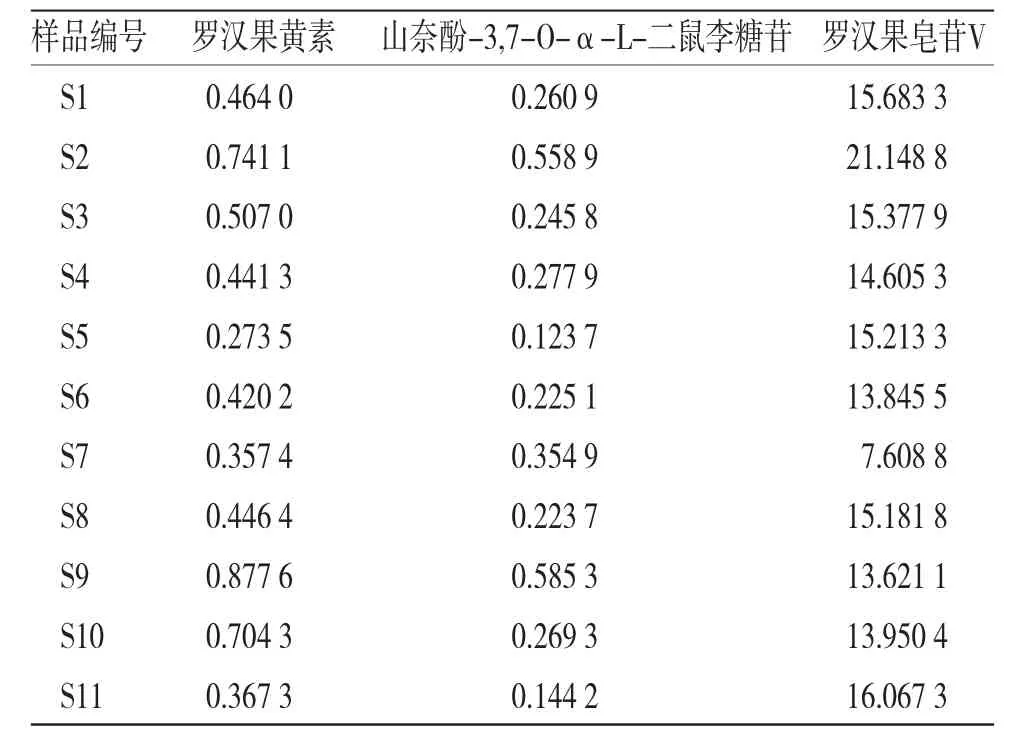
表5 11 批样品中3 个成分的含量(n=3,mg/g)
3 讨 论
3.1 测定指标的选择 罗汉果中罗汉果皂苷包括11-O-罗汉果苷V、罗汉果苷V、赛门苷I、罗汉果苷IV等[17-18],罗汉黄酮主要包含黄酮苷元山奈酚和槲皮素[19],黄酮苷槲皮素-3-Oβ-D-吡喃葡萄苷-7-O-α-L-鼠李糖苷、罗汉果黄素和山奈酚-3,7-O-α-L-二鼠李糖苷等[15-16,20]。因此本试验将罗汉果苷V、罗汉果黄素和山奈酚-3,7-O-α-L-二鼠李糖苷作为测定指标,评价罗汉果中皂苷、黄酮类成分的含量,能更全面综合地评价罗汉果的质量。
3.2 薄层色谱条件的考察 参照《中华人民共和国药典》(2015年版)一部罗汉果鉴别项下方法[11]进行试验,结果仅罗汉果皂苷V斑点清晰。考虑到罗汉果黄素、山奈酚-3,7-O-α-L-二鼠李糖苷具有较大的紫外吸收,故优化检视条件,即先喷以5%AlCl3乙醇液,加热后紫外365 nm下检视,结果罗汉果黄素、山奈酚-3,7-O-α-L-二鼠李糖苷斑点清晰,分离度好,再喷以2%香草醛溶液(以10%硫酸乙醇为溶剂),加热后日光下再检视,罗汉果皂苷V斑点清晰,分离度好,故确定该条件为最终的薄层色谱条件。
3.3 液相色谱条件的考察 采用UPLC法较普通HPLC法更节约时间,溶剂消耗量更少;考察了多种流动相系统,发现以乙腈-0.2%磷酸为流动相,所得色谱峰形好且稳定;通过PDA的全波长扫描发现,罗汉果黄素和山奈酚-3,7-O-α-L-二鼠李糖苷均在210nm后有两处最大吸收,分别为264 nm和342 nm,而罗汉果皂苷V在220 nm后没有最大吸收,《中华人民共和国药典》(2015年版)一部收载的罗汉果质量标准[11]和张彦东等[13]建立的罗汉果配方颗粒质量标准中罗汉果皂苷V的含量测定均在203 nm下进行,故本试验尝试以203 nm作为检测波长,结果基线更平稳且3个成分的峰面积均较大,故将203 nm确定为最终的检测波长。
3.4 指标的限量标准建议 在确定的色谱条件下测得11批罗汉果药材中罗汉果黄素、山奈酚-3,7-O-α-L-二鼠李糖苷和罗汉果皂苷V的含量,分别在0.273 5~0.877 6、0.123 7~0.585 3、7.608 8~21.148 8 mg/g之间,差异较大,因此参考含量最低值,拟定本品中罗汉果黄素(C33H40O19)含量不得少于0.27 mg/g,山奈酚-3,7-O-α-L-二鼠李糖苷(C27H30O14)含量不得少于0.12 mg/g,罗汉果皂苷V(C60H102O29)含量不得少于7.61 mg/g。与《中华人民共和国药典》(2015年版)一部罗汉果质量标准比较,增加了罗汉果黄素、山奈酚-3,7-O-α-L-二鼠李糖苷的含量限度,提高了罗汉果皂苷V的含量限度。
本试验建立了多成分的定量和定性方法,该方法简便、可靠,能有效地提高罗汉果的质量控制水平。

