右美托咪定联合利多卡因局麻对行椎体成形术的老年骨质疏松性骨折患者麻醉效果的影响
徐帅,韩丽春
(陕西省中医药大学附属医院·西安大兴医院麻醉科,陕西 西安 710000)
随着人口老龄化的加剧,骨质疏松性骨折发生率逐年增加[1]。对于骨折端的固定及复位主要有手术及非手术两种治疗方式,临床上可根据骨折部位及损伤程度决定治疗方式。手术治疗效果较理想,但老年患者骨骼修复能力差,且并发多种基础疾病,对常规手术的耐受性极差,围术期治疗风险高,再加上术后需长期卧床静养,关节功能的恢复受阻,甚至会出现一系列术后并发症。因此老年骨折患者的治疗需选择一类安全、有效的治疗方式[2-3]。椎体成形术(percutaneous vertebro plasty,PVP)是一种新型的微创手术,创伤小、效果确切、恢复快是其优点,但在临床治疗过程中,为了维持老年患者的生命体征,降低应激反应发生率,也需选择合理的麻醉方式以确保手术的顺利进行[4]。不同的麻醉药物对患者炎性反应及氧化应激反应的影响不同,右美托咪定可清醒镇痛,即使患者处于深度睡眠中也能被唤醒,且对呼吸功能的抑制较轻;利多卡因是一种抗心律失常的局部麻醉药,在局部微创手术中的应用优势较明显[5-6],但目前二者联合在老年骨质疏松性骨折患者PVP术中研究较少。本研究拟探讨利多卡因与右美托咪定联用对行PVP治疗的老年骨质疏松性骨折患者术中麻醉的效果,分析其对患者围术期循环功能稳定性、疼痛程度,认知功能的影响。
1 资料与方法
1.1 一般资料
收集2018年1月至2020年1月在陕西省中医药大学附属医院西安大兴医院行PVP手术治疗的106例老年骨质疏松性骨折患者,按照麻醉方式不同将分为研究组(n=57)和对照组(n=49)。研究组中,男性28例,女性29例;年龄61~80岁,平均(70.16±7.33)岁。对照组中,男性25例,女性24例;年龄60~81岁,平均(70.18±7.21)岁。两组一般资料比较,差异无统计学意义(P>0.05)。纳入标准:(1)均符合骨质疏松性骨折相关诊断标准[7];(2)均有手术指征,且需进行手术治疗者;(3)均知情并自愿参与本项研究者。排除标准:(1)合并严重心、肝、肾器质性功能障碍者;(2)窦性心动过缓者;(3)长期应用镇痛、镇静类药物治疗者;(4)严重意识障碍者。所有患者术前均知情并签署医院伦理委员会出具的知情同意书。
1.2 方法
患者入手术室,常规予以生命体征监测,开放静脉通道,2 L/min氧气经鼻导管吸入。两组患者均由同一麻醉医师进行围术期麻醉管理。患者取俯卧位,1.0%浓度利多卡因40 mL进行局部浸润麻醉,观察组随后使用右美托咪定(首次1.0 μg·kg-1·h-1,10 min后调整剂量为0.5μg·kg-1·h-1)以静脉持续泵入的形式直至手术结束;对照组患者给予同等剂量生理盐水静脉泵注,直至手术结束。
1.3 观察指标
(1)比较两组麻醉效果,包括感觉阻滞起效时间、运动阻滞起效时间、持续时间、最高平面、达最高平面时间。(2)以麻醉前(T0)、麻醉后20 min(T1)、麻醉后1 h(T2)为不同时间点,记录患者循环功能稳定性,包括心率(heart rate,HR)、平均动脉压(mean arterial pressure,MAP)、中心静脉压(central venous pressure,CVP)。(3)采用酶联免疫吸附测定(enzyme linked immunosorbent assay,ELISA)法检测患者T0、T1、T2时间点炎症因子水平变化情况,包含血清白细胞介素-6(interleukin,IL-6)、肿瘤坏死因子(tumor necrosis factor α,TNF-α)。(4)采用简易智力状态检查量表(mini-mental state examination,MMSE)对患者T0、T1、T2时刻认知功能进行评估,低于27分为认知功能障碍,采用疼痛视觉量表(visual analogue scale,VAS)对患者T0、T1、T2时刻疼痛程度,0分为无痛,10分为剧烈疼痛,得分越高,越疼痛。(5)记录两组不良反应发生率,包括头痛、低血压、心动过缓。
1.4 统计学分析
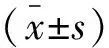
2 结果
2.1 两组麻醉效果比较
研究组感觉阻滞、运动阻滞起效时间均短于对照组,但持续时间均长于对照组,最高平面、达最高平面时间均低于对照组(P<0.05)。见表1。
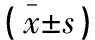
表1 两组麻醉效果比较
2.2 两组不同时期循环功能稳定性指标比较
两组在T0时期HR、MAP、CVP水平比较,差异无统计学意义(P>0.05);T1、T2时间段两组HR均升高,T1两组MAP、CVP均明显升高,而T2点以上指标较T1点低,且两组在T1、T2时间段的HR、MAP、CVP水平比较,差异有统计学意义(P<0.05)。见表2。
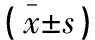
表2 比较两组不同时期循环功能稳定性指标变化情况
2.3 两组患者炎症因子指标比较
两组在T0时刻IL-6、TNF-α比较,差异无统计学意义(P>0.05);T1时刻两组IL-6、TNF-α较T0时刻升高,且研究组低于对照组(P<0.05);T2时刻两组IL-6、TNF-α指标均降低,研究组低于对照组(P<0.05)。见表3。
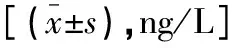
表3 不同麻醉方式对患者炎症因子指标的影响
2.4 两组患者认知功能及疼痛程度比较
两组在T0、T1、T2时刻MMSE评分比较,差异无统计学意义(P>0.05),两组在T0时刻VAS评分比较,差异无统计学意义(P>0.05),但在T1时刻两组VAS评分均降低,T2时刻两组VAS评分有所升高,但研究组在T1、T2时刻VAS评分均低于对照组(P<0.05)。见表4。
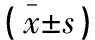
表4 不同麻醉方式对患者认知功能及疼痛程度的影响
2.5 不良反应比较
对照组不良反应发生率为12.24%,略高于研究组8.77%,但两组不良反应发生率比较差异无统计学意义(P>0.05)。见表5。
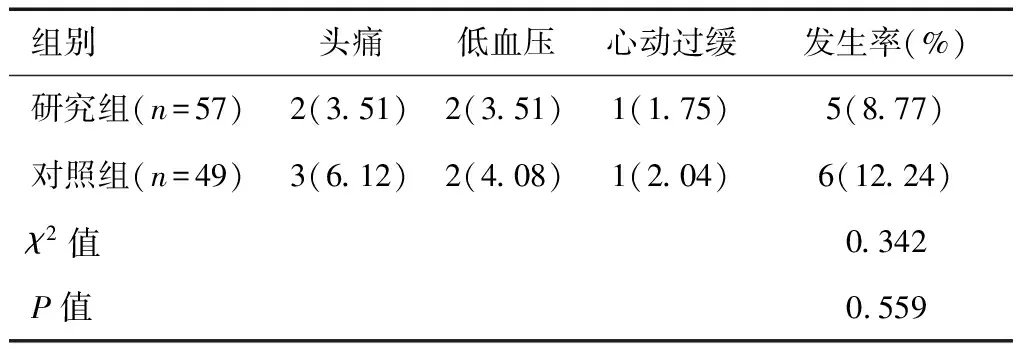
表5 不良反应比较[n(%)]
3 讨论
老年患者在围术期可能因机体创伤及身体机能降低导致出现剧烈疼痛及严重应急反应,导致在手术过程中出现无法有效稳定血流情况,进而导致机体交感神经在较长时间内处于兴奋状态,术后可能出现心、脑血管疾病等一系列并发症,增加围术期风险。因此,在麻醉管理中如何给予有效的处理以稳定老年手术患者的血流动力学,确保围术期安全与质量仍是当前临床工作的研究重点[8]。局部麻醉浸润在手术中通常能在一定程度上稳定患者血流动力学各项指标水平,但对于老年患者在缓解疼痛及改善循环功能稳定方面效果欠佳[9],因此选用合适的镇痛药物辅助是确保围术期麻醉安全与质量的关键。
本研究发现,研究组的感觉阻滞起效时间、运动阻滞起效时间、最高平面时间、达最高平面时间均明显短于对照组,但感觉阻滞和运动阻滞持续时间均长于对照组,提示右美托咪定联合利多卡因局麻在行PVP治疗的老年骨质疏松性骨折患者中的麻醉效果优于单独采用利多卡因局麻,可能是因为右美托咪定可广泛分布在周围神经系统及中枢神经系统中,通过刺激突出肾上腺素能受体进行负反馈调节,进一步导致局部神经细胞呈现超膜化,出现抑制运动及感觉的情况[10]。脑干蓝斑区主要集中脑部α2肾上腺素能受体,可控制睡眠及觉醒,参与去甲肾上腺素能传导。右美托咪定作用在蓝斑区α2肾上腺素能受体上时,则会产生、维持非动眼睡眠,随后有效维持呼吸系统稳定,因此在药效消失后患者可以迅速苏醒,不会对呼吸产生抑制[11-12]。本研究发现,两组患者在T0时期HR、MAP、CVP水平比较无显著差异,T1、T2时间段两组的HR均明显升高,T1两组MAP、CVP均明显升高,T2点较T1点明显降低,且两组在T1、T2时间段的HR、MAP、CVP水平比较有显著差异,提示利多卡因结合右美托咪定还可有效改善老年骨质疏松性骨折患者循环功能稳定性。针对在患者应用利多卡因局部侵润麻醉后,机体依旧会出现应激反应,考虑可能是受到围术期焦虑、恐惧心理影响,而右美托咪定的应用能直接作用人体,能起到良好的镇痛及镇静效果。虽然在临床使用会出现一定的血流动力学变化(心率减慢,血压降低),但不会对患者手术疗效及整体流程产生严重不良影响[13]。另外,本研究选择右美托咪定作为辅助麻醉药物,主要是利用该药物的镇静、镇痛效果及高选择性对交感神经的兴奋状态进行抑制,缓解机体疼痛感及焦虑感,进一步有效稳定患者围术期的血流动力学[14-15]。两组在T0时刻IL-6、TNF-α比较无显著差异,T1时刻IL-6、TNF-α较T0时刻明显升高,研究组以上指标低于对照组;T2时刻两组IL-6、TNF-α指标均明显降低,研究组以上指标也低于对照组,提示在应用右美托咪定联合利多卡因局麻后,较单独应用利多卡因局麻更能减轻机体炎症反应、减少认知障碍等神经功能异常的发生。推测其原因可能是炎症因子可在通过血脑屏障后增加细胞膜通透性,引起细胞水肿,使神经系统产生干扰,对突触连接功能产生影响,激活中枢神经中的小胶质细胞分泌炎症细胞因子后加重炎症反应,对海马区神经细胞产生影响,进一步加重认知功能障碍[16-17]。本研究还发现,两组在T0、T1、T2时刻MMSE评分比较均无显著差异;在T0时刻VAS评分比较无显著差异,但在T1时刻两组VAS评分均显著降低,T2时刻两组VAS评分均有所升高,但研究组在T1、T2时刻VAS评分均低于对照组,提示利多卡因、右美托咪定联合利多卡因均不会影响患者的认知功能,但联合麻醉更能降低患者疼痛程度。分析可能是因为右美托咪定有以下机制:(1)在给药后直接被吸收,产生良好镇痛效果,降低术后疼痛,改善疼痛引起的认知损伤;(2)降低机体急性炎症反应,避免术后出现的继发性损伤损害脑部认知功能;(3)促进黏着斑激酶磷酸化,进一步抑制机体中参与凋亡的相关蛋白酶表达,提高脑部细胞的存活率,保护脑部神经及功能;(4)对交感神经活性进行抑制,降低机体中血浆皮质醇,进一步降低对海马细胞的损伤[18]。本研究中两组不良反应发生率比较无显著差异,提示在利多卡因局麻基础上加用右美托咪定进行麻醉处理不会增加不良反应。
综上所述,行PVP治疗的老年骨质疏松性骨折患者在应用右美托咪定联合利多卡因局麻后机体炎症反应及疼痛程度明显减轻,安全有效,能极大的提升围术期质量与安全,利于加速康复外科的推广,值得临床推荐。

