同位素稀释液相色谱-串联质谱法检测血清睾酮候选参考方法的建立及应用
孙贺伟, 居 漪, 朱岭峰, 李 卿, 金中凎, 张素洁
(上海市临床检验中心,上海 200126 )
睾酮是一种类固醇类激素,由胆固醇经一系列酶促反应生成。准确的睾酮检测结果有助于男性性腺功能减退、肿瘤[1-2]和女性多囊卵巢综合征[3]等疾病的诊断。目前,血清睾酮检测多采用免疫学方法。临床常规方法在检测正常男性血清睾酮水平时具有较好的准确性,但在检测女性或儿童血清睾酮水平时并不准确[4]。因此,要想实现血清睾酮检测的标准化就必须建立参考方法。目前,德国临床化学和检验医学学会[5]、比利时根特大学[6]已建立了基于气相色谱质谱的参考方法;美国国家标准和技术研究院(the National Institute of Standards and Technology,NIST)[7]和美国疾病预防控制中心(the Centers for Disease Control and Prevention,CDC)[8]建立了基于液相色谱-串联质谱(liquid chromatography tandem mass spectrometry,LCMS/MS)的参考方法。在此基础上,本研究拟建立一种基于同位素稀释液相色谱-串联质谱(isotope dilution liquid chromatography tandem mass spectrometry,ID-LC-MS/MS)的精密度、准确度均良好,操作简便的候选参考方法,并对该方法的检测性能进行评价,同时采用该方法对临床常规检测方法(微粒子化学发光法)进行评价。
1 材料和方法
1.1 仪器与试剂
LC-MS/MS检测系统由5500 QTRP串联质谱仪(美国SCIEX公司)和Agilent1290UPLC液相色谱系统(美国Agilent公司)组成。Vortex-2涡旋混合器(美国Scientific Industries公司),5424R冷冻高速离心机(德国Eppendorf公司),TS-18824氮吹仪(美国ThermoFisher Scientific公司),Access 2全自动微粒子化学发光免疫分析仪(美国Beckman Coulter公司)及配套睾酮检测试剂(微粒子化学发光法)。睾酮标准品(纯度99%)购自德国Dr. Ehrenstorfer公司;睾酮同位素内标(睾酮-2,3,4-13C3)购自美国Cerilliant公司[(100.0±0.5)μg/mL];甲酸(质谱纯)、正已烷(质谱纯)、乙酸乙酯(质谱纯)、乙腈(质谱纯)均购自美国ThermoFisher Scientific公司。实验用水由本实验室采用Millipore纯水系统自制(18.2 MΩ)。
1.2 方法
1.2.1 色谱分析条件 分析柱为Kinetex XB C18 100A柱(2.1 mm×100 mm,1.7 μm,美国Phenomenex公司);流动相A为0.1%甲酸水溶液,流动相B为0.1%甲酸乙腈溶液,梯度洗脱(0~0.50 min 10%B;0.51~3.00 min 10%~100%B;3.01~4.50 min 100%B;4.51~6.00 min 10%B),流速为0.3 mL/min,进样体积为10 μL。
1.2.2 质谱分析条件 电喷雾电离(electrospray ionization,ESI)离子源,正离子模式。喷雾气为65,辅助加热气为65,气帘气为30,碰撞气为中等,离子源电压为5 500 V,离子源温度为400 ℃。多反应监测扫描分析睾酮的离子通道选择分别为289.2/97.1 amu、289.2/109.1 amu,睾酮同位素内标为292.2/100.1 amu、292.2/112.1 amu。
1.2.3 样本处理 吸取100~300 μL血清,加入内标工作液(10 ng/mL),使得睾酮与内标的质量比为1∶1,室温平衡1 h,再加入1 mL正已烷-乙酸乙酯(V∶V=1∶1)溶液,涡旋振荡10 min,然后14 087×g离心5 min,取上清液,30 ℃吹干,加入200 μL 50%乙腈重组,涡旋混匀2 min后,吸取100 μL转移至进样瓶,上机分析。
1.2.4 储备液及工作液配制 睾酮和同位素内标均用甲醇配成1 mg/mL的储备液,然后用50%甲醇将睾酮储备液稀释至10 ng/mL,作为标准曲线工作液,4 ℃保存。将同位素内标储备液稀释至50 ng/mL,作为内标工作液,4 ℃保存。分别吸取250、400、500、600、750 μL标准曲线工作液(10 ng/mL),与100 μL内标工作液(50 ng/mL)混匀,使标准曲线中睾酮与内标质量比分别为0.5、0.8、1.0、1.2、1.5。
1.3 方法学评价
参考美国临床实验室标准化协会(the Clinical and Laboratory Standards Institute,CLSI)C62-A文件[9]和EP15-A3文件[10],对本方法的方法残留、特异性、线性范围、精密度、准确度进行验证。
1.3.1 特异性 分析内标化合物对分析物的干扰。进样时,在标准曲线后添加1个只含内标不含分析物的样本(标记为QC0)。若每批次QC0样本的分析物色谱峰信噪比(signal-to-noise ratio,RSN)均<3∶1,则认为内标对分析物无干扰。
1.3.2 方法残留 取睾酮<0.01 ng/mL的低浓度血清,加入睾酮标准溶液,配制成睾酮浓度为20 ng/mL的高浓度样本(H),将不含分析物的50%甲醇作为空白样本(O)。经过样本预处理后,按照H→O的顺序重复进样3次。若空白样本O中分析物的RSN<3∶1,则认为该方法无残留。
1.3.3 精密度 依据CLSI EP15-A3文件对精密度的要求,测定2017年参考实验室外部质量评价计划(the International Federation of Clinical Chemistry and Laboratory Medicine External Quality Assessment Scheme for Reference Laboratories in Laboratory Medicine,RELA)比对样本,共测定3 d,每天分析1批。每个批次分析2个浓度RELA样本,每批次每个浓度预处理3次,并重复测定5次,计算每个浓度的批内变异系数(coefficient of variation,CV)和批间CV。
1.3.4 准确度 通过测定有证参考物质SRM971和参加RELA来评价本方法的准确度。每个样本共测定3个批次,每批次每个浓度预处理3次,并重复测定3次。
1.3.5 线性范围 收集睾酮<0.5 ng/mL的低浓度血清,添加睾酮储备液,配制成血清睾酮浓度为22.00 ng/mL 的高浓度样本(H),以睾酮浓度为0.034 ng/mL的混合血清样本为低浓度样本(L)。按照等体积对倍稀释方法稀释成11个浓度(0.034、1.14、2.78、4.15、5.53、8.27、11.02、13.76、16.51、19.25、22.00 ng/mL)。将稀释后的样本进行前处理后重复检测2次,计算实测值与理论值之间的线性关系。若r≥0.995,且残差<8.75%,则认为本方法在0.034~22.00 ng/mL范围内线性良好。
1.3.6 最低定量限 用50%甲醇对已知浓度(4.45 ng/mL)的血清样本进行稀释,得到理论浓度分别为50、20、10 pg/mL的定量限样本。将不同浓度定量限样本各分成10份,预处理后检测,得到实测值。将同时满足偏移≤10%、CV≤7%、RSN≥10的实测值定义为定量限。
1.3.7 基质效应 将6份血清(3份女性样本、3份男性样本)分别与等体积50%甲醇混合,得到6份混合血清。将原始血清样本和混合血清样本按样本预处理方法处理,按混合血清→候选基质(50%甲醇)的顺序重复进样3次,计算分析物/内标比值。若混合样本的分析物/内标比值与理论比值的偏差≤±20%,则判定为无相对基质效应。
1.4 临床常规检测方法(微粒子化学发光法)正确度评价
参考CLSI EP9-A3文件[11],使用建立的IDLC-MS/MS方法对微粒子化学发光法的正确性进行评价。收集临床血清样本122例,排除脂血、黄疸、脂浊等样本,分别采用微粒子化学发光法和本方法检测睾酮浓度。每份样本每种方法均重复检测3次,计算均值。以ID-LC-MS/MS结果为横坐标,以微粒子化学发光法结果为纵坐标,进行偏差分析。
1.5 不确定度初步评定
依据文献[12]对血清样本检测结果的不确定度的来源进行分析。其中,A类不确定度主要来自样本的重复测定;B类不确定度主要来源于睾酮标准物质纯度、睾酮标准物质称量、睾酮标准物质溶解、移液器移液过程引入的不确定度。
1.6 统计学方法
采用MedCalc 18.2.1软件、Excel 2013软件进行统计分析。采用五点包括法计算血清睾酮浓度。采用Passing-Bablok线性回归分析、Bland-Altman一致性分析对方法比对结果进行分析。
2 结果
2.1 方法建立及方法学评价
2.1.1 方法残留和特异性 ID-LC-MS/MS检测血清睾酮的分析时间为5 min,特异性好,无残留。见图1。

图1 ID-LC-MS/MS的残留和特异性
2.1.2 精密度 ID-LC-MS/MS的批内精密度≤2.3%,批间精密度≤2.2%。见表1。

表1 ID-LC-MS/MS检测血清睾酮的精密度
2.1.3 准确度 在2017年的RELA比对中,本实验室(编号为54)结果符合等效限要求(±8.75%)。本法测定有证参考物质SRM971的结果在规定的不确定度范围(6.44±0.15)ng/mL]内。见表2。

表2 ID-LC-MS/MS检测血清睾酮的准确度
2.1.4 线性范围 在0.034~22.00 ng/mL范围内,实测值和理论值的相关性良好(r=0.999)。见图2。

图2 ID-LC-MS/MS检测血清睾酮的线性范围
2.1.5 最低定量限 同时满足偏移≤10%、CV≤7%、RSN≥10的最低定量限为20 pg/mL。见表3。

表3 ID-LC-MS/MS检测血清睾酮的最低定量限
2.1.6 基质效应 6份混合样本的分析物/内标比值与理论比值的偏差(相对基质效应)分别为5.6%、2.7%、6.9%、2.8%、-4.4%、-1.50%。见表4。

表4 ID-LC-MS/MS检测血清睾酮的基质效应
2.2 临床常规检测方法(微粒子化学发光法)评价
当血清睾酮浓度为0.09~18.37 ng/mL时,微粒子化学发光法与ID-LC-MS/MS具有良好的相关性。2种方法的Passing-Bablok线性回归方程为Y微粒子化学发光法=0.880 597XID-LC-MS/MS-0.109 403(截距的95%可信区间为0.016 23~0.202 00,斜率的95%可信区间为0.840 2~0.930 8,r=0.963),见图3。2种方法检测结果之间的平均偏差为-24.4%,见图4。高浓度(睾酮>1 ng/mL)样本2种方法检测结果之间的平均偏差为6.3%,见图5。低浓度(睾酮≤1 ng/mL)样本2种方法检测结果之间的平均偏差为62.4%,见图6。
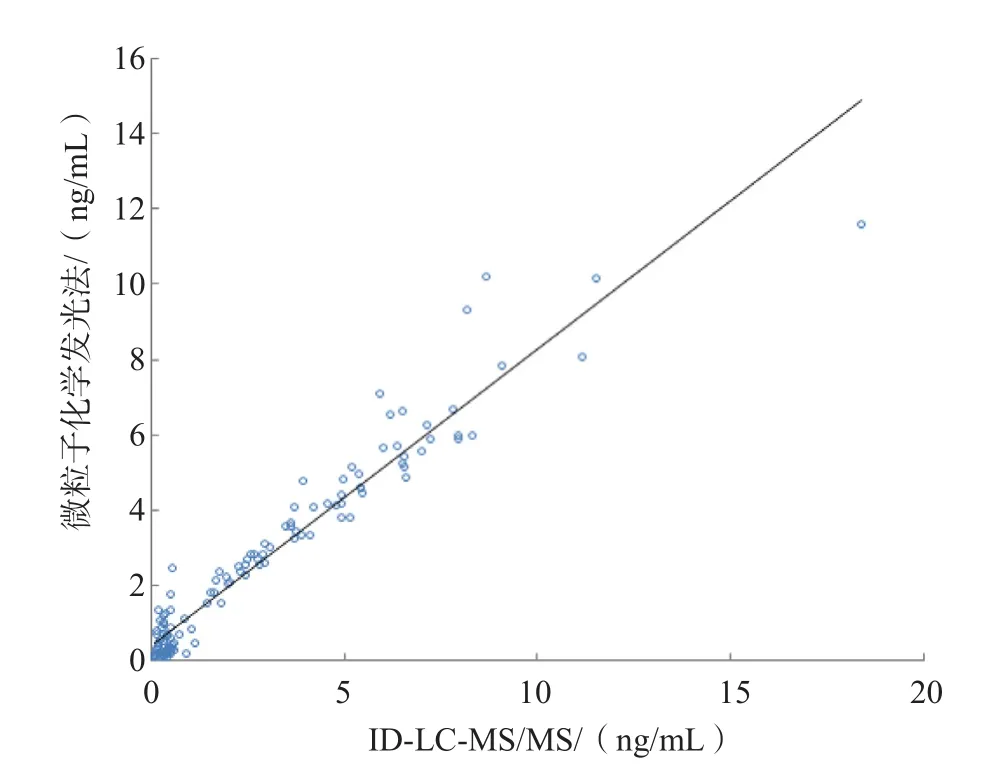
图3 微粒子化学发光法与ID-LC-MS/MS检测血清睾酮的相关性

图4 微粒子化学发光法与ID-LC-MS/MS血清睾酮检测结果的Bland-Altman图

图5 微粒子化学发光法与ID-LC-MS/MS检测高浓度(睾酮>1 ng/mL)样本的Bland-Altman图

图6 微粒子化学发光法与ID-LC-MS/MS检测低浓度(睾酮≤1 ng/mL)样本的Bland-Altman图
2.3 不确定度评定
以2017 RELA-A样本为例,对ID-LCM S/M S检测血清睾酮的不确定度进行评定,结果见表5。根据表5中各相对标准不确定度分量计算出合成相对标准不确定度为0.012 852。2017 RELA-A样本测定均值为4.32 ng/mL,扩展不确定度为0.11 ng/mL(包含因子k=2)。

表5 ID-LC-MS/MS检测2017 RELA-A样本的不确定度评定
3 讨论
本研究参考美国CDC的参考测量程序,建立了基于LC-MS/MS技术的血清睾酮候选参考方法。相对于气相色谱质谱参考方法的样本前处理过程,美国NIST和美国CDC分别基于LCMS/MS技术建立的2种参考方法的前处理过程相对简单,但操作步骤仍较多。美国NIST参考方法[7]的样本前处理需先经过液相萃取,再复溶,用正己烷进行2次液液萃取。美国CDC参考方法[8]的样本前处理需先调节样本pH值,再用乙酸乙酯-正已烷(V∶V=3∶2)溶液萃取2次,氮气吹干,然后用碳酸盐溶液复溶,之后再用正已烷萃取2次。复杂的样本前处理步骤有助于除去杂质对睾酮分析的干扰,提高质谱响应,但样本前处理时间会大大增加。在满足精密度和准确度要求的同时,本研究对样本前处理过程进行优化,采用正己烷-乙酸乙酯一步萃取。另外,美国NIST和美国CDC参考方法的色谱分析时间均较长(美国CDC方法为16 min,美国NIST方法为40 min),而本研究建立的ID-LC-MS/MS法采用超高压液相色谱串联质谱系统和粒径为1.7 μm的超高效液相色谱柱,色谱分析时间缩短至5 min。
采用LC-MS/MS技术实现准确测量的关键之一是排除与分析物结构相同或相似物质的干扰,BOTELHO等[8]证实18种与睾酮相对分子质量接近的化合物对美国CDC参考方法检测睾酮无影响。张天娇等[13]的研究结果显示,与睾酮相对分子质量相同的表雄酮经过液相分离,可以排除对睾酮检测的影响。本研究的不足之处在于未对睾酮结构类似物等物质进行干扰分析,但可以通过2点间接排除部分干扰物对IDLC-MS/MS法检测睾酮的影响:(1)相对于氘标记的同位素内标,采用13C标记的同位素内标在液相色谱和质谱中的变化与睾酮高度一致,且物理性状稳定,半衰期更长;(2)ID-LCMS/MS检测122例临床样本血清睾酮的定量色谱峰和定性色谱峰面积比值与标准曲线中两者的峰面积比值进行比较,无明显差异。
本研究结果显示,临床常规检测方法(微粒子化学发光法)与ID-LC-MS/MS法检测结果的相关性较好(r=0.963),但结果偏差较大,平均偏差为-24.4%。本研究根据ID-LC-MS/MS检测结果将临床样本分为高、低2个浓度,低浓度为血清睾酮≤1 ng/mL,高浓度为血清睾酮>1 ng/mL,然后再进行Bland-Altman一致性分析。结果显示,低浓度样本2种方法的平均偏差为-62.4%,高浓度样本2种方法的平均偏差为6.3%,与文献报道[14]一致。由此可见,微粒子化学发光法检测低浓度睾酮的正确性并不理想。原因可能是抗体与其他类固醇激素会产生交叉反应,也可能与睾酮低浓度标准工作液的准确性有关。具体原因仍需进一步研究。
综上所述,本研究建立了检测血清睾酮的ID-LC-MS/MS候选参考方法。该方法精密度、准确度均较好,且操作相对简便,分析时间短。临床常规检测方法(微粒子化学发光法)与ID-LC-MS/MS的相关性良好,但低浓度样本2种方法之间偏差较大,仍需加强血清睾酮临床常规检测方法的质量控制。开展正确度验证计划是提升临床血清睾酮检测质量的有效方法。本研究建立的候选参考方法可在临床血清睾酮检测质量改善中发挥积极作用。

