GC-MS测定西洋参中的腐霉利
朱日然,牛水蛟,刘 莹,张先勤,李启艳,林钰镓*
(1. 山东中医药大学附属医院,山东 济南250012;2. 山东省食品药品检验研究院/国家药品监督管理局 化妆品原料质量控制重点实验室,山东 济南 250101;3. 济南市历下区卫生和计划生育监督所,山东 济南 250021)
西洋参,五加科人参属植物西洋参(Panax quinquefolium L.)的干燥根[1],最初生长于北美洲原始森林中,主产于加拿大和美国,后经引进,在我国辽宁、山东、吉林、北京等地广泛种植[2]。西洋参性凉、味甘、微苦,补气养阴性能极佳,在治疗阴虚津伤、气阴两虚等方面较人参更为柔和,适宜于中老年及身体虚弱人群食用[3]。现代医学研究发现,西洋参作为临床贵重药材之一,在提高免疫力、抗癌、降血糖等方面有显著功效[4]。但作为一种外来名贵药材,西洋参同样面临多种病害的威胁,如西洋参1~2年生上立枯病、拌倒病的发病率较大,在3~4年生上黑斑病、白粉病的发病率较大[5]。庄绪静等[6]采用腐霉利对西洋参病害进行防治,得到了较好的效果。
腐霉利(速克灵、二甲菌核利),国际通用名:Procymidone,化学名称:N-(3,5-二氯苯胺)-1,2-二甲基环丙烷-1,2-二羰基亚胺,结构见图1,是一类环酰亚胺类农用内吸性杀菌剂,于1972年由日本住友化学株式会社研制成功。主要通过抑制菌体内甘油三酯合成,达到保护和治疗农作物病害的双重作用[7]。
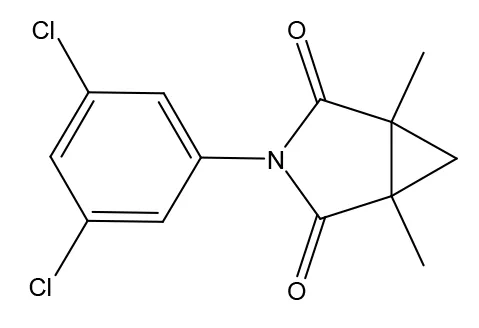
图1 腐霉利结构式
然而作为一种有机氯农药,腐霉利对人体和土壤环境均有一定危害,因此,欧盟和美国等国家或地区,相继对进口食品中的腐霉利残留量提出了严格的限量标准,如欧盟规定果蔬中腐霉利的最大残留限量(maximum residue limit,MRL)值为0.02 mg/kg,美国食品和药物管理局(FDA)和加拿大规定葡萄酒中腐霉利的MRL值分别为0.2 mg/kg和1.0 mg/kg,日本实行的“肯定列表制度”中有关食品限量的暂定标准规定腐霉利的MRL值为0.02 mg/kg,而对于其他在暂定标准以外的农业品实行“一律标准”,即0.01 mg/kg[8],我国也制定了蔬菜和油脂等产品中腐霉利残留的限量标准[9]。
目前腐霉利残留的检测方法主要有气相色谱法[10]、荧光光谱法[11]、高效液相色谱法[12]、气相色谱-串联质谱法[13]等。前处理方法主要有固相萃取法[14]、基质固相分散萃取[15]、QuEChERS法[16]等。QuEChERS法是一种较新颖的前处理方法,具有分析速度快,溶剂使用量少,简便、快速、灵敏、准确等优势,可简化繁杂的净化步骤。气相色谱-串联质谱法(GC-MS)具有定性、定量准确,灵敏度高,线性范围广等优点。本研究采用乙腈提取,QuEChERS净化,外标法定量,GC-MS法测定西洋参中腐霉利的残留量,以期建立一种快速检测西洋参中腐霉利残留量的分析方法。
1 材料与方法
1.1 仪器与试剂
Thermo TRACE 1300-ISQ气相色谱质谱联用仪(赛默飞公司);Mettler Toledo MS 电子天平(梅特勒-托利多仪器有限公司);Milli-Q超纯水机(Millipore有限公司); Universal320R高速冷冻离心机(德国Hettich公司);KQ-500DE 型数控超声仪(昆山市超声仪器有限公司)。
QuEChERS萃取盐包(4 g MgSO4+1 g NaCl+1 g柠檬酸钠+0.5 g柠檬酸氢二钠);QuEChERS净化管15 ml(400 mg PSA+400 mg C18+1200 mg MgSO4)。
腐霉利对照品,纯度99.8 %,批号B0003652,Be Pure公司;甲苯、乙酸乙酯、乙腈等有机溶剂均为分析纯;QuEChERS快速净化小柱。
1.2 仪器条件
色谱柱:DB-5MS,30 m×0.25 mm×0.25 μm;载气:氦气,纯度≥ 99.999 %;恒流流速:1.00 ml/min;进样方式:不分流;离子源:EI源,离子源温度:230 ℃;电离能量:70 eV;色质接口温度:250 ℃;传输线温度:280 ℃;进样量:1 μl,溶剂延迟:8 min。
升温程序:100 ℃保持1 min,以15 ℃/min速率升温至280 ℃,然后保持15 min,运行总时间28 min。
测定方式:全扫描和选择离子监测同时采集模式。全扫描离子(m/z):50-300;监测离子(m/z):96,254,283,285;定量离子:m/z 285。
1.3 样品溶液的制备
称取西洋参粉末(过三号筛)2.0 g置入50 ml具塞离心管中,先加入水10 ml涡旋混匀,再加入乙腈10 ml和QuEChERS萃取盐包,用力振摇1 min,4000 r/min离心5 min。先用2 ml甲苯预饱和净化管,混匀净化管,取6 ml乙腈层加入净化管中,涡旋混匀后4000 r/min离心3 min,然后取上清4 ml 40 ℃氮气吹干,加丙酮1 ml复溶后,过0.22 μm有机滤膜,滤液待测定。
1.4 标准溶液的制备
吸取一定量腐霉利对照品(in acetone)置入10 ml量瓶,用丙酮逐级稀释并定容得到0.5,1.0,2.5,5.0,10 μg/ml的腐霉利系列标准工作溶液,上机测定。
1.5 色谱及质谱行为
在上述仪器条件下,分别对标准溶液和样品进行测定,得其保留时间为14.59 min,丰度比m/z 96: 254: 283: 285 = 100: 3: 37: 23,见图2、图3。
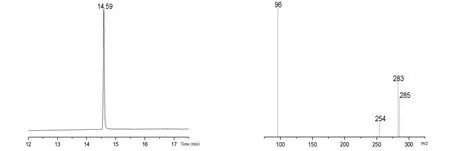
图2 标准溶液的总离子流图及选择离子流图
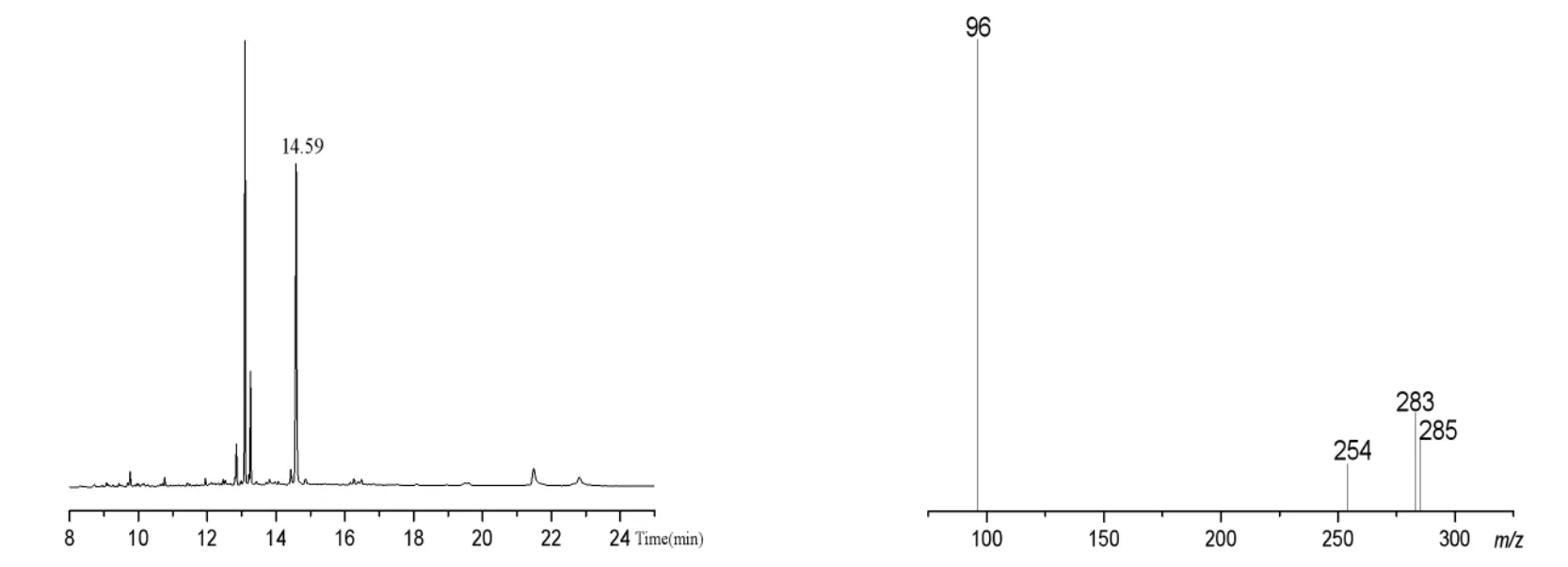
图3 样品溶液的总离子流图及选择离子流图
2 结果与分析
2.1 方法学验证
2.1.1 线性范围、检出限和定量限 测定“1.4”项中的标准溶液,以面积对浓度作图,浓度为横坐标,峰面积为纵坐标绘制标准曲线。同时,将标准溶液进行稀释并测定,以S/N=3时的浓度计算检出限,以S/N=10时的浓度计算定量限,结果见表1。

表1 腐霉利保留时间、线性范围、回归方程、相关系数、检出限和定量限
2.1.2 回收率 按“1.2”项方法对空白样品进行低、中、高3个水平的加标回收试验,每水平各测定6份,分别计算回收率及相对标准偏差(RSD),结果见表2。

表2 回收率试验结果(n=6)
2.1.3 稳定性 取浓度为5 μg/ml标准溶液对腐霉利进行稳定性测试,按上述仪器条件分别在0,2,4,8,12,24 h进行测定,根据测定的目标化合物峰面积计算RSD为1.99 %,表明该成分在24 h内稳定。
2.1.4 日内和日间精密度 取浓度为5 μg/ml标准溶液对腐霉利进行精密度研究,于一日内连续进样6次,计算峰面积日内精密度RSD为0.86 %;连续进样3天,每天6次,计算3天的峰面积日间精密度RSD为1.66 %,表明日内及日间精密度结果均良好。
2.1.5 重复性 取一批样品,精密称定6份,按“1.3”项法制备,按上述仪器条件分别进行测定,根据测定的目标化合物浓度计算RSD,结果为2.09 %,表明该方法重复性良好。
2.2 样品测定
本研究共收集不同产地的西洋参药材35批,采用上述方法对该35批样品进行前处理并测定,每批样品平行测定2份,结果表明,共有10批药材检出腐霉利,浓度为1.06~3.73 mg/kg。
3 讨论
3.1 提取溶剂的选择
QuEChERS法有多种提取溶剂,常用的有乙腈、乙酸乙酯、丙酮等,三者对有机化合物提取效果略有不同。本实验选用乙腈作为提取溶剂,主要有以下3个原因:(1)丙酮与水的互溶度较大,可能导致待测组分的回收率降低;(2) 提取弱极性的化合物时可选用乙酸乙酯,而对于较强极性的成分,乙酸乙酯提取效果不佳;(3)腐霉利结构中含有2个内酰胺键,极性较大,适合用乙腈提取,且乙腈对脂肪和色素的溶解性相较丙酮和乙酸乙酯最低,故选择乙腈作为提取溶剂。
3.2 前处理方法的选择
QuEChERS法是一种新颖的样品前处理技术,最初主要用于蔬菜水果样品中的农药残留分析,随着研究的深入,QuEChERS法已扩展应用到诸多领域。相对于传统的前处理方法,QuEChERS法是向提取液中加入硫酸镁等干燥剂和碳18等杂质吸附剂,简化了样品的前处理步骤,提高了前处理工作效率,降低了实验中各因素误差。
常用盐析试剂组合是醋酸钠和柠檬酸钠两种体系,本研究选择了含有4 g MgSO4、1 g NaCl、1 g柠檬酸钠、0.5 g柠檬酸氢二钠的缓冲盐体系,其中无水硫酸镁用于除去基质中的水分,其余的缓冲盐用于提供适宜的pH用于保证一些对酸碱敏感的农药可以有好的回收率。
常用的吸附剂有PSA/C18/GCB等,其中C18和GCB主要清除脂类和色素等非极性物质,PSA通过极性、阴离子交换作用力吸附除去极性较强的杂质,如糖类、脂肪酸、有机酸、多酚等。由于西洋参药材成分复杂,在前处理时有效地除去非目标物质,可防止假阳性的产生,本研究选择PSA 400 mg + C18400 mg作为吸附剂。
综上所述,本实验采用乙腈作为提取溶剂,经QuEChERS 方法提取、净化西洋参中的腐霉利,选取 PSA 400 mg + C18400 mg作为吸附剂,对西洋参中残留腐霉利进行GC-MS分析。结果表明,GC-MS法测定西洋参中的腐霉利快速简便,重复性和灵敏度均较好,在对市场中西洋参的腐霉利残留量进行检测的同时,也可为中药西洋参市场监督提供一定的技术支持。

