副波长对免疫比浊法检测尿微量清蛋白精密度的影响
李 光
南京医科大学附属老年医院/江苏省省级机关医院检验科,江苏南京 210024
尿微量清蛋白在临床实验室的检测已广泛普及,全自动化分析仪的使用极大地提高了工作效率和检测结果的精密度。但在实际临床工作中发现,雅培全自动生化分析仪没有尿微量清蛋白的原装配套试剂,国内大多数临床实验室在开展这个项目的时候,使用的都是国产试剂,而国产试剂生产厂家众多,各厂家提供的试剂说明书在检验方法中对副波长的要求也不尽相同,甚至有说明书对副波长只字未提,有些虽然在说明书中有要求,但厂家试剂应用工程师在仪器的参数设置中并未设置有副波长,本研究旨在通过根据ISO15189方法或性能验证的要求[1],比较添加副波长前后,尿微量清蛋白精密度的变化[2],评估副波长对尿微量清蛋白重复性的影响,同时观察不同浓度标本精密度的变化。
1材料与方法
1.1标本来源 收集2018年11月12-16日本院门诊和住院患者尿液标本4份,要求:微量清蛋白浓度分别为10、100、200、400 mg/L的尿液标本各一份,确保每份标本的总量足够25次检测,并对每份标本进行分装冷冻保存。
1.2仪器与试剂 雅培全自动生化分析仪C16000(尿微量蛋白波长参数:主波长340 nm,副波长700 nm)。中生北控生物科技股份有限公司生产的尿微量清蛋白检测试剂盒(R1、R2试剂)及配套校准品;朗道实验诊断有限公司提供的尿微量清蛋白质控品。
1.3精密度测定方法 按照美国临床和实验室标准协会 (CLSI)颁布的EP15-A2(医学实验室精密度和准确度的验证指南)中的精密度验证程序[3],在添加副波长前后分别做如下操作:检验程序按照5×1×5的方案检测标本。即:每个浓度标本检测5 d,每天一个分析批,每个分析批重复检测5次。在每个运行批内,运行标本。同时检测质控标本。如果质控结果超出可接受范围,那么拒绝这个运行批,丢弃该批次结果,纠正存在的问题,在下一个运行批中重新检测质控标本。
1.4统计学处理 按照EP15-A2文件进行试验数据的统计学处理,计算添加副波长前后批内精密度和总精密度,并与厂商声明的精密度性能指标进行比较。如果≤对应的允许不精密度,表示已验证批内精密度和总精密度的验证目标。反之,表示验证目标未得到临床实验室验证,实验室应查找原因,或与试剂厂商联系,并取得帮助。所有统计学处理在Excel2007软件上进行。
2 结 果
2.1添加副波长前后精密度变化 在10、100、200、400 mg/L 4个浓度的检测结果中,发现添加副波长前,各个浓度的批内精密度和总精密度均高于厂商声明的允许不精密度要求5%,见表1。添加副波长后,10、100 mg/L尿液标本的批内精密度和总精密度均高于厂商声明的允许不精密度要求5%。同时,添加副波长后,200 mg/L的尿液标本的批内精密度仍不符合厂商声明的允许不精密度要求5%,而200 mg/L的尿液标本总精密度,以及400 mg/L尿液标本的批内精密度、总精密度均符合厂商声明的允许不精密度要求5%,见表2。

表1 添加副波长前尿微量清蛋白精密度验证报告

表2 添加副波长后尿微量清蛋白精密度验证报告

图1 添加副波长前反应曲线
2.2添加副波长前后反应曲线的变化 添加副波长之前,在加入试剂R1和标本之后曲线有一明显跳点,加入试剂R2之后同样也存在一个明显的跳点,见图1。在添加副波长之后,这两个跳点均消失,见图2。
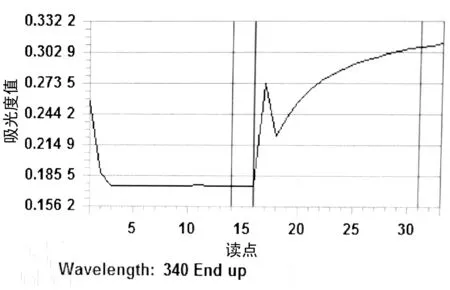
图2 添加副波长后反应曲线
3 讨 论
本研究采用双波长分光光度法[4],其理论基础是差吸光度和等吸收波长,它采用测量波长和参比波长同时检测某个标本溶液,以提高检测结果的精密度和准确度[5]。使用副波长的目的是有效减少杂散光影响;消除噪声干扰及降低标本脂浊、黄疸和溶血等干扰[6-7]。全自动生化分析仪在整个反应的全程监控中,主副波长同时监测,全过程每点主波长吸光度值都同时减去同点副波长吸光度值,结合凹面光栅进行后分光,分光后的各波长由8~16个固定监测器同时接收,对其中两个波长的信息用两个前置放大器进行对数放大,进而求出其吸光度差。通过分析表1和表2可以看出尿微量清蛋白检测同一浓度在添加副波长前后精密度有较大变化,虽然10、100 mg/L标本的批内精密度和总精密度,以及200 mg/L标本的批内精密度标本在添加副波长后仍未达到厂商规定的允许不精密度要求,但是添加副波长前标本的验证试验结果均明显高于添加后,说明添加副波长后相关的干扰因素得以消除或降低,检测值的稳定性得以明显改善。并且无论有无添加副波长,不精密度都会随着标本浓度的增加而减小,即使在添加了副波长之后,浓度在10、100 mg/L及部分200 mg/L的标本精密度验证结果仍然高于厂商声明的标准,说明该试剂在中低浓度,尤其低浓度区间的检测值稳定性较差。此外,正常的尿微量清蛋白反应曲线一般比较平滑,无明显跳点。而在加入副波长之前,分别加入R1试剂、尿液标本及R2试剂后均存在明显的跳点,说明在加入R1和R2之后均存在一个明显的干扰。而在添加副波长之后,这两个跳点均消失,曲线平滑,说明干扰被消除或有效降低。
由于尿微量清蛋白的允许不精密度要求无可供参考的卫生行业标准,因此,总精密度可参考卫生与计划生育委员会临检中心的1/3室间质评标准(允许总不精密度误差TEa)作为总允许不精密度要求[8],批内精密度参考1/4TEa,这样也能够表明该项目的室内质量控制监测项目允许不精密度要求符合质量目标。2018年临床检验室间质量评价计划尿微量清蛋白的允许总误差为30%,因此,尿微量清蛋白的总精密度应<10%,批内精密度应<7.5%,本研究发现添加副波长前200 mg/L标本的总精密度,以及400 mg/L的批内精密度和总精密度均符合本实验室的参考允许不精密度的要求。而添加副波长后100、200、400 mg/L尿液标本的批内精密度及总精密度均符合本实验室参考的允许不精密度的要求,表明除低浓度外,部分标本虽未通过厂商声明的允许不精密度,但并未超出本实验室的允许不精密度标准,而部分标本未通过精密度验证的原因有待进一步研究,可能是仪器造成的,因为在生化分析仪上进行免疫学测定,其不精密度可能比在特定蛋白仪上要大,但不排除部分国产试剂精密度性能指标可能存在虚标。除此以外,本研究还发现随着尿微量清蛋白水平的增加,尤其是浓度在200 mg/L以上的标本,不精密度值在添加副波长前后的变化明显小于低浓度区域,表明副波长对低浓度标本精密度的影响大于高浓度。

