改性水热炭同时吸附溶液中Cr(Ⅵ)和Cd(Ⅱ)
何苑静,张定定,王 曦,梁玺静,许士洪,李登新
(1. 东华大学 环境科学与工程学院,上海 201620;2. 东华大学 国家环境保护纺织污染防治工程技术中心,上海 201620;3. 台州市污染防治工程技术中心,浙江 台州 318000;4. 上海同济建设有限公司,上海 200092)
重金属污染具有持续时间长、移动性强和生物利用性高等特点,已成为环境保护领域的研究热点[1]。通常,重金属污染废水中会同时存在多种重金属离子[2]。Cr(Ⅵ)和Cd(Ⅱ)是重金属污染废水中两种典型的重金属离子,而复合重金属污染废水的治理难度远高于单一重金属污染废水。
水热炭(HC)是一种效果好且经济的新型吸附剂,可用于去除水中的重金属、农药和染料等难降解污染物[3-4]。改性可提高水热炭的比表面积、孔隙率和吸附容量,提高其吸附能力。碱改性水热炭可增加水热炭表面含氧官能团的数量,增大其比表面积,提高水热炭对水中阳离子的吸附容量[5]。ZnCl2改性水热炭的含碳量、比表面积和芳香性都明显提高,且表面富含羰基等含氧官能团,对亚甲基蓝有更好的吸附性能[6-8]。但是,关于NaOH和ZnCl2改性水热炭及其耦合用于同时去除水中Cr(Ⅵ)与Cd(Ⅱ)的研究还鲜见报道。
本研究采用竹屑制备HC,通过NaOH溶液和ZnCl2溶液改性制备了改性水热炭OHHC和ZHC,再将两种改性水热炭制成复合改性水热炭MHC,探讨不同水热炭对溶液中Cr(Ⅵ)和Cd(Ⅱ)的去除效果的差异与吸附机制。
1 实验部分
1.1 材料和试剂
竹屑;NaOH、CdCl2·2.5H2O、ZnCl2、盐酸和无水乙醇:均为分析纯;实验用水为去离子水。
1.2 HC的制备与改性
将竹屑去除杂质后破碎,过30目筛,加入去离子水,按固液比(竹屑质量(g)与去离子水体积(mL)之比)1∶8搅拌均匀,放入GSH-2L型水热反应釜(威海环宇化工仪器有限公司)中。升温至230 ℃,处理4 h,用无水乙醇清洗后烘干,得到HC。
将上述的去离子水分别替换为等体积的质量分数为3%的NaOH溶液和浓度为0.6 mol/L的ZnCl2溶液,其他步骤相同,分别得到OHHC和ZHC。将OHHC和ZHC按质量比1∶1混合均匀,制成复合改性水热炭MHC。
1.3 分析表征
采用Quadraorb SI型比表面积和孔结构分析仪(Quadrasorb公司)测定HC、OHHC和ZHC的BET比表面积和孔体积;采用S-4800型扫描电子显微镜(Hitachi公司)观察HC、OHHC和ZHC的表面微观形貌;采用VarioELⅢ型元素分析仪(ELEMENTAR公司)测定竹屑、HC、OHHC和ZHC的元素含量;采用NicoletIn10MX型傅里叶变换红外光谱仪(Thermo Nicolet公司)表征HC改性前后的官能团变化。
1.4 吸附实验
吸附实验在25℃恒温振荡箱(转速180 r/min)中进行。分别配制不同质量浓度的Cr(Ⅵ)、Cd(Ⅱ)混合溶液,用0.1 mol/L NaOH溶液和0.1 mol/L HCl调节溶液pH。
1.4.1 水热炭投加量对吸附性能的影响
分别称取0.2,0.4,0.6,0.8,1.0和1.2 g水热炭加入装有50 mL含 Cr(Ⅵ)和Cd(Ⅱ)(质量浓度均为100 mg/L)混合溶液中,调节溶液pH=4,恒温振荡24 h。然后离心过滤,收集滤液,采用ICP-Prodigyspace型电感耦合等离子体光谱仪(LEEMAN LABS公司)测定滤液中的Cr(Ⅵ)和Cd(Ⅱ)的质量浓度,计算Cr(Ⅵ)和Cd(Ⅱ)的去除率。
1.4.2 初始溶液pH对吸附性能的影响
称取一定量的水热炭,加入50 mL不同pH的含Cr(Ⅵ)和Cd(Ⅱ)(质量浓度均为100 mg/L)混合溶液中。其余设定及操作同1.4.1节。
1.4.3 吸附动力学实验
称取一定量的水热炭,加入50 mL含 Cr(Ⅵ)和Cd(Ⅱ)(质量浓度均为100 mg/L)混合溶液中,进行不同吸附时间(10,30,60,120,240,480,720,1 440,2 880 min)的吸附实验,其余设定及操作同1.4.1节。分别采用准一级动力学模型(式1)和准二级动力学模型(式2)对吸附结果进行拟合。

式中:Qt为吸附剂在t时刻的吸附量,mg/g;Qe为平衡吸附量,mg/g;t为吸附时间,min;k1为准一级动力学吸附速率常数,min-1;k2为准二级动力学吸附速率常数,mg/(g·min)。
1.4.4 等温吸附实验
配制不同Cr(Ⅵ)和Cd(Ⅱ)质量浓度(10,20,50,100,150,200,300,400 mg/L)的混合溶液,加入一定量的水热炭,在25℃下进行等温吸附实验,其余设定及操作同1.4.1节。并通过Langmuir(式3)和 Freundlich(式4)等温吸附模型对等温吸附实验结果进行拟合。

式中:Qm为最大吸附量,mg/g;ρe为吸附平衡时溶液中的金属离子质量浓度,mg/L;kL为Langmuir吸附常数,L/mg;kF为Freundlich吸附常数,(mg(1-n)·Ln)/g;n为经验参数。
2 结果与讨论
2.1 水热炭的表征结果
2.1.1 水热炭改性前后的元素组成
竹屑、HC、ZHC和OHHC的元素组成见表1。由表1可见:与HC相比,OHHC的C元素质量分数明显下降,这是因为在碱性水热条件下,纤维素在水解过程中分解速率加快,且会增加低分子量有机酸与生物质油等液相产物的生成量[9-11];而OHHC的高N含量则表明,NaOH改性可提高水热炭含氮官能团的数量;ZHC的n(H)/n(C)最低,表明其芳香化程度最高,在环境中有较高的稳定性。n(N+O)/n(C)常用来表示水热炭表面极性的高低[12],OHHC的n(N+O)/n(C)高于HC和ZHC,说明NaOH改性增加了水热炭中羟基、氨基等极性官能团的含量,有利于对溶液中重金属的吸附;n(O)/n(C)可判断水热炭的亲水性能,其值越大表示水热炭的亲水性越强,OHHC和ZHC的n(O)/n(C)均高于HC,表明两种改性方法具增强了水热炭的亲水性能。

表1 竹屑、HC、ZHC和OHHC的元素组成
2.1.2 水热炭表面形貌及结构分析
HC、ZHC和OHHC的SEM照片见图1。由图1可见:3种水热炭表面均较为粗糙且呈现丰富的孔结构;而ZHC的孔洞明显多于HC。这是因为ZnCl2在水热反应过程中可以促进竹屑的降解,并具有一定的造孔功能[13]。由图1还可以发现,OHHC表面的孔洞直径和孔深显著大于HC,这归因于NaOH加速竹屑碳化并破坏了水热炭表面的孔洞,使之塌陷或形成大孔径孔洞[14]。

图1 HC(a)、ZHC(b)和OHHC(c)的SEM照片
改性前后水热炭的比表面积和孔体积见表2。
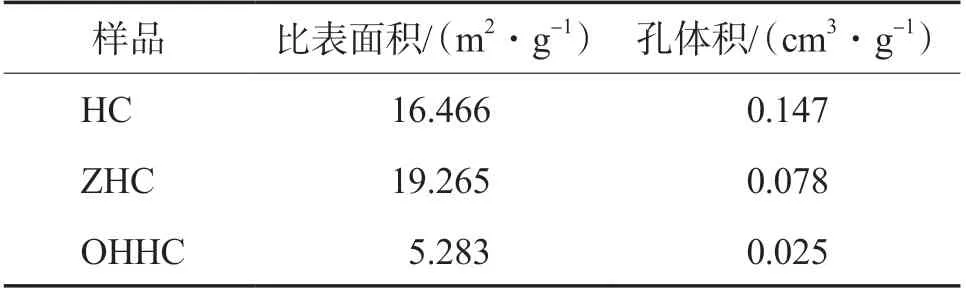
表2 改性前后水热炭的比表面积和孔体积
由表2可见:与HC相比,ZHC的比表面积有所增加,而OHHC的比表面积却明显下降;另外,ZHC的孔体积较HC下降,这可能是ZHC表面附着的锌化物颗粒堵塞部分孔洞所致[15]。
本研究根据GB 5085.3—2007 《危险废物鉴别标准浸出毒性鉴别》[16]对ZHC与MHC进行了毒性浸出实验,总Zn的浸出质量浓度分别为2.63 mg/L和1.89 mg/L,远低于危险废物浸出毒性鉴别标准值。
2.1.3 FTIR表征结果
改性前后水热炭的FTIR谱图见图2。由图2可见:3 441 cm-1附近的吸收峰归属于O—H键,2 924 cm-1附近的特征峰归属于C—H键,1 634 cm-1附近的吸收峰归属于C=O键,1 113 cm-1附近的吸收峰则为C—O—C振动产生[12,17];与HC相比,OHHC与ZHC在1 733 cm-1附近出现了由—CHO振动产生的吸收峰;在1 456 cm-1附近出现了代表酰胺基的N—H特征峰[18];ZHC在1 061 cm-1处出现了C—O特征峰,在2 924 cm-1附近峰强度增加,表明ZnCl2促进了竹屑在碳化过程中纤维素与半纤维素的分解,提高了其转化为芳香物质的效率[19]。

图2 改性前后水热炭的FTIR谱图
2.2 吸附性能的影响因素
2.2.1 水热炭投加量
在初始溶液pH=4的条件下,水热炭投加量对Cr(Ⅵ)和Cd(Ⅱ)去除率的影响见图3。由图3可见,随着水热炭投加量的增加,Cr(Ⅵ)去除率和Cd(Ⅱ)去除率均逐步提高。这归因于水热炭的增加扩大了其与重金属离子的接触面积并提供了更多的吸附位点[20]。
由图3a可知,ZHC的Cr(Ⅵ)去除率高于HC,而OHHC的Cr(Ⅵ)去除率低于HC。这是因为ZHC的微孔结构增多导致吸附位点增加,而OHHC的比表面积减小导致吸附位点减少所致[13]。
图3b可知,ZHC和OHHC对Cd(Ⅱ)的去除率均高于HC,因为NaOH和ZnCl2改性均增加了水热炭表面官能团的含量。此外,Cr(Ⅵ)与Cd(Ⅱ)存在竞争吸附,因此ZHC与OHHC对Cd(Ⅱ)去除率的提升效果不如Cr(Ⅵ)明显[21-22]。由图3还可以看出,与单一水热炭相比,MHC表现出更好的吸附性能。MHC投加量为16g/L时,溶液中Cr(Ⅵ)和Cd(Ⅱ)去除率分别高达98.98%和81.38%。
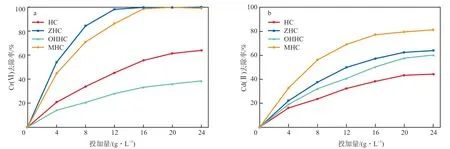
图3 水热炭投加量对Cr(Ⅵ)(a)和Cd(Ⅱ)(b)去除率的影响
2.2.2 初始溶液pH
在水热炭投加量为16 g/L的条件下,初始溶液pH对Cr(Ⅵ)和Cd(Ⅱ)去除率的影响见图4。

图4 初始溶液pH对Cr(Ⅵ)(a)和Cd(Ⅱ)(b)去除率的影响
由图4a可知,水热炭对Cr(Ⅵ)的去除率随初始溶液pH的增大而降低。这是因为Cr(Ⅵ)在溶液中一般以HCrO4-(pH=1)、Cr2O72-(pH=2~6)和CrO42-(pH> 7)等阴离子形态存在,在酸性条件下,H+介导水热炭表面官能团发生质子化反应,使碳材料表面富集大量正电荷,因此提高了Cr(Ⅵ)去除率。随着溶液pH升高,官能团发生去质子化反应,水热炭表面负电荷数量增加,导致Cr(Ⅵ)去除率降低[23]。由图4b可见,水热炭对Cd(Ⅱ)的去除率随初始溶液pH升高而增大。因为Cd以Cd(Ⅱ)形式存在[21,24],当pH较低时,H+与Cd(Ⅱ)发生竞争吸附;溶液 pH>8时,Cd(Ⅱ)会以Cd(OH)2沉淀的形式从液相脱除[25]。综合考虑重金属去除率和经济可行性,选择初始溶液pH为4最适宜。
2.3 吸附动力学
水热炭对Cr(Ⅵ)和Cd(Ⅱ)的吸附动力学曲线见图5。由图5可见,吸附过程分为快速吸附和吸附平衡两个阶段。Cr(Ⅵ)和Cd(Ⅱ)分别在240 min和720 min内被快速吸附,随后逐步趋于吸附平衡。快速吸附阶段,水热炭表面的活性吸附位点充裕,可以迅速吸附溶液中的Cr(Ⅵ)和Cd(Ⅱ)[26]。随着时间的推移,吸附位点逐步趋于饱和,吸附速率下降。

图5 水热炭对Cr(Ⅵ)(a)和Cd(Ⅱ)(b)的吸附动力学曲线
水热炭对Cr(Ⅵ)和Cd(Ⅱ)吸附的准一级动力学模型和准二级动力学模型拟合参数见表3[27]。由表3可见,3种改性水热炭吸附Cr(Ⅵ)和Cd(Ⅱ)的过程采用准二级动力学模型拟合效果更优,说明吸附过程主要受离子交换、表面络合和沉淀等化学吸附控制[28]。
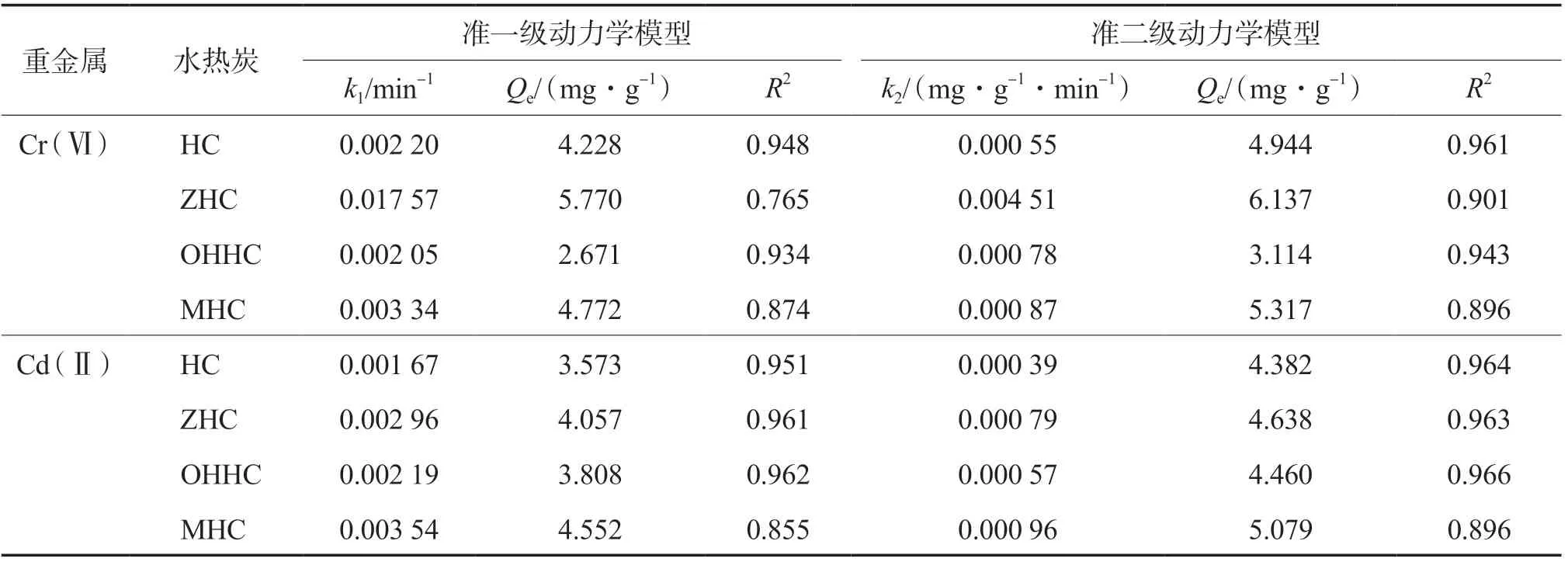
表3 水热炭对Cr(Ⅵ)和Cd(Ⅱ)的吸附动力学模型拟合参数
2.4 等温吸附模型
在25℃下,水热炭对Cr(Ⅵ)和Cd(Ⅱ)的等温吸附曲线见图6。由图6a可知,水热炭对Cr(Ⅵ)最大平衡吸附量大小顺序为ZHC>MHC>HC>OHHC。由图6b可知,随着平衡质量浓度的增大,水热炭对Cd(Ⅱ)的吸附量持续增加而未达到平衡,说明水热炭对Cd(Ⅱ)的吸附位点还未达到饱和。
水热炭对Cr(Ⅵ)和Cd(Ⅱ)的Langmuir 和Freundlich等温吸附模型拟合参数见表4。由表4可知,4种水热炭对Cr(Ⅵ)和Cd(Ⅱ)的吸附过程用Langmuir方程拟合结果均优于Freundlich方程,表明Langmuir 模型能很好描述水热炭的吸附过程,水热炭对Cr(Ⅵ)和Cd(Ⅱ)的吸附过程主要为单层 均匀吸附。

表4 水热炭对Cr(Ⅵ)和Cd(Ⅱ)的Langmuir 和 Freundlich等温吸附模型拟合参数
3 结论
a)ZnCl2改性可使水热炭的芳香性增高,比表面积增大,表面附着大量锌化物颗粒。NaOH改性扩大了水热炭孔径,并提高了含氧官能团含量。
b)MHC可以同时实现Cr(Ⅵ)和Cd(Ⅱ)的高效去除,在初始溶液pH =4、水热炭投加量为16 g/L的最佳条件下,Cr(Ⅵ)和Cd(Ⅱ)去除率分别达98.98%和81.38%。
c)水热炭对Cr(Ⅵ)和Cd(Ⅱ)的吸附数据拟合结果更符合准二级动力学模型,揭示吸附过程中主要为化学吸附。Langmuir等温吸附模型与水热炭对Cr(Ⅵ)和Cd(Ⅱ)的吸附等温线拟合效果较好,表明吸附过程主要为单层均匀吸附。

