PROTAC技术在抗病毒感染中的应用前景
刘杏,夏宇,李鑫,满荣勇,王炜,曹建中
作者单位:410208 长沙,湖南中医药大学中医诊断学湖南省重点实验室(刘杏、夏宇、李鑫、曹建中),药学院(王炜);418000 怀化,湖南省怀化市第一人民医院神经内科与医学实验中心(满荣勇)
新型冠状病毒肺炎(COVID-19)[1-2]暴发后在全球造成大流行,促使人们再一次重视传染病的危害和防治。尤其新发呼吸道病毒传染性强,一旦暴发,传播迅速,由于没有有效治疗方法,往往致死率高,严重危害人类健康,并造成严重经济损失。其他常见危害人类的病毒性疾病有病毒性肝炎、流感、艾滋病、狂犬病等,尤其艾滋病和病毒性肝炎患者需要长期服药,患者精神和经济压力大。在传染性疾病中,病毒感染约占 75%,所以对病毒性疾病的控制一直是生物医学界的一大难点。
药物依然是当前控制病毒感染的主要方法,其抑制病毒生活史的某个环节,如直接抑制或杀灭病毒、阻止病毒侵入细胞、抑制病毒基因组复制、病毒颗粒释放或增强宿主抗病毒能力等。以 SARS-CoV-2 为例,目前临床使用的抗 SARS-CoV-2 药物如核苷酸类似物法匹拉韦和瑞德西韦等[3],靶向 RNA 依赖性 RNA 聚合酶(RdRp),阻断病毒RNA 的合成;阿比朵尔[4]则是通过靶向 S 蛋白与其受体ACE2 的结合,阻止病毒进入细胞。这些药物均只能部分抑制病毒复制,无法终止病毒感染,因此寻找新的有效的能够直接终止病毒复制的药物一直是病毒学研究的努力方向。最近兴起的利用细胞各种蛋白酶降解系统降解病理蛋白的技术在肿瘤和神经性疾病等领域取得了很大进展,尤其以 26S蛋白酶系统为基础的蛋白质靶向降解嵌合体(proteolysis targeting chimera,PROTAC)技术或药物进展迅速,已经进入临床 II 期试验[5-6],有望成为研发抗病毒药物的利器。现将 PROTAC技术的原理、现状和在抗病毒方面的应用前景作一个介绍。
1 PROTAC技术的原理与应用
PROTAC 分子或药物是一个异质双功能小分子,由一个结合靶蛋白的配体小分子和一个结合 E3 连接酶的配体小分子通过一个小分子链构成[7]。PROTAC 分子进入细胞后,同时与靶蛋白和 E3 连接酶结合,利用 E3 连接酶招募 E2 对靶蛋白进行泛素化修饰,修饰后的靶蛋白通过26S 蛋白酶系统降解为氨基酸,释放出来的 PROTAC 分子可以重复使用(图 1)。PROTAC技术是一个颠覆传统药物概念的新技术,但是其应用场景与传统蛋白抑制剂一致。该技术最早发表于 2001年,此后一直由耶鲁大学 Crews教授实验室推动并在近几年得到其他药物研发实验室跟踪。和传统药物不同的是,PROTAC 药物不是抑制靶蛋白活性,而是直接降解靶蛋白,因此其控制靶蛋白活性的效果优于抑制剂。泛素-蛋白酶系统的正常生理功能是负责清除细胞中的变性、突变或有害蛋白[5]。一旦靶蛋白、PROTAC 分子、E3 泛素连接酶三元复合物形成,E2 泛素结合酶把泛素转移到靶蛋白表面上的赖氨酸残基,细胞内 26S 蛋白酶体识别赖氨酸多聚泛素化信号进而促进了靶蛋白的降解(图 1)。目前,PROTAC技术已经用于靶向多种细胞蛋白,如转录因子、骨架蛋白、酶和调节蛋白等[6]。在癌症和神经元疾病等领域,PROTAC 分子在细胞和动物实验中表现优异,部分 PROTAC 药物已经进入临床 I 期或 II 期。这些进展促使全球顶级制药公司联手新成立了 PROTAC 公司,开展PROTAC 药物研发,相信不久的将来 PROTAC 药物会不断出现,用于治疗人类的各种疾病。
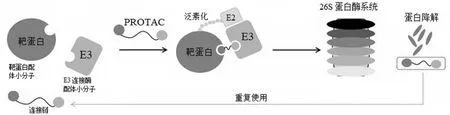
图1 PROTAC 原理
2 PROTAC技术的优势
PROTAC 的作用机制使得 PROTAC 分子在降解靶蛋白过程中具有两个重要特征。首先是形成靶蛋白、PROTAC和 E3 泛素连接酶的三元复合物。PROTAC 分子对靶蛋白的降解具有浓度依赖性[8]:在 PROTAC 分子浓度较低时,靶蛋白被降解的程度随浓度升高而逐渐提高;PROTAC分子浓度过高时,反而会出现靶蛋白水平回升。这是由于靶蛋白和 E3 泛素连接酶均被小分子占据,形成了二元复合物,降低了靶蛋白的降解效率。其次,PROTAC 分子对蛋白的降解起催化作用[9],靶蛋白通过 26S 蛋白酶途径降解后,PROTAC 分子被释放出来,继续参与降解下一个靶蛋白。因此,只需催化量的 PROTAC 分子就可以诱导靶蛋白降解。
大量研究发现,PROTAC技术具有以下显著优势:①用量小;②较低的药物暴露量降低了脱靶效应产生的可能性,减少毒副作用;③不会引起耐药;④不依赖于蛋白活性中心亲和力,可选择性高;⑤没有抑制剂和靶蛋白复合物堆积;⑥较少给药次数;⑦更重要的是,由于 PROTAC 只需要结合活性,触发靶蛋白与 E3 酶结合从而引发降解这一事件,属于“事件驱动”,与传统的小分子抑制剂的“占位驱动”不同,不需要直接抑制靶蛋白的活性,药物不需要与靶蛋白长时间和高强度的结合,因此可以靶向传统难以成药的蛋白[10]。
目前,Pubmed 上已经发表了 500 多篇关于 PROTAC技术的研究性论文,研究重点集中在肿瘤治疗领域。2021年3月,美国 Arvinas 公司宣布其开发的用于治疗前列腺癌的雄激素受体 AR 降解药物 ARV-110 和 ARV-471 进入II 期临床试验,标志着 PROTAC技术的研究进入新的阶段。表 1 总结了已经报道的重要 PROTAC 小分子化合物,以及对应的靶蛋白和 E3 配体分子[11]。

表1 在研 PROTAC 药物
3 PROTAC 在中药抗病毒中的应用前景
根据文献查询,PROTAC技术尚没有引起中医药领域的重视,尚未见在中医药方面的应用,因此我们针对中药抗病毒的作用靶点,探讨 PROTAC技术在中药抗病毒中的应用前景。
中药治疗病毒性疾病尤其急性感染的效果很好,且副作用相较化学药物来说要小很多,然而也面临很大挑战。首先,关于中药抗病毒作用的有效成分鉴定及潜在靶点的报道很多,然而有关生物学机制探讨不多;其次,对于 HIV-1 和HBV 这类慢性感染,缺少有效根治方法,患者需终身服药,精神和经济压力大。利用 PROTAC技术改造中药抗病毒小分子可以提高药物疗效。现有抗病毒中药小分子主要是抑制剂,通过改造成 PROTAC 药物,理论上可以使用较小的剂量,直接降解靶蛋白,从而终止病毒复制。PROTAC技术联合质谱以及 CRISPR/Cas9 基因编辑技术可以发现药物靶标,为进一步探讨药物作用机制、提高疗效提供基础。一些中药小分子具有结合病毒非酶类蛋白的功能,然而这种结合对于病毒的治疗有何作用尚不清楚,利用 PROTAC 改造后的小分子药物可以直接降解这些靶标蛋白,明确药物靶点。PROTAC 和酶抑制剂不一样,其药物分子能反复利用,对于慢性感染具有特别的意义,可以降低服药次数,减少副作用。针对某些感染,PROTAC 药物可以和中药方剂联用,提高其治疗效果。
以叶下珠这一中药为例,研究表明其通过活性成分没食子酸葡萄糖苷结合核衣壳蛋白 preC 而抑制乙肝病毒的复制[32],如果将没食子酸葡萄糖苷改造成 PROTAC 分子,就可以直接降解 preC,改善患者症状。
要充分发挥 PROTAC技术在中药小分子药物抗病毒中的潜力,需要面对以下挑战。首先,筛选合适的靶标和药物。目前在体外抑制病毒复制的中药活性成分有很多,部分药物的分子结构已经鉴定(表 2)。由于 PROTAC 分子依然是小分子,所以分子量小的生物利用度相对较高,比如大黄酸、麻黄素、氧化苦参碱等最有可能利用 PROTAC 改造,成为疗效更好的抗病毒药物。对于病毒感染尤其慢性感染,靶向病毒复制有关酶类如蛋白酶和复制酶,抗病毒效果会比较理想。其次,病毒感染往往引起机体炎症反应,过多的炎症和细胞因子“风暴”会导致组织与器官损伤,因此控制炎症和细胞因子在适当水平是非常重要的,利用 PROTAC 药物靶向炎症因子有可能达到需要的目标。
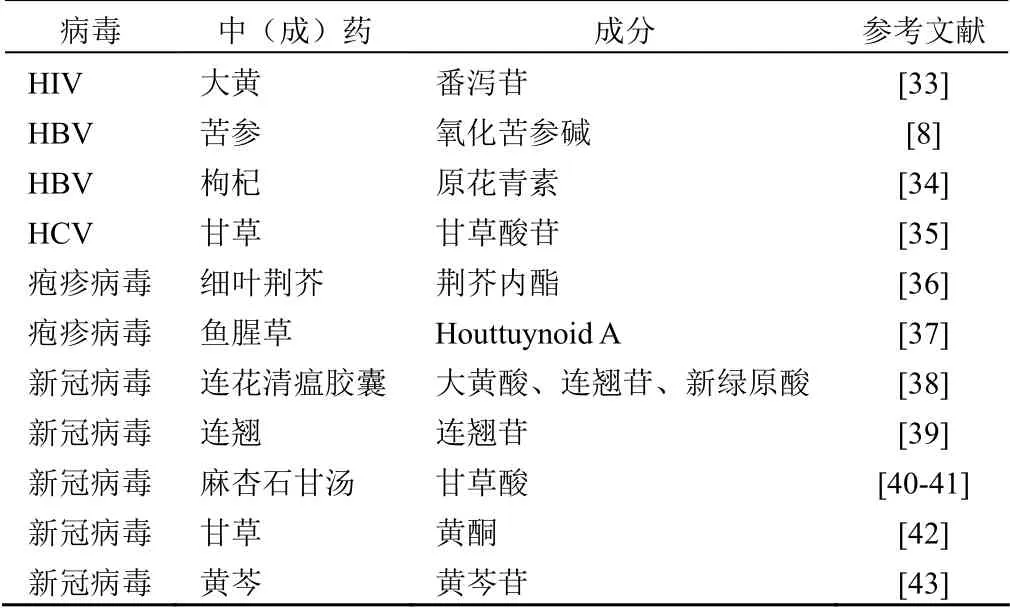
表2 抗病毒中药小分子
最后,如表 1所示,除了靶标,PROTAC 药物的 E3酶及其配体也是影响药物效果的重要因素,人类基因组编码超过 400 个 E3 酶,目前研究较多的不到 10 个,有合适配体而且用在 PROTAC 药物上面的以 CRBN、IAP 和VHL 为主,这些酶在病毒感染细胞中的表达水平尚没有报道,因此研究清楚这些酶在病毒感染细胞中的动态变化,对于采用合理的 E3 酶及其配体设计中药 PROTAC 小分子治疗病毒性疾病具有重大意义。
PROTAC技术是目前生物医药领域的一大革命性技术,在中药抗病毒领域具有非常好的前景,不仅可以解决靶标不清的问题,而且具有极大地提高疗效的潜力。利用这一技术,可以进一步提高中医药在抗病毒领域的价值,为人类健康做出更大贡献。

