外科升阶梯治疗重症急性胰腺炎合并胰周感染坏死的疗效:附34例报告
蔡翊,陈梅福,成伟,李国光,谢阳云
(湖南省人民医院胰脾外科/湖南师范大学胰腺疾病转化医学研究所,湖南长沙410005)
重症急性胰腺炎(severe acute pancreatitis,SAP)是常见的急腹症之一,病情重、并发症多、病死率较高,占急性胰腺炎(AP)发病率的10%~20%[1]。随着疾病的发展,10%~70%的SAP 中晚期患者可合并胰周感染性坏死(infected peripancreatic necrosis,IPN)[2]。近年来,以经皮穿刺置管引流(percutaneous catheter drainage,PCD)为基础的外科“升阶梯”治疗已成为治疗IPN 的主流策略[3-7],我科通过运用外科升阶梯治疗SAP 合并IPN 取得了良好的效果。现将结果报告如下。
1 资料与方法
1.1 一般资料
回顾性分析本院2017年1月—2019年6月收治的34 例SAP 并IPN 的临床资料,其中男21 例,女13 例;年龄31~79 岁,平均年龄51 岁。体查:34 例均有上腹部压痛体征,10 例有腰背部抬举痛及Grey-Tuner征;34 例患者术前血清淀粉酶14~2 024.4 U/L,平均246 U/L,TBIL 4.7~154.4 μmol/L 平均23 μmol/L,DBIL 2.1~101.3 μmol/L,平均为11.6 μmol/L;甘油三脂0.58~5.54 mmol/L,平均1.88 mmol/L;APACHE II评分均在8 分以上。入组标准:出现上腹部疼痛症状;B 超、CT 或MRI 提示胰周渗出并确诊为SAP 并IPN 形成(图1),所有入组患者均符合中华医学会外科学分会胰腺学组指南[8-10]。排除标准:经保守治疗可长时间缓解症状。所有患者均签署由医院伦理委员会批准的患者知情同意书,符合医学伦理学规定。
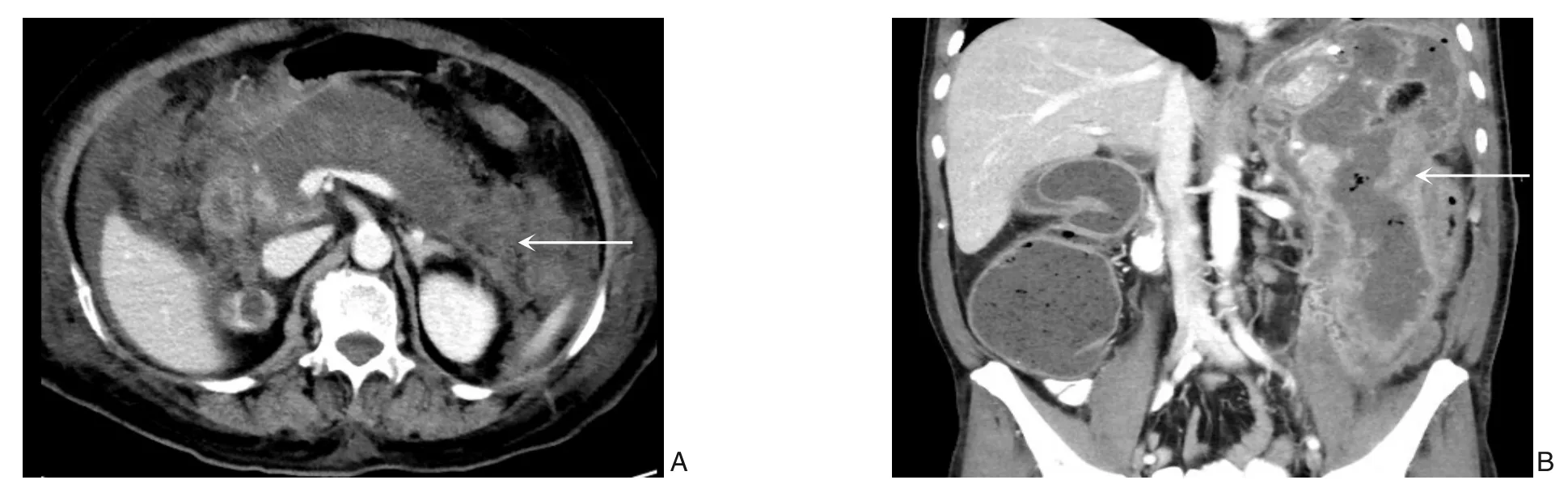
图1 SAP并IPN的影像学表现 A:矢状位;B:冠状位
1.2 方法
积极控制原发病,仔细阅读CT 片明确脓肿位置,所有患者均在有效抗生素治疗效果不佳后,经B 超引导下进行1 次或多次脓肿穿刺置管引流(图2A),经引流管进行脓腔冲洗,1 000~3 000 mL/d,根据脓液细菌培养出的结果进行针对性抗生素的使用,5~7 d 复查1 次CT。28 例复查CT 提示IPN 残留,伴腹痛、发热等症状,复查白细胞、中性粒细胞增高,分别行小切口联合肾镜IPN 清除或开腹扩大切口清除脓肿,术毕胰周放置多根腹腔引流管引流。
小切口联合肾镜IPN 清除:B 超定位下结合术前阅片结果在拟定切开处切开约4~6 cm 大小切口(图2B)。通常沿脓肿引流管做切口,能有效减少器官的负损伤。进腹后找到脓肿,硬质肾镜引导下卵圆钳钳夹坏死组织(图2C)。用动力冲水系统反复冲洗脓腔后吸尽脓液,脓腔内放置多侧孔腹腔引流管。
开腹脓肿清除术:经PCD、小切口联合肾镜清脓效果不佳,仍反复出现发热、腹胀腹痛等炎症症状者采用开腹手术清除脓液(图2D)。切口的拟定需根据脓腔的分布决定。切开入腹后先用稀释络合碘盐水反复冲洗腹腔,找到脓腔后分别打开,尽量多取坏死及脓性物。注意打开脓腔时候需用纱垫将未感染处隔离开,减少腹腔内感染。脓腔引流管的放置尽量顾及到所有脓腔,最好在脓腔的高位及低位分别放置,有利于术后的冲洗及引流。
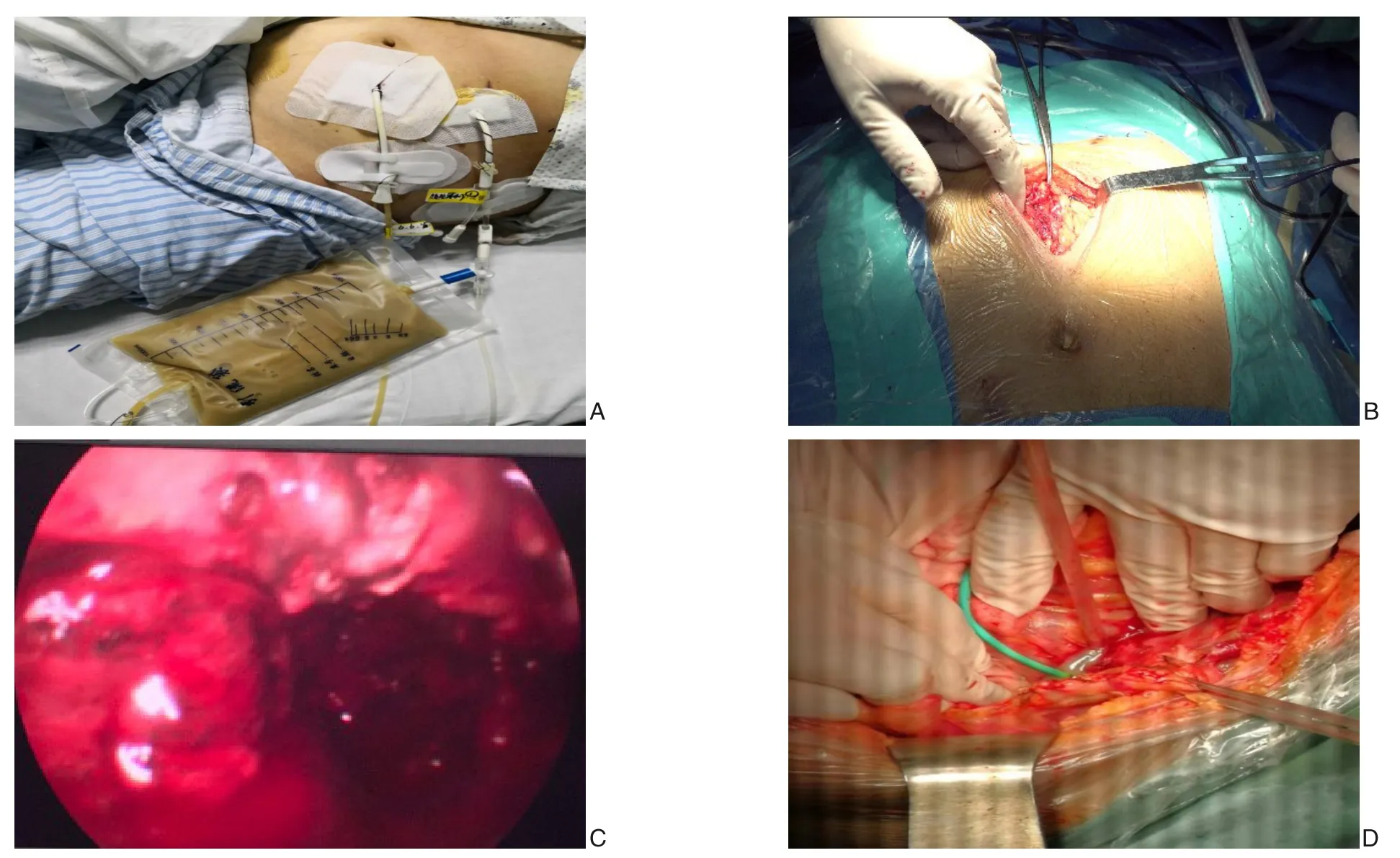
图2 治疗过程中相关图片 A:B超定位下胰腺脓肿穿刺引流;B:小切口脓肿切开引流;C:肾镜下清脓;D:开腹胰周脓肿清除术
1.3 观察指标
术后患者体温、脉搏等生命体征的波动及平复时间,引流管引流量及性状,复查CT 查看脓肿恢复情况,酌情升级治疗。
2 结 果
34 例患者均恢复顺利,术后体温、脉搏1~3 d恢复正常,引流管经生理盐水反复冲洗(1 000~3 000 mL/d)后脓腔引流液性状由褐色脓性液体转变为浅咖啡色液体或清亮白色液体;术后复查CT,脓腔均明显缩小(图3A)。术后随访5~30 个月,34 例患者均复查CT,提示脓肿均缩小或消失,引流管逐步拔除(图3B)。
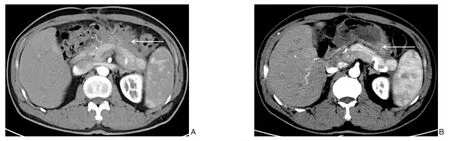
图3 治疗后复查CT A:术后CT;B:随访CT
3 讨 论
AP 是一种常见的急腹症,约15%发生胰腺实质和(或)胰周组织坏死(即坏死性胰腺炎)。坏死性胰腺炎患者病死率约为15%,其中约1/3 会发生感染,合并感染者病死率上升至30%[11]。
病程早期,胰腺坏死引发全身炎症反应综合征,进而诱发器官功能衰竭;病程后期,胰腺及胰周坏死组织继发感染导致脓毒症、出血、消化道瘘等并发症,是患者死亡的主要原因[12]。随着疾病的发展,10%~70%的SAP 中晚期患者可合并IPN,易引起多器官功能障碍综合征和脓毒症等严重并发症,病死率高达39%[13-15]。因此最大限度地清除感染坏死灶,充分引流坏死物质并尽可能地保留功能正常胰腺组织是治疗SAP 合并IPN 的原则[16]。
随着医学水平的提高,越来越多的SAP 患者得以渡过多器官功能不全(MODS)期,从而进入感染期。因此,IPN 已成为SAP 患者的主要死因之一[17]。本组34 例均严格按照胰腺炎“创伤递进”“升阶梯”的治疗原则[18]治疗,取得了良好的效果。患者分别采用PCD、小切口联合肾镜IPN 清除、开腹IPN 清除等方式。术后定期复查CT,脓腔均明显缩小或消失,所带腹腔引流管均逐根拔除。
外科升阶梯治疗SAP 合并IPN 的指征主要包括:(1)PCD 后脓毒症持续或反复,虽经积极的冲洗引流、换管及扩管等措施仍难以控制时;(2)PCD 后出现严重并发症,如肠瘘、大出血等,首选微创入路腹膜后胰腺坏死组织清除术,必要时可以升阶梯至开放胰腺坏死组织清除术[19]。
本组34 例均使用抗生素对症治疗效果不佳后,经1 次或多次IPN 穿刺引流,引流液送细菌培养并根据培养结果予针对性抗生素治疗;1 000~3 000 mL生理盐水反复冲洗脓腔及IPN,5~7 d 复查1 次CT,7 例患者生命体征平稳后带管出院回家休养,并医嘱保持脓腔引流管通畅及继续持续冲洗。3~5 个月复查,腹腔引流管无明显褐色或淡黄色脓液流出,CT 提示未见明显脓腔后逐根拔管。28 例经IPN 穿刺引流后脓液明显减少,但仍有发热,体温波动在38~39 ℃之间,依照抗菌谱予针对性抗生素治疗缓解不明显,复查CT 示原置管处脓液明显减少,但仍有坏死物质残留并导致脓液蓄积,引起感染发热症状。决定予患者行小切口+肾镜探查,清除IPN 及胰周脓液。术中证实术前诊断,在肾镜引导下将胰周坏死组织清除,并放置多根脓腔腹腔引流管,术后持续脓腔冲洗+引流。术后复查消化道碘油造影,无消化道瘘。虽然SAP 并IPN 传统外科手术并发症的发生率达34%~95%,病死率达11%~39%[14,21],但经穿刺置管、内镜等治疗后效果仍不佳的患者有明确的开放手术指征。本组11 例经PCD、小切口联合肾镜IPN 清除清除效果不佳,患者仍有发热等炎性症状,复查CT 仍有脓肿及坏死物残留,遂予患者行开腹手术治疗,清除IPN。术中于脓腔内放置多根含侧孔引流管,生理盐水1 000~3 000 mL/d 经引流管反复冲洗,术后患者恢复良好,术后1~3 d 肛门排气后进食流质,5~7 d复查1 次CT,脓液明显减少或消失。术后随访5~30 个月,1~3 个月复查1 次CT,提示脓肿均缩小或消失,引流管逐根拔除,患者均未出现腹胀、发热、呕吐等不适。
笔者运用外科升阶梯治疗SAP 并IPN 体会:(1)根据CT 等影像学资料明确SAP 的诊断及确定IPN 的位置、分布。(2)明确病因,考虑治疗是否能和并发症一并处理。(3)B 超定位下PCD,需要在脓腔的高位及低位分别置管,且需放置套管及管径内径较大的,保证冲洗、防止管腔被堵塞的同时可让脓液及坏死物质排出通畅。(4)置管引流的同时需进行盐水的冲洗,促进创面干洁,减少脓液的吸收。(5)小切口结合肾镜清脓的优点在于切口小,对患者刺激小术后恢复较快。但术前需仔细阅片确定脓肿位置并于皮肤上拟做切口,术中注意操作轻柔,切勿使用暴力或撕扯,以免出现大出血及器官损伤。如遇术中大出血或消化道瘘,及时中转开放手术,迅速扩大手术切口及视野,直视下止血及清脓。(6)术前术后常规服用造影剂,对比消化道是否通畅及是否有瘘的形成,脓腔消失后能否早期拔管或因引流管压迫消化道而需早期拔管。⑺开腹手术对于治疗SAP 并IPN 的患者仍有一定疗效,特别是对于PCD 及小切口联合肾镜下IPN 清除效果不佳时或IPN 范围较大分散时。
综上所述,升阶梯治疗在治疗SAP 合并IPN 上效果明显,但针对不同患者仍需采取个体化措施,及选择适当的干预时机,以求达到最好的效果。

