石墨烯负载Co-CeOx纳米复合物的制备及其对氨硼烷水解产氢的催化性能
邹爱华 ,徐晓梅 ,周 浪 ,林路贺 ,康志兵
(1.江西师范大学,化学化工学院,江西 南昌 330022;2.南昌航空大学,材料科学与工程学院,江西 南昌 330063;3.华中科技大学无锡研究院,江苏 无锡 214174)
氢能具有清洁、高效、可再生的优点,被誉为是未来最有发展前景的能源之一[1 − 3]。然而,氢气性质活泼,易燃易爆,密度低,难以实现高密度储存,同时在运输和使用时容易产生安全隐患。因而实现氢的规模储运,是氢能应用得到快速发展的关键[4, 5]。氨硼烷 (NH3BH3, AB)由于具有高的储氢含量(19.6%)和良好的稳定性,是理想的储氢材料之一[6, 7]。AB的脱氢方式有三种:热解、醇解和水解。与热解[8]和醇解[9, 10]相比较,水解室温下就能反应、成本低廉,是一种有效的产氢方式。其反应过程如式(1)所示,即1 mol AB完全反应可以释放 3 mol H2[11 − 13]。
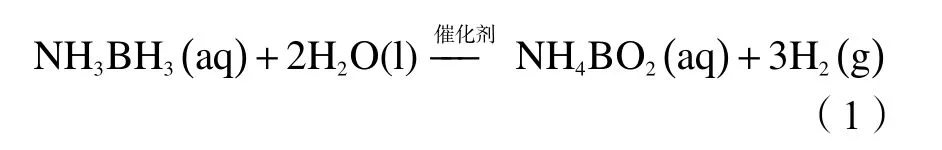
在未添加催化剂时(溶液pH值>7),该反应开始时间长且放氢缓慢。但是添加金属催化剂后,反应放氢时间明显缩短且具有好的可控性。到目前为止,贵金属纳米粒子如Pt、Pd、Ru、Rh等被认为是催化氨硼烷水解的最有效催化剂[14 − 17]。然而,由于其储量有限并且价格昂贵,限制了其在实际生产中的应用。近年来,非贵金属钴基催化剂在AB的催化水解方面被广泛地研究[18 − 22]。本课题组制备的还原氧化石墨烯负载非贵金属单质Co[21]以及双金属Co-Ni[22]催化剂对于AB水解都表现出良好的催化性能。然而,寻找到更加高效、稳定的非贵金属催化剂,且能够进一步改善催化剂的动力学性能,是实现AB水解制氢实际应用的关键问题之一。
稀土金属氧化物,得到越来越多的关注[23, 24]。稀土与金属之间的协同作用对提高催化剂的活性、增加其稳定性非常有利。石墨烯比表面积大,是一个优异的载体[24 − 26]。因此,如果将石墨烯作为载体,稀土作为助催化剂,钴作为催化活性金属,合成一种三组分的金属-氧化铈/石墨烯纳米复合材料,同时发挥石墨烯和稀土的优越性能,有望得到一个氨硼烷水解放氢的廉价高效催化剂。
基于此,本研究通过简单的浸渍还原的方法,在室温下合成了一种三组分Co-CeOx/graphene纳米复合材料,通过粉末X射线衍射、透射电镜、X射线光电子能谱等对材料进行了表征。并利用Co-CeOx/graphene作为AB水解放氢催化剂研究了其催化性能,探索了不同的稀土含量、负载量,不同的温度,不同的稀土类型等条件对催化性能的影响,测试了最优催化剂的活化能和循环使用性能。
1 实验部分
1.1 主要试剂及实验仪器
氨硼烷 (NH3BH3,90%)、硼氢化钠 (NaBH4,99%):Aldrich 公司;六水氯化钴 (CoCl2·6H2O,≥ 99%):国药集团化学试剂有限公司;六水硝酸铈(Ce(NO3)3·6H2O)、六水硝酸镧(La(NO3)3·6H2O)、六水硝酸镝(Dy(NO3)3·6H2O)、六水硝酸铽(Tb(NO3)3·6H2O)、六水硝酸钆(Gd(NO3)3·6H2O)、五水硝酸铒(Er(NO3)3·5H2O)、五水硝酸镱(Yb(NO3)3·5H2O)、99.9%:百灵威化学试剂有限公司);石墨烯(Graphene):碳美有限公司;去离子水实验室自制。
JEM-2010透射电子显微镜(TEM)、JEM-2010高分辨透射电镜 (HRTEM),日本 jeol公司;Rigaku RINT-2200 X 射线衍射仪 (XRD),日本理学公司;Thermo ESCALAB 250XI X 射线光电子能谱 (XPS),美国Thermo Fisher Scientific 公司。
1.2 催化剂的制备
Co-CeOx/graphene纳米催化剂是通过一种简单的共还原方法在室温下制备的。主要步骤如下:将10 mg石墨烯加入5 mL去离子水,在室温下超声分散30 min,得到分散良好的石墨烯悬浮液;然后将 11.89 mg CoCl2·6H2O 和 17.76 mg Ce(NO3)3·6H2O加入到石墨烯悬浮液中,搅拌30 min;然后将还原剂10 mg NaBH4加入到上述溶液中,搅拌至气泡停止产生,还原得到的黑色物质即为Co-CeOx/graphene。
采用上述方法,通过调整石墨烯的用量(分别为 5、10、15 mg),其他药品用量不变化,制备了不同石墨烯浓度的Co-CeOx/graphene催化剂。改变Ce(NO3)3·6H2O的含量,按照上述方法,合成了不同CeOx摩尔分数(10%、15%、28%、35%、45%、50%、55%)的Co-CeOx/graphene催化剂。改变不同的稀土类型,按照上述的方法,制备Co-ReOx/graphene(Re =La、Dy、Tb、Gd、Er、Yb; 45% of Re)催化剂。
1.3 催化制氢性能测试
将容量为50 mL的双颈圆底烧瓶置于298 K,大气环境下的水浴中,并将反应烧瓶的一个颈部连接到气体滴定管上。在反应瓶中加入合成的Co-CeOx/graphene 的悬浮液 (nCo= 0.05 mmol; 5 mL),在剧烈磁力搅拌下向反应烧瓶中加入34.3 mg AB(1 mmol),并将反应瓶另一个颈部迅速密封,开始进行催化反应。通过记录气体滴定管中水的位移来监测氢的释放,当气体逸出停止时反应完成。
用相同的方法测试AB水解的其他催化剂的活性。在所有催化反应中,nCo/nAB的物质的量比保持恒定在0.05。
1.4 计算方法
转化频率(TOF)表示单位时间内单位催化剂的转化率,是比较催化剂活性大小的根本依据,其计算公式如式(2)示。

式中,nH2为产生H2的摩尔数。nCo为催化剂中所用Co的摩尔数,而t为反应总时间,以min为单位。
2 结果与讨论
2.1 催化剂形貌及结构表征
采用透射电镜来分析合成催化剂的微观结构,图1(a)是石墨烯的微观结构图,从图中可以看到石墨烯是透明的,说明石墨烯的厚度很薄。同时还可观察到氧化石墨烯片层各区域颜色深浅不一,并且有一定的褶皱存在,这说明该石墨烯不全是单片层结构,而是由几个单片层叠加而成。从图1(b) Co/graphene的透射电镜照片中可以看到,Co纳米粒子虽然分散在石墨烯片层上,但金属颗粒聚集明显,这将导致纳米粒子表面积明显减小。而在图1(c), (d)的Co-CeOx/graphene透射电镜照片中可以看出,Co纳米粒子能够很好地分散在石墨烯片层和表面上,说明CeOx的加入能够获得分散更均匀的纳米粒子,金属、CeOx以及石墨烯之间具有一定的协同作用。此外对催化剂样品进行了EDS分析,如图2所示,验证了Co、Ce、O和C元素的存在。

图1 (a):graphene; (b):Co/graphene, (c)−(d):Co-CeOx/graphene催化剂的TEM照片Figure 1 TEM images of (a): graphene; (b): Co/graphene;(c)−(d): Co-CeOx/graphene

图2 Co-CeOx/graphene 催化剂的 EDX 谱图Figure 2 EDS spectrum of the Co-CeOx /graphene catalyst
利用XRD分析Ce的引入对该催化剂结构的影响。由图3(a)可以看出,在Co/graphene的XRD图中,25°左右出现的衍射峰为石墨烯(002)面的特征衍射峰,但在其他角度并未观察到明显的衍射峰。图3(b)中可以看出,当引入Ce后,其25°处的衍射峰明显降低,没有出现Co的特征衍射峰,资料表明[27 − 29],Co 也许为无定形的状态。将合成的样品在氮气保护下500 ℃煅烧4 h进行了XRD表征,如图3(c)所示,从图中可以观察到Co(111)和CeO2(111)面的特征峰。

图3 (a) Co/graphene, (b)Co-CeOx/graphene, (c)Co-CeOx/graphene 样品在氮气保护下 500 °C 煅烧 4 h 的 XRD 谱图Figure 3 XRD patterns of (a) Co /graphene, (b) Co-CeOx/graphene and (c) Co-CeOx/graphene annealed at 500 °C for 4 h under N2 in tube furnace
为了进一步确定Co-CeOx/graphene中Co和Ce的化学状态,对其进行了XPS分析,并与CeOx/graphene进行了比较。对于Co-CeOx/graphene催化剂中的Co 2p谱图而言,如图4(c)所示,在结合能为 776.98 eV 处的 Co 2p3/2峰被分配给 Co(0),与Co 金属(777.80 eV)相比,其负位移了 0.82 eV[30]。此外,还能在该谱图中观察到氧化态和卫星态钴衍射峰的存在。另一方面,从图4(d)的Ce 3d能谱图中能明显观察到Ce3+和Ce4+的信号,标记为V1、V3(3d5/2)、U1、U3、U4(3d3/2) 的五个峰值对应于 CeO2特征的自旋轨道峰,标记为V2(3d5/2)、U2(3d3/2) 的另外两个峰归因于Ce2O3。通过XPS测定分析Ce(IV):Ce(III) 的原子比约为 5∶2。据已有的报道表明[24, 31, 32],CeOx化合物的化合价和缺陷结构是很活跃的,并可能响应一些物理参数(如其他离子的存在、氧的分压和温度)而自发改变。因此,Co-CeOx/graphene催化剂中CeO2和Ce2O3的存在是合理的。以上结果表明,Co与CeOx之间存在较强电子相互作用,这种相互作用将进一步影响金属活性中心的键合构型,从而有利于提高催化活性。

图4 (a) Co-CeOx/graphene 的 XPS 谱图; (b) CeOx/graphene 的 XPS 谱图; 相对应的精细谱图 (c) Co 2p, (d) Ce 3dFigure 4 Survey XPS spectra of Co-CeOx/graphene (a) and CeOx/graphene (b);Co 2p XPS spectra (c) and Ce 3d XPS spectra (d) of the as-synthesized catalysts
2.2 催化剂的水解催化性能
为了比较不同催化剂对催化AB水解产氢性能的影响,在相同条件下采用排水集气法分别测试了 Co-CeOx/graphene、Co/graphene、Co、CeOx/graphene和graphene的催化性能。图5显示了不同催化剂催化AB水解的放氢速率。

图5 298 K 下催化 AB 水溶液 (200 mmol/L, 5 mL)放氢的生产率与反应时间的关系(Co/AB = 0.05)Figure 5 Hydrogen productivity vs.reaction time for hydrolysis of aqueous ammonia borane (200 mmol/L,5 mL) catalyzed by the different catalysts at 298 K(Co/AB = 0.05)
由图5可以看出,单独的Co完成反应需要15 min,且只能反应92%左右。Co/graphene催化水解速率虽有所提高,但也需要12 min才能完成,且产氢率只有95%左右。而Co-CeOx/graphene三组分催化剂则有着更为优异的催化性能,水解反应在1.33 min完成,且能够完全产氢,对应的TOF值为 45.1 min−1,大约是相同条件下 Co(3.68 min−1)及 Co/graphene(4.75 min−1)催化剂的 12.3 和 9.5 倍。通过对比文献(见表1),其TOF也高于大多数已报道的室温下AB水解制氢用非贵金属催化剂,几乎是目前采用单金属Co在此反应中的最高值。

表1 室温下水溶液中AB水解制氢各种非贵金属催化剂的催化活性Table 1 Catalytic performances of various non-noble metal catalysts for hydrogen generation from the hydrolysis of aqueous AB at room temperature
从图5还可以看出,无论是graphene还是CeOx/graphene都没有表现出任何催化活性。这在一定程度上反映Co-CeOx/graphene的催化活性主要来源于Co,而石墨烯和CeOx则协同作为增效剂,且上述结果表明,稀土金属氧化物CeOx在合成高活性石墨烯基多组分复合催化剂中起着关键作用。具体原因分析如下:一方面,从图1的TEM和图2的EDS分析可知,由于graphene、CeOx界面协同作用,有利于Co纳米粒子的支撑及分散,从而催化活性提高;另一方面,在催化反应条件下,铈(Ⅳ)和铈(Ⅲ)这两个氧化态可以相互转化,很容易形成铈(Ⅲ)缺陷,该缺陷的存在会导致在氧化物表面上积聚过多的负电荷,从而增强金属纳米颗粒与氧化物表面的配位,利于底物与金属的相互作用来增强催化剂的催化活性[33]。此外,由于graphene的高导电性,Co和CeOx在graphene界面上的电荷转移更快,其亲水和多孔表面也可使反应性分子能够较快到达Co-CeOx表面以参与脱氢反应。这种独特的协同作用可确保整个水解过程有效且快速有序地进行,从而有益于提高内部活性组分的利用效率[4]。
为了进一步研究Co-CeOx/graphene中CeOx以及graphene对催化性能的影响,分别调控了催化剂中CeOx以及graphene的含量。从图6可以看出,催化剂的活性显著地依赖于CeOx的含量。随着CeOx含量的增加,放氢所需时间先缩短后延长,在CeOx含量为45%时,其放氢所需时间最短,但随着CeOx含量的进一步增加导致完全产氢的时间显著延长,这可能是由于过量的CeOx限制了活性位点的存在。在目前的体系中,在CeOx含量为45%时,Co-CeOx/graphene在AB的水解脱氢反应中最为活跃。
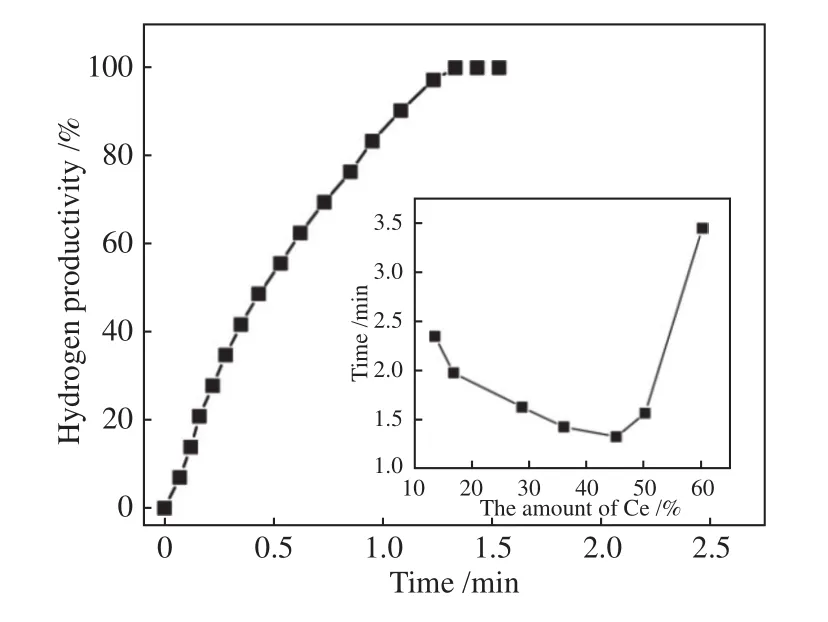
图6 Co-CeOx/graphene 催化剂在 298 K 下催化氢硼烷水溶液 (200 mmol/L, 5 mL)释放氢的生产率与反应时间的关系 (Co/AB = 0.05, Ce = 45%);插图显示了Co-CeOx/graphene在不同的Ce含量下催化AB水解脱氢的反应时间Figure 6 Hydrogen productivity vs.reaction time for hydrolysis of aqueous ammonia borane(200 mmol/L, 5 mL) catalyzed by the Co-CeOx/graphene catalyst at 298 K (Co/AB = 0.05,Ce = 45%); the inset shows the reaction time for the hydrolytic dehydrogenation of AB catalyzed by Co-CeOx/graphene with different molar contents of CeOx
由于氧化铈有效地提高了Co/graphene的催化活性。为了了解其他过渡元素金属化合物是否也可表现出和Co具有协同作用的性能,利用相同方法合成了Co-ReOx/graphene纳米复合材料(Re =La、Dy、Tb、Gd、Er、Yb; 45% of Re),并对它们水解AB的催化活性进行了比较,如图7所示。从图7可以看出,所合成的Co-ReOx/graphene均比Co/graphene(如图5)表现出更高的催化活性,几乎所有的催化剂都在1.5 min中内完成反应。这主要是因为稀土元素具有类似的物理化学特性,其外层电子较多,如上所述,这一特性将Co活性位点提高到了富电子态,有利于催化反应,从而提高其催化性能。在Co-ReOx/graphene这一类催化剂中,其催化性能顺序 Yb > Er > Ce > Dy > Tb > La。虽然Co-CeOx/graphene的催化性能并不是最好的,但其与Co-YbOx/graphene的TOF值相差并不大。考虑到稀土元素产量与稳定性等实际生产的要素,以CeOx加入催化剂最为合适。

图7 不同稀土元素的 Co-ReOx/graphene 催化剂催化氢硼烷水溶液 (200 mmol/L, 5 mL)释放氢的生产率与反应时间的关系 (Co/AB = 0.05, Re = Ce、La、Tb、Er、Dy and Yb, 45% of Re)Figure 7 Hydrogen generation from the hydrolysis of ammonia borane (200 mmol/L, 5 mL) catalyzed by Co-ReOx /graphene(Re = Ce, La, Tb, Er, Dy and Yb, 45% of Re) under ambient atmosphere at room temperature (Co/AB = 0.05)
从图8可以看出,随着graphene含量的增加,放氢所需时间不断缩短。这可能是由于graphene含量增加可以提供更多的成核位点使得Co-CeOx更为分散的分布在石墨烯上,导致其催化性能提高。但是考虑到石墨烯价格昂贵,且从图8可知,当石墨烯含量超过10 mg时,石墨烯的增加并不会使Co-CeOx/graphene的催化性能显著提高,因此,本文所采用的石墨烯含量为10 mg。

图8 不同石墨烯含量的 Co-CeOx/graphene 催化剂在298 K 下催化氢硼烷水溶液 (200 mmol/L,5 mL)释放氢的生产率与反应时间的关系(Co/AB = 0.05)Figure 8 Hydrogen productivity vs.reaction time for the hydrolysis of aqueous ammonia borane (200 mmol/L,5 mL) catalyzed by Co-CeOx /graphene with different amounts of graphene at 298 K
为了得到水解反应的活化能(Ea),本文进行了不同温度下 Co-CeOx/graphene、Co/graphene、Co 催化剂催化AB的水解测试,结果如图9所示。从图9((a)、(b)、(c))可以看出,当反应温度从 298 K升高到313 K时,产氢速率逐渐增加,说明较高的反应温度有利于提高催化性能。在水解反应后期,各图的产氢曲线有轻微偏差,这可能是由于催化反应进行到后期,AB浓度很低造成的扩散限制所致。在这种情况下,可以从每个小区的线性部分确定水解速率(k)。根据Arrhenius方程,如式(3)所示,分别计算得到了不同催化剂的活化能。

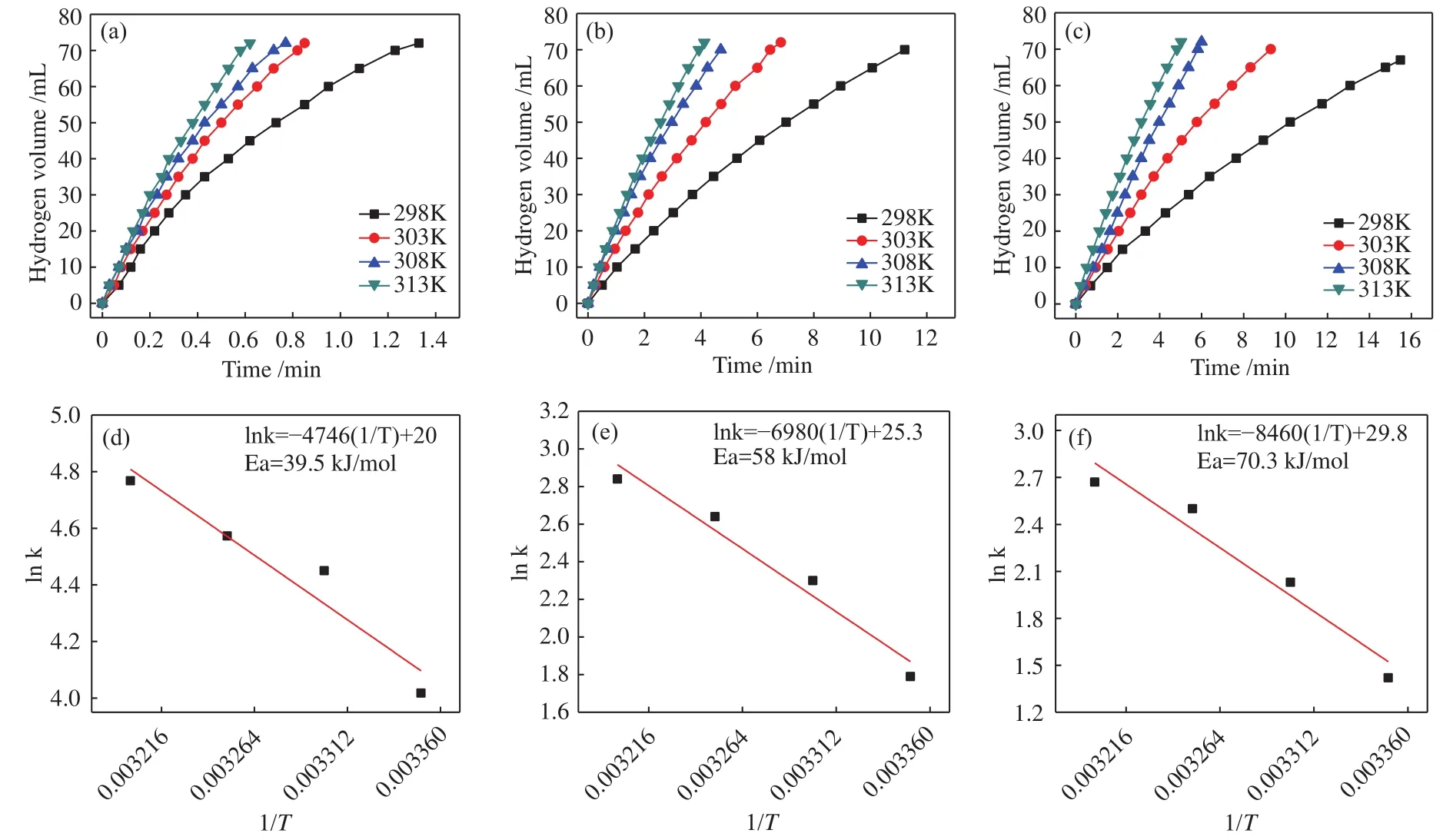
图9 (a) Co-CeOx/graphene, (b) Co/graphene, (c) Co 催化剂在 298−313 K 下催化氨硼烷溶液 (5 mmol/L, 5 mL)放氢量与时间的关系 (Co/AB = 0.05, Ce = 45%);(d), (e), (f)分别为 (a), (b), (c)对应的阿伦尼乌斯曲线图Figure 9 Evolution plots of hydrogen generated vs.time for the hydrolysis of ammonia borane (200 mmol/L, 5 mL, Co/AB=0.05)catalyzed by Co-CeOx /graphene (Ce = 45%) (a), Co/graphene (b) and Co (c) at different temperatures (298–313 K);Graphs (d), (e) and (f) are the Arrhenius plots obtained from the Graphs (a), (b) and (c), respectively
从图9(d)可以看出,Co-CeOx/graphene催化AB水解所需的活化能为39.5 kJ/mol,明显低于图9((e),(f))中Co/graphene和Co 所需为58 和 70.3 kJ/mol的活化能,以及低于同条件下大部分报道的反应活化能值(表1)。这说明了CeOx能显著改善AB水解制氢的反应动力学,这也进一步说明了相比于纯 Co 和 Co/graphene, Co-CeOx/graphene表现出了更优异的催化性能。
此外,催化剂的耐久性和可回收再利用性对实际应用至关重要。本文在298 K下对催化剂的循环使用性能进行了测试,结果如图10所示。

图10 Co-CeOx/graphene 催化剂催化氨硼烷水解脱氢循环使用性能图Figure 10 Stability characterization of Co-CeOx/graphene in fives run for hydrolytic dehydrogen of ammonia borane
Co-CeOx/graphene催化剂在五次循环催化AB放氢过程中,其水解催化完成时间由最初的1.33 mim延长到3.73 min,造成的活性损失可能是由于纳米粒子的聚集或者是催化剂表面沉积了偏硼酸。虽然反应活性有所降低,但对氨硼烷水解产氢反应仍能保持100%的产氢率,具有较好的循环稳定性。
3 结 论
本研究采用简单的共还原方法合成了Co-CeOx/graphene纳米复合材料,并将其应用于室温催化AB水解产氢。实验结果表明,稀土金属氧化物CeOx在石墨烯基多组分复合催化剂的高活性中发挥了关键作用,CeOx、非贵金属和石墨烯的结合明显增强了对AB水解脱氢的催化活性,并具有很高的稳定性。该催化反应的TOF和Ea分别为45.1 min−1和 39.5 kJ/mol,经五次循环催化后,催化产氢能力仍可达到100%。这种简单有效的合成方法有望推广到金属、稀土元素和石墨烯的催化体系,对于催化剂的应用和氨硼烷作为储氢材料发展具有较为广阔的应用前景。

