FER分子筛Lewis酸中心对异丁烯催化转化的影响
杨佳宝 ,惠 宇 ,秦玉才 ,张晓彤 ,王 焕 ,宋丽娟,,*
(1.辽宁石油化工大学 辽宁省石油化工催化科学与技术重点实验室,辽宁 抚顺 113001;2.中国石油大学(华东)化学工程学院,山东 青岛 266555)
2017年国家能源局等15部委联合发布了《关于扩大生物燃料乙醇生产和推广使用车用乙醇汽油的实施方案》,根据技术要求,MTBE作为调和组合加入到汽油中将受到限制,这将会导致异丁烯产能过剩,这使得如何高效利用C4资源,调节C4烯烃分布成为了一个迫在眉睫的问题。而在化工行业中,丁烯是重要的基础原料之一。其中,1-丁烯是合成仲丁醇、脱氢制丁二烯的原料,顺、反2-丁烯用于合成C4、C5衍生物及制取交联剂、增塑剂和叠合汽油等[1, 2]。值得注意的是,正丁烯在定向转化为丙烯、丁二烯等高值化学品的低碳烯烃转化工艺和C4深加工方面也有很好的应用前景。因此,将异丁烯骨架异构化为应用前景广泛的正丁烯是解决该问题的一条有效路径。
在石油化工领域,具有八元环和十元环垂直相交孔道结构的FER(HZSM-35)分子筛是常用的异构化催化剂,在C4烯烃异构化领域,已经有了一定的研究[3 − 9]。而近些年的研究大都集中于正丁烯骨架异构化为异丁烯,普遍认为,在该反应中反应机理主要有单分子机理[10, 11]和双分子机理[12, 13],其具体反应路径如图1和图2所示。在反应初始时,反应以双分子机理为主,产物表现出较低的选择性,随着反应的进行,单分子机理占据了主导地位,表现在选择性逐步提高直至稳定或催化剂失活[11]。目前,关于这两种反应机理的有效酸中心的认知还是不够清晰,而且关于异丁烯骨架异构化的反应机理研究还不够充分,之前世界各国也鲜有报道。虽然Gon等[14]早在1998年就进行过异丁烯骨架异构化为正丁烯的研究,但是他的研究着重于对比不同孔道结构和无定形催化剂在主反应选择性上表现出的差异,发现在FER上,异丁烯向正丁烯反向骨架异构化的选择性很高,但是并没有深入到特定酸中心这个理论水平上。而Sub Bong Hong 团队[15, 16]通过13C 标记法研究证明,在FER分子筛上正丁烯和异丁烯骨架异构化的活化能是有差异的,而且也只是在特定条件下,两者的反应机理才具有一致性。

图1 单分子反应路线机理图Figure 1 Mechanism diagram of single molecule reaction route
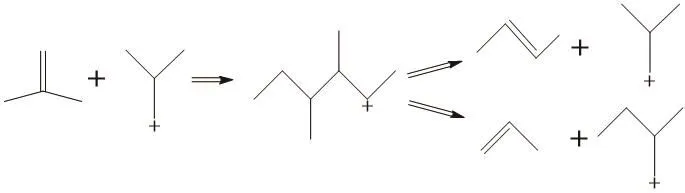
图2 双分子反应路线机理图Figure 2 Mechanism diagram of double molecule reaction route
本研究旨在通过比较正丁烯骨架异构化和异丁烯骨架异构化在不同反应温度条件下的差异来确定机理上的异同。此外,通过使用AHFS作为脱铝剂,研究不同程度脱铝处理后的FER分子筛对异丁烯骨架异构化反应性能的影响,并探索不同酸中心对异丁烯催化转化的影响。这在之前的研究报道还极少,这对于设计高效的催化剂具有重要意义。
1 实验部分
1.1 材料
HZSM-35分子筛采购于南开大学催化剂厂,高纯异丁烯气体采购于大连大特气体有限公司,氟硅酸铵采购于国药集团化学试剂有限公司。
本实验采用传统液相同晶置换的方法,对HZSM-35催化剂原粉进行改性处理。将HZSM-35分子筛分别与不同浓度的氟硅酸铵溶液进行混合(每1 g 分子筛与 20 mL 溶液混合),在 80 ℃ 下均匀搅拌 8 h,洗涤、抽滤、烘干,最后在 550 ℃ 下焙烧6 h,根据氟硅酸铵浓度不同分别记为Z-35AHSF(0.1)和Z-35AHSF(0.2),未经处理的样品则标记为Z-35。
1.2 催化剂的表征
原粉及氟硅酸铵改性所制样品的硅铝物质的量比(SAR)等采用通过美国铂金埃尔默(Perkin Elmer)公司的8000 OES型电感耦合等离子发射光谱仪(ICP-AES)测定。样品的物相分析采用日本理学株式会社D/MAX-RB型X射线衍射仪(XRD),Cu 靶Kα 射线,入射波长为 0.154 nm,管电压 40 kV,管电流 40 mA,5°−40°扫描,扫描步长为 0.02°,连续扫描。用扫描电子显微镜(SEM)来观察分析改性前后样品的表面微观形貌变化,所使用的仪器型号为日本Hitachi公司的SU-1510。而样品的比表面积和孔体积在美国麦克公司(Micromeritics)生产的ASAP 2020型物理吸附仪上测定,催化剂样品在623 K下抽真空预处理10 h,用液氮进行低温冷却至77 K,进行N2吸附-脱附实验,并利用BET (Brunauer-Emmett-Teller)法计算比表面积,HK(Horvath-Kawazoe)法计算微孔的孔容,BJH (Barrett-Joyner-Halenda)法计算介孔的孔容。
催化剂样品酸强度和酸密度等酸性质的表征采用的吸附NH3的程序升温脱附技术(NH3-TPD)以及傅里叶变换红外光谱技术(FT-IR)。用美国Perkin-Elmer公司的Frontier红外光谱仪上进行FTIR表征,具体操作过程参照文献[17]。用美国麦克公司(Micromeritics)生产的 Auto Chem Ⅱ型化学吸附仪完成NH3-TPD的测定,样品在He氛围活化之后吸附 NH3,并以 10 ℃/min 的升温速率从 120 ℃升高到600 ℃,同时脱附NH3并采集信号。
1.3 催化反应评价
称量 1 g 催化剂样品在 10 MPa下压片,破碎至20−40目,然后装在反应器的恒温区,两端装有20−40目的石英砂。反应前催化剂将样品在氮气氛围下升温至反应温度350 ℃,并在该温度下活化8 h,然后通入异丁烯原料气进行反应,WHSV =6 h−1,每隔 1 h 通过六通阀取样后进入安捷伦公司Na2SO4洗脱的Al2O3(HP-AL/S)色谱柱分离后进行气液相全组分在线分析。之后分别采用下式(1)−(3)计算异丁烯的转化率,正丁烯的选择性以及产率。在所研究的反应条件下,1-丁烯会迅速的发生顺反异构,生成顺-2-丁烯和反-2-丁烯,因此,将这1-丁烯、顺-2-丁烯和反-2-丁烯这三种线性丁烯都作为反应物进行计算,所以计算正丁烯转化率,异丁烯选择性及收率的公式为(4)−(6)。

式中,Atotal:总峰面积;A1-butene:1-丁烯峰面积;Acis-2-butene:顺-2-丁烯峰面积;Atrans-2-butene:反-2-丁烯峰面积;Aisobutene:异丁烯峰面积;f1:异丁烯相对摩尔校正因子;f2:正丁烯相对摩尔校正因子;
2 结果与讨论
2.1 不同温度对正丁烯和异丁烯骨架异构化反应性能影响
在通常情况下,丁烯大都是以1-丁烯、顺-2-丁烯、反-2-丁烯、异丁烯四种同分异构体组成的混合物形式存在,因此,反应温度对该反应的产物组成有很大的影响,本工作首先考察了不同反应温度对丁烯骨架异构化反应性能影响。图3表示的是常压下,四种丁烯同分异构体在不同温度下的热力学平衡图[18, 19]。从图3可以看出,随着温度的升高,异丁烯的热力学平衡含量逐渐下降,从热力学角度看,高温更有利于异丁烯骨架异构化为正丁烯,反之,低温则更利于异丁烯的生成。然而,由于分子筛的限域条件和反应动力学因素,正丁烯骨架异构化和异丁烯骨架异构化这两个反应的发生需要较高的温度和酸强度。所以,这两个反应的反应温度存在最优值。在300−410 ℃选取了五个温度点,对两个反应分别进行了反应评价,选取反应第8 h评价数据列于表1中。
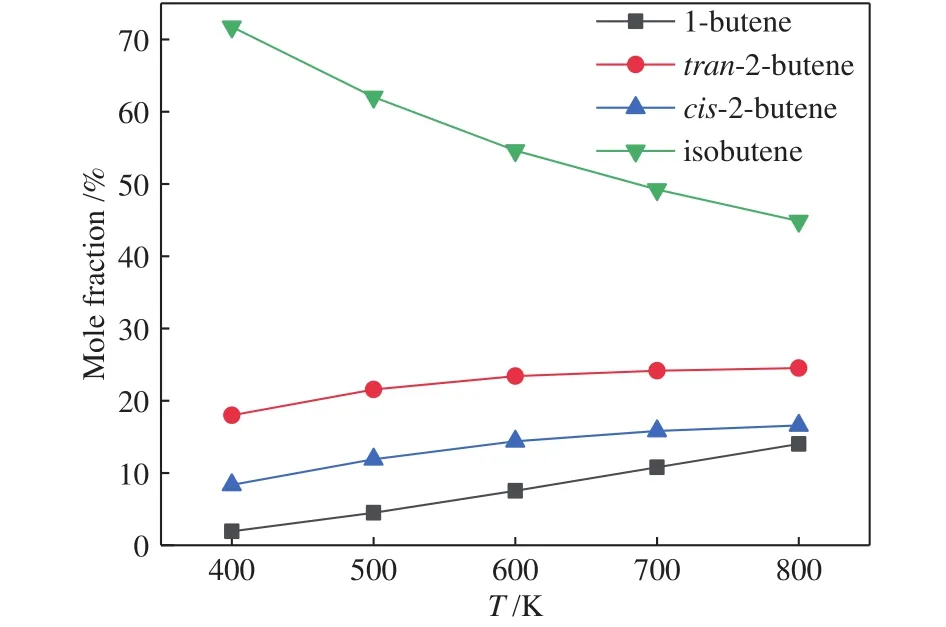
图3 四种丁烯在不同温度下的热力学平衡图Figure 3 Thermodynamic equilibrium diagrams of four butenes at different temperatures
从表1中可以看出,随着反应温度的升高,这两个反应的反应物转化率升高而产物选择性随之降低,且均在350 ℃时收率达到最优。但是从两个反应产物收率对比中可以看到差异性,对于正丁烯骨架异构化反应,在350和375 ℃两个反应温度下的收率相近,而异丁烯骨架异构化这个反应则存在一定差距。此外,两个反应在410 ℃下的产率的差异很大,对于异丁烯骨架异构化来说,高温下的收率很低,而正丁烯骨架异构化则不然,这表明了高温对正丁烯骨架异构化更有益。同时,在高温条件下,异丁烯作为原料进行异构化时,其转化率(81.00%,410 ℃)明显高于热力学平衡转化率[18, 19](50.28%,410 ℃),但是其正丁烯选择性却很低,这是由于在高温下,异丁烯分子更容易发生齐聚-裂化这个副反应,而齐聚-裂化反应遵循的是双分子反应路径。
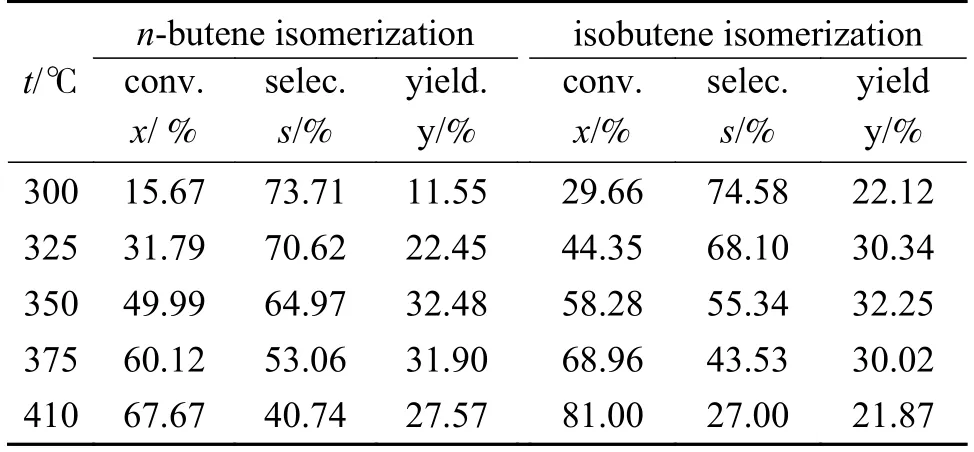
表1 不同温度下正丁烯骨架异构化和异丁烯骨架异构化反应评价表Table 1 Evaluation of isomerization reaction of n-butene and isobutene at different temperatures
从四种丁烯同分异构体之间的分布以及丁烯和其他副产物含量的比较这两个角度看,正丁烯骨架异构化和异丁烯骨架异构化这两个反应之间还存在一些差异。图4表示的是在不同反应温度下,两个反应体系中丁烯含量的对比结果。表2表明了在最优温度350 ℃、反应8 h时,各种丁烯产物占全部丁烯总含量的百分比结果。从中可以看出差异性,异丁烯异构化反应中,异丁烯的量高于该温度下的热力学平衡,相差2.73%;而正丁烯异构化反应中,正丁烯相比热力学平衡组成高了15.94%。产物的组成高于热力学平衡状态的组成是因为有部分C4烯烃是通过齐聚-裂化副反应产生的。此外,结合图4可以发现副反应的影响,异丁烯异构化反应体系中的副反应效应更强,生成的副产物更多。
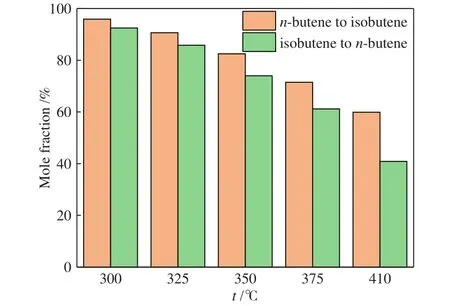
图4 不同反应温度产物中四种丁烯总含量对比Figure 4 Comparison of four butenes content in products at different reaction temperatures
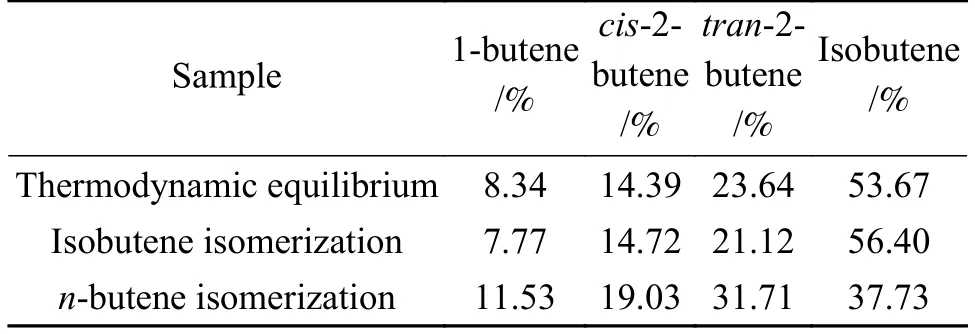
表2 两个反应的四种丁烯异构体产物分布Table 2 Distribution of four butene isomer products for two reactions
正是由于反应中所不希望的副反应的出现,提高主反应选择性这项工作的探索也一直没有停止。在这个反应体系中,由于齐聚-裂化反应和氢转移反应的存在,导致产物中出现了大量戊烯和烷烃。为了提高主反应的选择性,抑制齐聚-裂化等副反应的活性位点是十分必要的,而根据报道[20 − 25],对分子筛进行改性的方式都主要集中在元素改性、离子交换、表面修饰等方式,而其中提高分子筛的Si/Al比是提高主反应选择性的一种有效办法。
六氟硅酸铵(AHFS)是一种有效的脱铝剂,对提高HZSM-35的Si/Al比很有帮助。已经被广泛应用于获得表面富硅的分子筛,许多研究者通过使用AHFS为了进一步提高分子筛催化剂活性和热稳定性。根据文献报道[26, 27],通过六氟硅酸铵处理过的分子筛,其表面的铝原子可以有效移除,而分子筛孔道内的铝原子的变化可以忽略不计。但是,Kao等[28]在用AHFS对MOR分子筛进行脱铝改性时发现,脱下的Al还会残留在孔内,所形成的非骨架铝物种主要是[AlFx(H2O)6−x](3−x)+和AlFx(OH)3−x。但他们的工作主要着眼于非骨架铝物种的表征上,并没有对其对反应活性的影响进行讨论。
2.2 AHFS改性HZSM-35表征及其对异丁烯骨架异构化反应性能影响
2.2.1 织构性质表征
利用电感耦合等离子体原子发射光谱(ICPAES)测定Z-35原粉样品和不同浓度氟硅酸铵(AHFS)改性后的样品中Si元素和Al元素的含量,并计算得到SAR值,结果列于表3中。经过AHFS处理分子筛后,分子筛中的Al含量骤减,且随着AHFS处理浓度的增大,分子筛样品的SAR值也随之增大。

表3 不同浓度AHFS处理HZSM-35分子筛的织构性质Table 3 Basic physical parameters of the parent and AHFS modified HZSM-35 zeolites
图5为HZSM-35以及不同浓度AHFS改性后样品XRD谱图。由图5可知,HZSM-35分子筛在经AHFS处理污染前后均保有HSZM-35(FER)分子筛的特征衍射峰,特别是经不同浓度AHFS处理后,分子筛催化剂也没有出现其他杂峰,这说明其晶体结构依旧保持完整,并没有对分子筛骨架造成破坏。图6显示的是HZSM-35以及不同浓度AHFS改性后样品的SEM照片,从图6可以看出,改性前后的HZSM-35都保持了相似的晶体形态和晶体尺寸,这表明AHFS的处理对这些的影响较小。但是需要注意的是,对比AHFS处理前后的分子筛样品的SEM照片,可以发现,Z-35原粉样品的表面很光滑,而改性之后样品表面较为粗糙,表明AHFS对HZSM-35分子筛的外表面有一定刻蚀作用。

图5 HZSM-35 以及不同浓度 AHFS 改性后样品 XRD 谱图Figure 5 XRD patterns of the parent and AHFS modified HZSM-35 zeolites

图6 HZSM-35 以及不同浓度 AHFS 改性后样品的 SEM 照片Figure 6 SEM images of the parent and AHFS modified HZSM-35 zeolites(a)/(d): Z-35; (b)/(e): Z-35AHFS(0.1); (c)/(f): Z-35AHFS(0.2)
从表3中可以看出,三种不同SAR的FER样品总比表面积和微孔比表面积相差不大,而孔容却出现了较为明显的差异。经AHFS处理后,FER样品微孔孔容下降,而随着处理浓度的增大,介孔孔容先减小后增大。这在之后吸附吡啶的红外光谱结果中有进一步讨论。Z-35AHSF(0.2)孔径明显增大是由于高浓度的AHFS处理后,起到了一定的扩孔作用。
2.2.2 酸性质表征
图7的NH3-TPD谱图给出了不同浓度AHFS改性HZSM-35分子筛的酸强度和总酸量分布变化。因为NH3分子的动力学直径小于FER分子筛中八元环的直径,所以NH3-TPD可以代表总酸量情况[29]。由此可知,三种分子筛催化剂均在150−250 ℃ 和 300−450 ℃ 两个温度区间存在 NH3脱附峰,分别对应的是分子筛的弱酸性位和中强酸性位。总体上来讲,与未经处理的HZSM-35分子筛相比,经AHFS改性的样品总酸量有所降低。其中,对于低浓度AHFS处理后的样品,位于150−250 ℃的弱酸酸量最少,然而,对于高浓度AHFS处理后的样品,其中强酸中心酸量最少。另外,在酸量下降的同时NH3脱附峰向左迁移,说明经AHFS处理后弱酸进一步被削弱或者分子筛中产生了其他类型的弱酸,所以HZSM-35分子筛的弱酸强度被减弱。
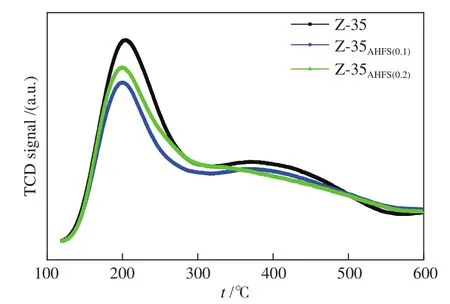
图7 HZSM-35 以及不同浓度 AHFS 改性后样品NH3-TPD谱图Figure 7 NH3-TPD patterns of the parent and AHFS modified HZSM-35 zeolites
图8为150 ℃下不同样品的原位红外光谱谱图,进一步分析改性前后分子筛羟基基团组成变化。图中3745 cm−1归属于分子筛外表面的末端硅羟基(Si−OH)振动特征峰,3722 cm−1归属于 FER脱铝之后新形成的 Si−OH 振动特征峰,3642 cm−1归属于非骨架铝羟基振动特征峰,3602 cm−1归属于硅铝桥羟基振动特征峰。根据谱图可清楚看出,Z-35AHFS(0.1)催化剂的硅铝桥羟基特征峰有所增加,非骨架铝羟基特征峰(Al(OH)2+、Al(OH)+)有所减小,这与上述的NH3-TPD结果讨论相一致。

图8 HZSM-35 以及不同浓度 AHFS 改性后样品的红外光谱谱图Figure 8 FT-IR spectra of the parent and AHFS modified HZSM-35 zeolites
另外,Z-35AHFS(0.2)的硅铝桥羟基振动峰面积减小,非骨架铝羟基振动峰面积增加,这可能是由于AHFS与骨架上的铝物种作用,致使骨架铝被脱除变成非骨架铝。此外,Z-35AHFS(0.1)催化剂的谱图出现了3722 cm−1的振动峰。这说明在AHFS脱除骨架铝物种的同时未及时补硅,进而产生了一些硅羟基。但是当 AHFS 增加到 0.2 mol/L 时,3722 cm−1振动峰减弱,此现象是由于Si含量的增加填充上了之前形成的缺陷位,导致硅羟基的减少。
为了进一步探究AHFS处理后活性位组成的变化,作者进行了吸附碱性探针分子吡啶的红外光谱表征,结果如图9。图中1455与 1445 cm−1是两种不同强度的L酸特征峰。由图9可知,与HZSM-35原粉相比,经脱铝剂改性过的Z-35AHFS(0.1)在1455与1445 cm−1两个位置新产生了两个特征峰,这就表明了AHFS改性处理使HZSM-35分子筛产生了两个新的L酸中心。当脱铝剂浓度增加至0.2 mol/L 时,1445 cm−1处的 L 酸特征峰消失,这表示脱铝剂除掉了一部分非骨架铝结构。结合图7的NH3-TPD表征可以发现,高浓度脱铝剂脱掉了分子筛骨架上一部分铝物种且未残留在孔道中,而低浓度AHFS处理的样品再次出现的中强酸中心,则证实了新形成的铝物种残留在孔道中且具有较强的酸性,对于催化反应有较强的反应活性。
根据文献报道[30, 31],在 150 ℃ 的脱附温度下,吡啶分子只跟FER分子筛的孔口酸性位相结合,而物理吸附的结果也表明,Z-35AHFS(0.1)和Z-35AHFS(0.2)样品的孔径都比未改性原粉的大,也就意味着改性后样品的酸性位点对吡啶表现出了更好的可接近性,所以Z-35AHFS(0.1)和Z-35AHFS(0.2)在1545和1490 cm−1的峰面积所代表的酸量都要比未改性原粉的大。
2.2.3 异丁烯异构化反应评价
前文已经提到,异丁烯在HZSM-35分子筛上的催化转化反应产物较为复杂,除主要组分异丁烯、正丁烯、顺-2-丁烯和反-2-丁烯以外,还有齐聚反应、裂解反应和氢转移等副反应生成的丙烯等烯烃和丁烷等烷烃以及碳数更高的液体产物。本研究采用采用安捷伦公司生产的Agilent Clars500气相色谱仪在HP-AL/S色谱柱上进行全组分定性和定量分析。并用公式(1)−(6)计算相关量。
从图10的反应评价可以看出,经脱铝剂处理后,改性分子筛催化剂上异丁烯转化率和正丁烯选择性均低于未改性分子筛催化剂。对比反应25 h后的数据,异丁烯转化率从53.80%下降到50.25%,正丁烯选择性从62.88%下降到58.95%。转化率的下降主要是因为脱铝处理后,中强Brønsted酸中心减少,而中强Brønsted酸中心又是发生异构化等反应的主要场所[32],所以改性后的分子筛转化率都比未改性分子筛的转化率低。此外还发现,对于两种不同AHFS浓度的改性样品来说,Z-35AHFS(0.1)脱铝产生的部分铝原子残留在分子筛的孔道内部形成了非骨架铝物种,即新的L酸中心,这对于异丁烯的转化也有一定贡献,所以Z-35AHFS(0.1)的异丁烯转化率高于Z-35AHFS(0.2),正是由于新的L酸中心的出现,作者观察到Z-35AHFS(0.1)的失活速率要比其他两种催化剂更快。
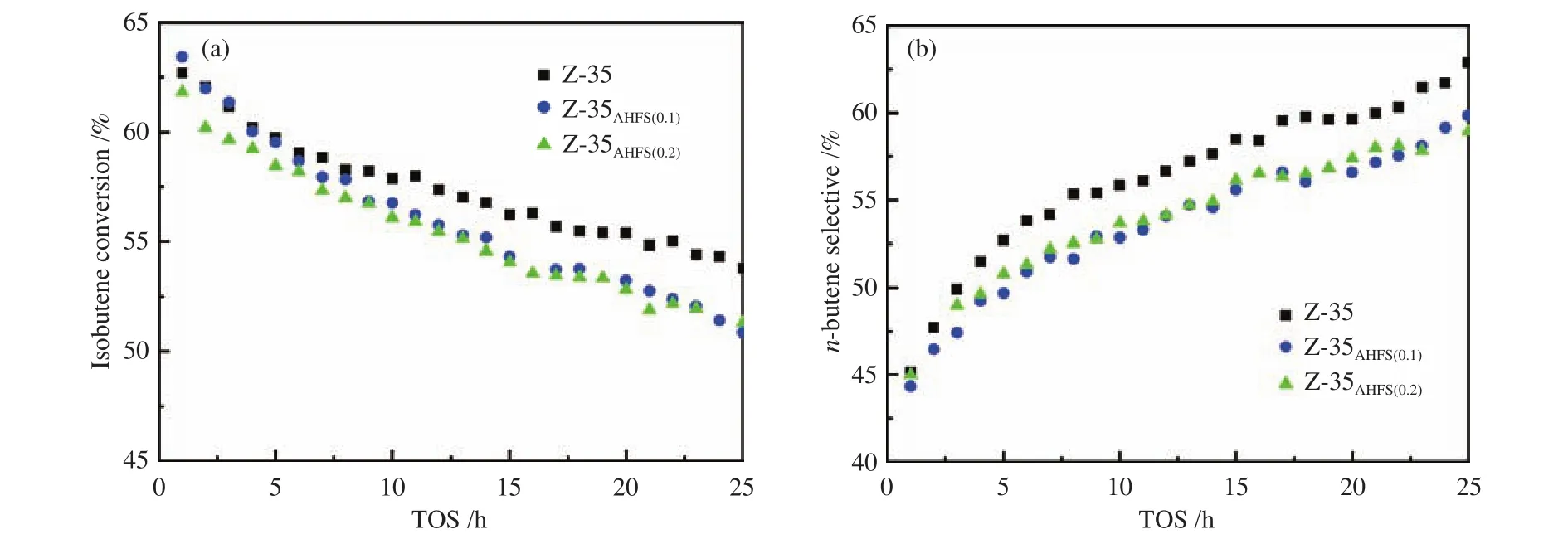
图10 HZSM-35以及不同浓度AHFS改性后样品异丁烯骨架异构化反应评价Figure 10 Evaluation of isomerization reaction of isobutene at parent and AHFS modified HZSM-35 zeolites(a): isobutene conversion; (b): n-butene selectivity reaction conditions: 350 ℃, 0.1 MPa, WHSV = 6 h−1
根据报道,在C4烯烃异构化领域,分子筛中的Brønsted酸和Lewis酸酸中心都可以催化骨架异构化过程[33],同样,本工作中Brønsted酸和Lewis酸酸中心都会促进异丁烯的转化。
异丁烯的催化转化路径是由分子筛的限域效应和酸中心附近微环境共同决定。宋丽娟团队[34 − 36]从理论和实验两个方面研究发现,非骨架铝物种(即Lewis酸中心)与邻近的硅铝桥羟基(即Brønsted酸中心)存在着协同作用,这种协同作用可以促进噻吩、烯烃等分子低聚反应的发生。同样,本工作中脱铝处理产生的非骨架铝物种作为一种新的Lewis酸,位于FER分子筛中Brønsted酸位置的附近,两者的协同作用促进了异丁烯齐聚-裂化反应的发生。
从三种催化剂的产物分布结果(图11)中可以看出,经脱铝剂处理后,异丁烯在HZSM-35分子筛上的催化转化产物种类并未发生改变,只是产物分布发生了变化。可以看到,在Z-35AHFS(0.1)催化剂上,产生的齐聚-裂化产物(C3 + C5)要比其余两种催化剂更多,氢转移产物(丁烷)更少,这是因为在Z-35AHFS(0.1)分子筛孔道内产生了两种强弱不同的L酸中心,更优先于催化齐聚-裂化反应的发生,这也是该分子筛的正丁烯选择性降低的原因。同时,这也解释了Z-35AHFS(0.1)样品的失活速率最快这一现象,图12的TG曲线也证实了在相同反应条件和反应时间下,曲线Z-35AHFS(0.1)积炭量最多。

图11 HZSM-35 以及不同浓度 AHFS 改性后样品催化异丁烯反应产物分布Figure 11 Product distribution of isomerization reaction of isobutene at parent and AHFS modified HZSM-35 zeolites
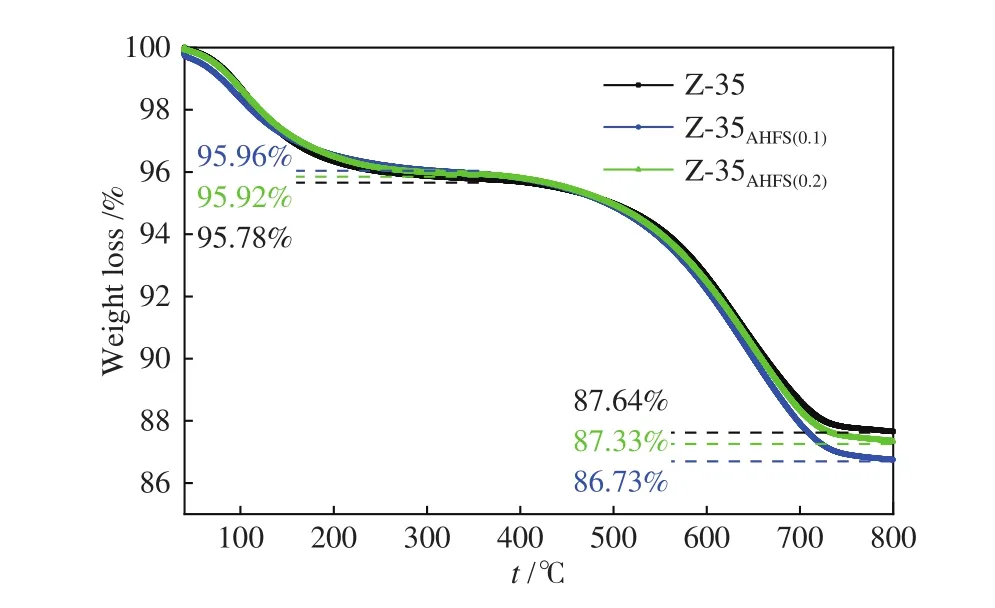
图12 HZSM-35 以及不同浓度 AHFS 改性后样品催化异丁烯反应25 h后的TG曲线Figure 12 TG diagram of the isobutene reaction at parent and AHFS modified HZSM-35 zeolites after 25 h
3 结 论
本研究探讨了不同温度下正丁烯和异丁烯分别作为反应物进行骨架异构化的反应评价结果及产物组成分布的差异,并结合热力学平衡数据分析C4烯烃在HZSM-35分子筛转化路径上的倾向性。结果表明,根据产物收率确定的两个反应的最佳温度都为350 ℃。而产物分布结果表明异丁烯作为反应物进行骨架异构化时,其副反应效应更强。采用表面脱铝处理的方式调控HZSM-35分子筛表面酸性质,辨析了改性前后分子筛样品酸类型,酸密度及可接近性等特征,并进一步结合反应评价结果探究分子筛不同酸性位对异丁烯骨架异构化反应的影响,结果表明,经低浓度的AHFS脱铝后的FER分子筛会形成两种强弱不同的新的Lewis酸中心,而经过产物分布的讨论发现新形成的Lewis酸中心对丁烯齐聚-裂化副反应是有利的,这也加速了异构化分子筛的失活。

