煤工尘肺合并晚期肺腺癌驱动基因突变与临床病理特征的关系
张建红,李 瑶,石金凤,温正军
(北京京煤集团总医院呼吸与危重症医学科,北京 102300)
煤工尘肺是我国最常见的职业病,随着病情的发展,症状会越来越严重,部分患者还会出现呼吸减弱、呼吸困难等症状。研究认为,煤工尘肺并发肺腺癌的风险更高,对患者的身心健康造成严重的影响,且煤工尘肺合并晚期肺腺癌患者临床症状容易被原发病掩盖,导致治疗难度增加[1]。目前,化疗是治疗煤工尘肺合并晚期肺腺癌主要手段之一,而其对患者的身体状况具有较高的要求,且经常伴有不良反应。分子靶向药物是在细胞分子水平上,针对已经明确的致癌位点,来设计相应的治疗药物,药物进入体内会特异性地选择致癌点来结合发生作用,使肿瘤细胞特异性死亡。近年来,研究发现分子靶向药物特异性高、不良反应小,对多种恶性肿瘤具有显著疗效[2]。本研究旨在探讨煤工尘肺合并晚期肺腺癌驱动基因突变,并分析其与临床病理特征的关系,为患者靶向治疗方案提供参照,报道如下。
1 资料与方法
1.1 一般资料 选择北京京煤集团总医院2014年1月至2020年1月救治的70例煤工尘肺合并晚期肺腺癌患者,并开展前瞻性研究。患者均为男性,年龄44~91岁,平均(71.43±10.89)岁;接尘时间4~35年,平均(20.87±7.40)年;无吸烟史9例,吸烟史61例;尘肺期别[3]:Ⅰ期15例,Ⅱ期50例,Ⅲ期5例;分化程度:低分化24例,中分化28例,高分化18例。纳入标准:年龄≥ 18岁者;既往经职业病鉴定机构诊断为煤工尘肺者;经病理确诊为原发性肺腺癌者;配合完善基因检测者。排除标准:临床资料不全者;合并心、肾等重要器官损伤者;中途退出者。本研究已经院内医学伦理委员会批准,且患者及家属均知情同意。
1.2 方法
1.2.1 组织DNA和RNA的提取 用刀片切取3张5 μm厚患者的石蜡包埋肺组织样本,放置1.5 mL EP管内,二甲苯脱蜡后,用甲醇固定包埋组织样本,并提取DNA与细胞总RNA,DNA和RNA分离后,用Nanodrop 2 000测定DNA和RNA的浓度。
1.2.2 蝎形探针扩增阻滞突变系统(ARMS)荧光定量PCR法 应用厦门艾德生物公司生产的测试试剂盒,依照试剂盒说明书操作。PCR反应条件:42 ℃ 5 min,1个循环为第一阶段;95 ℃ 25 s,64 ℃ 、72 ℃各 20 s,10 个循环为第二阶段;93 ℃ 25 s,60 ℃、72 ℃各 20 s,36 个循环为第三阶段。均于第三阶段60 ℃时提取FAM与HEX信号,执行PCR。
1.2.3 二代测序技术(NGS) 应用艾德生物公司的人类癌症多基因突变与检测试剂盒联合,依照试剂盒说明书操作。阳性判定值[4]:平均原始深度>10 000×,平均有效深度> 500×,突变比例不低于0.4%,突变绝对拷贝数不低于2,链平衡性介于0.1~10之间,同时满足以上条件时为阳性(基因突变);没有发生基因突变的为阴性。
1.3 观察指标 整理全部患者的病例资料,包括平均年龄、吸烟史、平均接尘时间、尘肺期别、分化程度等。①分析EGFR基因突变与临床、病理特征的关系。②分析KRAS基因突变与临床、病理特征的关系。③分析TP53基因突变与临床、病理特征的关系。
1.4 统计学分析 运用SPSS 22.0统计软件进行数据分析,计量资料以()表示,采用t检验;计数资料以[ 例(%)]表示,采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 EGFR基因突变与临床、病理特征的分析 70例患者中,EGFR基因突变率为11.43%(8/70)。阳性与阴性组患者平均年龄、接尘时间、尘肺级别、分化程度比较,差异均无统计学意义(均P>0.05);阳性组无吸烟的患者占比显著高于阴性组,吸烟的患者占比显著低于阴性组,差异有统计学意义(P<0.05),见表1。
2.2 KRAS基因突变与临床、病理特征的分析 KRAS基因突变率为21.43%(15/70)。阳性与阴性组患者平均年龄、吸烟、接尘时间、尘肺级别比较,差异均无统计学意义(均P>0.05);阳性组低分化程度的患者占比显著高于阴性组,差异有统计学意义(P<0.05),见表2。
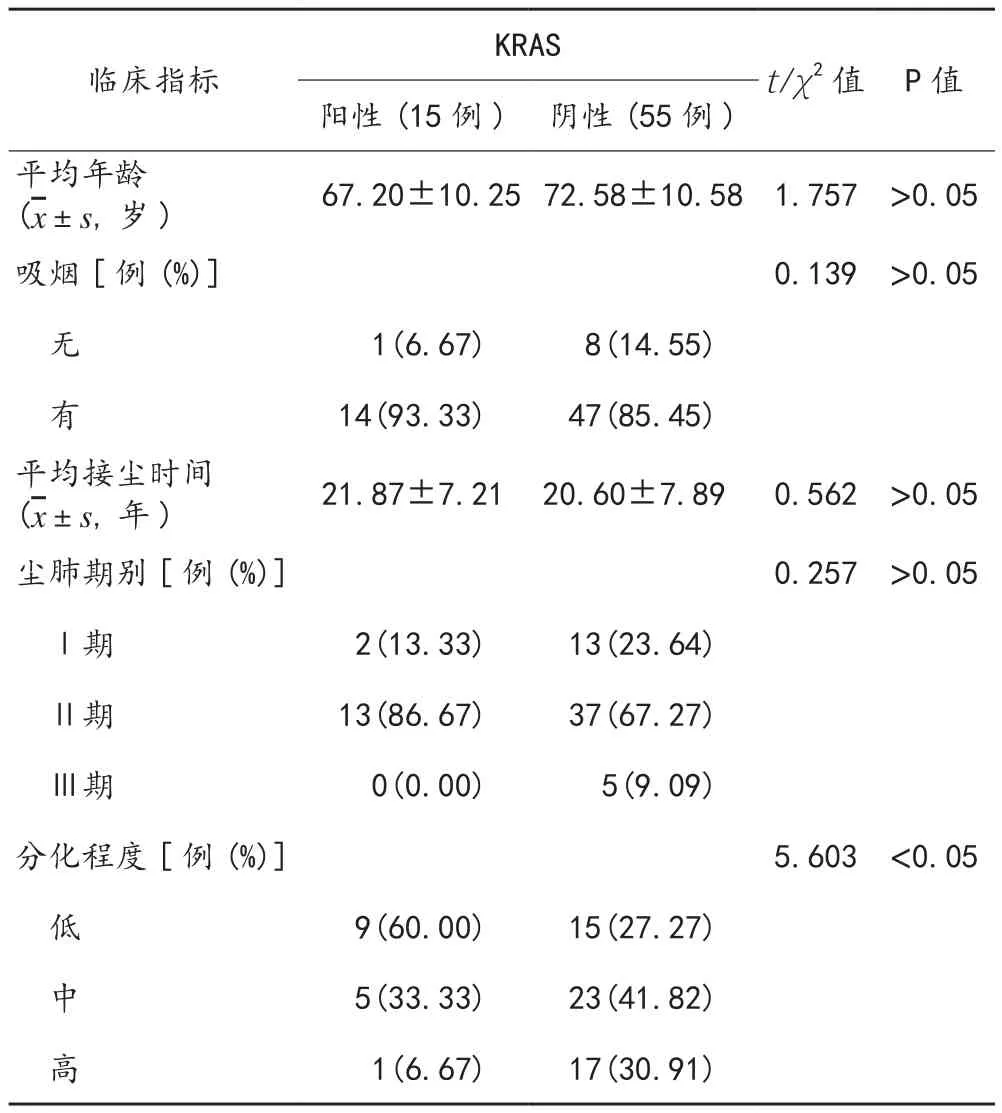
表2 KRAS基因突变与临床、病理特征的关系
2.3 TP53基因突变与临床、病理特征的分析 TP53基因突变率为48.57%(34/70)。阳性与阴性组患者平均年龄、吸烟、平均接尘时间、尘肺期别、分化程度比较,差异均无统计学意义(均P>0.05),见表3。

表3 TP53基因突变与临床、病理特征的关系
3 讨论
煤工尘肺是严重危害煤矿工人健康的一种职业病,容易与多种并发症同时发生,其中合并肺腺癌死亡率较高。近年来有报道,煤工尘肺患者合并肺腺癌的发生率明显高于普通人群,严重威胁患者生命健康与生活质量,化疗为其常用治疗方法,但临床效果欠佳。分子靶向药物利用肿瘤细胞与正常细胞之间分子生物学上的差异(包括基因、酶、信号转导等不同特性),抑制肿瘤细胞的生长增殖,最后使其死亡,相比于目前的化疗更加有效,不良反应少,属于一种更为安全的肿瘤治疗方法[5]。因此,探讨煤工尘肺合并晚期肺腺癌患者肺癌驱动基因突变与临床病理特征之间的关系,对后期临床治疗意义重大。
本研究发现EGFR基因突变的阳性率达11.43%,且主要集中在21外显子L858R、19外显子缺失。针对EGFR基因突变的靶向治疗是晚期肺腺癌最重要的治疗之一,只有EGFR基因突变的患者才能从靶向治疗中获益,因此,进一步证明了煤工尘肺合并晚期肺腺癌靶向治疗具有较高的难度[6]。本研究中煤工尘肺合并晚期肺腺癌患者EGFR 基因突变的阳性率较低,可能与尘肺病一定程度抑制EGFR的突变有关。本研究对驱动基因突变与临床病理特征的关系中发现,EGFR基因突变在平均年龄、尘肺级别、组织学类型、分化程度上,差异均无统计学意义,在吸烟上差异有统计学意义。有研究结果发现,EGFR基因突变与性别、吸烟情况存在显著相关关系,而与年龄无显著相关,且EGFR基因突变后的病理分析主要为腺泡型,其次为贴壁型[7]。还有研究人员进一步对EGFR基因突变的病例标本进行检测,EGFR不同位点的突变其病理类型也有不同,例如19外显子突变在乳头型中较高,其次为贴壁型;而21外显子突变为贴壁型中较高,其次为乳头型和实体型[8]。对于肺腺癌亚型与EGFR基因突变之间的关系在不同研究结果中并不一致,但是能肯定是EGFR基因的突变与病理类型之间仍存在一定联系。
KRAS基因突变多见于肺腺癌,鳞癌较少见,本研究中,KRAS基因突变率为21.43%,高于既往研究[9]报道。而KRAS基因突变在患者的分化程度上,差异有统计学意义,说明KRAS基因突变与低级别腺瘤向高级别腺瘤、癌变的多步骤演变过程相关。有研究报道,KRAS基因突变在男性患者中的突变率显著高于女性,在腺癌中的突变率显著高于非腺癌,在吸烟患者中的突变率显著高于不吸烟者,EGFR、KRAS突变与患者年龄、有无淋巴结转移无相关性[10]。这与本研究具有一定的差异,分析原因可能是基因的检测方法不同导致阳性率有偏差,而且阳性样本量普遍偏少致使结论不一。
TP53是一种抑癌基因,发生突变后,逐渐丧失对细胞生长、凋亡及 DNA 的修复能力,可由抑癌基因转变为促癌基因,影响患者的生存期,为常见突变,存在于近乎或者超过一半的非小细胞肺癌患者中,本研究结果显示,TP53基因突变率为48.57%,研究显示,TP53是目前已知人类肿瘤中突变率最高的基因,当TP53基因发生突变时,所表达的突变的P53蛋白丧失了正常功能[11]。丧失功能的P53蛋白会加速肿瘤的发生和进展,同时为肿瘤的侵袭及其转移创造条件。分析TP53患者基因突变情况与其临床病理特征结果对比,TP53突变在年龄、吸烟、接尘时间、尘肺级别、分化程度上,差异均无统计学意义。有研究报道,TP53突变与年龄具有显著性差异,而与性别、TNM分期、吸烟史、淋巴结转移、取材部位及肿瘤分化程度无显著相关性[12]。这与本研究结果类似,年龄具有一定差异的原因可能是该研究纳入样本量较少,与研究报道中的年龄选取存在一定差异性。
综上,煤工尘肺合并晚期肺腺癌患者肺癌驱动基因突变与临床病理特征之间的关系密切,吸烟和癌细胞分化程度与驱动基因阳性突变率有着密切联系。然而本研究的不足之处在于患者入组病例数量少,可能导致结论存在偏倚。

