高血压脑出血合并颈动脉瘤感染新型冠状病毒1例
栾涛 廉坤 王振 王帅颖 高永军 徐蔚 叶宝琴 张曙
新型冠状病毒肺炎(coronavirus disease 2019,COVID-19)疫情可能将在世界范围内长时间流行[1]。因此,总结早期救治经验对今后疫情防控有一定的参考价值。笔者报道2019年12月26日武汉市新洲区人民医院收治的1例高血压脑出血合并颈动脉瘤感染新型冠状病毒(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)患者的诊治经过,以期为临床诊治提供参考。
患者 女,69岁。2019年12月26日“因突发头昏头痛伴神志不清近2 h”入院。体格检查:体温36.8℃,脉搏77次/min,呼吸22次/min,血压191/107 mmHg;双侧瞳孔等大,直径约3 mm,光反射灵敏;格拉斯哥昏迷指数(Glasgow coma scale,GCS)9分(E2V3M4),口角左歪,吐字不清;左侧肢体偏瘫,肌力约0~1级,左侧病理征阳性;右侧肢体肌力、肌张力正常,右侧病理征未引出。急诊颅脑CT检查示:小脑出血破入脑室、脑室积血,见图1a;后急诊行“双侧脑室穿刺引流术”。术后第2天CT血管造影(CT angiography,CTA)检查示小脑积血,右侧颈内动脉海绵窦段动脉瘤;胸部CT检查示双肺正常,见图1b-c。与家属沟通后,动脉瘤暂不作处理,行左侧小脑开颅血肿清除术,术后患者病情平稳。当时预计患者需要较长时间(可能>2周)的人工气道和呼吸支持,12月30日行气管切开术。2020年1月6日拔除双侧引流管;1月9日患者意识逐渐清醒,GCS 15分,予以吡拉西坦注射液(4 g/次、1次/d)、银杏莫达注射液(20ml/次、1 次 /d)静脉滴注。在院康复治疗期间动态检查颅脑及胸部CT,见图2。

图1 2019年12月26日急诊颅脑CT检查及双侧脑室穿刺引流术后影像学检查所见(a:左侧小脑片状出血;b:右侧颈内动脉海绵窦段动脉瘤;c:双肺正常)
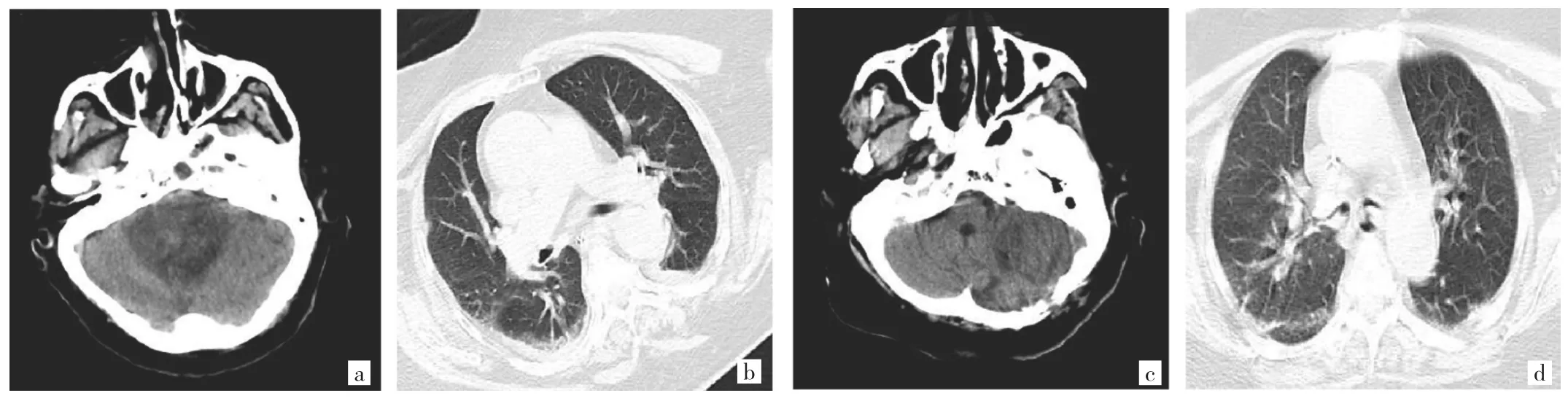
图2 患者院内康复期颅脑及胸部CT检查所见(a、b:1月6日小脑片状低密度软化灶,双肺正常;c、d:1月31日左侧小脑内血肿吸收良好,双肺纹理增多增粗,双下肺坠积性肺炎)
2月6日患者体温升高至38.4℃,嗜睡,GCS 14分(E3V5M6),复查 CT见四脑室扩大,右肺大面积感染,见图3a-b;根据痰培养予以左氧氟沙星(0.4 g/次、1次/d)静脉滴注;病毒核酸检测阴性。2月9日患者神志恍惚、躁动不安,GCS 12分(E3V4M5),心率较快、呼吸急促、全身紫绀,血氧饱和度60%,并发急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS),予以床边气管造瘘口插管,呼吸机正压给氧,血氧饱和度回升92%,复查CT见小脑软化灶吸收良好,双肺高密度影,重度感染,见图3c-d;病毒核酸检测阳性,确诊为COVID-19,加用洛匹那韦(400 mg/次,2 次 /d)、利巴韦林(0.4 g/次、4次 /d)、干扰素(600 U/次、2 次/d)、甲泼尼龙(40 mg/次、2次 /d)。2月10日转入ICU,患者浅昏迷,呼之不应,气管切开状态,双肺呼吸音粗,查血气分析:pH 7.45,PaCO231.8mmHg,PaO270mmHg。2 月11日患者浅昏迷,呼吸机辅助呼吸,呼吸模式间歇正压通气+呼气末正压通气5 cmH2O,氧浓度40%,支持压力16cmH2O,潮气量440 ml,复查CT见四脑室扩大,双肺感染面积较前扩大,见图3e-f;加用免疫球蛋白20 g抗感染。

图3 患者感染新型冠状病毒(SARS-CoV-2)前后颅脑及胸部CT检查所见[a、b:2月6日四脑室扩大,双肺肺纹理增多增粗、紊乱,散在斑片状模糊影,感染性病变,怀疑病毒性肺炎;c、d:2月9日小脑软化灶吸收良好,双肺大片磨玻璃样改变,结合病毒核酸检测结果确诊为新型冠状病毒肺炎(COVID-19);e、f:2月11日四脑室扩大,双肺弥漫性磨玻璃密度影,气管插管术后,上腔静脉见条形高密度影]
2月12至14日维持前期治疗方案。2月15日患者持续发热,加用抗生素头孢哌酮钠舒巴坦钠3 g,每6 h静脉滴注1次。2月16日脑钠肽(brain natriuretic peptide,BNP)8 552 ng/L,静脉推注呋塞米20 mg,减少液体摄入量。2月17日血氧饱和度95%,给予多巴胺8 mg/min静脉泵入,血压在102/65 mmHg左右。复查血气分析:pH 7.35,PaCO238.7 mmHg,PaO2112 mmHg,乳酸0.5 mmol/L;复查BNP 948 ng/L。2月18日给予多巴胺8 mg/min静脉泵入,血压在107/63mmHg左右,血氧饱和度95%,PO2152 mmHg,下调呼吸机氧浓度,为行快速容量复苏,行股静脉穿刺置管术。2月19日突发血压下降至70/43 mmHg,血氧饱和度下降至66%,抢救未成功死亡。
讨论 患者自2019年12月26日入院,急诊行双侧脑室穿刺引流术,术后第2天CTA检查见小脑积血,并查出有颈内动脉瘤,考虑患者年龄较大,其动脉瘤暂不作处理,行小脑血肿清除术,术后体征平稳,预计患者需要长时间(可能>2周)的人工气道与呼吸支持,遂行气管切开术[2],后在院康复治疗。2020年2月6日,患者出现呼吸困难,血氧饱和度不断下降,根据影像学表现,怀疑感染SARS-CoV-2,但病毒核酸检测阴性,暂不能确诊。2月9日,患者出现ARDS,且双肺大面积感染,病毒核酸检测阳性,确诊为COVID-19。根据《COVID-19诊疗方案(试行第六版)》:呼吸道飞沫和密切接触传播是SARSCoV-2的传播途径。在相对封闭的环境中,长时间暴露于高浓度气溶胶情况下存在经气溶胶传播的可能。考虑患者切开的气道暴露于空气中,可能是感染SARS-CoV-2的具体原因[3]。
病毒核酸检测是目前确诊COVID-19的“金标准”。但根据报道,一些临床高度疑似感染SARS-CoV-2的患者,核酸检测阳性率并不高,为30%~50%[4]。本例患者5次病毒核酸检测中有2次阴性,可能原因如下:(1)第1次阴性的检测时间为2月6日,而COVID-19患者IgM抗体一般在1周时出现峰值[5],故可能出现假阴性;(2)第2次阴性的检测时间为2月15日,自2月9日确诊COVID-19后,开始使用利巴韦林、洛匹那韦等抗病毒药物,可能使患者体内病毒量低于检测下限,从而造成假阴性[6]。
细胞因子风暴(cytokine storm,CSS)是决定肺外多器官功能衰竭的关键因素[7],血管紧张素转化酶2是介导SARS-CoV-2激活人体免疫系统产生CSS的关键环节。发生CSS后,患者淋巴细胞计数、氧合指数下降,乳酸脱氢酶、D-二聚体水平升高[8]。患者在2019年12月27日至2020年2月6日期间实验室检查结果趋于稳定,2月17至19日(死亡前3 d)多项实验室指标异常,肺部CT检查可见大片白色实变影,这些是CSS的具体表现[9]。糖皮质激素应用于病毒性肺炎的作用机制是通过降低炎症细胞因子来减轻对组织的损伤作用,即减轻肺的渗出、损伤和后期的肺纤维化[10]。本例患者在2月9至15日使用甲泼尼龙40 mg/次、2次/d;2月16日停用后,多项实验室指标出现大范围波动,病情继续恶化。目前尚无任何可靠证据证实某种药物对COVID-19有效[11],当前治疗核心仍是对症支持治疗,同时谨慎使用糖皮质激素。有研究报道冠状病毒累及神经系统[12-13]。患者自2月6日意识逐渐减弱、体温升高、脑室扩张,表现为中枢神经系统感染,给予左氧氟沙星治疗7 d未见疗效,后加用头孢哌酮钠舒巴坦钠也无明显好转。相关共识指出,对于中枢神经系统感染,治疗药物应选择易透过血脑屏障的抗生素,以静脉给药途径为主,治疗原则以最大药物剂量与长疗程治疗为主;对于静脉给药48~72 h效果不明显、病情严重者,可行脑室注射或腰椎穿刺鞘内注射给药[14-15]。本例患者若行腰椎穿刺,对脑脊液进行培养,再加用抗生素鞘内注射治疗中枢神经系统感染,可能会有积极效果。
综上所述,本例患者住院康复期间感染COVID-19,可能与院内流动人群传播有关。该患者感染SARS-CoV-2后病情迅速加重,呼吸功能逐渐减弱,实验室指标出现异常,但无颈动脉瘤破裂症状,死亡原因可能是CCS。笔者认为,若患者实验室指标出现紊乱,应注意CCS的发生,合理给予糖皮质激素;若COVID-19患者出现昏迷与神经反应性降低,应考虑中枢神经系统感染,积极给予相应治疗。

