SnO2/石墨分级纳米异质结构的合成及其电化学性能研究
栾照金,闫共芹,谈尚华
(广西科技大学机械与汽车工程学院,柳州 545616)
0 引 言
锂离子电池自问世以来,因具有环保、安全、高能量密度等优势,在移动通信设备、便携式设备以及新能源汽车等领域得到广泛的应用[1-3]。传统的锂离子电池负极材料是石墨,其理论容量较低,仅为372 mAh/g,因此寻找可替代石墨的高容量负极材料是材料学家们一直努力的方向。
近年来,各种金属氧化物(如Fe3O4、Co3O4、SnO2等)及其复合材料因具有较高的理论容量,可以用作锂离子电池负极材料[4-6]。其中,SnO2具有较低的合成成本和较高的理论容量(约780 mAh/g),因而备受科研人员的关注,被认为在锂离子电池领域具有广阔的应用前景,从而成为替代商业石墨的一种潜在负极材料。然而,SnO2负极材料在锂离子电池充放电过程中体积膨胀明显并且有严重的颗粒团聚,从而会导致较大的不可逆容量损失和较差的循环稳定性。为了解决以上难题,人们制备了具有不同形貌结构的SnO2纳米材料并将其与碳质材料复合,以提升其用作负极材料时锂离子电池性能。Zhou等[7]制备了一种一维空心核壳结构SnO2/C复合纤维,研究发现,由于复合材料独特的中空核-壳结构提供了足够的空隙,减轻了充放电循环过程中SnO2纳米粒子的体积变化,从而使得SnO2/C复合纤维具有优异的电化学性能。Yang等[8]制备了一种板栗状的SnO2/C复合材料,研究发现,由于具有有限的体积膨胀和出色的机械强度,一定程度增强了以其作为负极材料时锂离子电池的循环性能。Wang等[9]采用水热法合成了碳包覆介孔SnO2纳米球的核壳型SnO2/C纳米复合材料,研究发现,复合材料在经历100圈循环后放电比容量可维持在390 mAh/g左右,高于商用石墨(372 mAh/g)的理论值,拥有较好的循环性能。Ding等[10]合成了CNF/SnO2@C薄膜,该复合材料表现出优异锂储存性能,在0.05 A/g的电流密度下放电比容量为1 286 mAh/g。因此,制备不同形貌结构的SnO2/碳纳米复合材料可显著提升锂离子电池负极材料的储电性能和循环性能。
本文采用简单可控的一步水热法制备了SnO2/石墨分级纳米异质结构,研究了SnO2/石墨分级纳米异质结构作为锂离子电池负极的电化学性能。结果表明,充分利用石墨的良好导电性以及SnO2的高理论比容量等优点,发挥两者的优势协同作用,使得纳米异质结构作为锂离子电池负极材料表现出较高的储电容量和改善的循环稳定性。
1 实 验
1.1 实验原料
石墨碳粉,分析纯,上海华园化工有限公司;五水合四氯化锡(SnCl4·5H2O),分析纯,天津科密欧化学试剂有限公司;氢氧化钠(NaOH),分析纯,西陇化工股份有限公司;无水乙醇(C2H5OH),分析纯,国药集团化学试剂有限公司;导电炭黑,东莞市多普塑胶原料有限公司;聚偏氟乙烯(PVDF),东莞市多普塑胶原料有限公司;N-甲基-2-吡咯烷酮(NMP),上海五联化工厂有限公司;实验用水为实验室自制超纯水。
1.2 纳米复合异质结构的制备
将0.12 g石墨碳粉加入40 mL超纯水中,超声分散2 h,得到石墨悬浮液。然后,在石墨悬浮液中依次加入1.052 g(3 mmol)SnCl4·5H2O和1.40 g(35 mmol)NaOH。继续超声2 h后,将混合物移入80 mL聚四氟乙烯内衬的高压反应釜中,并在200 ℃下反应18 h。反应结束后自然冷却至室温,分离得到固体产物,并用去离子水和无水乙醇清洗多次,然后在65 ℃下干燥10 h,获得SnO2/石墨分级纳米异质结构。作为对照,采用类似的合成方法但不添加石墨,可获得单一的SnO2分级纳米异质结构。
1.3 形貌与成分表征
采用场发射扫描电子显微镜(德国蔡司公司,型号 SIGMA,扫描电压 10 kV)表征合成样品的形貌,并采用其附加的能量色散X射线谱仪(EDS)分析合成材料的元素构成;采用X射线衍射分析仪(丹东浩元仪器有限公司,Cu靶Kα射线,测试电压为40 kV,电流40 mA,扫描角度范围:10°~90°)分析合成样品的结构。采用XploRA INV 多功能拉曼及成像光谱仪(HORIBA 科技公司,波长:532 nm,测试范围:250~3 000 cm-1)测试合成样品的拉曼光谱。采用比表面与孔隙度分析仪(美国麦克仪器,型号ASAP 2020 Plus)测试合成样品的氮吸附-脱附等温曲线和孔径分布。
1.4 电化学性能测试
将上述制备的纳米材料(石墨、SnO2、SnO2/石墨分级纳米异质结构)、导电炭黑、PVDF按质量比7∶2∶1混合并与N-甲基-2-吡咯烷酮(NMP)混合制成浆料,均匀涂覆在铜箔上,在60 ℃干燥12 h后裁成圆片,即可得到锂离子电池负极。以锂片作为对电极,聚丙烯微孔膜为隔膜,浓度为1 mol/L的 LiPF6/EC+DMC溶液作为电解液,在手套箱中组装成纽扣电池。在室温下,通过高精度电池性能测试仪(型号:武汉蓝电CT2001/3001A)在不同电流密度(50 mA/g、100 mA/g、500 mA/g)和电压范围(0~3.0 V)下进行恒流充放电,测试电池的储电性能和循环性能。采用电化学工作站(型号:瑞士万通Metrohm Autolab 204)采集锂离子电池的循环伏安(CV)曲线和电化学阻抗谱(EIS),采集电压范围为0.005~3.0 V,扫描速度为0.5 mV/s,采集频率是0.01 Hz~100 kHz。
2 结果与讨论
2.1 成分与形貌分析
图1为纯石墨、通过上述实验获得的单一SnO2和SnO2/石墨分级纳米异质结构的X射线衍射图谱。其中图1(a)图谱在2θ=26.5°处的衍射峰对应于石墨的(002)晶面,图1(b)图谱在2θ=26.50°、33.90°、51.75°处存在尖锐的衍射峰,根据标准图谱(JCPDS:41-1445),这些衍射峰对应于四方金红石型SnO2的(110)、(101)、(211)晶面,这说明通过上述水热法在未添加石墨的情况下合成了四方金红石型SnO2。图1(c)图谱同样在2θ=26.50°、33.90°、51.75°处存在尖锐的衍射峰,但与图1(b)相比发现2θ=26.50°处的衍射峰明显增强。由于纯石墨(002)晶面的衍射峰与单一SnO2(110)晶面都在2θ=26.50°处,因此该处衍射峰为SnO2(110)晶面与石墨(002)晶面衍射峰的重叠,这说明成功合成了SnO2/石墨异质结构。同时,X射线衍射结果显示所有衍射峰均为尖锐的峰,且除了SnO2和石墨的特征衍射峰之外,未出现其他特征衍射峰,表明水热法合成的SnO2和SnO2/石墨异质结构具有良好的结晶度和纯度。

图1 石墨(a)、SnO2(b)、SnO2/石墨分级纳米异质 结构(c)的XRD图谱Fig.1 XRD patterns of graphite (a), SnO2 (b), SnO2/ graphite hierarchical nano-heterostructure (c)
为了进一步证明SnO2/石墨分级纳米异质结构的生成,测试了SnO2/石墨分级纳米异质结构的拉曼光谱,如图2所示。SnO2/石墨分级纳米异质结构在630 cm-1、1 352 cm-1、1 580 cm-1、2 700 cm-1等位置附近有特征峰,其中630 cm-1附近的峰为Sn-O键的伸缩振动峰,证明了异质结构中SnO2的存在[11]。此外,异质结构在1 352 cm-1、1 580 cm-1、2 700 cm-1位置出现三个特征峰,分别对应于石墨的D峰、G峰和2D峰[12],表明异质结构中石墨的存在。其中,在1 352 cm-1附近石墨D峰强度很弱,表明石墨边缘缺陷很少,整体质量较高;在1 580 cm-1附近出现的石墨G峰表明形成了碳sp2杂化键[13-14]。

图2 SnO2(a)、石墨(b)、SnO2/石墨分级纳米异质 结构(c)的拉曼光谱Fig.2 Raman spectra of SnO2 (a), graphite (b), SnO2/ graphite hierarchical nano-heterostructure (c)
通过场发射扫描电子显微镜(FESEM)表征了SnO2/石墨分级纳米异质结构的形貌,如图3所示。由图3(a、b)可知,直径约为450 nm的花状SnO2分级结构均匀地分布在石墨片上。通过高倍图片可知,结晶度良好的SnO2纳米线组装成截面为正方形的SnO2纳米棒,如图3(c、d)所示,纳米棒的截面尺寸约为100 nm,长度为200~300 nm,SnO2纳米棒进一步组装成花状结构(见图3(e、f)),并生长在石墨片上,呈现分级结构。

图3 SnO2/石墨分级纳米异质结构的场发射扫描电镜图。低倍率(a)、(b);高倍率(c)~(f)Fig.3 FESEM images of SnO2/graphite hierarchical nano-heterostructures. (a), (b) Low-magnification; (c)~(f) high-magnification
为了研究纳米异质结构的元素组成,通过FESEM附有的能量色散X射线光谱仪(EDS)对图4(a)选取部分区域进行了能谱测试,如图4所示。图4(b)能谱图显示了复合材料主要有Sn、O、C元素组成,Sn、O元素的同时存在证实了SnO2的成功合成。图4(c)所示为图4(a)的EDS面扫描结果,结果表明Sn、O、C较均匀地分布其中。结合XRD、FESEM、Raman分析,结果表明成功合成了SnO2/石墨分级纳米异质结构,SnO2均匀地生长在石墨上。

图4 SnO2/石墨分级纳米异质结构的FESEM图(a)和EDS能谱图(b)、(c)Fig.4 FESEM images (a) and EDS spectra (b), (c) of SnO2/graphite hierarchical nano-heterostructure
通过氮气吸/脱附方法对SnO2、SnO2/石墨分级纳米异质结构进行了孔结构及比表面积的测定与分析。如图5所示,SnO2、SnO2/石墨分级纳米异质结构的氮气吸/脱附等温线都属于Ⅳ型曲线(依据IUPAC分类)[15],而且存在典型的H1型滞后线,同时进一步证实了本文中合成的SnO2、SnO2/石墨分级纳米异质结构属于介孔纳米材料。如图5插图所示,SnO2/石墨分级纳米异质结构孔隙尺寸集中分布在2.49 nm附近,而单一SnO2的孔隙尺寸集中分布在3.773 nm附近。对测试数据分析计算,SnO2/石墨分级纳米异质结构的比表面积约为18.323 47 m2/g,比单一的花状SnO2(8.366 5 m2/g)大得多,说明石墨与花状SnO2的复合在一定程度上提高了其比表面积,这导致SnO2/石墨分级纳米异质结构的电化学反应活性位点增加,进一步提高锂离子电池的储锂性能。

图5 SnO2(a)、SnO2/石墨分级纳米异质结构(b)的氮气吸/脱附等温曲线及孔径分布(插图)Fig.5 N2 adsorption/desorption isotherms and pore-size distribution curves(in chart) of SnO2 (a), SnO2/graphite hierarchical nano-heterostructures (b)
2.2 电化学性能研究
为了探究合成的SnO2/石墨分级纳米异质结构是否具有改善的电化学性能,对单一SnO2、石墨和SnO2/石墨分级纳米异质结构进行相应的充放电循环测试,如图6所示。图6(c)为在0.01~3.0 V电压范围和50 mA/g电流密度下,SnO2/石墨分级纳米异质结构的第一次、第二次和第十次循环时的恒流充放电曲线。从图6(c)可知,SnO2/石墨分级纳米异质结构的首次放电比容量和充电比容量分别为1 567.2 mAh/g、825.9 mAh/g,明显高于石墨(首次放电和首次充电比容量分别为382.1 mAh/g、366.3 mAh/g,见图6(a)),相应的库仑效率为52.699%。同时可以发现,在首次放电过程中,SnO2/石墨分级纳米异质结构在0.65 V、1.0 V附近具有一个电压平台,这主要与Li2O和单质Sn的生成有关[16-17](如反应式:SnO2+Li++4e-→2Li2O+Sn)。由于循环过程中存在不可逆反应,SnO2首圈放电过程中在0.65 V附近出现的微弱电压平台随着循环的增加而消失。此外还可以发现,在充电过程中,SnO2、SnO2/石墨分级纳米异质结构分别在0.4 V、0.2 V附近出现了一个短暂的电压平台,如图6(b)、(c)所示,这主要归因于LixSn的去合金化和 LiC6的脱嵌过程。另外,首次循环过程中存在较大的容量损失,这主要是因为有固体电解质SEI膜的形成[18]。从第二次循环开始,库仑效率明显提高(>90%)。经过10次循环后,SnO2/石墨分级纳米异质结构仍具有 754.6 mAh/g 的可逆放电比容量,远高于单一SnO2(523.9 mAh/g,见图6(b))和石墨(335 mAh/g,见图6(a)),这主要得益于异质结构中二氧化锡和石墨之间的相互协同优势,二氧化锡保证了纳米复合结构的高比容量,石墨增强了纳米异质结构的电导率。
图6(d)为SnO2/石墨分级纳米异质结构、单一SnO2和石墨在不同的电流密度(50 mA/g、100 mA/g、500 mA/g、50 mA/g)下的倍率性能。由6(d)倍率性能图可知,与单一SnO2相比,SnO2/石墨分级纳米异质结构容量衰减率明显减小,具有更高的循环比容量,因而使异质结构同时具有二氧化锡理论容量高和石墨循环性好的优势。在电流密度为100 mA/g时经过10次循环后,SnO2/石墨分级纳米异质结构保持了508.5 mAh/g的可逆放电比容量,而此时单一SnO2和石墨的可逆放电比容量分别为259.5 mAh/g和284.9 mAh/g。在500 mA/g的电流密度下,SnO2/石墨分级纳米异质结构的放电比容量也远高于单一的二氧化锡。另外,经过不同的电流密度的40次循环之后回到初始电流密度50 mA/g时,SnO2/石墨分级纳米复合结构仍可获得689.5 mAh/g的可逆放电比容量。这说明SnO2分级纳米结构生长在石墨上形成纳米异质结构后能发挥SnO2和石墨的优势协同作用,从而明显改善了电化学性能,显示出良好的倍率性能。

图6 石墨(a)、SnO2(b)、SnO2/石墨分级纳米异质结构(c)在50 mA/g下的充放电曲线;(d)不同电流密度下的倍率性能; (e)100 mA/g下的循环性能Fig.6 Charge and discharge curves of graphite (a), SnO2 (b), SnO2/graphite hierarchical nano-heterostructure (c) at 50 mA/g; (d) rate performance at different current densities; (e) cyclic performance at 100 mA/g
图6(e)为SnO2/石墨分级纳米异质结构、单一SnO2和石墨在100 mA/g电流密度下的循环性能。相比较而言,单一SnO2作为锂离子电池负极材料尽管具有高的首次放电比容量(1 495.8 mAh/g),但随着循环次数的增加容量衰减严重,经过45圈循环后,放电比容量仅有290.9 mAh/g,明显低于商业石墨的理论容量,展现出了较差的循环性能,这主要因为SnO2在连续的充放电循环过程中体积膨胀严重(约300%),进而影响了其循环性能。而SnO2/石墨分级纳米异质结构经过40圈循环以后获得455.3 mAh/g的放电比容量,远高于单一SnO2(332.9 mAh/g)和石墨(316.9 mAh/g),同时经过120圈循环以后SnO2/石墨纳米异质结构的放电比容量稳定在450 mAh/g左右,容量衰减率变得很低。相比单一的SnO2、石墨,SnO2/石墨分级纳米异质结构获得了改善的循环稳定性,这主得益于石墨(导电性好等)和SnO2(理论比容量高)充分发挥了两者的优势协同效应,引入石墨作为生长基底,可以对SnO2在充放电循环过程中的体积膨胀效应起到保护作用,实现了循环性能的改善,同时库仑效率稳定在99%左右。
在0.005~3.0 V的电压范围和0.5 mV/s的扫描速度下,通过循环伏安法测试了SnO2/石墨分级纳米异质结构的循环伏安曲线(测试前半电池已在小电流密度下充放电循环激活),获得第一、二、三次循环的伏安曲线,如图7所示。由伏安曲线可知石墨和SnO2在循环过程中发生的电化学反应。由于测试前已经激活半电池,所以在首次循环过程中并没有形成强的还原峰。阴极曲线中,在0.01 V和0.25 V位置附近出现还原峰,其中,0.01 V附近的峰主要是因为Li嵌入石墨形成LiC6导致的[16],而0.25 V附近的还原峰可归因于LixSn合金的形成[19]。阳极曲线中,在0.275 V和0.5 V附近分别出现氧化峰,分别可归因于LiC6的Li脱嵌和LixSn合金的Li脱嵌。除此之外,半电池从第二次开始每次循环的伏安曲线几乎重叠在一起,由此可见SnO2/石墨分级纳米异质结构具有良好的循环稳定性[20]。

图7 SnO2/石墨分级纳米异质结构的循环伏安曲线Fig.7 CV curves of SnO2/graphite hierarchical nano-heterostructure
为了进一步探究SnO2/石墨分级纳米异质结构的储锂性能,在0.005~3.0 V的电压范围和0.5 mV/s的扫描速度下,通过循环伏安法对石墨、SnO2、SnO2/石墨分级纳米异质结构的电化学性能进行测试以获得电化学交流阻抗谱曲线,如图8所示。其等效拟合电路如图8插图所示,其中Rs、Rct、Zw分别代表欧姆电阻、电荷传递电阻和扩散Warburg 阻抗。通常来说,交流阻抗谱的中高频扁平半圆的直径对应于电荷传递电阻[21],电阻越大电化学反应动力学性能越差。从图8中可以看出,SnO2/石墨分级纳米异质结构在中高频处的半圆直径介于石墨和SnO2之间,其电阻较小(约33 Ω),略大于石墨(30 Ω)但小于SnO2(40 Ω),从而使得复合材料具有较好的导电性,这进一步说明了SnO2/石墨分级纳米异质结构具有较好的电化学反应动力学性能,因此SnO2/石墨分级纳米异质结构与石墨、SnO2相比表现出更好的锂存储性能。
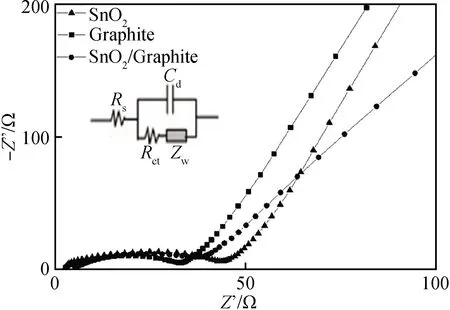
图8 石墨、SnO2、SnO2/石墨分级纳米异质结构的 电化学阻抗谱Fig.8 EIS spectra of graphite, SnO2, SnO2/graphite hierarchical nano-heterostructure
3 结 论
本文采用一步水热法合成了SnO2/石墨分级纳米异质结构,结晶度良好的SnO2纳米线组装成截面为正方形的纳米棒,纳米棒组装成直径约为450 nm的花状SnO2,并均匀地生长在石墨片上,呈现分级纳米结构。电化学测试结果表明,分级纳米异质结构首次放电/充电比容量为1 567.2 mAh/g、825.9 mAh/g。在不同的电流密度下循环40次之后仍可获得689.5 mAh/g的可逆放电比容量。SnO2/石墨分级纳米异质结构有良好的储锂容量、优异的倍率性能和改善的循环性能,得益于SnO2与石墨之间发生相互协同效应,主要原因分析如下:(1)纳米棒组装成花状SnO2导致纳米异质结构具有更大的比表面积,储锂反应位点增多,同时纳米棒可以缩短锂离子的扩散长度;(2)引入石墨作为生长基底,增强了纳米异质结构的导电性,减缓了SnO2严重的体积膨胀效应;(3)SnO2可以保证纳米异质结构更高的比容量。

