益肾化浊法联合洛汀新治疗贝伐珠单抗诱发老年晚期结直肠癌患者蛋白尿肾虚兼湿浊证的临床观察
孙怡婕,黄春锦,韩力,陈玺,张栩
1.复旦大学附属华东医院中医科,复旦大学中西医结合研究院老年医学研究所老年保健技术和传承研究室,上海200040;2.复旦大学附属华东医院普外科,上海200040;3.复旦大学附属华东医院肿瘤科,上海200040
我国结直肠癌发病率占全球的18.6%,结直肠死亡总例数占全球的20.1%,均居首位[1]。75 岁以上老年人的结直肠癌发病约为7.82 万/年,约占全球的18.08%;与全人群及55~74 岁年龄组相比,发病和死亡风险更高,发病率上升速度更快,双重负担尤为明显;且发病后5年生存率显著低于全人群[2]。由于本病患者大多在早期缺乏临床症状,确诊时常常已处于疾病晚期(超过75%),手术根治可能性低,5年生存率低于10%[3-4]。美国FDA 批准贝伐珠单抗联合常规化疗治疗晚期结直肠癌,但其蛋白尿的副作用常使治疗中断,影响抗肿瘤疗效。本研究用益肾化浊法联合洛汀新治疗老年晚期结直肠癌因贝伐珠单抗诱发蛋白尿之肾虚湿浊证,取得满意疗效,现报道如下。
1 资料与方法
1.1 一般资料 选择2019年1月-2021年1月在华东医院就诊的老年晚期结直肠癌因贝伐珠单抗诱发的蛋白尿肾虚湿浊证患者76 例,随机分为观察组(n=38)和对照组(n=38)。本研究中观察组脱落1 例,对照组脱落2 例。观察组37 例,其中男性24 例,女性13例;平均年龄为(72.2±6.0)岁;蛋白尿平均病程(2.08±1.86)周。对照组36 例,其中男性22 例,女性14 例;平均年龄为(71.7±5.3)岁;蛋白尿平均病程(1.87±1.64)周。2 组一般资料差异无统计学意义(>0.05),具可比性。见表1。本研究获得华东医院伦理学备案(临床研究伦理号:2019K001)。
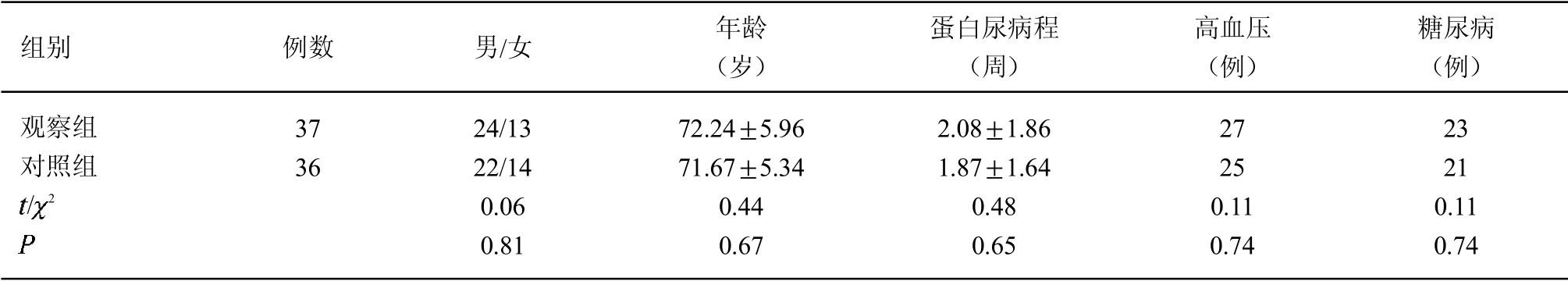
表1 2 组一般资料比较
1.2 诊断标准
1.2.1 西医诊断标准组织病理学或影像学确诊晚期结直肠癌[5],参考NCI-CTCAE Version 4.0 不良反应分级[6]制定贝伐珠单抗不良反应(蛋白尿)的诊断标准。
1.2.2 中医肾虚湿浊证诊断标准[7]主症:腰膝酸软,口中粘腻。次症:纳呆,脘腹胀满,疲倦乏力,浮肿,夜尿频多。舌脉:舌质淡或暗,舌苔腻,脉细或无力。以上主症2 项必备;次症≥2 项,结合舌脉象即可。
1.3 纳入与排除标准
1.3.1 纳入标准(1)符合西医晚期结直肠癌诊断,使用贝伐珠单抗静注出现蛋白尿(5 mg/kg,1 次/2 周),24 h 尿蛋白定量在0.15~2 g 之间;(2)符合中医肾虚湿浊症候诊断标准,主症2 项必备;次症≥2 项;(3)年龄60~85 岁;(4)预计生存期>6 个月,Karnofsky评分均≥60 分;(5)签署知情同意书。符合以上全部标准的患者纳入本研究。
1.3.2 排除标准(1)年龄<60 或>85 岁者;(2)因原发性肾脏病或继发于其他疾病导致蛋白尿的受试者;(3)合并全身其他系统严重原发性疾病者,其中肝酶(谷丙转氨酶或谷草转氨酶)超过正常范围2.5 倍以上,eGFR<60 mL·min-1·1.73 m-2者;(4)近3月使用可能影响尿蛋白代谢的其他药物者;(5)过敏者。具备以上任意1 项标准的病例不入组。
1.3.3 剔除和退出标准(1)依从性差,不配合者,未完成试验(包括脱落和失访);(2)试验开始后发现不符合纳入标准;(3)发生如血栓性微血管病等并发症不宜继续试验。
1.4 样本量估算[8]以尿蛋白作为指标,本课题组既往研究[9]显示24 h 尿蛋白定量 (标准差0.62),预设治疗后下调0.5 g。假设α=0.05,β=0.1,公式计算:n=(α,β) 为10.5,估算样本量n=32,考虑20%脱落,确定n=38,2 组按1∶1 比例分配,病例总数76 例。
1.5 治疗方法 对照组:ACEI 类药物,洛汀新(盐酸贝那普利片,北京诺华制药有限公司,国药准字H20000292),10 mg,1 片/d,口服。观察组:洛汀新同对照组;配合中药饮片(黄芪30g,鹿晗草15g,米仁根30g,蚕茧壳14 只,六月雪30g,玉米须15g)。2次/d,150 mL/d,水煎服。疗程:6 周为1 个疗程,参考减毒增效原则[7]制定。
1.6 观测指标及方法(1)靶向药物不良反应:24 h 尿蛋白定量。(2)中医证候积分量表评估:肾虚湿浊证。(3)一般情况及安全性指标:血尿粪常规、心电图、肝肾功能、血压。上述指标于治疗前后各检测1 次。(4)疗效判定标准参考减毒增效原则[7]及NCI-CTCAE Version 4.0 不良反应分级[6]。蛋白尿毒性分级标准详见表2;中医疗效积分标准详见表3;减毒疗效、临床疗效和中医疗效判定标准详见表4。疗效指数(n)=(疗前积分—疗后积分)/疗前积分×100%。

表2 毒性分级标准[6]

表3 中医症状积分标准[7](分)

表4 减毒疗效、临床疗效、中医疗效标准[7]
1.7 统计学分析 采用SPSS 21.0 进行统计学分析。以均数±标准差(±s)表示计量资料,经正态性检验与方差齐性检验后,正态分布且方差齐性的计量资料,2 组间比较行独立样本t 检验,组内比较用配对样本 检验;偏态分布的资料采取秩和检验。以例数和百分率表示计数资料,采用2检验<0.05表示数据差异有统计学意义。
2 结果
2.1 2 组减毒疗效比较 2 组治疗前尿蛋白分级差异无统计学意义(>0.05),具可比性。见表5。治疗后观察组尿蛋白减毒疗效优于对照组(<0.05)。见表6。
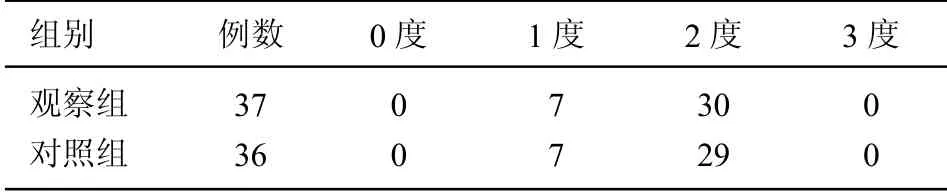
表5 治疗前2 组尿蛋白分级(例)

表6 2 组减毒疗效
2.2 2 组临床疗效比较 观察组总有效率89.19%,对照组75.00%,观察组临床疗效优于对照组(<0.01)。见表7。

表7 2 组临床疗效比较
2.3 2 组中医证候疗效比较治疗前2 组中医证候积分差异无统计学意义(>0.05)。治疗后2 组积分均较同组治疗前下降,观察组治疗前后差异有统计学意义(<0.01),对照组治疗前后差异无统计学意义(>0.05)。治疗后2 组治疗前后证候积分差值差异有统计学意义(<0.01)。见表8。

表8 2 组中医证候疗效比较
2.4 2 组肾功能和尿蛋白检测值比较 治疗前2 组尿蛋白定量、肌酐、尿素、eGFR 差异无统计学意义(>0.05),具可比性。治疗后2 组尿蛋白、肌酐、尿素均较治疗前下降、eGFR 较前升高;观察组蛋白尿、eGFR 治疗前后差异有统计学意义(<0.01);对照组尿蛋白差异有统计学意义(<0.05)。2 组治疗后尿蛋白差值、肌酐差值、eGFR 差值的差异有统计学差异(<0.05)。余差异无统计学意义(>0.05)。见表9。2.5 2 组血压比较治疗前2 组血压差异无统计学意义(>0.05)。治疗后2 组血压均较治疗前下降,差异均有统计学意义(<0.01)。2 组治疗后血压差值的差异无统计学意义(>0.05)。见表10。
表9 2 组24 h 尿蛋白定量、血肌酐、尿素氮和eGFR 检测值比较(±s)
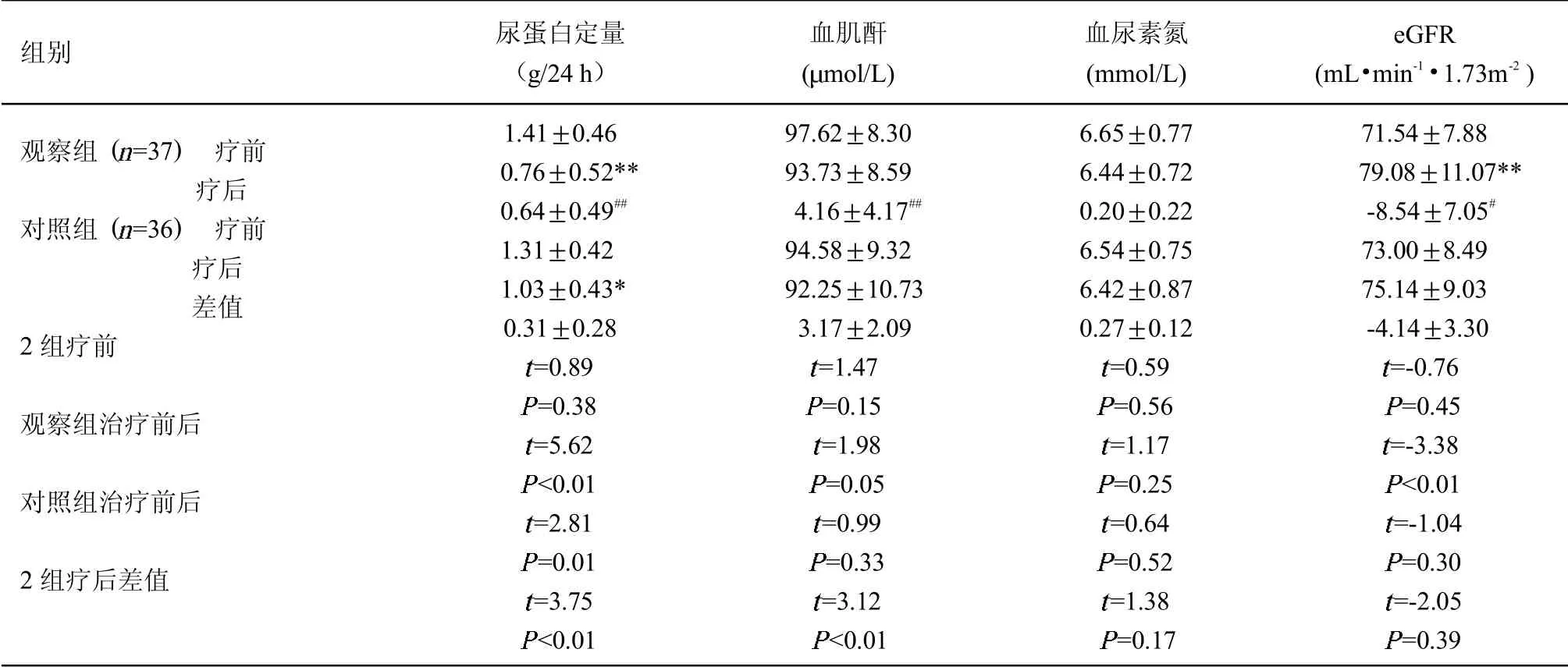
表9 2 组24 h 尿蛋白定量、血肌酐、尿素氮和eGFR 检测值比较(±s)
注:与同组治疗前比较,*<0.05,**<0.01;与对照组比较,#<0.05,##<0.01
组别尿蛋白定量(g/24 h)血肌酐( mol/L)血尿素氮(mmol/L)eGFR(mL·min-1·1.73m-2)观察组(n=37) 疗前疗后对照组(n=36) 疗前疗后差值2 组疗前观察组治疗前后对照组治疗前后2 组疗后差值1.41±0.46 0.76±0.52**0.64±0.49##1.31±0.42 1.03±0.43*0.31±0.28=0.89images/BZ_149_886_2159_909_2183.png=0.38=5.62images/BZ_149_886_2259_909_2283.png<0.01=2.81images/BZ_149_886_2359_909_2383.png=0.01=3.75images/BZ_149_886_2459_909_2483.png<0.01 97.62±8.30 93.73±8.59 4.16±4.17##94.58±9.32 92.25±10.73 3.17±2.09=1.47images/BZ_149_1251_2159_1274_2183.png=0.15=1.98images/BZ_149_1256_2259_1278_2283.png=0.05=0.99images/BZ_149_1256_2359_1278_2383.png=0.33=3.12images/BZ_149_1260_2459_1282_2483.png<0.01 6.65±0.77 6.44±0.72 0.20±0.22 6.54±0.75 6.42±0.87 0.27±0.12=0.59images/BZ_149_1625_2159_1647_2183.png=0.56=1.17images/BZ_149_1625_2259_1647_2283.png=0.25=0.64images/BZ_149_1625_2359_1647_2383.png=0.52=1.38images/BZ_149_1629_2459_1651_2483.png=0.17 71.54±7.88 79.08±11.07**-8.54±7.05#73.00±8.49 75.14±9.03-4.14±3.30=-0.76images/BZ_149_1994_2159_2016_2183.png=0.45=-3.38images/BZ_149_1994_2259_2016_2283.png<0.01=-1.04images/BZ_149_1994_2359_2016_2383.png=0.30=-2.05images/BZ_149_1994_2459_2016_2483.png=0.39
表10 2 组血压比较(±s,mmHg)

表10 2 组血压比较(±s,mmHg)
注:与同组治疗前比较,*<0.01
组别收缩压舒展压观察组(n=37)对照组(n=36)疗前疗后差值疗前疗后差值139.19±10.64 122.98±9.89*16.22±9.24 137.64±10.52 120.42±10.58*17.22±8.23 87.70±6.30 72.30±6.41*15.41±5.82 86.25±8.65 72.22±9.14*14.03±6.30
3 讨论
基于肿瘤细胞信号转导通路的研究,以血管内皮生长因子(vascular endothelial growth factor,VEGF)为靶点的单克隆抗体成为目前应用于晚期结直肠癌的靶向药物之一,贝伐珠单抗是其代表药物。作为与VEGF 结合的重组人源化单克隆抗体,通过特异性的结合VEGF-A,抑制其促进有丝分裂、增加内皮细胞血管通透性的活性,血管新生被抑制后,肿瘤生长所必须的血供、氧供受阻。化疗联合靶向药物治疗可以达到抗肿瘤、增加生存期的目标[10]。中国结直肠癌诊疗规范2017年版治疗晚期或复发转移性结直肠癌推荐对于一般状况较好患者建议考虑FOLFOXIRI+贝伐珠单抗的一线治疗[5],可延长总生存期及无进展生存期。我国老龄化加剧,老年甚至高龄的结直肠癌患者陡然增加,由于存在较多基础疾病,尤其是心血管及消化道疾病的伴发,这类人群是否具有相同的药物有效性需进一步验证,而药物安全性也需格外注意,应严格控制用药指征[11]。
贝伐珠单抗致蛋白尿是其常见的不良反应之一,发生率的报道不尽相同,约为21%~64%,与药物使用剂量、疗程、是否合并其他肾毒性药物、基础疾病(肾脏病)、肿瘤病理类型(晚期结直肠癌发生率约为23%~38%)、以及其他(包括种族、年龄、样本量)因素均有相关性[12]。其诱发蛋白尿的形成机制可能与其干扰VEGF 信号轴功能,下调足细胞连接蛋白表达,改变肾小球血流动力学、渗透压,从而破坏肾小球滤过屏障功能有关[13]。血管紧张素转化酶抑制剂或血管紧张素受体抑制剂是目前被推荐治疗此类蛋白尿的药物[14]。大多数研究显示其蛋白尿的损伤是可逆的,治疗前及治疗期间需要监测尿蛋白,当尿蛋白≥2g/24 h 时暂停治疗,待<1 g/24 h 再恢复用药,CTC-4 级蛋白尿应永久停用[15]。蛋白尿的产生对贝伐珠单抗的临床运用产生较大的限制,中断、延缓甚至阻止了肿瘤患者的抗血管生成治疗,降低了临床疗效。故而急需针对性的药物以预防、延缓与治疗蛋白尿。而中医学对治疗蛋白尿具有相当大的优势和特色。
对晚期结直肠癌患者而言,中医中药治疗具有不可或缺性,其能改善临床症状、提高生存质量、减毒增效、预防肿瘤的复发转移、延长生存期、增加生存率[16-17]。中医理论认为结直肠癌的发病机理是由于正气不足,脾胃运化失司,湿毒内生,久而化热,邪毒湿热蕴结,下注浸淫肠道,局部气血运行不畅,湿毒瘀滞凝结而成肿块[18]。而蛋白尿属于属中医“淋证、水肿”等范畴,我院名老中医经验认为其病机为正气衰败,湿热潴留,2 者均属于本虚标实之证。根据中医“异病同治”的治疗特点,结合我科多年的临床实践,应用益肾化浊法治疗由贝伐珠单抗诱发的老年晚期结直肠癌蛋白尿肾虚兼湿浊证。既往研究显示以黄芪、鹿晗草补益肺脾肾;六月雪、玉米须、米仁根利水除湿为主的中药方剂可通过降低血可溶性血管内皮细胞生长因子受体1 的水平,抑制其与循环中的VEGF结合,上调下游信号的活化,促进VEGF 生物学作用,改善肾小管血管内皮细胞功能,从而降低蛋白尿产生[9,19-21]。
研究结果表明观察组减毒疗效优于对照组,56.76%的观察组患者蛋白尿分级下降一度,其他患者蛋白尿分度均稳定,无恶化病例。观察组临床总有效率、中医证候疗效均显著优于对照组。蛋白尿降低幅度大于对照组,显著改善患者eGFR 水平,对肾功能无损害。
既往研究提示糖尿病、高血压患者接受贝伐珠单抗后蛋白尿的风险可能增加[13],而高血压本身也是贝伐珠单抗最常见的不良反应之一。治疗前,研究比较2 组患者基础疾病,在高血压、糖尿病的患病率上差异无统计学意义。而由于本次试验在样本量和设计方案上的局限性,期待后续的试验研究此两种基础疾病与蛋白尿的相对危险度
试验期间,2 组患者均无肝功能、心电图与血常规异常,未发现其他用药相关的不良反应。期间尚未发现动脉血栓栓塞、出血、伤口愈合并发症、胃肠道穿孔与白细胞减少等其他与贝伐珠单抗有关的不良反应,考虑可能与本次研究贝伐珠单抗非高剂量有关,而高剂量组发生VEGF 不良反应的风险更高[22]。
益肾化浊法联合洛汀新治疗因贝伐珠单抗诱发的老年晚期结直肠癌患者蛋白尿之肾虚兼湿浊证疗效佳,可能通过促进VEGF 生物学作用,修复肾小球内皮功能,减少蛋白尿,减轻靶向药物的不良反应,安全性高,可改善老年晚期结直肠癌患者的临床症状。

