内镜黏膜下剥离术与内镜下黏膜切除术治疗早期胃癌的效果及术后出血的影响因素分析
李静, 徐有青
胃癌是起源于胃黏膜上皮细胞的恶性肿瘤,当癌组织局限于胃黏膜层及黏膜下层,不论是否有淋巴转移,均为早期胃癌。目前,早期胃癌主要以手术治疗及内镜下治疗为主,5年生存率达90%~95%,且手术治疗对于病变局限于黏膜内的早期胃癌具有显著效果[1]。内镜下治疗早期胃癌具有手术并发症少、术后创伤小、患者恢复快等优点,已广泛应用于临床[2-3]。内镜黏膜下剥离术(ESD)与内镜下黏膜切除术(EMR)治疗早期胃癌均有较好的效果及安全性[4-5],但临床上如何选择这两种术式尚无统一共识。本研究通过比较ESD与EMR治疗早期胃癌的效果,分析术后出血的影响因素,以期为早期胃癌患者选取合适的术式,预防术后出血提供依据。
1 资料与方法
1.1 一般资料
选取2017年8月至2019年5月首都医科大学附属北京天坛医院收治的92例早期胃癌患者,纳入标准:①经病理检查确诊为早期胃癌,且有内镜切除术适应证;②手术前心电图检查正常;③患者临床资料完整,且能配合本研究。排除标准:①存在凝血功能异常;②无法耐受手术;③对手术涉及的药物存在过敏史;④术中肌层有损伤者。按治疗方法的不同,将本组92例患者分为ESD组(52例)与EMR组(40例)。两组患者一般资料比较差异无统计学意义(P>0.05,表1)。本研究得到患者及其家属的知情同意,均签署知情同意书。
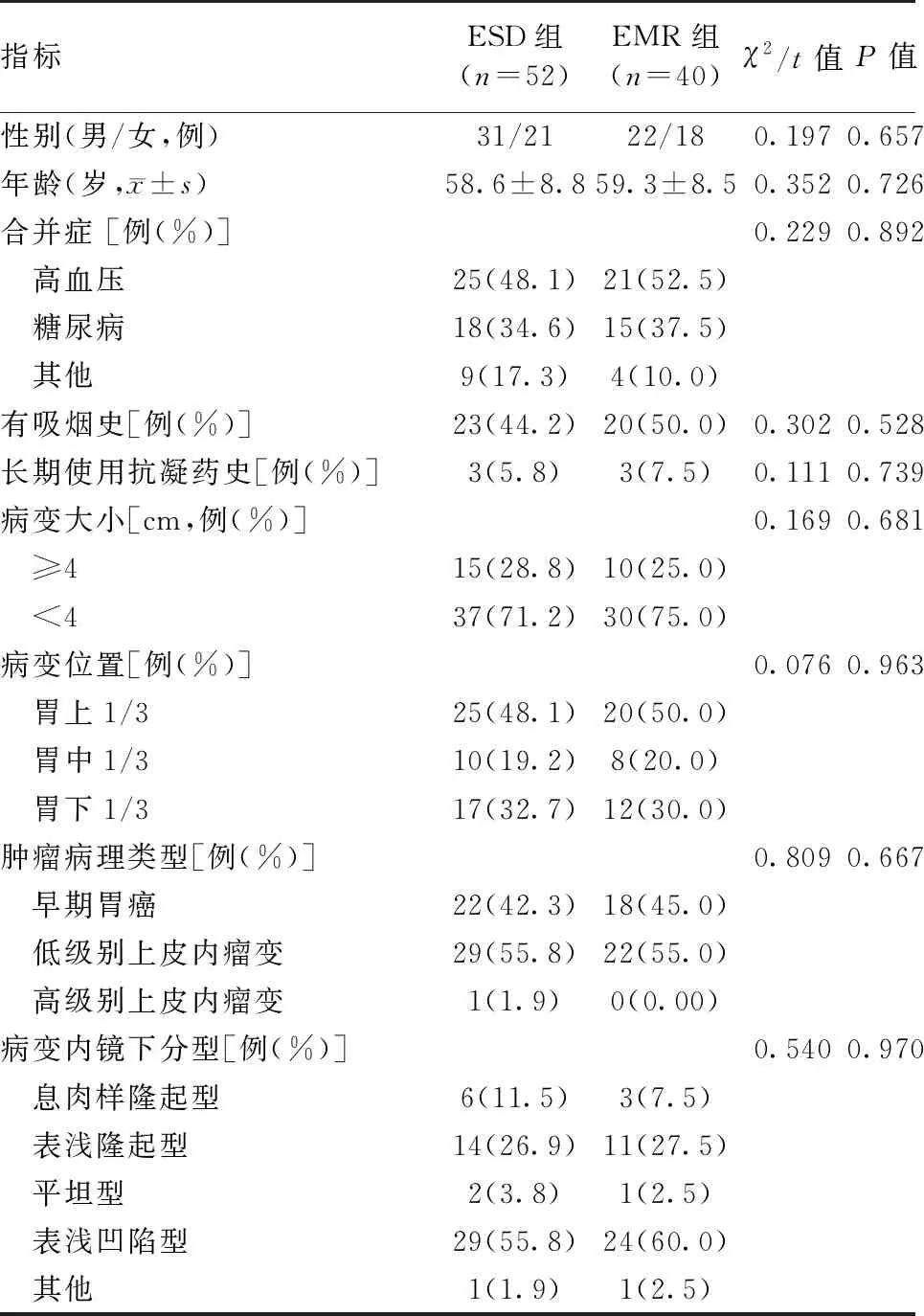
表1 内镜黏膜下剥离术组和内镜下黏膜切除术组患者一般资料比较
1.2 手术方法
1.2.1 ESD组 在病灶周围大约0.5 cm处进行电凝标记,每个标记点之间约间隔2 mm,在标记点周围黏膜下注射生理盐水、靛胭脂及肾上腺素混合物,充分显露黏膜,沿标记点用勾刀切开病灶边缘黏膜,选择末端绝缘手术刀(IT刀)剥离病变组织,对创面进行止血处理,将切下的标本进行病理组织学检查。
1.2.2 EMR组 行透明帽法:在病灶边缘黏膜下注入含有肾上腺素的生理盐水,使病灶充分显露,再将高频电凝圈置于透明帽,然后将透明帽套于内镜前端,利用负压将病灶黏膜吸入透明套内,用圈套器切割,再将无法一次性切除的病灶进行多次分割,创面止血后,将切除的标本进行病理组织学检查。
两组患者术后均禁止饮食,进行补液、抑酸及保护黏膜等处理,全程密切监测患者各项体征情况。
1.3 观察指标
①切除效果:包括完整切除率、治愈性切除率。完整切除即整块切除标本,病理学检查显示水平、垂直切缘均为阴性。治愈性切除指无或低淋巴转移风险的完整切除。②并发症情况:术后出血、术中穿孔等并发症。③手术时长及切除病灶直径。
1.4 术后出血的诊断标准
符合以下2项即可诊断为术后出血:①术后血红蛋白较术前降低幅度>20 g/L;②术后血压较术前下降超过20 mmHg或心率升高超过20次/min;③胃镜检查确定有术后出血;④患者术后出现头晕、黑便、呕血等情况。按此标准,本组92例患者中术后出血8例,未出血84例。
1.5 统计学方法

2 结果
2.1 ESD组与EMR组手术切除效果、手术时长、切除病灶直径及并发症发生情况比较
两组患者均顺利完成手术,ESD组的完整切除率及治愈性切除率均高于EMR组(P<0.05);ESD组的手术时长及切除病灶直径均大于EMR组(P<0.05);ESD组术后出血及术中穿孔发生率与EMR组差异无统计学意义(P>0.05)详见表2。出血患者采用经内镜下止血钳及氩气刀治疗均成功,穿孔患者经内镜下钛夹缝合治疗,术后禁食、抑酸、减压等保守治疗均成功。

表2 内镜黏膜下剥离术组与内镜下黏膜切除术组手术结果及并发症比较
2.2 术后出血组与未出血组的临床资料比较
两组临床资料比较详见表3。

表3 术后出血组与未出血组的临床资料比较 [例(%)]
两组患者性别、年龄、合并症、肿瘤病理类型、病变内镜下分型及切除病灶直径差异无统计学意义(P>0.05);与未出血组比较,出血组长期使用抗凝药史患者的比例高,病灶直径大,手术时间长、病灶位置为胃上1/3的比例高,差异有统计学意义(P<0.05)。
2.3 影响早期胃癌患者术后出血的多因素Logistic回归分析
以术后是否出血为因变量(无=0,有=1),以长期使用抗凝药物(无=0,有=1)、病灶直径(<4 cm=0,≥4 cm=1)、病灶位置(不是胃上1/3=0,胃上1/3=1)、手术时间(<90 min=0,≥90 min=1)为自变量进行多因素Logistic分析,结果显示:长期使用抗凝药物、病灶直径大、病灶位置为胃上1/3及手术时间长是影响早期胃癌患者术后出血的危险因素(P<0.05),见表4。
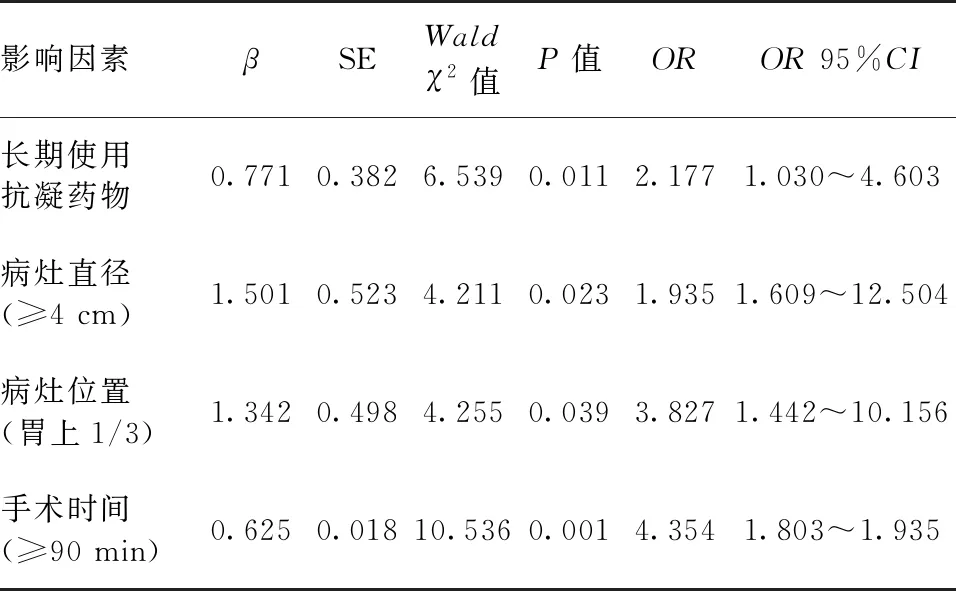
表4 多因素Logistic回归分析早期胃癌患者术后出血的影响因素
3 讨论
随着内镜技术的不断提升,早期胃癌的检出率逐渐增加,及时有效的治疗可延长患者的生存时间[6-7]。ESD是在EMR的基础上衍生的一种微创技术,虽然能提高整块切除率,减少疾病的复发概率,但比EMR更容易发生出血、穿孔等并发症[8-9]。本研究结果显示,ESD组的手术时间长于EMR组,但ESD组的完整切除率及治愈性切除率均高于EMR组,ESD可以完整切除范围较大的病灶组织,降低肿瘤的复发率,但由于手术操作过程较为复杂,术后并发症较多,其中最常见的是术后出血,影响了患者的后期恢复。采用ESD治疗的早期胃癌患者更易出现出血、穿孔等并发症,本研究中ESD组的术后出血率(9.6%)略高于EMR组(7.5%),与以往研究一致[10]。本研究结果还显示:长期使用抗凝药物、病灶直径大、病灶位置为胃上1/3及手术时间长是影响早期胃癌患者术后出血的危险因素。原因可能是术前长期使用抗凝药物导致患者的凝血功能发生改变,增加了患者术后出血的危险性[11];病变过大会导致剥离创面大,增加了术后出血的风险;胃上1/3的黏膜血管直径大于胃下1/3,致使出血的风险加大,且胃底部分的视野受限,增加了手术的难度及用时,易引起出血等并发症的发生。

