加热湿化高流量鼻导管辅助通气在新生儿呼吸窘迫综合征中的应用
杨欢,杜丹丹
(济源市第二人民医院 儿科,河南 济源 459000)
新生儿呼吸窘迫综合征(neonatal respiratory distress syndrome,NRDS)是因肺结构发育不成熟所致,若未及时治疗,易引起缺氧、呼吸衰竭等症状[1]。临床常采用经鼻持续气道正压通气(nasal-type continuous positive airway pressure,NCPAP)治疗新生儿呼吸问题,但易导致鼻黏膜溃疡、鼻子变形、吞咽功能障碍等并发症[2]。加热湿化高流量鼻导管(heated humidified high flow nasal cannula,HHFNC)作为新型无创辅助呼吸治疗手段,能改善患儿通气状态,降低并发症发生率[3-4]。本研究选取2019年5月至2020年2月济源市第二人民医院收治的84例NRDS患儿作为研究对象,探讨HHFNC辅助通气的治疗效果。
1 资料与方法
1.1 一般资料选取2019年5月至2020年2月济源市第二人民医院收治的84例NRDS患儿作为研究对象,按照治疗方案分为常规组(41例)与观察组(43例),常规组接受NCPAP治疗,观察组接受HHFNC辅助通气治疗。常规组:男19例,女22例;患儿母亲孕周30~36周,平均(32.96±1.22)周;患儿出生体质量1 197.2~1 778.7 g,平均(1 435.27±110.18)g。观察组:男23例,女20例;患儿母亲孕周28~35周,平均(32.51±1.07)周;患儿出生体质量1 235.1~1 803.2 g,平均(1 452.34±106.07)g。两组患儿性别、患儿母亲孕周、患儿出生体质量比较,差异无统计学意义(P>0.05)。本研究经济源市第二人民医院医学伦理委员会审批通过。
1.2 选取标准(1)纳入标准:①符合《早产儿呼吸窘迫综合征早期防治专家共识》中NRDS诊断标准;②伴有呻吟气促、呼吸困难、吸气性三凹征、紫绀等呼吸窘迫表现,且呈进行性加重;③双肺呼吸音减弱;④经胸片检查伴有白肺、毛玻璃样改变、支气管充气征等,确诊为NRDS;⑤家长签署知情同意书。(2)排除标准:①已进行插管治疗;②先天性肺组织发育不良或心脏病;③重度呼吸性酸中毒,动脉血二氧化碳分压(partial pressure of carbon dioxide in arterial blood,PaCO2)>60 mmHg(1 mmHg=0.133 kPa);④合并自身免疫性疾病、胎粪吸入、先天性畸形、颅内出血、严重感染、肺出血及贫血等严重疾病;⑤合并心肝肾等重要器官功能障碍;⑥严重高胆红素血症;⑦遗传代谢性疾病。
1.3 治疗方法两组均接受插管后将气管内分泌物抽吸干净,取仰卧位,滴入猪肺磷脂注射液(Chiesi Farmaceutici S.p.A,批准文号H20181202),每次70 mg·kg-1,气囊加压给氧1~2 min,拔出插管;对于烦躁、哭闹不安的依从性较差患儿给予镇静治疗,并在呼吸支持治疗期间给予常规留置胃管,进行胃肠减压,防止胃肠胀气;若治疗过程中出现严重呼吸性酸中毒或呼吸暂停频繁发作,则转为有创通气;给予适当保暖措施,按照体质量、孕周、病情补液;给予抗生素预防感染等常规对症治疗。
1.3.1常规组 NCPAP治疗。英国EME公司呼吸机通气治疗,氧流量3~6 L·min-1,吸入氧浓度30%~40%,加温至37 ℃,呼气末正压4~7 cmH2O(1 cmH2O=98.06 Pa),根据患儿病情调整吸入氧浓度及气道压力,于鼻塞与帽子之间固定,形成密闭空间。若患儿临床情况好转,血气情况良好,可考虑撤机。
1.3.2观察组 HHFNC治疗。CE0120呼吸机通气治疗(Flexicare Medical Ltd),鼻导管外径0.2 cm,根据患儿病情调整吸入氧浓度及流量,吸入氧浓度由空氧混合仪调节,流量由流量表调节,适用范围4~6 L·min-1,气道湿化温度37 ℃,鼻导管与鼻腔之间不形成密闭空间。若患儿临床情况好转,血气情况良好,可考虑撤机。
1.4 观察指标(1)疗效。显效:治疗3 d后面色红润,呻吟气促、呼吸困难等临床症状消失,血氧浓度维持在正常水平。有效:治疗3 d后临床症状、血氧浓度明显改善。无效:未达到上述标准。总有效率为显效例数与有效例数之和占总例数的比率。(2)治疗前与治疗72 h后患儿血气分析指标[动脉血氧分压(partial pressure of oxygen in arterial blood,PaO2)、动脉血氧饱和度(oxygen saturation in arterial blood,SaO2)、PaCO2]。(3)临床指标(无创通气时间、呼吸困难改善时间、住院时间)。(4)并发症[鼻损伤、腹胀、二氧化碳(carbon dioxide,CO2)潴留、新生儿坏死性小肠结肠炎(neonatal necrotizing enterocolitis,NEC)、院内感染]发生率。

2 结果
2.1 疗效观察组总有效率高于常规组(P<0.05)。见表1。
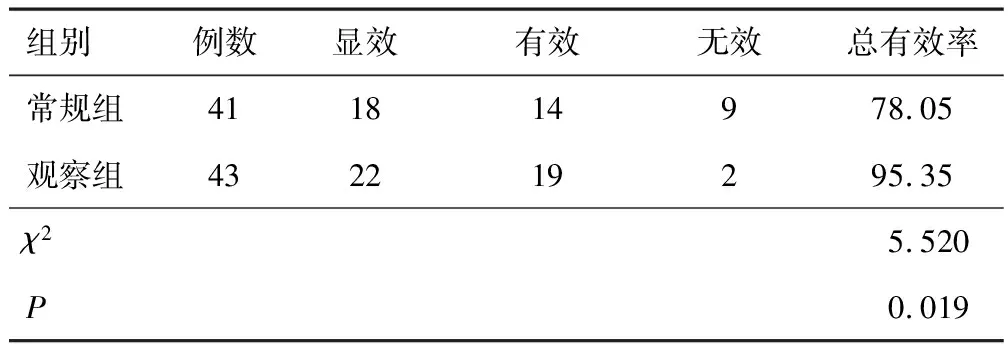
表1 两组疗效比较(n,%)
2.2 血气分析指标治疗前,两组PaO2、SaO2、PaCO2水平比较,差异无统计学意义(P>0.05);治疗72 h后,两组PaO2、SaO2均升高,PaCO2均降低,且观察组SaO2水平高于常规组(P<0.05);观察组PaO2、PaCO2水平与常规组比较,差异无统计学意义(P>0.05)。见表2。
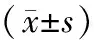
表2 两组患者治疗前后血气分析指标比较
2.3 临床指标两组无创通气时间比较,差异无统计学意义(P>0.05);观察组呼吸困难改善时间、住院时间均短于常规组(P<0.05)。见表3。
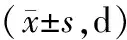
表3 两组临床指标比较
2.4 并发症发生率两组鼻损伤、NEC、院内感染发生率比较,差异无统计学意义(P>0.05);观察组腹胀及CO2潴留发生率均低于常规组(P<0.05)。见表4。
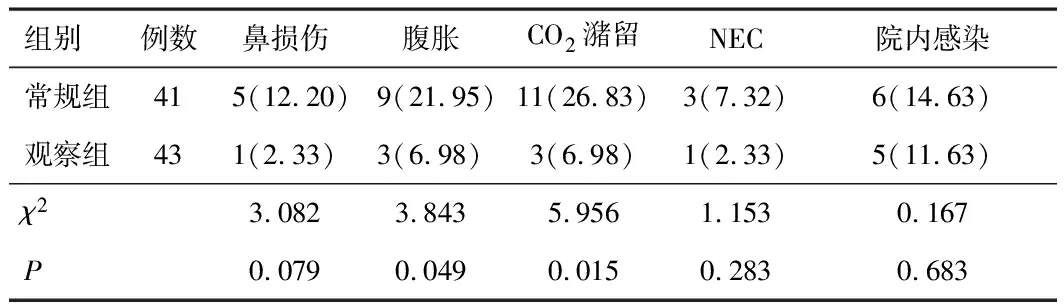
表4 两组患者并发症发生率比较[n(%)]
3 讨论
NRDS多发于早产儿,主要因缺乏肺表面活性物质,导致呼吸窘迫。有研究表明,26~27周早产儿NRDS发生率为88%,28~29周早产儿NRDS发生率为74%[5]。选择合适辅助呼吸模式治疗,不仅能减少治疗过程中出现的并发症,还能促进患儿临床症状迅速改善。早期为NRDS患儿提供安全有效的呼吸支持,是提高其存活率的关键。临床常使用NCPAP治疗NRDS,NCPAP通过使患儿持续吸入氧气,确保呼吸相能得到NCPAP提供的正压,促使呼吸周期内气道压力均为正压[6]。但长期治疗过程中,需使患儿维持固定体位,易导致头部变形,且未加热气体难以在湿化器中充分湿化,易造成肺功能受损,治疗过程中易导致腹胀、面部皮肤损伤、排痰不畅、食管反流等并发症,治疗效果欠理想。
HHFNC将鼻导管温度加热至接近人体温度,患儿吸入经过加热加湿后的氧气,可降低对呼吸道的刺激,增加气道湿润性,使痰液变得稀薄,利于排出,能有效降低小气道阻塞发生率,保证气道通畅,改善通气情况。高流量氧疗可减轻呼吸道塌陷,促使肺泡复张,降低呼吸频率,增加呼气肺容积,优化氧合[7],且能减少空气夹带,根据病情调节氧浓度,防止肺泡和小气道萎缩,同时通过冲刷鼻咽腔及上呼吸道,降低PaCO2,稳定肺泡,减少肺间质蛋白渗出,达到患儿生理需要,避免因吸入气体过于干燥、寒冷,对患儿呼吸道产生影响[8]。本研究结果显示,观察组总有效率高于常规组,治疗72 h后SaO2水平高于常规组,呼吸困难改善时间、住院时间均短于常规组,腹胀及CO2潴留并发症发生率均低于常规组,提示HHFNC辅助通气治疗NRDS患儿效果较好,可改善血气指标,缩短呼吸困难改善时间、住院时间,降低并发症发生率。
综上所述,将HHFNC辅助通气应用于NRDS患儿疗效明确,能更有效改善血气指标,促进病情恢复,减少并发症的发生。

