阿替普酶联合丁苯酞注射液治疗急性脑梗死的临床疗效
周荣海
作为神经内科中一类常见的疾病,急性脑梗死主要由脑动脉粥样硬化造成血栓阻塞于脑部动脉或管腔狭窄,引起缺氧缺血性脑部组织软化或坏死的一类急危症[1]。急性脑梗死的发病急骤,危害大,致残与致死率较高,且随着我国生活水平的改变及人口老龄化的加剧,该病的发病率呈不断上升趋势,严重威胁患者的生活质量与生命健康[2]。临床研究显示,急性脑梗死患者的梗死面积、迟发性神经细胞死亡、缺血再灌注伤害等与患者机体的炎性反应存在一定的相关性,即炎性反应越轻的患者,梗死面积越小,神经细胞死亡越少,缺血再灌注伤害越轻[3]。本研究以本院100 例急性脑梗死患者为研究对象,分析阿替普酶与丁苯酞注射液联合治疗急性脑梗死的临床效果及不良反应,现报告如下。
1 资料与方法
1.1 一般资料 选择本院2019 年6 月~2020 年7 月100 例急性脑梗死患者作为研究对象。纳入标准:①经CT 与磁共振成像(MRI)等检查诊断确诊为急性脑梗死;②均为首次发作;③伦理委员会批准了本次研究,入选患者及家属均了解本研究内容且自愿参与,并签订知情协议。排除标准:①存在智力或精神障碍者;②存在心、肾、肝等重要脏器疾病者;③哺乳期或妊娠期女性患者;④对本次使用药物过敏者。根据治疗方法不同将患者分为对照组和观察组,每组50 例。对照组中男22 例,女28 例;年龄49~78 岁,平均年龄(63.6±11.4)岁;病程2~6 h,平均病程(4.5±0.9)h。观察组中男21 例,女29 例;年龄50~79 岁,平均年龄(64.4±11.5)岁;病程2~6 h,平均病程(4.0±0.7)h。两组患者性别、年龄、病程等一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法 所有患者均接受基础对症治疗,包括降低颅内压、纠正电解质紊乱、吸氧、补液等。对照组给予阿替普酶(德国 Boehringer Ingelheim Pharma GmbH &Co.KG,注册证号S20110052)治疗,剂量为0.9 mg/kg,1 次/d,起初10%的剂量通过静脉推注给药,剩余90%的剂量则与100 ml 0.9%的氯化钠注射液混合后静脉滴注,滴注时间≤1 h。观察组在对照组基础上给予丁苯酞注射液(石药集团恩必普药业有限公司,国药准字H20100041)静脉滴注治疗,剂量为100 ml/次,滴注时间>50 min,2 次/d。所有患者的治疗时间均为0.5 个月。
1.3 观察指标及判定标准[4,5]比较两组患者的NIHSS 评分、巴氏指数、炎性因子水平及临床疗效、不良反应发生情况。①采取NIHSS 评估两组患者治疗前后的神经功能,分值0~42 分,患者神经功能缺损越严重,评分越高。②采用巴氏指数(Barthel Index)评估两组患者治疗前后的日常生活活动能力,分值0~100 分,评分高低与患者的日常生活活动能力呈正相关。③以酶联免疫吸附法对两组患者治疗前后的C 反应蛋白、白细胞介素-6、白细胞介素-8 水平进行检测。④疗效评判标准:患者无任何病残结果,可自理生活,NIHSS 评分较治疗前至少减少≥90%,视为基本治愈;患者的病残程度为1~3 级,基本可自理生活,NIHSS 评分较治疗前减少46%~89%,视为显效;患者恢复了部分自理能力,NIHSS 评分较治疗前减少18%~45%,视为有效;无效:未达到以上标准。总有效率=(基本治愈+显效+有效)/总例数×100%。⑤不良反应主要包括皮肤瘙痒、头晕恶心、消化道出血、牙龈出血等。
1.4 统计学方法 采用SPSS24.0 统计学软件对研究数据进行统计分析。计量资料以均数±标准差(±s)表示,采用t检验;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组患者的NIHSS 评分、巴氏指数对比 治疗前,两组患者的NIHSS 评分、巴氏指数对比,差异无统计学意义(P>0.05);治疗后,观察组患者的NIHSS 评分低于对照组,巴氏指数高于对照组,差异具有统计学意义(P<0.05)。见表1。
表1 两组患者的NIHSS 评分、巴氏指数比较(±s,分)
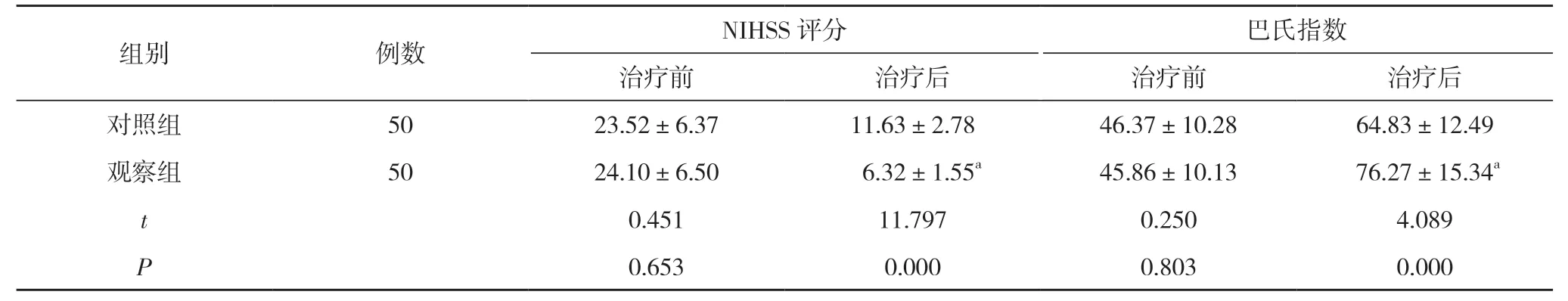
表1 两组患者的NIHSS 评分、巴氏指数比较(±s,分)
注:与对照组治疗后比较,aP<0.05
2.2 两组患者的炎性因子水平比较 治疗前,两组患者的 C 反应蛋白、白细胞介素-6、白细胞介素-8 水平对比,差异无统计学意义(P>0.05);治疗后,观察组患者的 C 反应蛋白、白细胞介素-6、白细胞介素-8水平均低于对照组,差异具有统计学意义(P<0.05)。见表2。
表2 两组患者的炎性因子水平比较(±s)
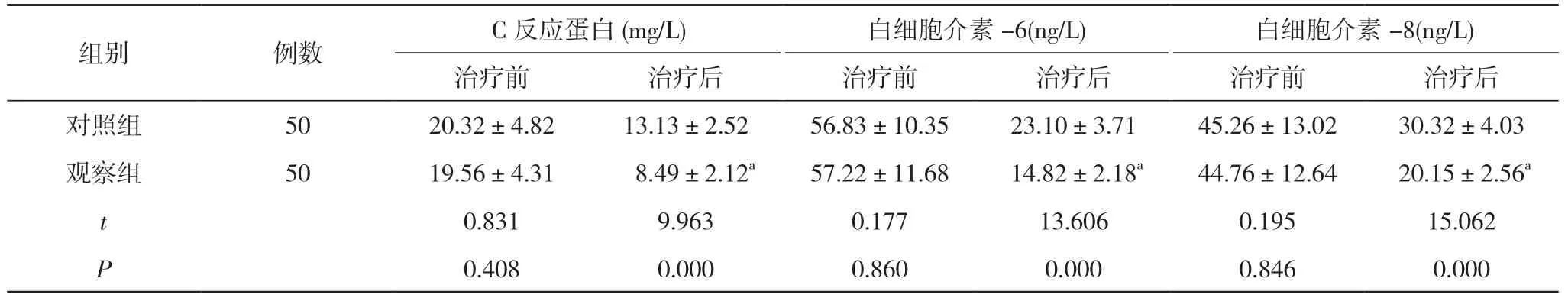
表2 两组患者的炎性因子水平比较(±s)
注:与对照组治疗后比较,aP<0.05
2.3 两组患者的临床治疗效果比较 观察组患者的治疗总有效率为92.00%,高于对照组的74.00%,差异具有统计学意义(P<0.05)。见表3。

表3 两组患者的临床治疗效果比较[n,n(%)]
2.4 两组患者的不良反应发生情况比较 观察组患者的不良反应发生率为18.00%,与对照组的20.00%比较差异无统计学意义(P>0.05)。见表4。

表4 两组患者的不良反应发生情况对比[n,n(%)]
3 讨论
急性脑梗死好发于中老年群体,大多数患者由于发病后突然丧失神经功能和自理能力,容易引起较大心理落差,而产生焦虑、不安、抑郁、狂躁等不良情绪,不利于病情的好转,甚至加重病情[6]。临床多采用抗血小板凝聚、降低颅内压、溶栓、将纤、抗凝等途径治疗急性脑梗死患者,但疗效不甚理想。有学者采取阿替普酶与丁苯酞注射液联合用药的方案治疗急性脑梗死,结果发现,临床效果确切,不仅能有效降低患者的神经功能缺损评分,还能恢复一定的自理能力[7]。作为第三代新型溶栓药物,阿替普酶能通过减少侧支循环的阻力,对血小板聚集起到抑制作用,降低血液粘稠度,改善微循环,实现血管的再通,但临床发现,单用阿替普酶时,患者的溶栓治疗容易受到时间窗限制,引起出血等并发症,且对血管的扩张作用一般[8]。丁苯酞则对脑血管直径具有扩张作用,从而加速患者的局部脑血液微循环,增强抗氧化应激、抗血栓和血小板聚集、保护线粒体,改善细胞的能量代谢,减轻炎性反应,从而保护神经元,对神经功能缺损情况予以有效修复,且临床不良反应较轻[9]。阿替普酶与丁苯酞注射液联合治疗急性脑梗死,能弥补单一阿替普酶治疗的不足,协同发挥药效,确保治疗效果[10]。
本次研究中,本院观察组患者经阿替普酶与丁苯酞注射液联合治疗,结果显示:治疗后,观察组患者的NIHSS 评分(6.32±1.55)分低于对照组的(11.63±2.78)分,巴氏指数(76.27±15.34)分高于对照组的(64.83±12.49)分,差异具有统计学意义(P<0.05),提示阿替普酶与丁苯酞注射液联合治疗可有效恢复患者的神经功能缺损情况,提高患者的日常生活活动能力。治疗后,观察组患者的 C 反应蛋白、白细胞介素-6、白细胞介素-8 水平均低于对照组,差异具有统计学意义(P<0.05),表明阿替普酶与丁苯酞注射液联合治疗能明显减轻患者的炎性反应,从而缩小梗死面积,减轻缺血再灌注损伤。观察组患者的治疗总有效率为92.00%,高于对照组的74.00%,差异具有统计学意义(P<0.05),说明阿替普酶与丁苯酞注射液联合治疗能显著提高患者的临床治疗效果,缓解患者的临床症状。观察组患者的不良反应发生率为18.00%,与对照组的20.00%比较差异无统计学意义(P>0.05)。证实了阿替普酶与丁苯酞注射液联合治疗的安全性与可靠性较高。
综上所述,阿替普酶与丁苯酞注射液联合治疗急性脑梗死的临床效果确切,能在显著改善患者的神经功能的同时,提高日常生活活动能力,降低患者的炎性反应,控制不良反应的发生,建议在临床治疗中推广应用。

