沙库巴曲缬沙坦治疗心肾综合征患者的早期临床疗效和安全性分析
曾筱曼,成水芹,李 喆,陈文萃,弓思文,周婷婷,俞雨生,左 科,王金泉
0 引 言
心肾综合征(cardiorenal syndrome,CRS)是由于心脏和肾疾病之间存在的双向交互作用,其中一个器官的急性或慢性功能不全所诱发另一个器官的急性或慢性功能障碍,是临床常见的综合征之一,CRS共包括5种类型[1],其中临床常见的为3型和4型。有文献报道估算的肾小球滤过率(eGFR)每降低10 mL/min,患者死亡率约增加15%[2]。CRS的发病机制复杂,包括肾素-血管紧张素-醛固酮系统(RAAS)和交感神经系统的慢性激活,增加氧化应激,从而导致心、肾损伤和水、钠潴留等。因此RAAS抑制剂[RASI,如血管紧张素转换酶抑制剂(ACEI )/血管紧张素受体拮抗剂(ARB)等]是治疗CRS的非常有效的药物。近年来研究发现血管紧张素受体脑啡肽酶抑制剂(ARNI)沙库巴曲缬沙坦可显著改善心功能衰竭(HF)症状[3],使肾功能稳定,改善患者的生活质量。ARNI对于CRS研究较少,本研究回顾性分析接受沙库巴曲缬沙坦3 个月以上的CRS患者的近期效果和不良反应,以评估沙库巴曲缬沙坦对CRS患者的疗效和安全性。
1 资料与方法
1.1 一般资料回顾性分析2017年11月至2020年 12 月期间在东部战区总医院国家肾脏疾病临床医学研究中心接受沙库巴曲缬沙坦治疗的25例CRS患者的临床资料。纳入标准:①年龄18~70 岁;②符合CRS诊断标准[1];③心功能为纽约心脏病协会(NYHA)分级Ⅱ~Ⅳ级;④治疗至少3个月。排除标准:①血流动力学不稳定者;②安装辅助循环装置者;③合并甲状腺功能亢进性心脏病、心肌炎、心肌淀粉样变性、重度主动脉瓣狭窄、重度肺动脉高压、恶性心律失常、心源性休克、恶性肿瘤者;④伴有消化道出血、严重脱水、休克等血容量严重不足者。
1.2 治疗方法沙库巴曲缬沙坦(北京诺华制药有限公司生产,国药准字H20170344),根据患者血压、肾功能等情况一般予以起始剂量50~100 mg/次,2次/日,根据患者耐受情况2~4周后逐渐增加剂量,最大剂量为400 mg/日,治疗前停用ACEI或ARB 36 h后再加用沙库巴曲缬沙坦。
1.3 观察指标收集患者一般资料、实验室检查及不良反应。其中一般资料包括性别、年龄、身高、体重、血压、心率、心功能NYHA分级、合并基础疾病、肾原发病、沙库巴曲缬沙坦服药时间、药物起始剂量、药物最大剂量、患者随访时间、是否死亡等。实验室检查包括血清肌酐、尿素氮、eGFR、血钾、白蛋白、谷丙转氨酶(ALT)、谷草转氨酶(AST)、氨基末端脑钠肽(NT-proBNP)、左心室射血分数(LVEF)、心胸比等。
1.4 统计学分析使用SPSS 20.0统计学软件分析数据,符合正态分布的计量资料用均数±标准差表示,组间比较采用t检验;非正态分布的计量资料用中位数和四分位数间距表示,组间比较采用秩和检验;分类资料用百分比表示,组间比较采用χ2检验。以P≤0.05为差异具有统计学意义。
2 结 果
2.1 患者基本情况特征25例中,男12例,女13例,开始服药时平均年龄(43.5±11.8)岁,包括10例非透析的肾功能不全、4例血液透析及11例腹膜透析患者。其中7例(28%)体重指数>25 kg/m2,4例(16%)<18 kg/m2,治疗前22例(88%)合并高血压,3例(12%)合并糖尿病,5例(20%)合并冠状动脉疾病,4例(16%)接受血液透析治疗,11例(44%)接受腹膜透析治疗,6例(24%)为慢性肾功能不全但未接受肾脏替代治疗,4例(16%)合并急性肾损伤。肾原发疾病方面14例(56%)为慢性肾小球肾炎,5例(20%)为高血压肾损害,3例(12%)为狼疮性肾炎,紫癜性肾炎、ANCA相关性血管炎及糖尿病肾病各1例。CRS分型: 1型1例,2型及3型各2例,4型18例,5型2例。平均使用沙库巴曲缬沙坦 8(4.5~14)个月,随访时间16(8~29.5)个月。
2.2 治疗前后肾功能指标变化经沙库巴曲缬沙坦治疗后患者肾功能稳定,与治疗前相比差异无统计学意义(P>0.05),见表1。将非透析患者进行治疗前后肾功能对比,差异仍无统计学意义(P>0.05),见图1。
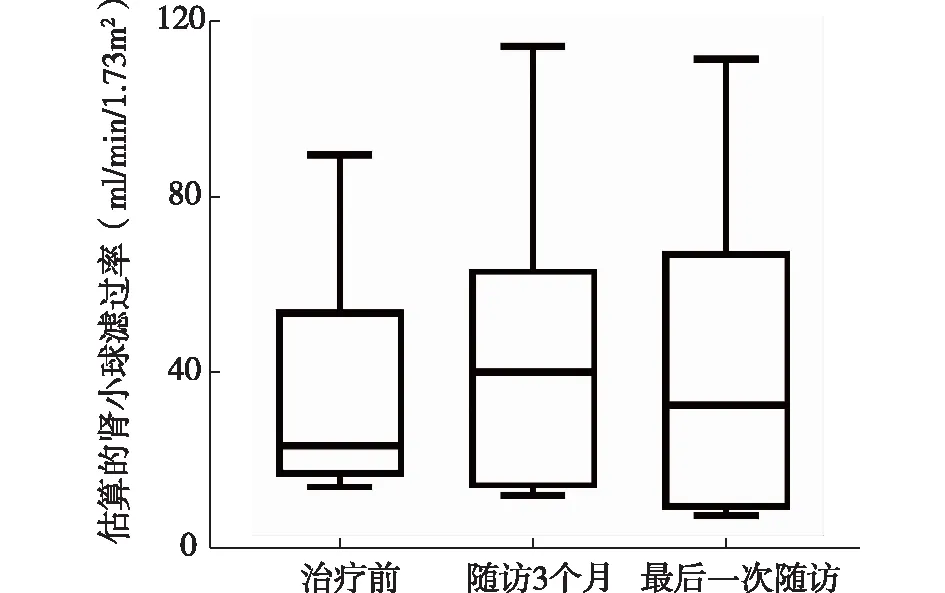
图1 非透析心肾综合征患者经沙库巴曲缬沙坦治疗前后肾功能变化
2.3 治疗前后心功能指标变化与治疗前相比,沙库巴曲缬沙坦治疗3个月及随访至最后一次后,氨基末端脑钠肽(NT-proBNP)、MAP、心率、心功能NYHA 分级等心功能的指标改善。沙库巴曲缬沙坦治疗3个月时 LVEF及心胸比与治疗前相比差异无统计学意义(P>0.05),但在最后一次随访时与治疗前比较差异有统计学意义(P<0.01),见表1。
2.4 治疗前后其他指标变化治疗3个月及随访至最后一次时血白蛋白均较与治疗前上升(P<0.01),患者在治疗后血钾、谷丙转氨酶、谷草转氨酶等指标与治疗前相比差异无统计学意义(P>0.05)。见表1。
2.5 不良反应及转归患者经治疗后出现头晕、周围性水肿、低血压、高钾血症、血肌酐上升各1例。药物减量后上述症状可显著改善、指标降至正常,余未见不良反应。至最后一次随访,1例患者因腰椎骨折后肺部感染死亡,其余患者均处于生存状态,未出现心功能不全急性发作或再次住院情况。
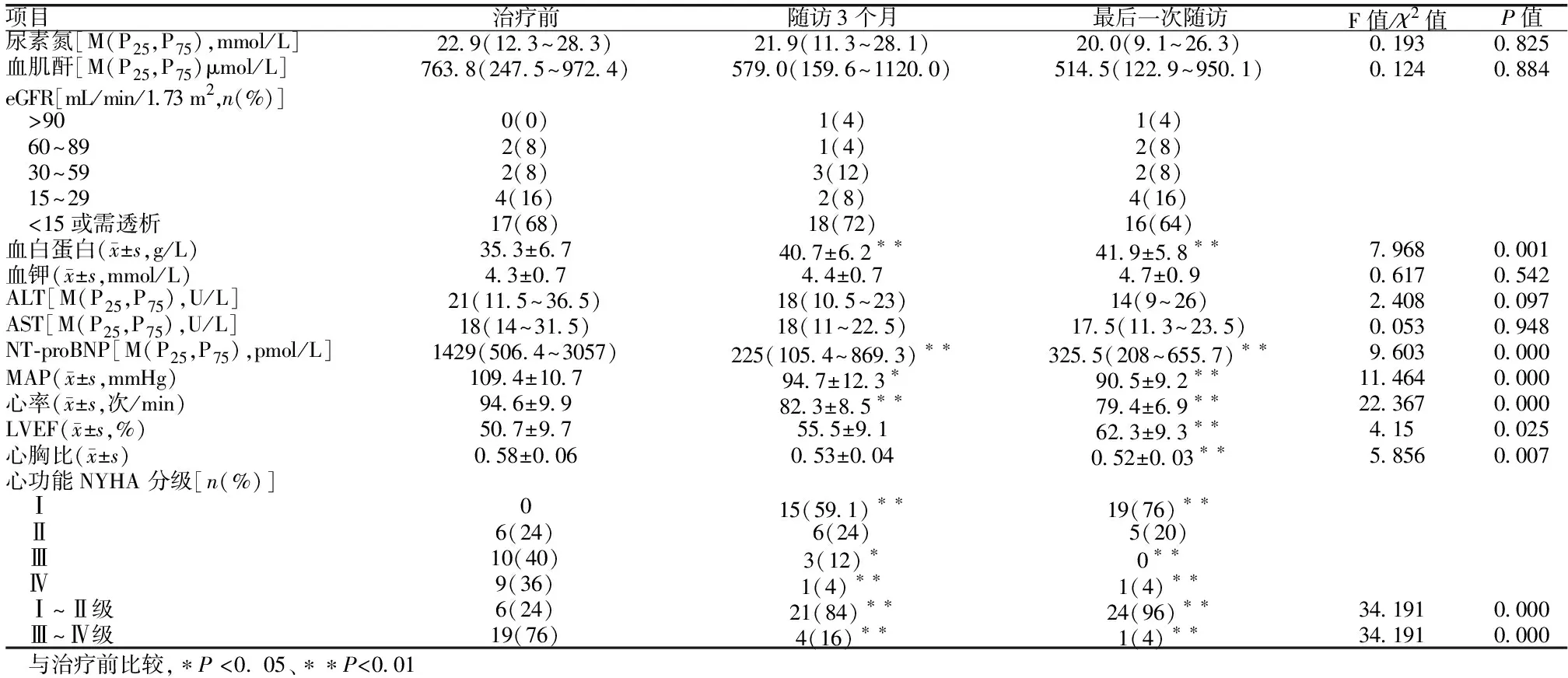
表1 25例CRS患者经沙库巴曲缬沙坦治疗前后主要指标变化
3 讨 论
CRS为心内科及肾科临床上常见的难治性症候群[4-5],由于心脏和肾的相互作用,心功能不全与肾功能损伤相互加重,形成恶性循环[6]。心房肌细胞可以分泌利钠肽,与相应受体结合产生较强的利钠、利尿、舒张血管、抑制RAAS和抗血管平滑肌细胞及内皮细胞增殖等作用,对于阻断CRS的恶性循环可以起到多个方面的积极作用,但在生理情况下,利钠肽在人体内易被脑啡肽酶水解,难以发挥其对心脏和肾的保护作用。因此,理论上如果能阻断脑啡肽酶的活性,升高利钠肽水平,对心功能不全或CRS具有重要治疗意义。但实际研究表明,单用ARNI对心功能不全的疗效不佳,原因可能在于其升高了利钠肽的同时也进一步激活血管紧张素Ⅱ(AT-II),而AT-II的激活可能导致心肌重构以及肾小球内压升高,小管间质纤维化等,最终两者的作用相互抵消[7-8]。
沙库巴曲缬沙坦是沙库巴曲和缬沙坦两种成分以1∶1摩尔比例结合而成的盐复合物,是针对上述机制研制的既能够升高利钠肽水平又能抑制AT-Ⅱ从而发挥保护心脏的作用。有研究显示沙库巴曲缬沙坦相对于传统的RASI能降低心血管死亡风险20%,降低HF住院风险21%,改善HF症状和生活质量的同时,咳嗽、高钾血症以及肾功能损害等不良反应更低[8]。本研究25例CRS患者中,10例非透析患者,15例为血液或腹膜透析患者,是国内首次成系列观察沙库巴曲缬沙坦治疗CRS患者。结果显示,所有患者心功能均获得不同程度的改善,患者的血清 NT-ProBNP水平显著降低,LVEF升高,NYHA分级改善。此外患者血压尤其是收缩压经治疗后亦有显著降低,有效减少患者心脏后负荷。
值得指出的是,与普通HF患者相比,CRS患者由于肾功能减退,导致常用的RASI类药物应用常常受限。本研究显示,入组的10例非透析患者经沙库巴曲缬沙坦治疗后肾功能总体情况平稳,血肌酐较治疗前水平无明显差异,其中部分患者因治疗后心功能改善,肾灌注增强,GFR有所升高。此外本研究提示大部分患者接受沙库巴曲缬沙坦治疗后,电解质均平稳,仅1例患者出现血钾升高(5.8 mmol/L),药物剂量减量且服用降钾药物后血钾降至正常,后续未再出现高钾血症,较传统RASI药物显示了更好的安全性。
既往Januzzi等[9]观察到沙库巴曲缬沙坦治疗HF现的不良反应包括低血压(17.6%)、头晕(16.8%)、高钾血症(13.2%)、血肌酐升高(12.3%)、血管性水肿(0.3%)。上述发生的常见不良反应与本研究相似,但本研究不良反应反应总体发生率较低,可能和患者年龄相对较轻、基线射血分数相对较高等因素相关。有研究报道的沙库巴曲缬沙坦可导致一些少见的并发症包括:低钠血症、肌肉不自觉的抖动、横纹肌溶解综合征等[10-11],未在本研究患者中出现。
因此在监测肾功能的前提下,CRS患者使用沙库巴曲缬沙坦是安全的,相比较于传统的RASI,沙库巴曲缬沙坦在疗效和安全性上具有一定优势。同时本研究也存在一些不足:病例数较少,个别患者服药时间较短,且为单中心的研究,需在今后的临床中增加样本量,延长观察时间,进一步观察长期疗效和不良反应。
综上所述,CRS患者中应用沙库巴曲缬沙坦,可有效改善患者的心功能、降低患者的血压,并且观察到患者肾功能及血钾基本稳定, 不良反应发生率较低,预后好,可在临床中安全有效的应用。

