早期及全程营养干预对食管癌同期放化疗患者生活质量和疲乏的影响
宋海侠 安跟会 郭丽云 董玉梅 徐丽君 魏世鸿
甘肃省肿瘤医院,甘肃 兰州730050
食管癌是临床常见的恶性肿瘤,我国是食管癌高发地区,发病率约占全球的50%,且有逐年增长的趋势[1]。食管癌以食欲下降、进行性吞咽困难为主要表现,食管癌患者营养不良发生率高达60%~85%,位居所有肿瘤之首[2]。局部晚期食管癌患者进行同步放化疗过程又会加重营养不良的发生。既往研究表明,恰当的营养干预可以改善营养不良的程度,进而减轻治疗相关反应,提高治疗疗效,延长生存时间[3-5]。随着医学模式的发展,关注评价患者延长生命期间的生活质量具有重要意义。本研究评价三种不同模式的营养干预对食管癌患者同期放化疗的生活质量及肿瘤相关疲乏的影响,报告如下。
1 资料与方法
1.1 一般资料 选取我院放疗科2018年1月至2020年6月收治的90例食管癌同期放化疗患者,根据营养干预方式不同分为对照组、正常营养干预组、早期营养干预组,每组各30例。三组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。见表1。
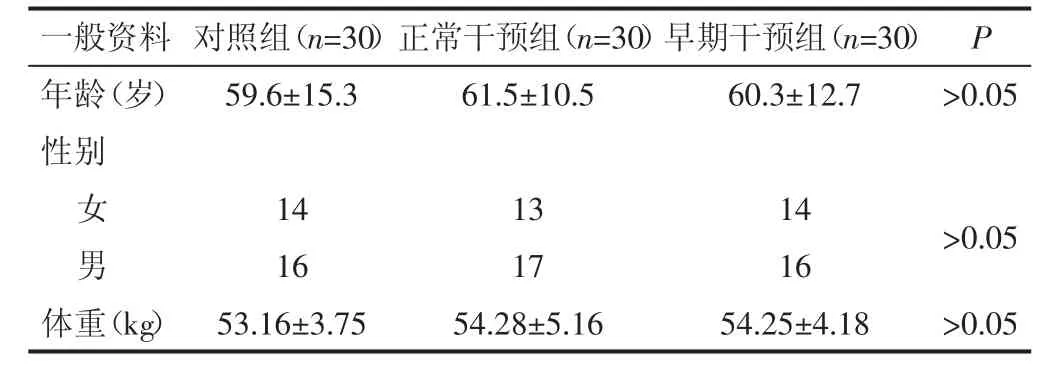
表1 三组患者一般资料比较(例)
1.2 入选标准 纳入标准:(1)根据临床病史、症状、体征和影像学资料诊断为局部晚期食管癌,且为初诊初治、经病理学证实为鳞状细胞癌的患者;(2)拟行放射治疗联合同步化疗;(3)肝功能:血胆红素≤1.5ULN,ALT≤2.0ULN;肾功能:CR≤1.2ULN,BUN≤1.2ULN。(ULN为正常值上限);(4)骨髓储备:WBC≥4.0×109/L,ANC≥2.0×109/L,BPC≥100×109/L,HB≥8.0g/L;(5)KPS≥70,ZPS≤2,PG-SGA评分≥4分,预期生存期≥3个月;(6)体重下降,但小于10%;饮食量下降,但大于目标喂养量60%。(7)签署知情同意书。排除标准:(1)肠道功能严重受损或肠内营养不能耐受者;(2)无营养不良或营养不良风险者;(3)重度营养不良,无法耐受放化疗者;(4)严重消化道反应、消化道出血、肠梗阻者;(5)消化道梗阻,无法经口进食也无法或不愿意行营养置管者。
1.3 方法 所有患者均采用调强适形放射治疗方式,模拟CT下定位,以统一的标准勾画放射靶区,TPS设计放疗计划:200cGy/(次·d),每周5d,总剂量6000~6600cGy。多西他赛60mg/m2,静脉滴注15min以上,d1,顺铂25mg/m2,静脉滴注,d1~3,21~28天为1周期。放疗期间至少完成2周期同步化疗,放疗结束后,根据患者身体情况行辅助化疗1~2周期。
入院后2小时内对营养干预组患者(早期干预组和正常干预组)进行初步筛查。医护人员及临床营养师在24小时内完成综合评定(病史、体格检查、实验室检查、人体测量),完成PG-SGA评分及营养风险筛查表(NRS2002),确定营养等级,根据CSCO肿瘤营养治疗专家委员会推荐,以25~30kcal/(kg·d)来估算一般放化疗患者的每日所需量(2B类),根据患者进食梗阻情况,个体化计算所需能量,完全梗阻者行管饲能全素营养,热量25kcal/(kg·d),蛋白质1~1.2g/(kg·d);不完全梗阻者行口服能全素营养为主,热量20kcal/(kg·d),蛋白质0.8~1.0g/(kg·d),并鼓励患者进食;无梗阻患者以自己进食为主,辅助口服能全素营养治疗,热量15kcal/(kg·d),蛋白质0.5~0.8g/(kg·d)。在临床营养师的指导下,医师根据患者具体情况,动态调整肠内营养,必要时加用肠外营养。早期营养干预组在放化疗前1周开始行营养评估,给予营养干预;正常营养干预组在放化疗开始时进行营养评估,给予营养干预;对照组不给予营养评估,在放化疗开始自行饮食,必要时给予肠外营养支持。
1.4 观察指标 采用欧洲癌症研究组织研发的测定量表EORTC QLQ-C30评估患者生活质量(QOL),该量表的信度及效度均较好[6-7]。量表包含9个症状领域以及1个总体健康领域。功能及总体健康领域得分越低表示QOL越低,症状领域得分越低QOL越高。多维度疲乏症状量表-简表(multi-dimensional fatigue symptom inventory-short form,MFSI-SF)具有良好的信效度,可以评估疲乏程度[8]。该量表共30个条目,测量5个维度,每个维度含6个条目,得分越高,疲乏程度越重。早期营养干预组在放疗前1周及放化疗结束后1d评估,正常营养干预组与对照组均在放疗前1d及放化疗结束后1d评估。
1.5 统计学方法 应用SPSS21.0统计软件分析数据。正态分布数据采用方差分析进行分析,采用LSD-t检验进行两两比较。P<0.05为差异有统计学意义。
2 结果
2.1 三组患者疲乏程度比较 放化疗后,对照组MFSI-SF评分较放疗前升高,早期干预组较放疗前降低(均P<0.05),正常干预组放疗前后无统计学差异(P>0.05)。与对照组比较,早期干预组、正常干预组MFSI-SF评分低于对照组,早期干预组低于正常干预组(均P<0.05)。见表2。
表2 三组患者疲乏程度比较(分,±s)

表2 三组患者疲乏程度比较(分,±s)
注:与治疗前比较,1)P<0.05;与对照组比较,2)P<0.05;于正常干预组比较,3)P<0.05
?
2.2 三组患者QLQ-C30中功能领域及总体健康评分比较 在生活质量方面,放化疗结束时,对照组患者在躯体、角色、情绪、社交功能和总体健康领域得分均降低(均P<0.05)。正常营养干预组患者在躯体、角色、社交功能和总体健康领域得分均降低(均P<0.05)。早期营养干预组患者在角色、社交功能领域得分均降低(均P<0.05)。三组组间相比较,正常干预组与对照组比较,在患者的躯体、情绪方面具有优势(均P<0.05);早期干预组与对照组及正常干预组比较,在患者躯体、情绪、总体健康方面均有很好优势(均P<0.05)。在认知和角色功能方面,各组间无明显差异(均P>0.05)。见表3。
表3 三组患者QLQ-C30中功能领域及总体健康评分比较(分,±s)
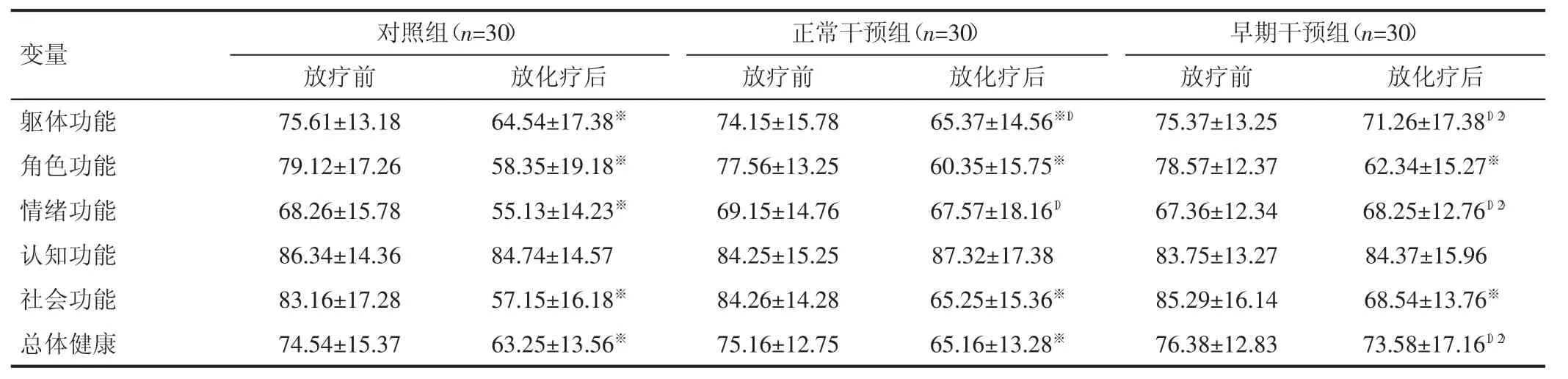
表3 三组患者QLQ-C30中功能领域及总体健康评分比较(分,±s)
注:组内治疗前后比较,※P<0.05;组间治疗后相比较,与对照组比较,1)P<0.05,与正常干预组比较,2)P<0.05
?
3 讨论
食管癌早期起病比较隐匿,多无明显临床症状,不易发现。首次就诊的食管癌患者绝大多数处于晚期和局部晚期阶段,丧失了手术治疗机会,且患者常伴有不同程度的进食困难,合并不同程度的营养不良。目前,对食管癌患者临床多采用同步放化疗的治疗方式。放射治疗是利用放射线杀伤肿瘤细胞,而放射线在消灭肿瘤细胞的同时,也会引起食管正常黏膜的损伤,影响进食,加剧营养不良。化疗药物的胃肠道反应也会影响患者的进食,诱发营养不良,影响患者的生活质量。肿瘤相关性疲乏是一种与肿瘤或肿瘤治疗相关的、影响正常功能的主观性和持续性的劳累感[9-10]。这种疲乏通过休息不易得到改善,且干扰患者的正常生活,影响患者的生活质量。肿瘤相关疲乏也是肿瘤患者生活质量量表症状领域中很重要的一项内容。有研究表明,治疗过程中给予营养干预能够提高食管癌患者治疗的耐受性,降低治疗相关反应,提高近期疗效,提高生活质量[11-12]。也有研究表明,通过营养支持治疗可以改善患者乏力状况,提高生活质量[13-14]。
本研究结果表明,同步放化疗对食管癌患者的生活质量的功能领域及疲乏症状均产生了影响,这与吕亚娟等[15]研究结论相似。而与正常营养干预组的患者相比,早期营养干预组在躯体功能状态及肿瘤相关疲乏症状的改善及总体健康的恢复方面更有优势,可能因为通过营养干预降低治疗相关的毒副反应,降低治疗对患者进食的影响[16]。及早进行营养干预会让患者的身体状态在治疗前就可以达到一个好的状态水平,提高其耐受性,更好地保障患者治疗过程中的生活质量。另外本研究还表明,不管是进行正常营养干预还是早期营养干预,患者的角色功能及社会功能方面均无明显好转,可能因为食管癌患者存在焦虑、忧虑、抑郁等多种心理问题,影响饮食、睡眠等多个方面,进而影响了日常生活[17-20]。因此,除了关注患者营养状况之外,应该对患者进行及时有效的心理干预,使患者一定程度上了解疾病及其治疗原理,并给予必要的心理健康疏导,可能对其相关抗肿瘤治疗的顺利进行也会起到一定作用。
总之,随着肿瘤治疗模式的转变,不仅要关注肿瘤临床治疗效果,而且要重视患者日常生活质量变化。早期营养干预能很好改善患者躯体相关功能状态及缓解肿瘤相关疲乏症状,提高生活质量。而在改善心理和社会功能方面作用有限,需要多学科协作,共同提高患者生活质量。

