人血白蛋白非胶体作用在救治危重症患者中的应用价值
陈 鸣,虞文魁
0 引 言
自20世纪40年代人血白蛋白(human serum albumin, HSA)用于临床以来,大量研究对其生化特性和潜在的临床益处进行了深入的探索,发现除了增加血容量和维持血浆胶体渗透压外,HSA复杂的三级结构还使其具有物质结合和转运、抗氧化、抗炎、降低毛细血管通透性以及免疫调节等多种生物功能[1-2]。这些功能对脓毒症、肝功能衰竭等危重症患者的治疗具有积极意义,不应被忽视。因此本文重点对HSA非胶体作用和潜在治疗价值进行阐述。
1 物质结合与转运
HSA的多种物质结合和转运功能依赖于其特殊的分子结构。其一级结构为包含585个氨基酸残基的单一多肽链,其中的大量的半胱氨酸残基形成二硫键(-S-S)用于维持二级结构的稳定,在34位留下一个游离的Cys34残基,构成血浆中的主要巯基库。在二级结构的基础上进一步盘绕和折叠构成了3个同源亚结构域(亚结构域I、II和III),组成心形的三级结构,该三级结构包含疏水性内部和亲水性外部。见图1。这种结构稳定而灵活,其结合位点允许与各种配体相互作用,可逆性结合包括阳离子、胆红素、激素、脂肪酸和各种聚合物、药物等。
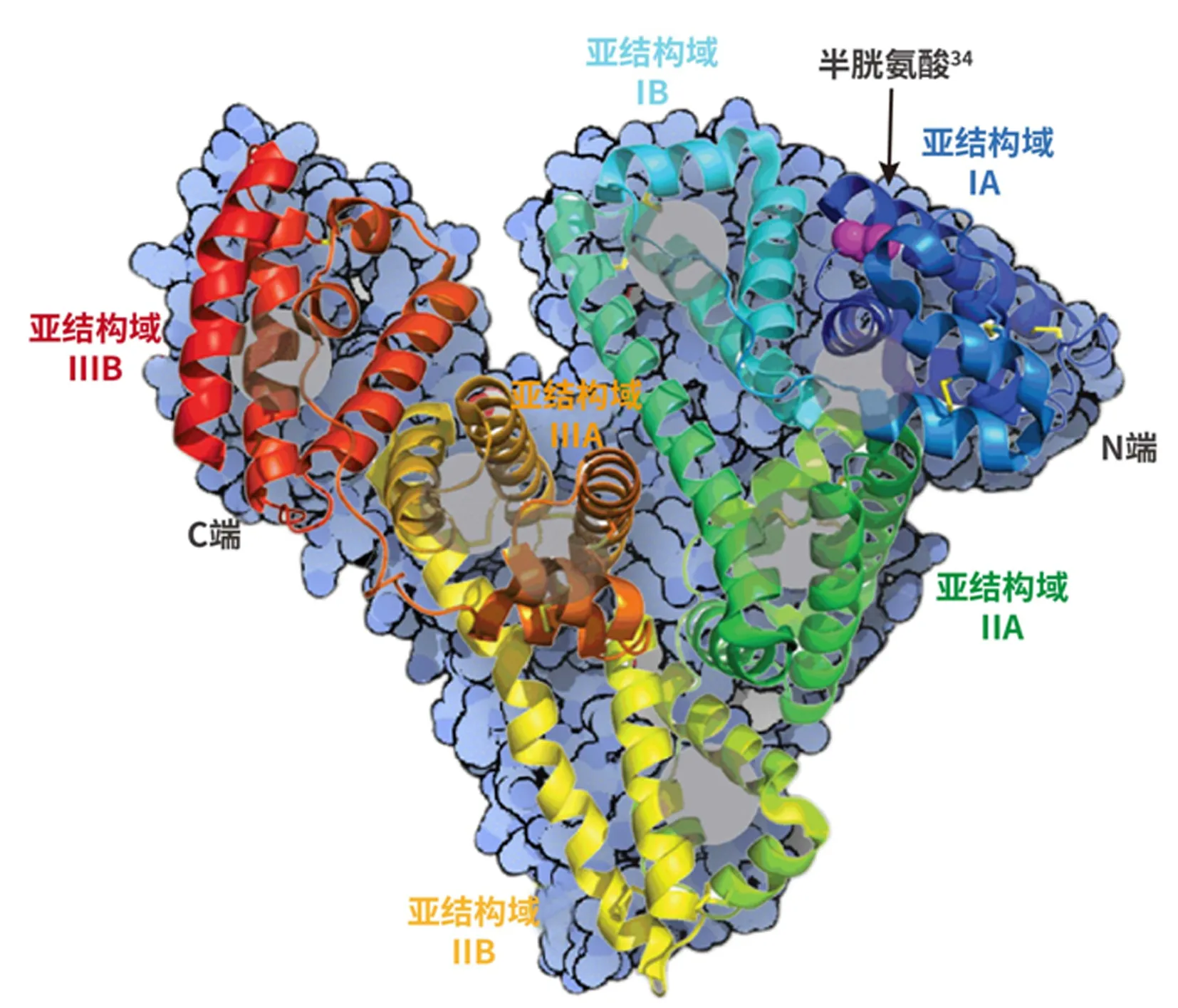
图1 HSA结构示意图Figure 1 Tertiary structure of human serum albumin
1.1胆红素和胆汁酸胆红素为血红蛋白分解后产生的有毒不溶性代谢物,可以被HSA结合,并单独运输到肝细胞与葡萄糖醛酸结合,通过胆汁-肠道系统排出体外[3]。此外,肝硬化患者常常因肝功能障碍导致血清胆汁酸浓度增加,而HSA可以与游离胆汁酸结合,因此对肝硬化患者补充HSA可以降低其血清游离胆汁酸浓度,改善其临床症状[4-5]。
1.2细菌毒素与抗菌药物HSA可与多种细菌产物结合,如革兰阴性菌的脂多糖和革兰阳性菌的其他成分,包括脂壁酸和肽聚糖[6]。在内毒素血症模型动物中,HSA可显著改善脂多糖引起的血管舒张和收缩能力异常[7]。同时部分抗菌药物药效发挥依赖于HSA与药物结合,发挥增加药物可溶性、降低药物毒性、将药物运输至特定组织和器官等作用[8]。低白蛋白血症可导致蛋白结合率高的抗菌药物的表观分布容积和清除率(CL)增加,从而使血清有效药物浓度降低[9]。有研究通过模拟血清药物浓度和游离药物浓度,探讨体外条件下HSA对酮康唑和伊曲康唑的抗菌活性的影响,其结果表明与4%的HSA联用可以提高伊曲康唑的抗真菌活性[10]。
临床研究也发现使用HSA对于感染患者可能有积极意义,揭苏平等[11]探究头孢噻肟钠与HSA联用对自发性腹膜炎患者的临床疗效及其对肝功能的影响,对照组患者仅给予头孢噻肟钠静脉滴注;观察组患者在对照组基础上加用HSA静脉滴注,其用量根据患者水肿程度决定HSA的剂量(轻度水肿5 g/d、中度水肿8 g/d、重度水肿10 g/d)。治疗1周后结果显示采用头孢噻肟钠与HSA联用治疗自发性腹膜炎患者的有效率优于单用头孢噻肟钠(94.29%vs.77.14%),治疗组患者体温、腹痛、腹水、腹部压痛等复常时间也均早于对照组(P<0.05),谷丙转氨酶(ALT)和总胆红素(TBIL)均低于对照组(P<0.05),结果显示HSA有效促进了患者腹膜炎体征和肝功能的改善,提高了临床疗效。
虽然水肿减轻和器官功能改善亦可能与HSA的胶体作用相关,难以完全剥离,但有2点积极作用已经明确:首先,HSA强大的结合能力既赋予其物质运输的载体的功能,也让其成为机体对有毒代谢物质的缓冲屏障,降低有毒代谢物质的游离浓度对减轻其造成的病理生理损害理应有积极意义;其次,HSA对包括抗菌药物在内多种药物的药代动力学的影响是明确存在的,但是否都利于药效的充分发挥仍然存在疑惑。未来仍需要通过科学严谨的试验研究以探讨HSA结合有毒代谢物质的作用对危重患者病理生理进程和预后的影响,以及寻找将HSA的药代动力学作用转化为药效学收益的精准治疗措施。
2 炎症反应的调控作用
2.1 抗氧化应激HSA分子中的半胱氨酸34(Cys34)上的巯基占血液中所有巯基的80%,是血管内最重要的抗氧化基团。HSA通过半胱氨酸(Cys)基团来清除自由基:健康状态下,当HSA中的Cys34未与其他物质结合而处于游离状态时, Cys34基团主要为巯基态,即还原态,其抗氧化能力强;当HSA中的Cys34基团主要为两种非巯基态即氧化态时,其抗氧化能力弱[12]。氧化应激是危重症患者病情进展的关键病理基础[13]。在脓毒症和肝功能衰竭状态下处于非巯基态的HSA比例明显升高,此时外源性补充巯基态HSA可以增强危重症患者的内源性抗氧化保护,具有积极意义[14-17]。
Quinlan等[18]对20例急性肺损伤患者分别给予HSA和安慰剂,发现白蛋白和血浆硫醇浓度以及白蛋白和抗氧化能力之间存在正相关关系,在HSA治疗组硫醇和抗氧化能力之间有很强的相关性,而在安慰剂组中未见这种相关性。说明HSA的补充增加了血浆硫醇水平,并改善了血浆巯基依赖的抗氧化特性;另一项对100例平均血清白蛋白水平在23.2~23.7 g/L的综合ICU危重患者的研究表明,每天补充200 mL的20%HSA以维持血清白蛋白>31 g/L的患者器官功能障碍评分(SOFA评分)下降更明显,这些临床受益可能与HSA的抗氧化功能有关[19]。
2.2减轻炎症损伤炎症损伤时,炎症因子和生长因子诱导毛细血管通透性增加,血管生成增加,细胞和血浆中的白蛋白进入伤口,促进组织生长,肌肉、肝、肾等组织中的白蛋白均以更高的速率进入间质,所以危重患者的炎症损伤会导致低白蛋白血症。健康状态下,白蛋白代谢速率较低,肝合成白蛋白速率与降解速率适度,两者处于动态平衡状态;炎症状态下的白蛋白降解速率加快,白蛋白合成速度远低于降解速度,上述因素均会导致全身白蛋白总量减少[20]。此时可能更需要补充的HSA参与调节炎症反应,研究显示白蛋白能够下调TNF-α、 IL-1及 IL-6、CRP、MMP-8的表达通过减少抑制性转运,从而发挥其抑制炎症因子、阻断“炎症风暴”的作用。此外,白蛋白与由EGFR、ERK1和ERK2表达调控的各种组织蛋白的转录密切相关,能够通过上调激活NF-κB途径[21],从而减轻炎症损伤[22-23]。
一项前瞻性研究旨在评估使用低剂量(1 g/kg体重,每2周1次)和高剂量(1.5 g/kg体重,每周1次)HSA长期治疗(12周)对失代偿性肝硬化患者血清白蛋白、血浆肾素、心血管功能、门静脉压和血浆细胞因子水平的影响[24]。收集18例来自Pilot-PRECIOSA研究中的无细菌感染的失代偿期肝硬化患者,结果显示长期高剂量补充HSA与血清白蛋白水平正常化、改善循环稳定性和左心室功能有关,同时还可显著降低血浆细胞因子的水平,从而减少全身炎症反应。另一项前瞻性对照研究探讨HSA对于内毒素、细胞因子和一氧化氮产物(NOx)的影响,共纳入30例肝硬化伴SBP患者,结果显示HSA治疗可显著降低血浆和腹水中促炎细胞因子TNF-α、IL-6水平,从而达到抗炎作用[21]。
2.3免疫修复作用在脓毒症发病过程中,HSA既可以通过广谱的抗原结合作用调理及中和微生物、毒素等,抑制炎症,修复机体对感染的过度炎症性免疫反应,也可通过减少免疫细胞的细胞凋亡,解除FCγ受体封锁,缓解免疫抑制[25]。同时,研究还发现HSA能够增强抗原递呈细胞(antigen presenting cells, APC)的免疫激活,在两种APC培养基中加入卵白蛋白作为外来抗原,可以诱导APC合成和分泌IL-2。而在培养基中加入HSA则能显著增强这种免疫应答[26]。
一项旨在评估HSA潜在的免疫修复作用是否通过其对前列腺素E2和其他脂质的作用来介导的研究中,纳入ATTIRE 试验中收集的79例接受20%HSA治疗的急性失代偿与急性-慢性肝功能衰竭(AD/ACLF)患者,通过比较巨噬细胞功能来评估免疫功能。发现与治疗前相比较,HSA治疗后可显著增加单核细胞衍生的巨噬细胞肿瘤坏死因子的产生,达14.3%(P=0.0013);与治疗前相比较,HSA治疗后可显著增加血浆蛋白与PEG2的结合能力,平均增加8.7%(P<0.0001)[27]。
氧化应激-炎症损伤-继发免疫抑制既是危重患者各阶段炎症和免疫应答的主要特征,也是危重患者各阶段病情进一步恶化的基础。HSA对氧化应激、炎症损伤、免疫修复的积极作用和氧化态HSA的存在可以成为HSA透析、置换等疗法在危重症治疗领域的理论基础,未来还需要更多的大样本研究来评价这些疗法的实际临床疗效和性价比。
3 维护血管内皮功能
血管内皮具有维持血管稳态,调节血管张力、血栓形成、纤维蛋白形成和维护血管壁屏障完整性的功能。HSA调节炎症、减少氧化损伤和干预中性粒细胞粘附的能力可能会影响内皮功能[28-29]。内皮细胞表面被一种带负电荷的类似网状结构的由糖蛋白、蛋白多糖和可溶性生物大分子成分组成的糖萼所覆盖,糖萼的脱落改变了毛细血管腔和被糖萼层保护的富含蛋白质区域之间的胶体渗透梯度,导致毛细血管泄漏增加,血小板和中性粒细胞的黏附增加[30]。HSA能与糖萼结合,增强糖萼维持内皮细胞的稳定性,减少白细胞和血小板对内皮的黏附[31-32],同时通过结合内皮细胞上的糖萼后参与小分子物质的转运和抗氧化以此来维持内皮细胞正常的功能[33-34]。
一项随机、非盲研究探讨了HSA和HES 200/0.5对血浆内皮因子(血管假性血友病因子,vWF)水平和血清中NO代谢物、硝酸盐和亚硝酸盐水平的影响[35],以评估两者对内皮功能影响的可能差异,结果显示HSA可显著降低内皮功能活化标志物vWF的水平,而HES组无明显变化,提示HSA对于内皮功能具有保护作用。
HSA对内皮细胞功能的保护作用是其除了维持胶体渗透压以外,减少患者组织水肿,维持微循环功能稳定的另一项重要机制,同时也说明HSA在理论上可能对内皮细胞损伤后凝血反应激活、血栓形成等病变有预防作用,而这些作用是人工胶体目前所不具备的。因此,我们在选择胶体液时不应仅仅考虑相对分子质量、稳定性、可能的不良反应和价格,其潜在的治疗作用也应纳入考量范围。以HSA为代表的天然胶体与人工胶体之争在未来还将继续,也必将更精彩纷呈。
4 抗凝血作用
HSA的复杂结构决定了其能够结合和携带多种物质,其中白蛋白分子结合NO后硝基化的HSA(HSA-NO)具有扩张血管和抑制血小板聚集的潜在临床作用,对血细胞和血小板有良好的保护功能[6]。HSA具有与肝素有类似的抗凝血活性,两者空间结构相似,且均带有大量的负电荷,肝素属于一类糖胺聚糖,其硫酸基团带负电荷,与带正电荷的抗凝血酶III结合,进而发挥抗凝作用。HSA同样带负电荷,作用机制可能与肝素相似,肝素和HSA都可以减少组蛋白引起的血小板聚集, 并可减轻因血小板激活而导致的组织损伤[36-37]。在血液透析时,使用HSA可以降低患者对于抗凝剂的需要量[38-39]。
此外,HSA对需体外循环的外科手术患者的凝血功能维护也有积极作用。在心肺分流术(cardiopulmonary bypass,CPB)时,炎症和凝血系统被迅速激活(纤维蛋白的形成、血小板激活/消费和内皮损伤), 如CPB术中予以3%HSA作为CPB 预充液时不仅可保持渗透压,防止间质水肿,保护内皮细胞并保持组织微循环功能,同时也能防止纤维蛋白原和血小板黏附,因此HSA可能对心脏手术期间的止血有积极辅助作用[40]。在一项纳入21个临床对照试验、共计1346名接受心脏手术的成人和儿童患者的Meta分析中,根据体外通路预充液选择HSA或晶体液分组,以患者术后血小板计数、血浆胶体渗透压、术后体重改变为主要终点,结果显示HSA对比晶体而言,除对胶体渗透压、术后体重增加有良好的影响外,还能够更好地保持血小板数量[41]。总之,现有研究资料表明HSA在体外循环时具有辅助抗凝作用,能够减少此类患者的凝血系统激活。虽然HSA是否对所有的体外循环管路都有相同的抗凝效果不得而知,但其对体外循环患者凝血激活和消耗的保护作用将是具有前景的研究方向。
5 调节酸碱平衡
HSA的输注对血浆pH值的影响微乎其微。Mallat等[42]为了评估20%HSA对于酸碱平衡状态的影响,纳入了30例接受20%HSA的危重症低白蛋白血症患者,发现在20%HSA给药后,一方面强离子差的增加引起碱化作用;另一方面因血清白蛋白浓度升高,导致游离的非挥发性血浆弱酸浓度的增加而引起酸化作用,两者达到平衡,因此血浆pH值没有变化。在此前的一项纳入16名手术的患者随机前瞻性临床研究结果也是如此[43]。然而,由于表面的离子化侧链如组氨酸咪唑残基结构的存在,HSA带净电荷,其等电位点pH值约为5.67[42]。因此在血浆中HSA带负电荷,赋予了其作为缓冲剂维持体内酸碱平衡的功能,尤其是由于呼吸循环障碍、严重感染及创伤、温度变化和代谢改变等因素导致的酸中毒具有良好的缓冲作用[42]。低蛋白血症患者的阴离子间隙下降(血清白蛋白水平每下降10 g/L,阴离子间隙参考值下降2 mmol/L),其缓冲对抗内环境酸碱紊乱的能力同样下降,我们在临床评估与治疗合并低白蛋白血症的危重患者时应加以重视。
6 结 语
综上所述,HSA是一种具有多种生物学性能和作用的多功能蛋白。其在治疗危重患者中的应用不应仅仅局限于一种复苏胶体液和低蛋白血症的纠正,更应该考虑发挥其多项生物学功能。当然,确立HSA的“治疗药物”属性依然任重道远,尚有许多疑问待解答:HSA非胶体作用疗效的前瞻性临床试验还有待丰富,仍需大量临床数据来解决使用HSA治疗疾病的获益与风险和成本的争议,明确其最佳给药剂量和给药时间及其对远期预后的影响,确定哪些患者将从长期给药中获益最多等等。这些均有待于临床医师和科研工作者的深入探索。

