三维多孔MnOx@In2O3立方盒子的构筑及储锌性能
樊小勇,毋 妍,孙瑞波,苟 蕾,李东林
(长安大学材料科学与工程学院,西安 710061)
传统化石类能源储量不足及其过度使用造成严重的环境污染问题,促使新能源如太阳能、风能、地热能和生物质能等的高速发展[1~3].然而,这些新能源具有间歇性和不可控等缺点,亟需高效、低成本和高安全性的储能器件.锂离子电池具有能量/功率密度高、循环寿命长等优点,已几乎完全占据便携式电子产品市场[4,5].然而,地壳中锂储量低、成本高及安全性差等问题严重限制了锂离子电池在规模化储能中的应用[6].由于采用不可燃的水溶液做电解液,储量丰富、价格便宜、低氧化还原电位(-0.763 Vvs.SHE)和较高理论比容量(819 mA·h/g)的金属锌做负极,水体系锌离子电池在规模化储能领域显示出巨大的优势[7~9].目前,锌离子电池正极材料主要采用锰基氧化物如MnO2[10~13],Mn2O3[14,15]和Mn3O4[16,17],其具有资源丰富、价格低廉及工作电压(>1.2 V)和输出容量(>200 mA·h/g)较高等特点.然而,其低电子/离子电导率及电化学循环过程中不可逆相变、锰的溶解和电极/电解质界面不稳定导致其在小电流密度、深度放电条件下的循环性能差;低反应动力学及倍率性能差[18~20].
为解决这些问题,将锰基氧化物与碳纳米管(CNT)和还原石墨烯(rGO)复合,提高其电子/离子传输能力和循环过程中的结构稳定性,获得较高的容量和优异循环稳定性[21~23].Ma等[23]以CNT纤维负载MnO2为正极,Zn线为负极,制备了柔性可充电锌离子微电池,采用水溶液电解质和凝胶聚合物电解质分别显示322 和290 mA·h/g 的比容量.Mao 等[24]合成了MnO2/rGO/PANI(聚苯胺)复合气凝胶,不仅具有高电导率,且有效抑制锰的溶解;该复合物在0.1C倍率下释放241.1 mA·h/g的高容量,600次循环后的容量保持率为82.7%.此外,将锰基氧化物构筑成3D多孔结构和对其进行表面包覆,不仅可为锌离子提供快速传输通道,且可缓解由于锌离子嵌入/脱出造成的体积变化,抑制其循环过程中锰的溶解和不可逆相转变,稳定电极/电解质界面[25~29].Yuan等[25]制备了聚吡咯(PPy)包覆三维(3D)Mn2O3复合物,其含有丰富的约30 nm的通孔,为锌离子提供快速传输通道;PPy层作为导电网络确保快速电子传输,同时减缓Mn2O3在循环过程中锰的溶解.因此,其作为锌离子电池正极经过2000次循环后容量几乎无衰减[26].然而,如何提高锰基氧化物在小电流密度、深度放电条件下循环寿命短的问题仍是一大挑战.Wang 等[30]构筑了聚苯胺插层层状二氧化锰,消除相转变和提升电荷储存性.该锰基氧化物在200 mA/g电流密度下循环200次后仍保持280 mA·h/g的容量.
本文采用水热法制备出三维(3D)多孔MnOx立方盒子,然后在其表面包覆In2O3层,获得3D 多孔MnOx@In2O3立方盒子.对该3D多孔结构进行了结构和形貌的表征,并对其电化学性能进行了测试.
1 实验部分
1.1 试剂与仪器
四水硝酸锰[Mn(NO3)2·4H2O]、四水氯化铟(InCl3·4H2O)和聚偏二氟乙烯(PVDF)均为分析纯,购自上海沃凯化学试剂有限公司;尿素(CH4N2O)、葡萄糖(C6H12O6·H2O)、七水合硫酸锌(ZnSO4·7H2O)、七水合硫酸锰(MnSO4·7H2O)和无水乙醇(C2H5OH)均为分析纯,购自国药集团化学试剂有限公司;导电炭黑(Super-p,分析纯)购自上海凯茵化工有限公司;N-甲基吡咯烷酮(C5H9NO,分析纯)购自滨州裕能化工有限公司;锌片和不锈钢箔均为分析纯,购自深圳源德莱工业材料有限公司;1823-047型GF/D玻璃纤维滤膜购自上海未熹生物科技有限公司;2025 型扣式电池壳购自兴化市慕鑫新能源材料有限公司.
NOVA 2000型比表面积及孔径分析仪[安东帕商贸(上海)有限公司];Hitachi S-4800型场发射扫描电子显微镜(SEM,日本日立公司);AXS D8 ADVANCE 型X 射线衍射仪(XRD,德国Bruker,AXS 公司,CuKα射线,扫描范围10°~80°,扫描速率2°/min);CT-3008型全自动电池程控测试仪(深圳市新威尔电子有限公司);CHI660E型电化学工作站(上海辰华仪器有限公司);Versa STAT3型电化学工作站[阿美特克商贸(上海)有限公司].
1.2 3D多孔MnOx立方盒子的合成
采用水热法和高温煅烧制备了MnOx立方盒子.如Scheme 1 所示,参照文献[31]的方法,首先将2.51 g Mn(NO3)2·4H2O和3.0 g CH4N2O溶解于40 mL去离子水中,在100 ℃条件下水热反应16 h.反应完成后,用去离子水和无水乙醇清洗和过滤3~5次,获得红棕色的产物(MnCO3).将MnCO3放入马弗炉中,于550 ℃下热处理4 h,随炉冷却至室温获得最终产物MnOx.
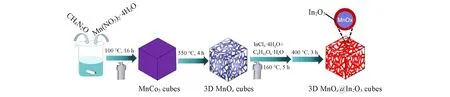
Scheme 1 Schematic diagram for the synthesis of MnOx@ln2O3
1.3 3D多孔MnOx@In2O3立方盒子的合成
将0.24 g MnOx立方盒子加入35 mL 去离子水中,超声分散30 min.将0.01 g InCl3·4H2O 和0.03 g C6H12O6·H2O依次加入MnOx立方盒子分散液中,磁力搅拌3 h使其混合均匀,然后转移到100 mL内衬为聚四氟乙烯反应釜中,于160 ℃下水热反应5 h.反应完毕,用去离子水和无水乙醇洗涤3~5次,将其放入马弗炉中于400 ℃下煅烧3 h,获得MnOx@In2O3立方盒子.其反应原理为:水热条件下,脱水后的葡萄糖会形成线性或支化的低聚物,附着在MnOx立方盒子表面;金属铟离子(In3+)与表面的羟基(—OH)通过配位作用或静电吸引作用产生共轭反应生成In(OH)3;最后,In(OH)3在400°C条件下,空气中煅烧分解为In2O3[32].理论上,通过该实验获得的In2O3包覆量为MnOx@In2O3的2.5%(质量分数).
1.4 电化学测试
分别称取0.07 g 3D MnOx或3D MnOx@In2O3,0.02 g PVDF和0.01 g导电炭黑(质量比7∶2∶1).首先将PVDF溶解于适量N-甲基吡咯烷酮中;然后依次加入导电炭黑和活性材料,搅拌4 h获得浆料;随后将浆料涂布于不锈钢片上,于100 ℃条件下真空干燥12 h,获得活性电极.活性物质的负载量为0.4 mg/cm2.以涂布获得的电极为正极,2 mol/L ZnSO4和0.1 mol/L MnSO4水溶液作为电解液,锌片为负极,组装成2025型扣式电池.在电池测试仪上,在1.0~1.8 V电压范围内,不同电流密度下进行恒电流充放电测试.在CHI660E电化学工作站上,电位窗口为1.8~1.0 V,不同扫描速率进行循环伏安(CV)测试.电化学阻抗谱(EIS)在电化学工作站(Versa STAT3)上测试,频率范围为100 kHz~10 mHz,振幅为5 mV.
2 结果与讨论
2.1 材料的结构与形貌分析
图1为3D多孔MnOx和3D多孔MnOx@In2O3的XRD谱图,可见,3D多孔MnOx和3D多孔MnOx@In2O3在2θ=23.1°,32.9°,38.2°,45.1°,49.3°,55.1°和65.7°处的衍射峰分别对应于Mn2O3(JCPDS No.24-0508)的(211),(222),(400),(323),(413),(044)和(622)晶面.3D 多孔MnOx@In2O3在2θ=28.9°,32.3°,36.1°,37.9°,59.8°和65.4°处的衍射峰对应于Mn3O4(JCPDS No.24-0734)的(112),(103),(211),(004),(224)和(323)晶面.结果显示,3D 多孔MnOx主要由Mn2O3组成,而3D 多孔MnOx@In2O3主要由Mn2O3和Mn3O4混合组成.3D 多孔MnOx@In2O3中所含大量Mn3O4主要是由于葡萄糖衍生碳还原了部分的Mn2O3所生成的.3D 多孔MnOx@In2O3的XRD 谱图中,在2θ=30.1°处出现了新的衍射峰,对应In2O3(JCPDS No.22-0336)的(104)晶面,说明了In2O3层已包覆于MnOx表面.
由图2(A)可见,3D 多孔MnOx立方盒子为边长约10 μm 的立方盒子,含有蜂窝状无序多孔结构.多孔结构主要来自于MnCO3立方盒子高温煅烧释放CO2气体所致.3D 多孔结构有利于H+和Zn2+的传输.其X射线能谱(EDS)图显示C,Mn和O元素均匀分布[图2(B)~(E)].3D多孔MnOx立方盒子表面包覆In2O3后,材料表面形貌没有发生明显变化,仅孔径略减小,孔的骨架略增粗[图3(A)].3D 多孔MnOx@In2O3立方盒子的EDS图[图3(B)~(E)]显示,In元素主要集中、均匀分布在MnOx立方盒子表面,表明该方法可在MnOx立方盒子表面均匀包覆In2O3层.

Fig.1 XRD patterns of 3D MnOx and 3D MnOx@ln2O3 cubes

Fig.2 SEM(A,B)and corresponding EDS mapping images of C(C),Mn(D)and O(E)of 3D MnOx cubes

Fig.3 SEM(A,B)and corresponding EDS mapping images of C(C),Mn(D)and In(E)of 3D MnOx@In2O3 cubes
为进一步表征3D 多孔MnOx@In2O3立方盒子的多孔特性,对其比表面积和孔径分布进行了测试.由图4(A)可见,3D多孔MnOx和3D多孔MnOx@In2O3立方盒子均属于Ⅳ型吸附-脱附等温线,BET比表面积分别为22.0和12.9 m²/g.孔径分布曲线显示3D多孔MnOx和3D多孔MnOx@In2O3立方盒子的孔径大小分别为31.2和9.7 nm[图4(B)].3D多孔MnOx@In2O3比表面积和孔径的减小,可能是由于包覆处理过程中部分In2O3填入MnOx的孔隙所致.

Fig.4 N2 absorption/desorption isotherm(A) and pore distribution(B) profiles of 3D MnOx and 3D MnOx@In2O3 cubes
2.2 电化学性能分析
采用中性电解液的水体系锌离子电池在高电流密度下能循环上万次,然而在小电流密度、高放电深度条件下循环性能并不理想.主要归因于在小电流和高放电深度下,锰基氧化物正极在电化学循环过程中锰的溶解、不可逆相转变和电极/电解质界面稳定性差[30].为了改善锰基氧化物的结构和界面稳定性,在锰基氧化物表面包覆了In2O3层.图5给出了3D多孔MnOx和3D多孔MnOx@In2O3在0.3 A/g电流密度下的充放电曲线及循环性能曲线.在首次放电过程中,3D多孔MnOx仅在1.1 V附近出现1个电压平台[图5(A)],归因于Mn3+转变为Mn2+[33];而3D 多孔MnOx@In2O3在首次放电过程中几乎无容量[图5(B)].可能因为3D MnOx@In2O3的主要成分为Mn2O3和Mn3O4(图1),部分Mn2O3在包覆In2O3层过程中已被还原为Mn3O4,其Mn3+的量较少,且表面非活性In2O3包覆层在活化初期可能增大电化学极化.经过首次放电后,3D多孔MnOx在1.4和1.2 V附近出现2个新的放电电压平台,分别对应于H+和Zn2+的嵌入[图5(A)][18];在随后4 次循环过程中,充放电曲线变化较小.经过首次放电后,3D 多孔MnOx@In2O3开始出现容量,且在随后的4次循环过程中逐渐增大,其也在1.4和1.2 V附近显示2个明显的放电电压平台[图5(B)].随着循环的进行,3D多孔MnOx的放电曲线开始出现变形,400次循环后出现严重变形,说明其循环过程中相转变严重[图5(C)];而3D多孔MnOx@In2O3电极的充放电曲线无明显变化,400次循环后仅在1.2 V附近放电电压平台略有缩短,说明其在电化学循环过程中维持了良好的结构稳定性,相转变不明显[图5(D)].由图5(E)可见,随着循环次数增加,3D多孔MnOx@In2O3电极的比容量逐渐增大,200 次循环后达到稳定,且经过400 次稳定循环后,仍然保持260 mA·h/g 的容量,容量保持率达到86.6%,优于大多数文献报道[34~45](表1).然而,随着循环次数的增加,3D 多孔MnOx电极的放电比容量呈现快速衰减的趋势,400次循环后,其放电比容量衰减至81.9 mA·h/g,容量保持率仅为37.75%.结果表明,In2O3包覆可以显著提高MnOx电极的循环稳定性,抑制容量衰减,可能由于In2O3层可抑制锰在电解液中的溶解,提高材料的结构稳定性,进而提高循环寿命.

Fig.5 Charge/discharge profiles of 3D MnOx(A,C) and 3D MnOx@In2O3(B,D) cubes,and their cyclability profiles(E)at 0.3 A/g

Table 1 Comparison of electrochemical performance of reported Mn-based oxides and this work
图6给出了3D多孔MnOx和3D多孔MnOx@In2O3在1.8 A/g电流密度下的充放电曲线及循环性能曲线.由图6(A)和(B)可见,3D多孔MnOx和3D多孔MnOx@In2O3在首次放电过程中几乎均无容量,主要原因是Mn3+还原为Mn2+过程较困难,在大电流密度下难出现.经过首次放电后,3D多孔MnOx在1.4 V附近出现长的放电电压平台,但在1.2 V的放电电压平台不明显;随后的4次循环中显示相似的放电电压平台[图6(A)].3D多孔MnOx@In2O3在初始的5次循环特性与0.3 A/g电流密度的情况相似,容量逐渐增大,在1.4和1.2 V附近显示两个明显放电电压平台[图6(B)].在1.2 V附近电压平台的存在说明其经过电化学活化后具有更小的电化学极化.随着循环次数的增加,3D多孔MnOx电极的电压平台变化大,说明其结构在电化学循环过程中遭到严重破坏[图6(C)].相比之下,随着循环次数的增大,3D多孔MnOx@In2O3电极的放电电压平台变化较小,即使经过4000 次循环后与100 次循环曲线几乎重合[图6(D)].由图6(E)可见,3D多孔MnOx@In2O3电极具有优异的循环稳定性,经过4000次循环后容量仍保持81 mA·h/g,优于大多数文献报道[34~45](表1).然而,3D 多孔MnOx电极经过4000 次循环后仅保持31.5 mA·h/g.

Fig.6 Charge/discharge profiles of 3D MnOx(A,C) and 3D MnOx@In2O3(B,D) cubes,and their cyclability profiles(E)at 1.8 A/g
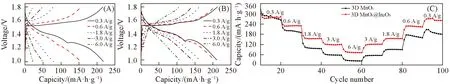
Fig.7 Charge/discharge profiles of 3D MnOx(A) and 3D MnOx@In2O3(B) cubes and their cyclability profiles(C)at different current densities
图7给出了3D多孔MnOx和3D多孔MnOx@In2O3在不同电流密度下的充放电曲线及循环性能曲线.由图7(A)可见,3D多孔MnOx电极的放电曲线随着电流密度增大变形严重.然而,3D多孔MnOx@In2O3电极的放电曲线变形较小,说明In2O3包覆层可降低电化学极化[图7(B)].由图7(C)可见,3D 多孔MnOx@In2O3电极在0.3,0.6,1.8,3和6 A/g 电流密度下的容量分别为275.3,229.3,153.8,119.3和73.4 mA·h/g.即使在高电流密度6.0 A/g 下仍保持73.4 mA·h/g 的高可逆容量,展示了优异的倍率性能.当电流密度再次回到0.3 A/g时,可逆容量由于活化影响增加到了260.9 mA·h/g.3D多孔MnOx电极在0.3 A/g电流密度下的比容量与3D多孔MnOx@In2O3电极接近;然而,随着电流密度的增加,3D多孔MnOx电极的容量明显低于3D多孔MnOx@In2O3电极,在6 A/g电流密度下仅保持24.8 mA·h/g的比容量.当电流密度再次回到0.3 A/g 时,3D 多孔MnOx电极的容量仅保持178.9 mA·h/g,远低于3D 多孔MnOx@In2O3电极.上述结果表明,In2O3包覆层可极大提升3D多孔MnOx电极的高倍率容量.
2.3 电极/电解质界面研究
为表征In2O3包覆层对3D多孔MnOx立方盒子在储锌过程中的电化学反应动力学的提升作用,分别用3D多孔MnOx和3D多孔MnOx@In2O3电极与锌片组装成电池,在120 mA/g的电流密度下充放电40次后进行了恒电流间歇滴定(GITT)测试[图8(A)].可见,3D多孔MnOx@In2O3电极的极化明显低于3D多孔MnOx电极,说明In2O3包覆层有利于减小MnOx电极在循环过程中的电化学极化.
为了表征3D 多孔MnOx和3D 多孔MnOx@In2O3电极的储锌过程,测试了它们的循环伏安曲线.图8(B)给出了它们在0.1 mV/s下的循环伏安曲线,可见,3D多孔MnOx@In2O3电极分别在1.38和1.23 V 处出现两个明显的还原峰,分别对应H+和Zn2+的插入使Mn4+被还原为Mn3+和Mn3+被还原为Mn2+的过程[18].同时,在1.52 和1.56 V 处出现两个明显的氧化峰,分别对应H+和Zn2+的脱出使Mn2+被氧化为Mn3+和Mn3+被氧化为Mn4+的过程[18].3D多孔MnOx和3D多孔MnOx@In2O3电极显示相似的氧化/还原电流峰,但3D多孔MnOx电极在1.52和1.56 V附近的氧化电流峰分离不明显,说明电化学极化较大.为进一步表征H+和Zn2+的扩散,测试3D多孔MnOx和3D多孔MnOx@In2O3电极在不同扫描速率下的循环伏安曲线.图8(C)和(D)分别给出了它们在不同扫描速率下的循环伏安曲线,可见,峰值电流随着扫描速率的增大而增大.图8(E)~(H)分别给出了3D 多孔MnOx和3D 多孔MnOx@In2O3电极的CV 曲线的Peak1,Peak2,Peak3 和Peak4 的Ip-v1/2关系曲线,均呈线性关系,其斜率如表2 所示.其中,3D 多孔MnOx@In2O3电极的Ip-v1/2曲线的斜率均大于3D 多孔MnOx电极,说明前者具有更大的H+和Zn2+扩散系数.可能由于In2O3包覆层有利于稳定电极/电解质界面,减小电极表面副产物的量,有利于离子扩散.
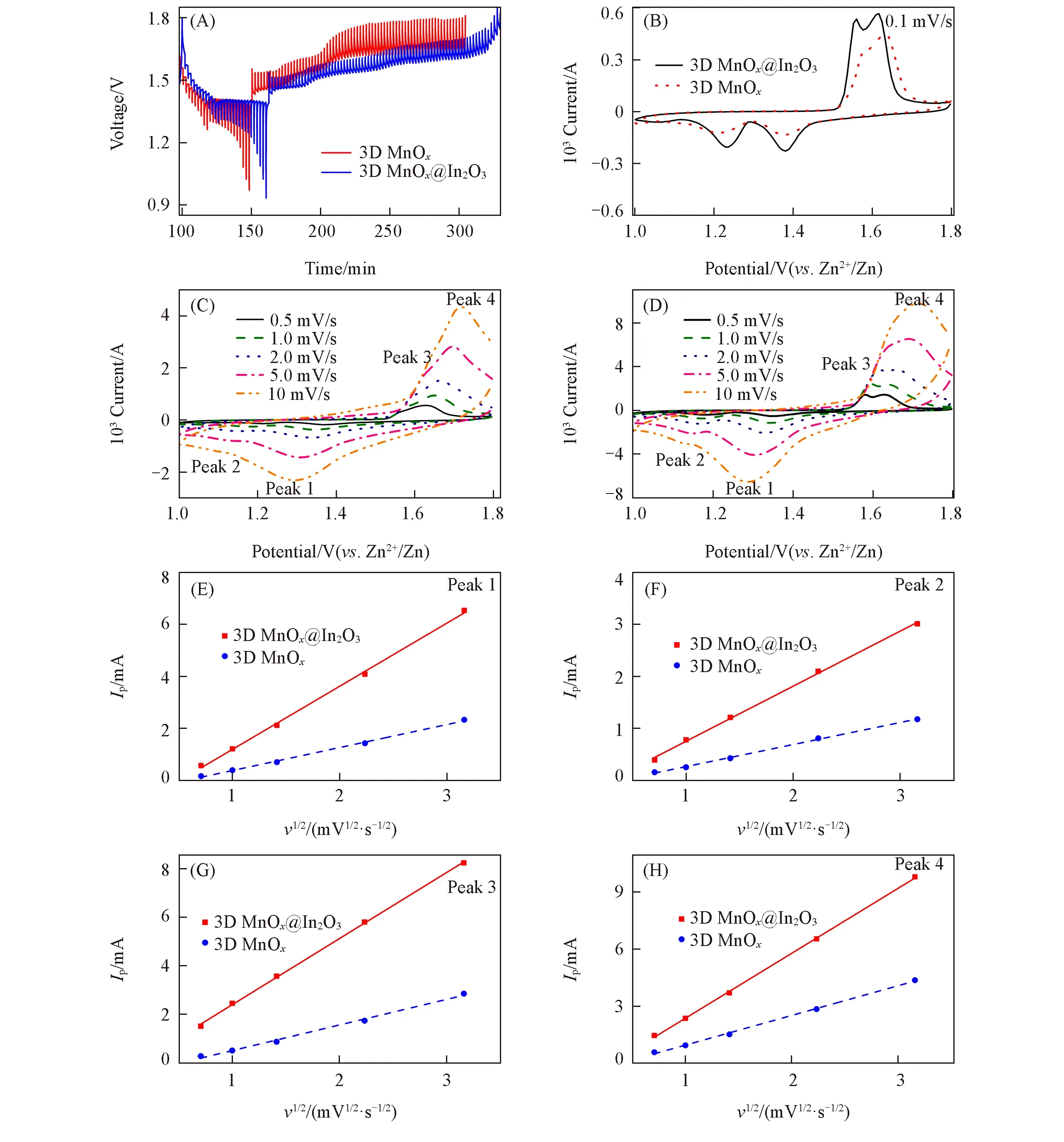
Fig.8 GITT profiles(A) and CV profiles(B) at 0.1 mV/s of 3D MnOx and 3D MnOx@In2O3 cubes,the CV profiles of 3D MnOx(C)and 3D MnOx@In2O3cubes(D)at different scanning rates and their Ip-v1/2 profiles(E―H)
为表征In2O3包覆层对MnOx电极/电解质界面的改善,测试了3D多孔MnOx和3D多孔MnOx@In2O3电极经过1 次、1000 次和2000 次循环后的电化学阻抗(图9).由图9(A)可见,经过1次循环后的Nyquist曲线均由高频圆弧和低频斜线组成.其中高频圆弧代表电荷传递阻抗,低频斜线代表离子扩散.其中,3D多孔MnOx@In2O3电极的高频圆弧略小于3D多孔MnOx电极,说明前者具有较小的电荷传递阻抗和更高的电化学反应活性.3D多孔MnOx@In2O3电极低频斜线的斜率大于3D多孔MnOx电极,说明前者具有更高的离子扩散速率,与CV结果一致.经过1000次循环后,3D多孔MnOx@In2O3电极的高频圆弧大小基本无变化,说明其电荷传递阻抗变化较小,电化学活性仍保持较好;同时其低频斜线略增加,说明其离子扩散速率增大[图9(B)].然而,3D 多孔MnOx电极经过1000 次循环后的高频圆弧明显增大,说明经过循环后其电化学活性降低[图9(B)].经过2000次循环后,3D多孔MnOx@In2O3电极的高频圆弧略增加,然而三维多孔MnOx电极的高频圆弧进一步明显增大.可能由于In2O3包覆层的存在可减少电极表面副产物的生成;比较图5(A)和(B)及图6(A)和(B)可知,3D MnOx电极经过循环后,充放电曲线变形严重,说明其经过循环后相转变严重,增大了阻抗.以上结果表明,3D多孔MnOx@In2O3电极不仅可提高电化学反应活性和离子扩散速率,且其电极/电解质界面稳定性好,经过2000次循环界面阻抗增加较小[图9(C)],这是其电化学性能表现优异的一个重要原因.

Table 2 Slopes of Ip-v1/2 profiles
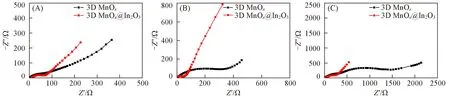
Fig.9 Nyquist plots of 3D MnOxand 3D MnOx@In2O3cubes suffered 1st(A),1000th(B)and 2000th(C)cycles
图10 给出了3D 多孔MnOx和3D 多孔MnOx@In2O3电极在1.8 A/g 的电流密度下循环2000 次后的SEM 照片.可见,经过2000 次循环后,它们的结构均发生明显塌陷[图10(A)和(B)],其中3D 多孔MnOx的结构塌陷更为严重.经过2000 次循环后,3D 多孔MnOx@In2O3电极表面仍然显示少量In 元素[图10(C)~(F)],说明仍然有少量In2O3包覆于MnOx活性材料表面,确保MnOx电极的优异循环性能.

Fig.10 SEM(A,C) and corresponding EDS mapping(D―F) images of 3D MnOx@In2O3 cubes suffered 2000 cycles,SEM image(B)of 3D MnOx cubes suffered 2000 cycles
3 结 论
采用水热法和高温煅烧法制备了In2O3包覆的3D多孔MnOx立方盒子(MnOx@In2O3).该方法工艺简单,其微米级粒子更有利于商业化应用.结果表明,MnOx@In2O3立方盒子的3D多孔结构有利于离子快速传输,In2O3包覆层改善了电化学反应活性,提高了电极/电解质界面的稳定性.电化学结果表明,3D多孔MnOx@In2O3电极在0.3 A/g的小电流密度下循环400次后仍保持260 mA·h/g的容量,在1.8 A/g电流密度下可稳定循环4000次以上,容量保持81 mA·h/g,即使在高电流密度6.0 A/g下仍保持73.4 mA·h/g的高可逆容量.

